高考化学大二轮复习 第1部分 知识整合 专题5 选考模块 第15讲 物质结构与性质课件
- 格式:ppt
- 大小:13.92 MB
- 文档页数:56


专题十五物质结构与性质(选考)[考纲要求]1。
原子结构与元素的性质:(1)了解原子核外电子的排布原理及能级分布,能用电子排布式表示常见元素(1~36号)原子核外电子、价电子的排布,了解原子核外电子的运动状态;(2)了解元素电离能的含义,并能用以说明元素的某些性质;(3)了解原子核外电子在一定条件下会发生跃迁,了解其简单应用;(4)了解电负性的概念,知道元素的性质与电负性的关系。
2.化学键与物质的性质:(1)理解离子键的形成,能根据离子化合物的结构特征解释其物理性质;(2)了解共价键的形成,能用键能、键长、键角等说明简单分子的某些性质;(3)了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系;(4)理解金属键的含义,能用金属键理论解释金属的一些物理性质,了解金属晶体的常见堆积方式;(5)了解杂化轨道理论及常见的杂化轨道类型(sp、sp2、sp3),能用价层电子对互斥理论或者杂化轨道理论推测常见的简单分子或者离子的空间结构.3。
分子间作用力与物质的性质:(1)了解化学键和分子间作用力的区别;(2)了解氢键的存在对物质性质的影响,能列举含有氢键的物质;(3)了解分子晶体与原子晶体、离子晶体、金属晶体的结构微粒、微粒间作用力的区别;(4)能根据晶胞确定晶体的组成并进行相关的计算;(5)了解晶格能的概念及其对离子晶体性质的影响.1.排布规律(1)能量最低原理:基态原子核外电子优先占据能量最低的原子轨道,如Ge:1s22s22p63s23p63d104s24p2。
(2)泡利原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子。
(3)洪特规则:原子核外电子在能量相同的各轨道上排布时,电子总是优先单独占据一个轨道,且自旋状态相同。
2.表示方法(1)电子排布式按电子排入各电子层中各能级的先后顺序,用能级符号依次写出各能级中的电子数,同时注意特例。
如:Cu:1s22s22p63s23p63d104s1(2)简化电子排布式“[稀有气体]+价层电子”的形式表示。

第15题:有机物结构与性质满分:70分1.下列与有机物结构、性质相关的叙述错误的是A.乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2B.蛋白质和油脂都属于高分子化合物,一定条件下都能水解C.甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同D.苯不能使溴的四氯化碳溶液发生化学反应褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键2.下列叙述中,错误的是( )A.苯酚具有弱酸性,但不能使紫色石蕊变红B.因发生化学反应而使溴水褪色的物质一定是和溴水发生加成反应C.用核磁共振氢谱鉴别1溴丙烷和2溴丙烷D.含醛基的有机物都能发生银镜反应3.下列关于常见有机物的说法正确的是A.乙烯和苯都能和溴水发生化学反应而使溴水褪色B.乙烷可使酸性高锰酸钾溶液褪色C.糖类和蛋白质都是高分子化合物D.乙酸和油脂都能与氢氧化钠溶液反应4.关于有机物主要特点的下列说法中不正确的有A.大多数有机物难溶于水,易溶于汽油、酒精、苯等有机溶剂B.有机物的熔点低、受热易分解,且都能燃烧C.绝大多数有机物是非电解质,不易导电D.有机物的化学反应比较复杂一般较慢且有副反应5.下列关于碳原子的成键特点及成键方式的理解,正确的是()A.饱和碳原子不能发生化学反应B.C原子只能与C原子形成不饱和键C.任何有机物中H原子数目不可能为奇数D.五个C原子之间能够形成五个碳碳单键6.下列说法不正确的是()A. 法国化学家维勒首次提出有机化学的概念;德国化学家贝采里乌斯由氰酸铵合成了尿素,首次打破了有机物和无机物的界限B. 李比希用燃烧法来测定有机化合物中碳氢元素质量分数C. 用核磁共振氢谱和红外光谱法可以区别乙醇和二甲醚(CH3OCH3)D. 用“同位素示踪法”是研究有机化学反应历程的手段之一7.下列关于有机化学发展史的说法错误的是网]A. 中国科学家成功合成了结晶牛胰岛素,标志着人类合成蛋白质时代的开始B. 德国化学家李比希提出运用同位素示踪法研究化学反应历程C. 瑞典科学家贝采利乌斯提出有机化学的概念,使之成为化学的一个重要分支D. 德国化学家维勒用氰酸铵合成尿素,从而打破了无机物和有机物的界限8.下列关于一些有机物在合适条件下的化学反应说法正确的是()A .能催化氧化生成醛B .能在浓硫酸的作用下生成烯C.CH3Br 能在氢氧化钠的乙醇溶液的作用下生成醇D .既能与酸反应也能与碱反应生成盐9.下列说法不正确的是()A.李比希燃烧法、钠熔法、铜丝燃烧法都是用来分析有机物元素组成的方法B.红外光谱法、紫外光谱法、核磁共振、质谱仪等都是现代化学测定有机物结构的常用方法C.同位素示踪法是研究化学反应历程的手段之一D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别10.下列说法正确的是A. 沸点:邻二甲苯>间二甲苯>对二甲苯B. 鸡蛋淸在NH4Cl溶液中能发生盐析,但是不能和盐酸发生化学反应C. 有机物A的分子式为C16H16O3D. 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键11.有关下列物质分子结构特征描述正确的是A.1 mol CH3CH2OH与Na完全反应只生成0.5 mol H2,不能说明乙醇分子中有一个氢原子与其它氢原子不同B.苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构C.CHCl HCl和CClH HCl属于同一种物质,不能用来解释甲烷是一种正四面体结构D.乙烯容易与溴的四氯化碳溶液发生反应,且1 mol乙烯完全加成消耗1 mol溴单质,证明乙烯分子里含有一个碳碳双键12.有关下列物质分子结构特征描述正确的是A.乙烯分子中碳、氢原子个数比为1:2,证明乙烯分子里含有一个碳碳双键B.表示苯分子的结构,因此能解释邻二甲苯有CH3CH3和CH3CH3两种结构C.因为甲烷是一种正四面体结构,所以CHCl HCl和CClH HCl属于同一种物质D.苯的分子式是C6H6,分子式中碳原子远没有饱和,因此苯能使溴水褪色13.下列与有机物的结构、性质有关的叙述正确的是A.苯、油脂均不能使酸性KMnO4溶液褪色B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应C.葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体D.乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同14.下列说法不正确...的是A.利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学B .蔗糖、淀粉、油脂及其水解产物均为非电解质C .通过红外光谱分析可以区分乙醇和乙酸乙酯D .石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃. 15.下列说法正确的是A .按系统命名法,化合物CH 2CHCH 2CH(CH 3)2CH 3CH 2CH(CH 3)2的名称为2,6-二甲基-5-乙基庚烷B .丙氨酸和苯丙氨酸脱水,最多可生成3种二肽C .化合物是苯的同系物D .三硝酸甘油酯的分子式为C 3H 5N 3O 9 16.下列关于有机物的叙述正确的是A.乙醇不能发生取代反应B.C 4H 10 有三种同分异构体C.氨基酸、淀粉均属于高分子化合物D.乙烯和甲烷可用溴的四氯化碳溶液鉴别 17.(2014届浙江省金丽衢十二校高三第二次联考理综化学试卷) 下列说法正确的是 A.按系统命名法的名称为2一甲基一3,5一二乙基己烷B.用Na 2 C03溶液能区分CH 3COOH 、CH 3CH 2OH,苯、硝基苯四种物质C .等质量的甲烷、乙烯、1,3一丁二烯分别充分燃烧,所耗氧气的量依次增加D.下列物质的沸点按由低到高顺序为:(CH 3CH 2)2CH 3<(CH 3)3CH <CH 3(CH 2)3CH 3<(CH 3)2CHCH 2CH 3 18.下列叙述中,错误的是( )A.苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯B.苯乙烯在合适条件下催化加氢可生成乙基环己烷C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯19.(2014届浙江省嘉兴市高三教学测试(二)理综化学试卷) 下列说法正确的是A .按系统命名法,化合物 的名称为2,4—二乙基—6—丙基辛烷B .月桂烯 ()所有碳原子一定在同一平面上C .取卤代烃,加入氢氧化钠的乙醇溶液加热一段时间后冷却,再加入稀硝酸酸化的硝酸银溶液,一定会产生沉淀,并根据沉淀颜色判断卤代烃中卤原子的种类D .通常条件下,1mol 的 分别与H 2 和浓溴水完全反应时,消耗的H 2和Br 2的物质的量分别是 4mol 、3mol20.(2014届浙江省金华十校高考模拟考试理综化学试卷) 下列说法正确的是A .按系统命名法,有机物的名称为3,7一二.甲基-4-乙基辛烷B .高聚物脲醛树脂()的合成单体之一是C .1 mol 葡萄糖能水解生成2 rnol CH 3CH 2OH 和2 mol CO 2D .在酸性条件下,CH 3CO 18OC 2 H 5的水解产物是CH 3CO 18OH 和C 2H 5OH 21.下列对有机物结构或性质的描述,错误..的是 A .乙酸与乙醇在一定条件下发生酯化反应,加入浓H 2SO 4有利于酯化反应的进行B .鉴别己烯中是否混有少量甲苯,先加足量的酸性高锰酸钾溶液,然后再加入溴水C .乙烷和丙烯的物质的量各1mol ,完成燃烧生成3molH 2OD .蛋白质溶液中分别加入饱和(NH 4)2SO 4和CuSO 4溶液,均出现白色沉淀,但原理不同 22.下列有机物结构、性质相关的叙述错误的是A 、乙酸分子中含有羧基,可与NaHCO 3溶液反应生成CO 2B 、蛋白质和油脂都属于高分子化合物,一定条件下都能水解C 、甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同D 、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 23.下列对有机物结构或性质的描述,错误..的是 A .一定条件下,乙醇可以发生取代反应或消去反应B .苯酚钠溶液中通入CO 2生成苯酚,则碳酸的酸性比苯酚弱C .乙烷和丙烯的物质的量各1mol ,完全燃烧都生成3molH 2OD .光照下2,2—二甲基丙烷与Cl 2反应,其一氯取代物只有二种 24.下列对有机物结构或性质的描述,错误的是A .一定条件下,Cl 2可在甲苯的苯环或侧链上发生取代反应B .苯酚钠溶液中通入CO 2生成苯酚,则碳酸的酸性比苯酚弱C .乙烷和丙烯的物质的量共1mol ,完成燃烧生成3molH 2OD .光照下2,2—二甲基丙烷与Br 2反应其一溴取代物只有一种 25.下列对有机物结构或性质的描述错误的是A .乙酸与乙醇在一定条件下发生酯化反应,加入浓H 2SO 4有利于酯化反应的进行B .鉴别己烯中是否混有少量苯,加入少量溴水C .乙烷和丙烯的物质的量各1mol ,完全燃烧均生成3molH 2OD .蛋白质溶液中分别加入饱和(NH 4)2SO 4和CuSO 4溶液,均有白色沉淀,但原理不同 26.下列对有机物结构或性质的描述,错误..的是 A .苯酚钠溶液中通入CO 2生成苯酚,则碳酸的酸性比苯酚弱 B .一定条件下,Cl 2可在甲苯的苯环或侧链上发生取代反应 C .乙烷和丙烯的物质的量共1mol ,完全燃烧生成3molH 2O D .硬脂酸甘油酯的皂化反应的两种产物均可溶于水 27.下列与有机物结构、性质相关的叙述错误的是A .甲烷与氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同B .溴水、酸性高锰酸钾溶液均可用于鉴别乙烯和乙烷,也均可以除去乙烷中的乙烯C .核磁共振氢谱可以鉴别某些不同物质,质谱可快速、准确测定物质的分子量D .实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol 、-3747 kJ/mol 和-3265 kJ/mol ,可以证明在苯分子中不存在独立的碳碳双键 28.下列与有机物结构、性质相关的叙述错误的是A.乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2B.蛋白质和油脂都属于高分子化合物,一定条件下能水解C.甲烷和氯气反应生成一氯甲烷、苯和硝酸反应生成硝基苯的反应类型相同D.苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键29.下列对有机物结构或性质的描述,错误..的是A.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应B.甲苯与浓硝酸和浓硫酸的混酸反应制TNT体现了苯环对侧链的影响。




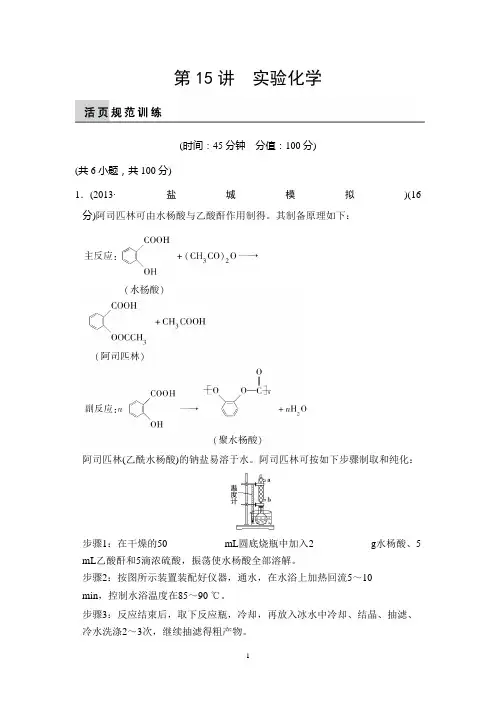
第15讲实验化学(时间:45分钟分值:100分)(共6小题,共100分)1.(2013·盐城模拟)(16分)阿司匹林可由水杨酸与乙酸酐作用制得。
其制备原理如下:阿司匹林(乙酰水杨酸)的钠盐易溶于水。
阿司匹林可按如下步骤制取和纯化:步骤1:在干燥的50 mL圆底烧瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡使水杨酸全部溶解。
步骤2:按图所示装置装配好仪器,通水,在水浴上加热回流5~10min,控制水浴温度在85~90 ℃。
步骤3:反应结束后,取下反应瓶,冷却,再放入冰水中冷却、结晶、抽滤、冷水洗涤2~3次,继续抽滤得粗产物。
步骤4:将粗产物转移至150 mL烧杯中,在搅拌下加入25mL饱和碳酸氢钠溶液,充分搅拌,然后过滤。
步骤5:将滤液倒入10 mL 4 mol·L-1盐酸,搅拌,将烧杯置于冰浴中冷却,使结晶完全。
抽滤,再用冷水洗涤2~3次。
(1)步骤1浓硫酸的作用可能是________。
(2)步骤2中,冷凝管通水,水应从________口进(填“a”或“b”)。
(3)步骤3抽滤时,有时滤纸会穿孔,避免滤纸穿孔的措施是________________ ______________________________________________。
(4)步骤4发生主要反应的化学方程式为_____________________;过滤得到的固体为________。
(5)取几粒步骤5获得的晶体加入盛有5mL水的试管中,加入1~2滴1%三氯化铁溶液,发现溶液变紫色,可采用____ ____方法,进一步纯化晶体。
解析(1)由制备原理可以看出,浓硫酸的作用是在该反应中作为催化剂。
(2)冷凝水的流向是“下进上出”,故从b管进水,a管出水。
(3)避免滤纸穿孔的措施是减小真空度或者加一层(或多层)滤纸。
(4)根据产物的结构特点可知是羧基(—COOH)与NaHCO3发生反应+NaHCO3―→+CO2↑+H2O;粗产品还有可能发生副反应得到聚水杨酸。

有机化合物—2024届高考化学二轮复习一有机物组成、结构1.C、H、O、N、X(X=F、Cl、Br、I)等常见原子成键特点(1)碳原子成键特点C最外层4个电子,差4个达到8电子稳定结构,所以C形成4个共价键;具体类型有①四个单键:(烷烃与环烷烃均为此结构),②两个单键+一个双键:(烯烃为此种结构),③一个单键+一个三键:(炔烃为这种结构),④两个双键:C(CO2为此结构、有机物中这种结构一般不稳定),⑤三个单键+1大π键:(芳香烃及其衍6生物为此结构)。
(2)氢原子及卤素原子(X)成键特点:H差1个电子达2电子稳定结构,X是第ⅦA族,差1个电子达8电子稳定结构,所以H、X一般只能形成单键,也就是—H和—X,所以H、X只能处在分子的“端位”一般不能成环。
(3)O原子成键特点:O是第ⅥA族,最外层6个电子,差 2个电子达8电子稳定结构,所以一般可以形成2个共价键,也就是O或—O—。
(4)N原子成键特点N是第ⅤA族,最外层5个电子,差3个电子达8电子稳定结构,所以N一般可以形成3个共价键,也就是①一个三键:≡N(N2或氰基就是此结构),②一个单键+一个双键:—N(嘧啶、嘌呤含有此结构),③三个单键:(氨气、氨基有此结构),注意铵根结构较特殊:[]+存在一个“配位键”所以形成4个共价键。
(5)C、N、O均可成环,也可以成链,但H、X不能成环。
2.有机物原子共线、共面问题(1)数学背景知识①某条直线与某个平面有两个公共点,则该直线属于该平面。
②两个平面若存在三个不共线的公共点,则两个平面是同一个平面。
③若两个平面具有两个公共点(或三个共线的公共点),则两平面相交或是同一个平面。
(2)化学背景知识①结构属于四面体构型(若四个成键原子相同一般为正四面体,不同则为变形四面体),一旦出现此种结构则所有原子不可能共线,也不可能共面。
②凡是双键(或)部位一定属于平面构型。
③凡是三键(—C≡C—或—C≡N)部位一定属于直线构型。

专题一物质的组成、分类1.(2023·新课标卷)化学在文物的研究和修复中有重要作用。
下列说法错误的是( ) A.竹简的成分之一纤维素属于天然高分子B.龟甲的成分之一羟基磷灰石属于无机物C.古陶瓷修复所用的熟石膏,其成分为Ca(OH)2D.古壁画颜料中所用的铁红,其成分为Fe2O3解析:纤维素是一种天然化合物,其分子式为(C6H10O5)n,其相对分子质量较高,是一种天然高分子,A项正确;羟基磷灰石又称羟磷灰石、碱式磷酸钙,其化学式为[Ca10(PO4)6(OH)2],属于无机物,B项正确;熟石膏主要成分为2CaSO4·H2O,Ca(OH)2是熟石灰的主要成分,C项错误;Fe2O3为红色,常被用于油漆、涂料、油墨和橡胶的红色颜料,俗称铁红,D项正确。
故选C。
答案:C2.(2023·湖南卷)下列化学用语表述错误的是( )A.HClO的电子式:B.中子数为10的氧原子:18 8OC.NH3分子的VSEPR模型:D.基态N原子的价层电子排布图:解析:HClO中O与H和Cl形成两个共价键,因此HClO的电子式为,A项正确;中子数为10,质子数为8的O原子其质量数为10+8=18,其原子表示为18 8O,B项正确;根据VSEPR模型计算,NH3分子中有1对孤电子对,N还连接有3个H原子,因此NH3的VSEPR模型为四面体形,C项错误;基态N原子的价层电子排布为2s22p3,其电子排布图为,D项正确。
故选C。
答案:C3.(2023·全国甲卷)化学与生活密切相关,下列说法正确的是( )A.苯甲酸钠可作为食品防腐剂由于其具有酸性B.豆浆能产生丁达尔效应是由于胶体粒子对光线的散射C.SO2可用于丝织品漂白是由于其能氧化丝织品中有色成分D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化解析:苯甲酸钠属于强碱弱酸盐,其水溶液呈碱性,可作为食品防腐剂是因为苯甲酸能使蛋白质变性,而不是由于其具有酸性,A项不正确;胶体具有丁达尔效应,是因为胶体粒子对光线发生了散射,豆浆属于胶体,因此,其能产生丁达尔效应是由于胶体粒子对光线的散射,B项正确;SO2可用于丝织品漂白是由于其能与丝织品中有色成分化合为不稳定的无色物质,C项不正确;维生素C具有很强的还原性,因此,其可用作水果罐头的抗氧化剂是由于其容易被氧气氧化,从而防止水果被氧化,D项不正确。

模块综合复习一、模块知识结构 1. 原子结构理论1. 各层最多容纳的电子数目=2n 22. 最外层电子数目不超过8个(K 层为最外层不超过2个)3. 次外层电子数目不超过18个,倒数第三层电子数目不 超过32个4. 填充电子时,所遵循的原理:构造原理;能量最低原理; 泡利不相容原理和洪特规则5. 最外层电子数未满时,结构不稳定,有得失电子形成 稳定结构的趋势。
主族元素的最外层电子数=主族数质子――Z 个,决定元素种类。
质子数=核电荷数=原子序数 中子――N 个,Z 相同,N 不同的原子互称为同位素质子数+中子数=质量数原子核 核外电子决定元素的化学性质。
原子的电子数=质子数=原子序数运动特点: 电子云运动状态 1. 电子云的大小(电子层) 2. 电子云的形状(电子亚层)3. 电子云伸展方向(轨道)4. 电子的自旋 排布规律原子2.元素周期律元素周期律的实质:原子核外电子排布的周期性周期表结构周期(7个周期)族(7个主族、7个副族、1个Ⅷ族、1个0族分区(按电子层结构分):s区、p区、d区、ds区、f 区递变规律变化内容:金属性、非金属性、原子半径、化合价、第一电离能、电负性等金属性逐渐减弱,非金属性逐渐增强;原子半径逐渐减小(稀有气体比相邻的卤素大);最高正价由+1→+7(F、O无最高正价),最低价由-4→-1;第一电离能逐渐增大(ⅡA、ⅤA比相邻的大);电负性逐渐增大。
同周期:(从左到右)同主族:(从上到下)金属性逐渐增强,非金属性逐渐减弱;原子半径逐渐增大;价态特点相似;第一电离能逐渐减小;电负性逐渐减小。
元素性质的规律性3. 物质构成理论一是中心原子所有价电子都参与成键,如CO 2等;二是分子中极性键的极性向量和是否等于零,如 C 2H 2、C 2H 4、C 2H 6等; 三是ABn 型分子中,A 的化合价数=价电子数, 如CO 2、BF 3、CCl 4、SO 3、PCl 5等 化学键意义、实质:相邻的两个或多个原子之间强烈的相互作用 离子键分类金属键共价键 按成键方式分类 σ键π键 按有无极性分类极性键 饱和性 非极性键 方向性 配位键 键长、键角、键能 氢键 分子间作用力范德华力分子间氢键分子内氢键分子类型 极性分子非极性分子手性分子:必须键合四个不同的原子或原子团 空间构型 杂化轨道理论杂化轨道数=键合原子数+孤对电子数sp 杂化:如BeCl 2、C 2H 2,直线型sp 2杂化:如BF 3、SO 3,平面正角形 C 2H 4,平面形结构 sp 3杂化:如CH 4、CCl 4,正四面体型sp 3d 杂化:如PCl 5,三角双棱锥型sp 3d 2杂化:如SF 6,正八面体型 孤对电子对共用电子对的排斥作用价层电子对互斥理论: 配合物:一方原子提供孤对电子,另一方提供空轨道而形成的共价键物质的构成4.晶体结构理论要点:[Cu ( NH3 )4内界(配离子)中心原配位原配位体配位数界离离子键配位键配合物组成:(1)中心离子或原子必须有空轨道;(2)配位原子必须有孤对电子。
高三化学高考复习第二轮专题一鲁教版【本讲教育信息】一. 教学内容:高考复习第二轮专题一物质的组成、分类、性质和变化二. 教学目的1. 学习比较、分类等科学方法,知道比较、分类等科学方法是化学研究和学习的常用方法。
2. 能根据物质的组成和性质对物质进行分类。
3. 了解常见物质及变化的分类方法。
4. 认同分类法对于化学研究和化学学习的重要作用。
5. 知道根据分散质粒子的大小,把分散系分为溶液、胶体和浊液。
6. 知道胶体的丁达尔现象。
了解胶体的重要应用。
三. 重点和难点1、根据物质的组成和性质对物质进行分类。
2、常见物质变化及分类方法。
3、分散系及分散系的分类,胶体的性质,胶体的应用。
四. 考点分析本专题内容在高考中的主要考查点是:1、物质的组成及分类。
2、物质变化的分类。
3、分散系、胶体的性质及胶体的应用。
五. 知识网络2. 分散系分散质粒子大小/nm外观特征能否通过滤纸 有无丁达尔效应 实例溶液 小于1均匀、透明、稳定能没有NaCl 、蔗糖溶液胶体 在1~100之间均匀、有的透明、较稳定能有()3OH Fe 胶体 浊液 大于100不均匀、不透明、不稳定不能没有泥水四大基本反应类型化合:322SO 2O SO 2△催化剂+分解:O H CO CO Na NaHCO 222323+↑+△置换:22I KCl 2KI 2Cl +=+ 复分解:()O H 2NH 2CaCl OH Ca Cl NH 223224+↑++△是否有离子参与反应(电解质在水溶液中) 离子反应:HClO HCl O H Cl 22+=+ 非离子反应:32FeCl 2Cl 3Fe 2=+是否有元素电子得失或偏移(有升降价) 氧化还原反应:↑+=+22H NaOH 2O H 2Na 2 非氧化还原反应:()O H 2NaAlO NaOH OH Al 223+=+ 热量的放出或吸收放热反应:432O Fe O 2Fe 3△+【典型例题】例1 下列叙述中,正确的是A. 棉花、羊毛都属于纤维素B. 生产水泥和普通玻璃的原料中都有石灰石C. 饱和硫酸铵溶液可以使蛋白质变性D. 煤的干馏为物理变化分析:A 项棉花属于纤维素,而羊毛属于蛋白质;B 项生产水泥的原料为石灰石和粘土,生产普通玻璃的原料为石灰石、石英和纯碱;C 项饱和硫酸铵溶液可以使蛋白质盐析,盐析可逆而变性不可逆;D 项煤的干馏为化学变化。