课程设计第四章缓冲溶液
- 格式:docx
- 大小:82.88 KB
- 文档页数:8







第四章1 基本要求 [TOP]缓冲溶液1.1 掌握缓冲溶液的概念、组成和作用机制;影响缓冲溶液 pH 的因素、Henderson-Hasselbalch 方程 式及应用;缓冲容量的概念、影响因素及有关计算。
1.2 熟悉缓冲溶液的配制原则、方法和步骤;血液中的主要缓冲系及其在稳定血液 pH 过程中的作用。
1.3 了解 医学上常用的缓冲溶液的配方和标准缓冲溶液的组成。
2 重点难点 [TOP]2.1 重点 缓冲溶液的概念、组成和缓冲作用的机理;影响缓冲溶液 pH 的因素及缓冲溶液 pH 的计算;缓冲溶 液的配制原则、方法和步骤;缓冲容量的概念及缓冲容量的有关计算。
2.2 难点 缓冲容量的概念及缓冲容量的有关计算。
3 讲授学时 建议 4 学时 4 内容提要 [TOP] 第一节 第二节 第三节 第四节 第五节 [TOP]4.1 第一节 缓冲溶液及缓冲机制 4.1.1 缓冲溶液及其作用机制 能够抵抗外来少量强酸、强碱,或在一定范围内稀释时,保持溶液 pH 基本不变的溶液称为缓冲溶 液。
其对溶液 pH 的稳定作用称为缓冲作用。
以足量 HAc 和 Ac 组成的缓冲溶液为例,缓冲溶液中存在同离子效应: HAc(aq)+H2O(l)+ -H3O (aq) + Ac (aq)+-加入少量强碱(OH )时,其接受 H3O 传递的质子,使平衡右移,溶液中大量存在的 HAc 解离以补充 被 OH 消耗掉的 H3O ,从而保持 pH 基本不变。
加入少量强酸(H3O )时,大量存在的 Ac 接受其传递的质子生成 HAc, 使平衡左移,因而[H3O ]无 明显增加,保持 pH 基本不变。
4.1.2 缓冲溶液的组成 缓冲溶液一般由足够浓度、一定比例的共轭酸碱对组成。
组成共轭酸碱对的两种物质称为缓冲系或1+ + +缓冲对,其中共轭酸起到抗碱作用,称为抗碱成分;共轭碱起到抗酸作用,称为抗酸成分。
4.2 第二节 缓冲溶液的 pH [TOP]4.2.1 缓冲溶液 pH 的近似计算公式 (一)基本公式——Henderson-Hasselbalch 方程式 在 HB-B 组成的缓冲溶液中,HB 和 B 之间存在如下质子转移平衡 HB(aq) + H2O(l) 由平衡可得+ [H3O ]=Ka × [ HB] [B− ] -H3O (aq) + B (aq)+-(4.1)− pH=pKa + lg [B ] =pKa + lg [共轭碱][ HB][共轭酸](4.2) 此式即计算缓冲溶液 pH 的 Henderson—Hasselbalch 方程式。

《缓冲溶液》教学设计范文《缓冲溶液》教学设计范文作为一名默默奉献的教育工作者,总归要编写教学设计,教学设计要遵循教学过程的基本规律,选择教学目标,以解决教什么的问题。
那么优秀的教学设计是什么样的呢?下面是小编收集整理的《缓冲溶液》教学设计范文,希望能够帮助到大家。
教学目标:通过缓冲溶液的`定义、作用、组成及作用机制的介绍,使学生对缓冲体系有一个基本的了解,为以后学习人体缓冲体系打下理论基础。
教学方式:多媒体结合板书进行讲解式教学。
教学内容:1、缓冲溶液的定义;2、缓冲溶液的作用;3、缓冲溶液的组成;4、缓冲溶液的作用机制。
教学重点及难点:缓冲溶液的组成、缓冲溶液的作用机制。
教学过程:引言:通过医学常识我们知道正常人的血液pH范围为7.35~7.45,pH 值不因代谢过程中产生酸、碱性物质而变化。
为什么血液的pH的范围能保持在7.35~7.45?知识准备:1.弱电解质的电离平衡。
2.盐类水解。
一、缓冲溶液的概念(由实验引出)缓冲溶液:能抵抗外加少量强酸或强碱,而维持pH基本不发生变化的溶液。
缓冲作用:缓冲溶液所具有的抵抗外加少量强酸或强碱的作用。
提问:1.缓冲溶液的组成是怎样的?2.缓冲溶液为什么能对抗外来少量强酸、强碱或适当稀释,而保持溶液的pH几乎不变的?二、缓冲溶液的组成和作用机制1.缓冲溶液的组成。
根据缓冲对不同,缓冲溶液分为三种:弱酸及其盐。
弱碱及其盐。
多元弱酸的酸式盐与其次级盐。
2.缓冲溶液的作用机制。
以HAc—NaAc为例,HAc、NaAc足量。
HAc+H23O++Ac-+左移3O+抗酸成分+抗碱成分右移-2H2O共轭酸—抗碱成分共轭碱—抗酸成分三、讨论:NH3—NH4Cl的缓冲原理。
四、练习:五、小结:概念:缓冲溶液。
缓冲溶液组成和缓冲作用。
缓冲原理。
六、作业:搜集资料:缓冲溶液在日常生活中的应用。

《缓冲溶液》微课程设计受生源影响,高职院校学生知识水平普遍偏低,大部分学生或缺乏良好的学习方法或对学习产生厌烦心理,传统教学效果较差。
因此,依托现代信息技术与网络平台,构建更为丰富实用的教学资源来提高教学效果显得尤为重要。
微课具有时间短、内容精、形式新、针对性强等特点,目前已成为国内外教学改革的热门手段,各种微课宣传、微课培训和微课赛事正在如火如荼地进行。
将微课引入传统教学课堂,可以显著提高教学效果。
本文以高职无机化学课程中“缓冲溶液”为内容设计微课,探索在传统化学教学中通过引入微课丰富教学资源,提高教学效果。
一、分析“缓冲溶液”教学内容选自高等院校“十二五”规划教材《无机化学》第七章第六节,共计1学时。
这一内容是高职药学专业学生无机化学学习的一个实用点,也与学生多门专业课程如药物化学、生物化学等相关联,因而是一个教学重点。
学生通过本章前五个小节的内容(解质溶液理论、水的解离、酸碱质子理论、弱电解质的电离平衡、溶液的酸碱性和pH)的学习,已具备了一定的理论基础。
但长时间的传统理论教学让学生感觉枯燥乏味,注意力下降。
要想激发学生兴趣,提高教学效果,就必须改进课堂教学方法,基于以上思考,笔者尝试利用微课进行视频教学。
二、设计根据《无机化学》课程培养方案,结合药学专业人才培养方案,笔者制定了如下目标:(1)掌握缓冲溶液的概念和组成。
(2)会用缓冲溶液的工作原理解释人体pH保持稳定的原因。
(3)了解缓冲溶液的应用。
为了帮助学生顺利达成目标,笔者设计了“课前预习任务单”,它由以下三个部分组成:(1)基础理论学习。
学生自主学习书本内容,能基本了解缓冲溶液的概念和组成,了解缓冲溶液的应用。
(2)应用拓展学习。
教师上传“血液中缓冲溶液的工作原理”学习视频至QQ群,学生下载观看,了解血液中缓冲溶液的工作原理,拓展知识面。
(3)重点难点记录。
学生记录自主学习过程中遇到的各种问题,以便课堂上重点学习。
三、制作笔者制作了微课视频帮助学生顺利完成学习任务。

中医学院《医用化学》课程设计(首页)课程名称:医用化学任课教师:职称:所在系部:医学技术系教研室:化学教研室授课对象:医学影像授课时间:课程类型:必修基础课授课章节:第四章缓冲溶液基本教材:祖期主编《基础化学》第八版, 人民卫生,2013年3月。
自学资源:1、《无机化学》许善锦主编,人民卫生.2、《基础化学》第五版.祖期主编,人民卫生.3、《基础化学》徐春祥主编,高等教育.4、《现代化学基础》朱裕贞主编,化学工业.5、《现代化学基础》胡忠鲠主编,高等教育.教学目标:(一)知识目标:1. 掌握缓冲溶液的概念、组成和作用机制;影响缓冲溶液pH的因素、Henderson-Hasselbalch方程式及应用;缓冲容量的概念、影响因素及有关计算。
2. 熟悉缓冲溶液的配制原则、方法和步骤;血液中的主要缓冲系及其在稳定血液pH过程中的作用。
3. 了解医学上常用的缓冲溶液的配方和标准缓冲溶液的组成。
(二)能力目标:通过本章节的学习,使学生初步掌握缓冲溶液的组成、缓冲溶液的缓冲机理、缓冲溶液的配制方法、缓冲溶液PH值的计算、缓冲围、影响缓冲容量的因素以及缓冲溶液在医学上的应用等等,培养学生独立的分析问题和解决问题能力。
(三)情感目标通过缓冲溶液的学习,学生特点分析:本课程针对临床专业大一学生开设,学生在中学阶段选修课程部分容不讲解,知识结构不系统,在讲解时要精讲,并结合临床专业的实例,调动学生的积极性,培养他们学习化学课程的兴趣。
教学重点:1.缓冲溶液的概念、组成和缓冲作用的机理;影响缓冲溶液pH的因素及缓冲溶液pH的计算;缓冲溶液的配制原则、方法和步骤;缓冲容量的概念及缓冲容量的有关计算。
教学难点:1.缓冲容量的概念及缓冲容量的有关计算。
2.缓冲对的选择。
解决方法和处理措施:1. 通过实验教学设置相关的实验容,让学生首先了解缓冲容量的概念和影响缓冲容量的因素,然后通过结合实验结果讲述这些因素对缓冲容量的影响情况,并且引出如何计算缓冲容量。
《缓冲溶液》教案教案标题:缓冲溶液教案目标:1.理解缓冲溶液的概念和作用。
2.学习如何制备和调节缓冲溶液。
3.掌握缓冲溶液的pH值计算和调节方法。
教学重点:1.缓冲溶液的定义和作用。
2.缓冲溶液的制备方法。
3.缓冲溶液的pH值计算和调节方法。
教学难点:1.缓冲溶液的pH值计算和调节方法。
2.学生对缓冲溶液的理解和应用能力。
教学准备:1.学生用品:笔、纸、计算器。
2.教师用品:课件、实验仪器设备。
教学过程:一、导入(15分钟)1.教师简要介绍缓冲溶液的概念和作用,并向学生提问:你们对缓冲溶液了解多少?它有什么作用?2.学生回答后,教师对其回答进行点评和补充,并引导学生思考缓冲溶液的重要性。
二、缓冲溶液的定义和作用(15分钟)1.教师通过投影课件,详细讲解缓冲溶液的定义和作用,并强调其在生物和化学领域的重要性。
2.教师通过具体例子和实验现象,解释缓冲溶液能够稳定溶液的pH 值,并避免溶液中pH值的剧烈变化。
三、缓冲溶液的制备方法(20分钟)1.教师介绍常用的制备缓冲溶液的方法,如添加弱酸和其盐或弱碱和其盐等。
2.教师进行实验演示,展示如何制备缓冲溶液,包括实验装置和步骤。
3.学生根据所学内容和实验演示,讨论并总结缓冲溶液的制备方法,并与教师进行互动。
四、缓冲溶液的pH值计算和调节方法(30分钟)1.教师简要介绍缓冲溶液的pH值计算方法,包括弱酸和弱碱的离解常数的计算,并通过例题进行演示。
2.学生进行小组讨论,共同解决几道缓冲溶液的pH值计算题目,并与教师进行互动。
3.教师介绍如何调节缓冲溶液的pH值,包括添加弱酸或弱碱,以及调节其浓度等方法。
五、拓展练习(10分钟)1.学生进行个人练习,完成教师提供的缓冲溶液计算题目,并检查答案。
2.学生互相交流讨论,对有疑问的问题进行解答和讨论。
六、总结和归纳(10分钟)1.教师对本节课的内容进行总结和归纳,强调重要知识点。
2.学生进行自我总结并提出问题,教师进行解答和指导。
第二节缓冲溶液复习目标1、掌握缓冲溶液的概念及组成2、理解缓冲溶液的作用原理3、掌握影响缓冲容量大小的因素及缓冲溶液的缓冲范围4、了解有关缓冲溶液pH的计算5、了解缓冲溶液的选择原则复习过程1、缓冲溶液具有作用,在反应生成或外加少量的强酸强碱后,也能保持溶液的基本不变。
2、缓冲溶液的组成(1)(2)(3)3、对于弱酸及其盐组成的缓冲溶液,pH= ;对于弱碱及其盐组成的缓冲溶液,pH= ;两性化合物组成的缓冲溶液,pH= 。
4、衡量缓冲溶液缓冲能力大小的是,其大小与有关。
5、酸式缓冲溶液缓冲范围的公式:;碱式缓冲溶液缓冲范围的公式:6、根据布朗斯太特的酸碱质子理论,酸是能给出质子(H+)的物质,碱是能接受质子的物质。
一种碱(B),接受质子后其生成物(HB+)便成为酸;同理,一种酸给出质子后余下部分便为碱。
酸与碱的这种关系可表示如下:B+ H+HB+(碱)(酸)可见,酸与碱彼此是不可分开的,具有相互依存的关系。
HB+- B称为共轭酸碱对。
共轭酸碱之间,彼此只相差一个质子。
7、缓冲溶液的选择原则是什么?【随堂练习】1、根据酸碱质子理论,找出下列反应中的酸和碱。
HAc H++Ac-NH4+H+NH3H2PO4—H++ HPO42—HPO42—H++ PO43—2、下列各组溶液不是缓冲溶液的是()A.NaH2PO4- Na2HPO4混合液B.0.2mol/L NH4Cl与0.1mol/LNaOH等体积混合液C.0.1mol/LNaOH与0.1mol/L HAc等体积混合液D.NH4Cl- NH3.H2O3、H2PO4-的共轭碱是()A.H3PO4B.HPO42-C.PO43-D.OH-4、下列各组物质,哪些可以用来制备缓冲溶液?⑴ HCL—NaCL ⑵HAc—NaOH ⑶ NH3—HCL ⑷ H2PO4—NaH2PO4⑸ H2CO3—NaHCO3⑹ NH3.H2O—NH4Cl5、根据缓冲溶液的选择原则,判断下列三种酸可以用来配制PH=3的缓冲溶液?HCOOH Ka=1.7×10-4HAC Ka=1.8×10-5CLCH2COOH Ka=1.4×10-36、以HAc-NaAc为例说明缓冲溶液的缓冲原理。
陕西中医学院《医用化学》课程设计(首页)
课程名称:医用化学任课教师:职称:
所在系部:医学技术系教研室:化学教研室
授课对象:医学影像授课时间:
课程类型:必修基础课
授课章节:第四章缓冲溶液
基本教材:魏祖期主编《基础化学》第八版, 人民卫生出版社,2013年3月。
自学资源:
1、《无机化学》许善锦主编,人民卫生出版社.
2、《基础化学》第五版.魏祖期主编,人民卫生出版社.
3、《基础化学》徐春祥主编,高等教育出版社.
4、《现代化学基础》朱裕贞主编,化学工业出版社.
5、《现代化学基础》胡忠鲠主编,高等教育出版社.
教学目标:
(一)知识目标:
1. 掌握缓冲溶液的概念、组成和作用机制;影响缓冲溶液pH的因素、Henderson-Hasselbalch方程式及应用;缓冲容量的概念、影响因素及有关计算。
2. 熟悉缓冲溶液的配制原则、方法和步骤;血液中的主要缓冲系及其在稳定血液pH过程中的作用。
3. 了解医学上常用的缓冲溶液的配方和标准缓冲溶液的组成。
(二)能力目标:
通过本章节的学习,使学生初步掌握缓冲溶液的组成、缓冲溶液的缓冲机理、缓冲溶液的配制方法、缓冲溶液PH值的计算、缓冲范围、影响缓冲容量的因素以及缓冲溶液在医学上的应用等等,培养学生独立的分析问题和解决问题能力。
(三)情感目标
通过缓冲溶液的学习,
学生特点分析:
本课程针对临床专业大一学生开设,学生在中学阶段选修课程部分内容不讲解,知识结构不系统,在讲解时要精讲,并结合临床专业的实例,调动学生的积极性,培养他们学习化学课程的兴趣。
教学重点:
1.缓冲溶液的概念、组成和缓冲作用的机理;影响缓冲溶液pH的因素及缓冲溶液pH的计算;缓冲溶液的配制原则、方法和步骤;缓冲容量的概念及缓冲容量的有关计算。
教学难点:
1.缓冲容量的概念及缓冲容量的有关计算。
2.缓冲对的选择。
解决方法和处理措施:
1. 通过实验教学设置相关的实验内容,让学生首先了解缓冲容量的概念和影响缓冲容量的因素,然后通过结合实验结果讲述这些因素对缓冲容量的影响情况,并且引出如何计算缓冲容量。
2. 通过医学上的实例说明所选择的缓冲对,然后通过计算得出缓冲溶液的PH值,再说明决定缓冲溶液PH值的因素,进而指出如何选择缓冲对。
教学内容与教学活动:
本章内容知识点多,过程中可以采用多种教学活动,比如人体中的重要缓冲系、人体如何通过呼吸调节自身PH值基本恒定不变,小孩为什么消化能力比成人差等等,均可以采用设问,然后通过平衡的移动等来进行解释。
增强学生通过化学原理来解释一些现实问题的能力,培养他们解决问题的能力。
教学媒体的选择和使用方法:
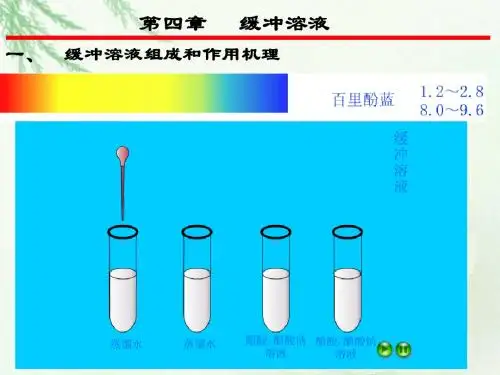
通过动画展示向加有酚酞的NaAc溶液和NaAc-HAc溶液中加入氢氧化钠溶液,溶液颜色的深浅差异,说明这两种溶液性质上的差异,通过讲解引出NaAc-HAc溶液具有缓冲作用,同时可以调动学生的学习积极性。
教学反思与评价:
基本概念学生易接受,但是缓冲对的选择是难点,应该重点从缓冲溶液PH 值的计算公式入手,重点讲解影响缓冲溶液PH的主要因素为缓冲对中的共轭算的,因此总结出确定缓冲对的首要问题是依据所需要的PH,选择最接近的此PH 的Ka共轭酸,随之算的共轭碱也确定,缓冲对随之确定。
然后通过举例进行加强,可获得较好的教学效果。
板书设计和课件:
本课程采用自制的多媒体课件,通过大量的图片进行感官刺激,达到增强学生记忆公示的目的。
板书设计如下:
第四章缓冲溶液
第一节缓冲溶液及缓冲机制
一、缓冲溶液
二、缓冲机制
四、缓冲溶液的组成
第三节缓冲容量和缓冲范围
一、缓冲容量β =
dpH d
)b(a
V
n
二、影响缓冲容量的因素β=2.303×[HB][B-]/c总
三、有效缓冲范围 PH=PKa±1
第四节缓冲溶液的配制
二、标准缓冲溶液
第五节血液中的缓冲系
教学改革:
1.
2.
陕西中医学院《医用化学》课程设计(续页)。