电解精炼铜电镀ppt课件
- 格式:ppt
- 大小:1.11 MB
- 文档页数:41





1.2.3 电解原理的应用——电解精炼铜、电镀课型:新授课主备人:李琴审核人:万社娟韩守霞学习目标:学会运用电解的原理分析铜的电解精炼;通过学习电镀的内容,了解具有一定特殊性的、另一种电解原理的应用方法,并进一步体会电解对人类社会的重要贡献。
重点难点:铜的电解精炼和电镀的原理旧知链接:1.离子放电顺序:常见阳离子放电顺序为:常见阴离子放电顺序为:2. 写出用惰性电极电解下列溶液的电极反应式:①CuCl2②H2SO4③ CuSO4①阳极:阴极:②阳极:阴极:③阳极:阴极:预习检测:1、铜的电解精炼:粗铜中含Fe、Zn、Ni、Ag、Pt、Au等少量杂质金属,下图为电解法精炼铜的装置。
其中阳极为,阴极为,电解质溶液为。
(并标在图上)阳极发生的主要反应为:(杂质Fe、Zn、Ni也发生电极反应:由于Pt、Ag、Au的金属性比Cu弱且量又少,这三种金属不反应,以单质的形式沉积在底部,得到阳极泥)。
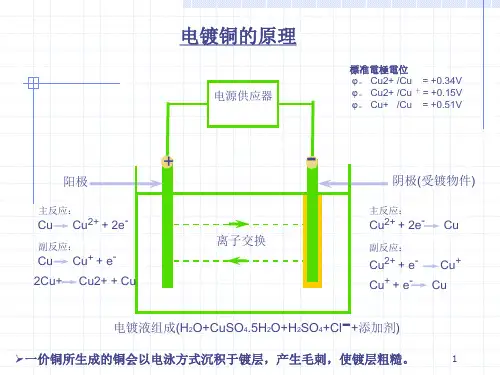
阴极的反应为分析电解精炼过程中电解质溶液的变化:总结:阳极:电解精炼装置的构成阴极:电解质溶液:2、电镀阅读教材,设计试验,在铁制品上镀铜(教材第17页“活动·探究)。
要求:画出电镀铜的实验装置图,指出电极材料和电解质溶液,写出电极反应式。
总结:(1)电镀:阳极:(2)电镀池的构成阴极:电镀液:交流·研讨:1.下列叙述中不正确的是()A.电解池的阳极上发生氧化反应,阴极上发生还原反应B.不能自发进行的氧化还原反应可通过电解的原理实现C.电镀时,电镀池里的阳极材料发生氧化反应D.电解饱和食盐水时,阳极得到氢氧化钠溶液和氢气2.金属镍有广泛的用途。
粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(氧化性Fe2+<Ni2+<Cu2+)( )A.阳极发生还原反应,其电极反应式:Ni2++2e-→NiB.电解过程中,阳极质量的减少与阴极质量的增加相等C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+D.电解后,电解槽底部的阳极泥中只有Cu和Pt3、下列关于铜电极的叙述正确的是( )A、铜锌原电池中铜是负极B、用电解法精炼铜时纯铜作阳极C、在镀件上电镀铜时可用金属铜作阳极D、电解稀硫酸制H2、O2时铜作阳极4、将分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联 , 在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为( )A 、1∶2∶3B 、3∶2∶1C 、6∶3∶1D 、6∶3∶25.电解原理在化学工业中有广泛应用。



