摩尔气体常数的测定PPT课件
- 格式:ppt
- 大小:4.57 MB
- 文档页数:8


实验十六摩尔气体常数的测定一、实验目的1、了解分析天平的结构、计量性能,学习并掌握直接称量法;2、学习测量气体体积的操作:装置的安装、检漏、量气管液面的观察与读数;3、学习气体分压的概念;4、学习误差的表示、数据的取舍、有效数字及其应用规划5、学习用洗液洗涤特殊仪器。
二、预习内容电子天平的使用及称量方法⑴使用步骤端坐在天平前,放置干燥器、烧杯等物的搪瓷盘放在天平的左边,实验报告本等放在天平的右边。
查看天平水平仪,气泡是否在黑圈内,如不在黑圈内表示天平不水平,要通过水平调节脚调至水平。
接通电源,预热60分钟后方可开启显示器进行操作使用。
称量前要用标准砝码校正天平。
轻按ON显示器键,等出现0.0000g称量模式后方可称量。
将称量物轻放在称盘上,关严天平门,这时显示器上数字不断变化,待数字稳定并出现质量单位g后,即可读数,并记录称量结果。
称量结束后,取出称量物,按关闭键OFF。
检查天平内清洁与否,如有试样洒落,一定要打扫干净。
关上天平门,罩好布罩,填写登记卡。
⑵称量方法直接称量法:对一些在空气中无吸湿性的试样或试剂,如金属或合金等可用直接法称量。
称量时将试样放在干净而干燥的小表面皿上或油光纸上,一次称取一定质量的试样。
先称出干燥洁净的表面皿或油光纸的质量,按去皮键TAR,显示“0.0000”后,打开天平门,缓缓往表面皿中加入试样,当达到所需质量时停止加样,关上天平门,显示平衡后即可记录所称试样的净质量。
差减称量法:如果试样是粉末或易吸湿的物质,则需把试样装在称量瓶内称量。
倒出一份试样前后两次质量之差,即为该份试样的质量。
称量时,用纸条叠成宽度适中的两三层纸带,毛边朝下套在称量瓶上。
左手拇指与食指拿住纸条,由天平的左门放在天平左盘的正中,取下纸带,称出瓶和试样的质量。
然后左手仍用纸带把称量瓶从盘上取下,放在容器上方。
右手用另一小纸片衬垫打开瓶盖,但勿使瓶盖离开容器上方。
慢慢倾斜瓶身至接近水平,瓶底略低于瓶口,切勿使瓶底高于瓶口,以防试样冲出。

实验6摩尔气体常数的测定
摩尔气体常数(Molar Gas Constant)是为了表示一单位物质的构成,它是物质在单位体积下所拥有的分子总数。
它是摩尔定律(Avogadro's Law)的重要化学常数,也是进行化学变化计算时必须用到的常数。
实验6摩尔气体常数的测定是一种用于测量摩尔气体常数的实验过程,概括起来就是将气体和液体注入烧瓶,并再用大气压力恢复其体积,最后通过量来测定所得结果。
实验室准备:
主要仪器:烧瓶、密封弹簧、检测仪、稀释液、烧杯和金属支架等。
实验步骤:
(1)将空烧瓶安装支架,并用密封弹簧紧固;
(2)将烧杯中含有固体的有机物质溶解在液体中,当液体完全溶解时,倒入烧瓶,放入烧杯;
(3)把烧瓶装到恒温水槽中,恒温60℃,维持烧瓶温度;
(4)将检测仪中的游标拨至“读数”位置,用检测仪测量烧瓶中的压力;
(6)把检测仪中的游标拨至“溶液”位置,采用由大气压力恢复的方法,夹住烧瓶和烧杯,让溶液直至完全挥发;
(8)根据上述所获数据进行计算,推导出摩尔气体常数的值。
数据计算:
计算公式:n=PV/RT
其中,n表示摩尔气体常数,P表示收缩压力(单位:atm),V表示体积(单位:litre),R表示气体常数(单位:atm. litre/mole.K),T表示温度(单位:K)。
实验结果:
根据上述计算公式,计算出所得摩尔气体常数为:n = xxx。
结论:
通过实验6摩尔气体常数的测定,我们可以测得这一化学常数的实际值,从而了解物质在特定温度下拥有多少分子,有助于对物质进行计算和模拟,从而获得更好的化学实验效果。

摩尔⽓体常数的测定实验⼗六摩尔⽓体常数的测定⼀、实验⽬的1、了解分析天平的结构、计量性能,学习并掌握直接称量法;2、学习测量⽓体体积的操作:装置的安装、检漏、量⽓管液⾯的观察与读数;3、学习⽓体分压的概念;4、学习误差的表⽰、数据的取舍、有效数字及其应⽤规划5、学习⽤洗液洗涤特殊仪器。
⼆、预习内容电⼦天平的使⽤及称量⽅法⑴使⽤步骤端坐在天平前,放置⼲燥器、烧杯等物的搪瓷盘放在天平的左边,实验报告本等放在天平的右边。
查看天平⽔平仪,⽓泡是否在⿊圈内,如不在⿊圈内表⽰天平不⽔平,要通过⽔平调节脚调⾄⽔平。
接通电源,预热60 分钟后⽅可开启显⽰器进⾏操作使⽤。
称量前要⽤标准砝码校正天平。
轻按ON显⽰器键,等出现O.OOOOg称量模式后⽅可称量。
将称量物轻放在称盘上,关严天平门,这时显⽰器上数字不断变化,待数字稳定并出现质量单位g后,即可读数,并记录称量结果。
称量结束后,取出称量物,按关闭键OFF检查天平内清洁与否,如有试样洒落,⼀定要打扫⼲净。
关上天平门,罩好布罩,填写登记卡。
⑵称量⽅法直接称量法:对⼀些在空⽓中⽆吸湿性的试样或试剂,如⾦属或合⾦等可⽤直接法称量。
称量时将试样放在⼲净⽽⼲燥的⼩表⾯⽫上或油光纸上,⼀次称取⼀定质量的试样。
先称出⼲燥洁净的表⾯⽫或油光纸的质量,按去⽪键TAR显⽰“0.0000 ”后,打开天平门,缓缓往表⾯⽫中加⼊试样,当达到所需质量时停⽌加样,关上天平门,显⽰平衡后即可记录所称试样的净质量。
差减称量法:如果试样是粉末或易吸湿的物质,则需把试样装在称量瓶内称量。
倒出⼀份试样前后两次质量之差,即为该份试样的质量。
称量时,⽤纸条叠成宽度适中的两三层纸带,⽑边朝下套在称量瓶上。
左⼿拇指与⾷指拿住纸条,由天平的左门放在天平左盘的正中,取下纸带,称出瓶和试样的质量。
然后左⼿仍⽤纸带把称量瓶从盘上取下,放在容器上⽅。
右⼿⽤另⼀⼩纸⽚衬垫打开瓶盖,但勿使瓶盖离开容器上⽅。
慢慢倾斜瓶⾝⾄接近⽔平,瓶底略低于瓶⼝,切勿使瓶底⾼于瓶⼝,以防试样冲出。

学校教案
(首页)
课程名称物理化学审阅签名
授课班级授课形式实验
授课内容摩尔气体常数的测定
授课时间20 年月日∕第周星期∕第 1 ~ 4 节( 4 学时)
实验目的1、掌握理想气体状态方程及分压定律的应用
2、了解摩尔气体常数的测定方法
教学重点掌握理想气体状态方程的应用
教学难点实验的具体步骤
作业实验报告
课时分配组织教学10分钟+ 讲授40分钟+ 巡回指导120分钟+ 小结10分钟
课前准备内容
仪器
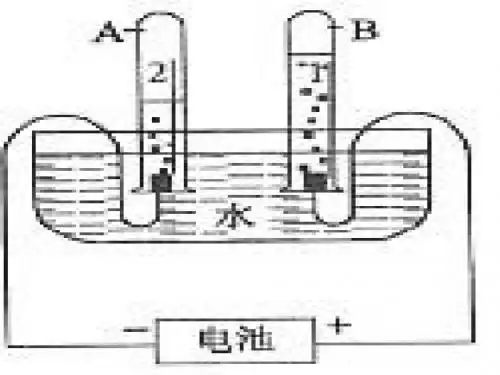
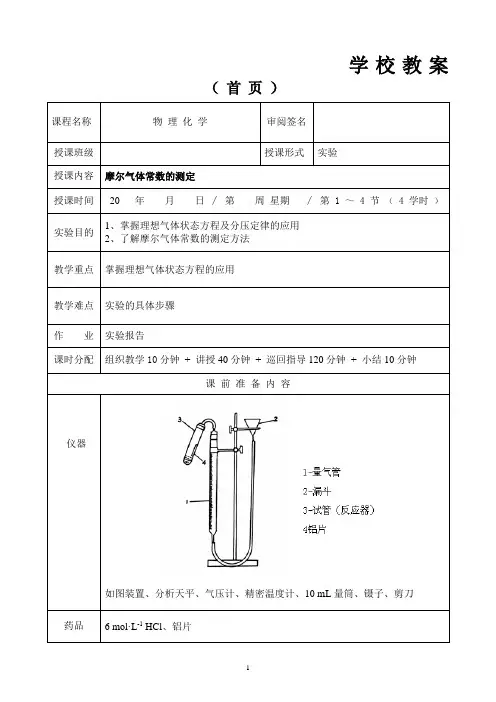
如图装置、分析天平、气压计、精密温度计、10 mL量筒、镊子、剪刀药品 6 mol·L-1 HCl、铝片
(续页)第2页
4。




实验十六摩尔气体常数的测定一、实验目的1、了解分析天平的结构、计量性能,学习并掌握直接称量法;2、学习测量气体体积的操作:装置的安装、检漏、量气管液面的观察与读数;3、学习气体分压的概念;4、学习误差的表示、数据的取舍、有效数字及其应用规划5、学习用洗液洗涤特殊仪器。
二、预习内容电子天平的使用及称量方法⑴使用步骤端坐在天平前,放置干燥器、烧杯等物的搪瓷盘放在天平的左边,实验报告本等放在天平的右边。
查看天平水平仪,气泡是否在黑圈内,如不在黑圈内表示天平不水平,要通过水平调节脚调至水平。
接通电源,预热60分钟后方可开启显示器进行操作使用。
称量前要用标准砝码校正天平。
轻按ON显示器键,等出现0.0000g称量模式后方可称量。
将称量物轻放在称盘上,关严天平门,这时显示器上数字不断变化,待数字稳定并出现质量单位g后,即可读数,并记录称量结果。
称量结束后,取出称量物,按关闭键OFF。
检查天平内清洁与否,如有试样洒落,一定要打扫干净。
关上天平门,罩好布罩,填写登记卡。
⑵称量方法直接称量法:对一些在空气中无吸湿性的试样或试剂,如金属或合金等可用直接法称量。
称量时将试样放在干净而干燥的小表面皿上或油光纸上,一次称取一定质量的试样。
先称出干燥洁净的表面皿或油光纸的质量,按去皮键TAR,显示“0.0000”后,打开天平门,缓缓往表面皿中加入试样,当达到所需质量时停止加样,关上天平门,显示平衡后即可记录所称试样的净质量。
差减称量法:如果试样是粉末或易吸湿的物质,则需把试样装在称量瓶内称量。
倒出一份试样前后两次质量之差,即为该份试样的质量。
称量时,用纸条叠成宽度适中的两三层纸带,毛边朝下套在称量瓶上。
左手拇指与食指拿住纸条,由天平的左门放在天平左盘的正中,取下纸带,称出瓶和试样的质量。
然后左手仍用纸带把称量瓶从盘上取下,放在容器上方。
右手用另一小纸片衬垫打开瓶盖,但勿使瓶盖离开容器上方。
慢慢倾斜瓶身至接近水平,瓶底略低于瓶口,切勿使瓶底高于瓶口,以防试样冲出。