青蒿琥脂片溶出度测定的方法学验证
- 格式:doc
- 大小:34.50 KB
- 文档页数:5

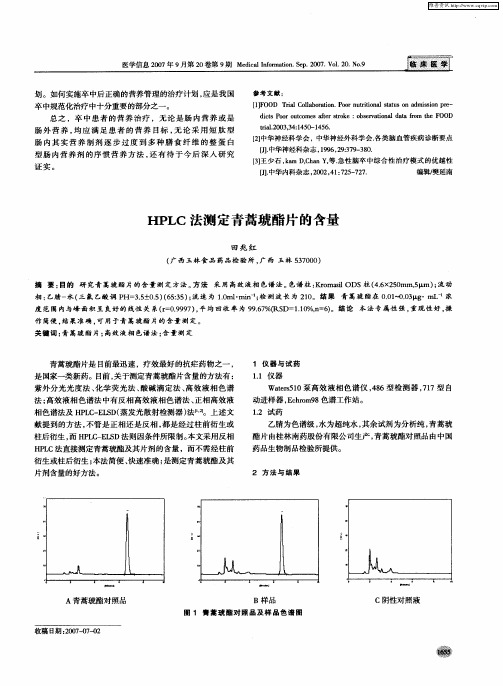

青蒿琥酯及注射用青蒿琥酯中有关物质的HPLC测定
谢蓓
【期刊名称】《中国医药工业杂志》
【年(卷),期】2004(35)9
【摘要】建立了反相高效液相色谱法测定青蒿琥酯及注射用青蒿琥酯中杂质二氢青蒿素及其它有关物质。
采用KromasilC18色谱柱,以乙腈-磷酸盐缓冲液(pH 3.0)(1∶1)为流动相,流速0.8ml/min,检测波长210nm。
二氢青蒿素在6~
60mg/ml浓度范围内,线性关系良好(r=0.9999)。
稳定性试验结果显示,样品溶液配制后须立即进样。
【总页数】3页(P540-542)
【关键词】青蒿琥酯;二氢青蒿素;有关物质;高效液相色谱;测定
【作者】谢蓓
【作者单位】上海第二医科大学附属瑞金医院卢湾分院药剂科
【正文语种】中文
【中图分类】TQ460.72;O657.72
【相关文献】
1.HPLC法测定中国白酒中的γ-氨基丁酸和核苷类物质 [J], 郭莹;李景辉;李霄霄;李研科;王国明;尹翠娟;张翠英
2.右美托咪定有关物质测定中HPLC法盐酸测定的应用及其临床价值探讨 [J], 徐栋鸿;曹伊郦;章艳
3.高效液相色谱法测定青蒿琥酯中的有关物质 [J], 刘向红;何虹;卢日刚;甘盛
4.RP-HPLC法定量测定呱西替柳中水杨酸愈创木酚酯和其有关物质HPLC-MS鉴别研究 [J], 孙国祥;丁楠;宋宇晴;王真;宋良伟
5.HPLC与荧光分光光度计联机测定尿中儿茶酚胺类物质在嗜铬细胞瘤诊断中的应用 [J], 杨世杰;张伟;岳海涛;石育原;李胜文;鲁学军;陈光荣;安伟奇;李毅
因版权原因,仅展示原文概要,查看原文内容请购买。

RP-HPLC法测定青蒿琥酯阿莫地喹片中主药的含量胡志强;蒋锋;姚忠【摘要】A method for the determination of artesunate and amodiaquine hydrochloride tablets by RP-HPLC was established.The agilent C18(4.6 mm×15 cm)column was used,and the detection wavelength of artesunate was 210 nm.The mobile phase of artesunate was acetonitrile and the buffer solution.The detection wavelength of amodiaquine hydrochloride was 224 nm.The mobile phase of amodiaquine hydrochloride wasmethanol:phosphate buffer.The linear ranges of artesu-nate (0.500 5-2.002 mg/mL)and amodiaquine hydrochloride (25.03-100.1μg/mL)were good (r=0.999)with the average recovery rates of 98.6%and 99.5%.The method is simple and accurate,and it can be used for the determination of artesunate and amodiaquine hydrochloride tablets.%建立RP-HPLC法测定青蒿琥酯阿莫地喹片中主药的含量。
色谱柱为安捷伦的C18柱(4.6 mm×15 cm),测定青蒿琥酯的流动相为乙腈-磷酸盐缓冲液,检测波长为210 nm,测定阿莫地喹的流动相为甲醇-磷酸盐缓冲液,检测波长为224 nm。

高效液相色谱法NIFDC—PT—099对注射用青蒿琥酯含量测定能力验证结果与讨论目的探讨NIFDC-PT-099注射用青蒿琥酯含量测定能力验证方法和结果。
方法按照《中国药典》2015年版二部593页注射用青蒿琥酯[含量测定]项下方法进行测定。
结果编号为QA0099-0011的NIFDC-PT-099注射用青蒿琥酯含量测定能力验证样品测定结果为101.20%,指定值为101.32%,能力验证标准差为0.433,Z比分数-0.27,其中|Z|≤2为满意结果。
结论测定结果满意。
该实验室具有很好的液相色谱测定能力。
标签:注射用青蒿琥酯;含量测定;能力验证[Abstract] Objective This paper tries to investigate the ability verification method and results of NIFDC-PT-099 Determination of artesunate for injection. Methods In accordance with the “Chinese Pharmacopoeia” 2015,version two,page 593,injection of artesunate[assessment] measured under the method. Results The NIFDC-PT-099 Determination of Injectable Artesunate Content numbered QA0099-0011 demonstrated a test result of 101.20%,a specified value of 101.32%,a standard deviation of proficiency test of 0.433,and a Z-score of -0.27. |Z|≤2 was a satisfactory result. Conclusion The test results is satisfactory. The laboratory has a good liquid chromatography determination capability.[Key words] Artesunate for injection;Content determination;Proficiency testingNIFDC-PT-099注射用青蒿琥酯含量測定能力验证计划是由中国食品药品检定研究院组织、广西壮族自治区食品药品检验所实施的能力验证计划[1]。

青蒿琥酯纳米乳中青蒿琥酯的分光光度法和HPLC法分析李均亮;李冰;周绪正;张继瑜【期刊名称】《湖北农业科学》【年(卷),期】2012(51)8【摘要】比较了HPLC法和紫外分光光度法测定青蒿琥酯的含量,HPLC法和紫外分光光度法的线性范围分别为5~50μg/mL (R2=0.9992)和5~100 μg/mL(R2=0.9967),两种方法的分析结果无明显差异,表明这两种方法可较为准确地测定青蒿琥酯纳米乳中青蒿琥酯的含量,其中紫外分光光度法的操作简单,适合分析杂质含量低的样品,而HPLC法分辨率高,适用于成分复杂青蒿琥酯制剂的检测.%The comparison of HPLC and spectrophotometry methods for detecting artesunate was carried out. The results showed that the linear rang of artemisinin was 5~50 μg/mL (,R2=0.999 2) in HPLC, and 5~100μg/mL (R2=0.996 7) in spectrophotometry. Both methods for determining the content in artesunate in artesunate-nanoemulsion showed no significant difference. Spectrophotometry was suitable for the detection of sample with low impurity, HPLC was used for complex sample.【总页数】3页(P1678-1680)【作者】李均亮;李冰;周绪正;张继瑜【作者单位】中国农业科学院兰州畜牧与兽药研究所/农业部兽用药物创制重点实验室/甘肃省新兽药工程重点实验室,兰州730050;中国农业科学院兰州畜牧与兽药研究所/农业部兽用药物创制重点实验室/甘肃省新兽药工程重点实验室,兰州730050;中国农业科学院兰州畜牧与兽药研究所/农业部兽用药物创制重点实验室/甘肃省新兽药工程重点实验室,兰州730050;中国农业科学院兰州畜牧与兽药研究所/农业部兽用药物创制重点实验室/甘肃省新兽药工程重点实验室,兰州730050【正文语种】中文【中图分类】O657.33;O657.7【相关文献】1.RP-HPLC法测定青蒿琥酯阿莫地喹片中主药的含量 [J], 胡志强;蒋锋;姚忠2.青蒿琥酯白蛋白纳米粒的制备及抗肿瘤活性初步研究 [J], 程瑶;孟岩;郑岩;金迪;赵亮3.HPLC法测定青蒿琥酯阿莫地喹片中青蒿琥酯的含量 [J], 蒋红艳;曾雪;陈义娟4.HPLC法测定青蒿琥酯片的含量 [J], 田兆红5.青蒿琥酯纳米结构脂质载体的处方设计、优化与质量评价 [J], 方宁因版权原因,仅展示原文概要,查看原文内容请购买。
验证编码:RR-QC-QHHZWJFRJXYJ -2012-01 桂林南药股份有限公司青蒿琥酯无菌粉溶解性研究报告目录1.研究报告审批表2.目的3.相关人员4.相关文件5.使用仪器及校验期6.试剂7.人员培训8.检验方法及结果判定9.检验结果10.偏差及漏项说明11.结论1.研究报告审批表2. 目的因青蒿琥酯无菌粉的处方工艺变更,参考《溶解性指导原则》,对处方工艺的变更前后各3个批号的青蒿琥酯无菌粉进行溶解性试验研究,以考察该药物在一般溶剂和不同PH缓冲液中的溶解性。
3.相关人员5. 使用仪器及校验期8.检测方法及结果判定8.1 试验法:除另有规定外,称取研成细粉的供试品或量取液体供试品,于20℃一定容量的溶剂(在生理pH范围(pH1.2~6.8)内温度为37±0.5℃),每隔5分钟强力振摇30秒钟;观察30分钟内的溶解情况,如无目视可见的溶质颗粒或液滴时,即视为完全溶解。
8.2药品的溶解性特征描述与界定极易溶解系指溶质1g(ml)能在溶剂不到1ml中溶解;易溶系指溶质1g(ml)能在溶剂1~不到10ml中溶解;溶解系指溶质1g(ml)能在溶剂10~不到30ml中溶解;略溶系指溶质1g(ml)能在溶剂30~不到100ml中溶解;微溶系指溶质1g(ml)能在溶剂100~不到1000ml中溶解;极微溶解系指溶质1g(ml)能在溶剂1000~不到10000ml中溶解;几乎不溶或不溶系指溶质1g(ml)能在溶剂10000ml中不能完全溶解。
9.检验结果表1. 变更前3批青蒿琥酯无菌粉(批号:W A120701 、W A120702、W A120703)在一般溶剂中的溶解度检验结果(20℃)表2. 变更后3批青蒿琥酯无菌粉(批号:W A20120901 、W A20121001、W A20121002)在一般溶剂中的溶解度检验结果(20℃)表3. 变更前3批青蒿琥酯无菌粉(批号:W A120701 、W A120702、W A120703)在不同的pH缓冲液中的溶解度检验结果(37±0.5℃)表4. 变更后3批青蒿琥酯无菌粉批号:W A20120901 、W A20121001、W A20121002)在不同的pH缓冲液中的溶解度检验结果(37±0.5℃)10.偏差及漏项说明无偏差及漏项11.结论根据《药物溶解性试验指导原则》,检测工艺变更前后各3批青蒿琥酯无菌粉,可知,青蒿琥酯无菌粉在丙酮、二氯甲烷、乙醇、甲醇、乙酸乙酯、三氯甲烷、5%碳酸氢钠溶液中易溶,在水中极微溶解;在强酸性缓冲液中极微溶解,在弱酸性缓冲液中微溶。
青蒿琥酯片中乙醇溶剂残留的液固顶空气相色谱法测定
潘勇;唐庆华
【期刊名称】《生命科学仪器》
【年(卷),期】2009(007)005
【摘要】建立液固顶空气相色谱法分析青蒿琥酯片中乙醇溶剂残留.采用DB-1大口径毛细管柱,以正丙醇为内标进行定量.乙醇的线性范围为556~4448μg-mL-
1(r=0.9997),回收率为100.4%,RSD为0.79%.本方法简单、准确、灵敏度高、重现性好.
【总页数】3页(P35-37)
【作者】潘勇;唐庆华
【作者单位】广西桂林南药股份有限公司,桂林,541002;广西桂林南药股份有限公司,桂林,541002
【正文语种】中文
【中图分类】R9
【相关文献】
1.液体顶空气相色谱法测定磷酸哌喹中乙醇溶剂残留 [J], 潘勇;唐庆华
2.磷酸左旋咪唑中乙醇溶剂残留的液体顶空气相色谱法测定 [J], 唐庆华
3.顶空气相色谱法测定聚明胶肽注射液中的丙酮溶剂残留 [J], 杨佳佩;倪赞
4.顶空气相色谱法测定氟[18F]脱氧葡糖注射液中有机溶剂残留量 [J], 王庆芬;杨丽娜;倪晓霞;林跃松;刘威宏
5.顶空气相色谱法测定鱼肝油酸钠注射液中有机溶剂残留量 [J], 戴黎黎;李苗
因版权原因,仅展示原文概要,查看原文内容请购买。
青蒿琥酯平衡溶解度和表观油水分配系数的测定
目的:测定青蒿琥酯的平衡溶解度及表观油水分配系数。
方法:采用HPLC测定青蒿琥酯在各类溶媒中平衡溶解度,色谱条件为DiamonsilC18(2)色谱柱(4.6mm×250mm,5μm),流动相乙腈一磷酸盐缓冲液(60:40),流速1.0mL·min^-1,检测波长210nm,柱温30℃。
采用摇瓶法测定青蒿琥酯在正辛醇-水/磷酸缓冲盐中油水分配系数。
结果:32.0℃时青蒿琥酯在纯水、三氯甲烷、丙酮、无水乙醇中溶解度分别为(0.36±0.016),(598.7±13.11),(284.63±7.96),(186.03±8.27)g·L^-1。
32.0℃时青蒿琥酯在正辛醇一水体系中油水分配系数(249.03±3.76),logPapp=(2.40±0.0065)。
结论:青蒿琥酯脂溶性强,pH对其溶解度和油水分配系数均具有较大影响。
在磷酸盐缓冲体系中,青蒿琥酯在pH5.50~7.43时溶解度随pH的增大而增加,油水分配系数随pH 的增大而减小,但logPapp保持〉2.0,说明青蒿琥酯在体内、外环境下均具有较强的生物膜通透能力。
青蒿琥脂片溶出度测定的方法学验证目的对青蒿琥脂片的溶出度检查进行方法学验证。
方法参照《中国药典》2010年版二部附录ⅩC第二法对其溶出度进行检查[1]。
采用紫外分光光度法,在289 nm的波长处测定吸光度,进行方法学验证。
结果采用该方法测定青蒿琥脂片,分别在pH1.2、4.5、6.8、水四种溶出介质中,以浓度对吸收度进行线性回归,青蒿琥酯在10~60 μg/mL范围内浓度与吸收度呈良好的线性关系。
在以上四种溶出介质中的平均回收率和标准偏差均符合要求。
结论本法测定青蒿琥酯片溶出量方法尚可,可用于该产品的质量控制。
标签:青蒿琥脂片;溶出度测定;方法学验证青蒿琥酯是具有倍半萜结构的抗疟青蒿素的衍生物之一[1],作为新型的抗疟药,青蒿琥酯具有高效、速效、低毒等特点,而且不易产生耐受性[2]。
对原虫无性体有较强的杀灭作用,能迅速控制疟疾发作,适用于脑型疟疾及各种危重疟疾的治疗[3]。
除抗疟外,尚有治疗弓形虫病、抗肿瘤等作用[4]。
青蒿琥酯片收载于国际药典第三版以及中国药典2010年版二部,溶出度测定作为反映或模拟体内药物吸收情况的实验方法在评定口服固体制剂的质量时有重要意义[5]。
本文参考有关相关文献对青蒿琥酯片的体外溶出实验进行了方法研究[6,7],可用于该产品制定质量标准的参考。
1仪器与试药ZRS-8G智能溶出仪(天大天发科技有限公司);T90+紫外分光光度计(PG.Instruments Ltd);青蒿琥酯对照品(美国USP品牌,批号:100200-200202);青蒿琥酯原料药(来源:武汉三洹医药化工有限公司);青蒿琥酯片(来源:安徽新和成皖南药业有限公司)。
所用试剂均为分析纯,水为去离子水。
2溶出度测定的方法学验证[8]2.1 衍生化方法的确定参考中国药典2010年版二部青蒿琥酯片溶出度测定方法。
青蒿琥酯碱水解条件受到水解温度、碱液浓度、水解时间影响。
因此,需要对其测定方法进行再验证与优化。
精密称取青蒿琥酯原料药50 mg,加水溶解并制成1 000 mL,作为考察溶液。
2.1.1 水解温度考察精密量取上述溶液20 mL,置25 mL量瓶中,加1M氢氧化钠溶液2.5 mL,加水稀释至刻度,摇匀,共6份,分别置40℃、50℃、60℃、70℃、80℃、90℃水浴温度下保温45 min,取出,立即冷却至室温,另取相应试剂同法制成各自空白溶液。
在200~400 nm的波长范围内进行紫外扫描,记录最大吸收波长及吸光度。
结果:水解温度在50℃时吸光度变化最小,最大吸收波长为288 nm。
参考中国药典收载的青蒿琥酯片溶出度测定检测波长,确定检测波长为289 nm。
2.1.2 碱液浓度考察精密量取上述溶液20 mL,置25 mL量瓶中,共6份,分别加0.5、1、2、3、4、5M氢氧化钠溶液2.5 mL,加水稀释至刻度,摇匀,同置50℃水浴保温45 min,取出,立即冷却至室温,另取相应试剂同法制成各自空白溶液。
在200~400 nm的波长范围内进行紫外扫描,记录最大吸收波长及吸光度。
结果:碱液浓度在1M,水解液碱度在0.1M时吸光度最大,最大吸收波长在288 nm。
2.1.3 水解时间考察精密量取上述溶液20 mL,置25 mL量瓶中,加1M氢氧化钠溶液2.5 mL,加水稀释至刻度,摇匀,共6份,同置50℃水浴保温,于15、30、45、60、75、90 min取出1份,立即冷却至室温,另取相应试剂同法制成各自空白溶液。
在200~400 nm的波长范围内进行紫外扫描,记录最大吸收波长及吸光度。
结果:水解时间在45 min时吸光度最大,且最大吸收波长在289 nm 左右。
2.1.4 测定溶液稳定性考察精密量取上述溶液20 mL,置25 mL量瓶中,加1M氢氧化钠溶液2.5 mL,加水稀释至刻度,摇匀,置50℃水浴保温45 min,取出,立即冷却至室温,在289 nm的波长处测定吸光度,并在实验环境下放置,在不同时间测定吸光度。
结果:在上述衍生化条件下的水解液在2 h内吸收值稳定,故应在水解后2 h内测定完毕。
2.1.5 结论根据上述序贯试验结果得出溶出量测定衍生化最佳方法为:精密量取上述溶液20 mL,置25 mL量瓶中,加1M氢氧化钠溶液2.5 mL,加水稀释至刻度,摇匀,置50℃水浴保温45 min,取出,立即冷却至室温,在289 nm的波长处测定吸光度。
2.2 系统适用性此项内容主要对青蒿琥酯在pH1.2、4.5、6.8缓冲溶出介质(PhInt4)及水中的系统适用性进行验证。
验证内容:检测波长、测定精密度、滤膜吸附性试验等。
由于pH1.2缓冲液介质20 mL需要消耗1M氢氧化钠溶液1.5 mL,因此,为达到0.1M的水解液碱度,需加入1M氢氧化钠溶液4 mL。
2.2.1 检测波长确定①取供试品适量,精密称定重量,研细,精密称取相当于1片量的粉末,分别置1 000 mL pH1.2、4.5、6.8、水四种介质中,置37℃保温桨法100 r/min搅拌1 h,取溶液经0.8 μm微孔滤膜滤过,精密量取滤液20 mL,置25 mL量瓶中,加1 mol/L氢氧化钠溶液2.5 mL(pH1.2缓冲液加入4 mL),加水稀释至刻度,摇匀,作为供试品溶液。
②取青蒿琥酯对照品10 mg,置250 mL 量瓶中,分别加pH1.2、4.5、6.8、水四种溶出介质200 mL,超声使溶解,加1 mol/L 氢氧化钠溶液25 mL(pH1.2缓冲液加入40 mL),加水稀释至刻度,搖匀,作为对照品溶液。
③取缺青蒿琥酯阴性粉末230 mg,分别置1 000 mL pH1.2、4.5、6.8、水四种介质中,置37℃保温桨法100 r/min搅拌1 h,取溶液经滤膜滤过,精密量取滤液20 mL,置25 mL量瓶中,加1 mol/L氢氧化钠溶液2.5 mL(pH1.2缓冲液加入4mL),加水稀释至刻度,摇匀,作为阴性对照溶液。
④取供试品溶液、阴性对照溶液、对照品溶液同置(50±1)℃水浴中保温45 min,迅速冷却至室温,在200~400 nm的波长范围进行扫描。
⑤结果表明:在pH 1.2、4.5、6.8、水四种溶出介质中,供试品溶液与对照品溶液最大吸收波长均为289 nm,阴性对照溶液在此波长下均无吸收。
因而,确定检测波长为289 nm。
2.2.3 滤膜吸附性试验取不经滤膜过滤的溶出液,再取适量,经滤膜过滤,将此次过滤前后的溶出液照上述溶出量测定方法测定其吸光度,过滤前后吸光度差值应小于1%。
结果表明:滤膜对被测组分有一定程度的吸附。
2.3 专属性取上述供试品溶液、对照品溶液、阴性对照溶液,在289 nm的检测波长下分别测定吸光度。
结果表明:阴性对照溶液在此波长下无吸收,说明处方辅料不干扰本法的测定;阴性样品在水、pH1.2、pH4.5三种介质中的干扰率大于2%,有一定程度的干扰。
此法有待进一步的提高。
2.4 线性2.4.1方法①pH1.2缓冲液:取青蒿琥酯对照品25 mg,精密称定,置250 mL 量瓶中,加pH1.2缓冲液适量超声处理10 min,并稀释至刻度,摇匀。
精密量取5、10、15、20、25、30 mL,分别置50 mL量瓶中,加上述介质稀释至刻度,摇匀,作为各对照品溶液。
精密量取各对照品溶液20 mL,分别置25 mL量瓶中,加1 mol/L氢氧化钠溶液4 mL(以下的溶出介质加入2.5 mL),加水稀释至刻度,摇匀,同置(50±1)℃水浴中保温45 min,迅速冷却至室温,在289 nm的波长处测定吸光度,以对照品浓度为横坐标,吸光度为纵坐标进行线性回归,得回归方程Y=0.0036X-0.0003(日内)、r=0.9988,Y=0.0029X+0.0101(日间)、r=0.9984。
②pH4.5缓冲液:同pH1.2缓冲液项下配制测定,得回归方程Y=0.0028X-0.0006(日内)、r=0.9960,Y=0.0020X-0.0059(日间)、r=0.9940。
③pH6.8缓冲液:同pH1.2缓冲液项下配制测定,得回归方程Y=0.0037X+0.0044(日内)、r=0.99998,Y=0.0036X+0.0014(日间)、r=0.9995。
④水:同pH1.2缓冲液项下配制测定,得回归方程Y=0.0036X-0.0050(日内)、r=0.9990,Y=0.0028X-0.0005(日间)、r=0.9990。
2.4.2 范围结果显示:青蒿琥酯在(10~60)μg/mL(相当于标示浓度的20%~120%)的浓度范围内,方法的线性良好。
因而,确定本法的线性范围为20%~120%。
2.5 准确度(回收率)2.5.1方法①pH1.2缓冲液:取缺青蒿琥酯阴性230 mg,置1 000 mL量瓶中,共9份,分别精密称取青蒿琥酯工作对照品30 mg、40 mg、50 mg,各3份,分别置上述量瓶中,加相应溶出介质适量超声处理10 min,并稀释至刻度,经0.8 μm微孔滤膜滤过,精密量取续滤液20 mL,置25 mL量瓶中,加1 mol/L氢氧化钠溶液4 mL(以下的溶出介质加入2.5 mL),加水稀释至刻度,摇匀,作为供试品溶液。
另取青蒿琥酯对照品10 mg,置250 mL量瓶中,加上述介质200 mL,加1 mol/L氢氧化钠溶液40 mL(以下的溶出介质加入25 mL)振摇使溶解,加水稀释至刻度,摇匀,作为对照品溶液。
取供试品溶液与对照品溶液,同置50℃水浴保温45 min,立即冷却至室温,在289 nm的波长处测定吸光度,计算测得量。
根据测得量与加入量比值计算本法回收率。
②pH4.5缓冲液:同pH1.2缓冲液项下配制测定。
③pH6.8缓冲液:同pH1.2缓冲液项下配制测定。
④水:同pH1.2缓冲液项下配制测定。
3讨论由于青蒿琥酯化学结构中仅琥珀酸基团含有生色团,其最大吸收波长在216 nm左右,但吸收系数很小,需要较高的测定浓度,超过了溶出度测定的浓度要求(50 mg→1000 mL,50 μg/mL),但遇稀碱后结构发生定量转化,其产物在289 nm 处有一强吸收峰,紫外分光光度法就是利用青蒿琥酯这一性质建立的定量分析方法。
采用高效液相色谱法测定溶液的浓度要在4 mg/mL左右,若进行溶出量测定,需将系统灵敏度增强80倍,势必造成基線噪音增强,测定的准确度下降。
因而,采用衍生化的方法,通过碱水解生成助色基团,使吸收峰红移,吸收系数增加,达到紫外分光光度法测定要求。
青蒿素类化合物难溶于水、稀酸、稀碱、表面活性剂,易溶于非极性有机溶剂,但固体制剂在上述溶剂中难以崩解,更谈不上溶出。
对于难溶于水的药物,一般不采用有机溶剂用于溶出度测定[10,11]。
由于青蒿琥酯较差的溶解性,目前市场上相应的剂型较少,另外青蒿琥酯具有诱导肝药酶的作用,首过效应明显,且在体内代谢快,导致用药次数频繁;若能通过改变剂型,使其在体内缓释,提高药物的生物有效利用度,则能克服上述缺点,达到更有效治疗的目的。