【华南理工考研 有机化学】17 周环反应
- 格式:pptx
- 大小:2.20 MB
- 文档页数:35
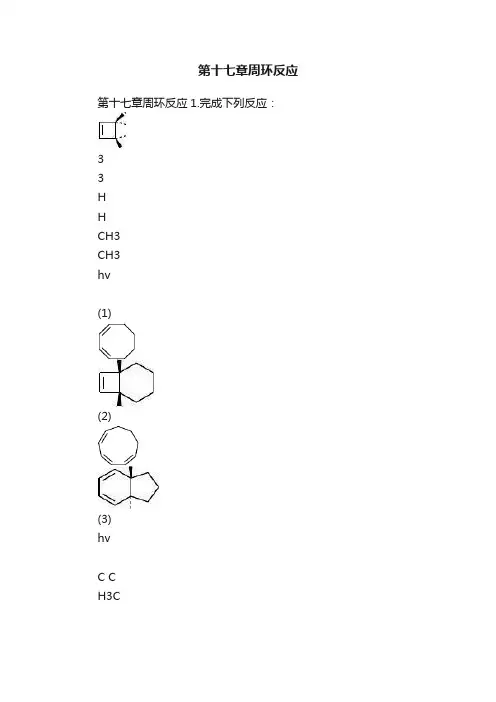
第十七章周环反应第十七章周环反应1.完成下列反应:33HHCH3CH3hv(1)(2)(3)hvC CH3CH32(4)(5)+OOO室温150℃?COOCH3CΔ(6)?ΔO CH2CH2CHCH3 (7)CH2+CCCO2CH3CO2CH3Δ(8)2.用前线轨道理论解释下列反应在加热条件下(1)是可以发生的,(2)是不能发生的。
ΔCH2+CCCO2CH3CO2CH3(1)CO2CH3CO2CH3+CCCO2CH3CO2CH3(2)CH23.乙烯与丁二烯在175℃及高压下反应,得到以下产物:环己烯(85%),4-乙烯基-1-环己烯(12%)及乙烯基环丁烷(0.02%)。
写出反应式,并指出为何乙烯基环丁烷产率极低。
4.为何双环庚二烯在光照和加热条件下的产物不同?+HC CH5.下列重排得到产物(A )和(B ),它们是如何产生的?画出分子轨道的变化。
+333C 2H H 3C 2H (A)(B) 6.解释下列的重排反应:*O*OH7. 解释下列反应机理:ΔCCNC CN+8.2,3-二甲基-1,3-丁二烯和乙炔二羧酸加热后,得到一个产物,其分子式为C 16H 20O 3(A ),含有两个双键。
(A )在丙酮中经光照加热后得出一个(A )的异构体(B ),但不含双键,探讨(A )及(B )的结构。
hv ΔCCHOOC +H 2CCH 3CH 2CH 3C 16H 20O 3C 16H 20O 3(A)(B)。






第十七章周环反应第一节周环反应的理论一周环反应1.定义:在最近的五十年里,有机化学家研究有机化学机理,主要有两种。
一种是游离基型反应,一种是离子型反应,它们都生成稳定或不稳定的中间体。
离子型或游离基型反应:反应物→中间体→产物另一种机理是,在反应中不形成离子或游离基的中间体,而认为是有电子重新组织经过四或六中心环的过渡态而进行的。
这类反应不受溶剂极性的影响,不被碱或酸所催化,没有发现任何引发剂对反应有什么关系。
这类反应似乎表明化学键的断裂和生成是同时发生的。
这种一步完成的多种心反应叫周环反应。
周环反应:反应物→产物2.周环反应的特征:①反应进行的动力,是加热或光照。
②反应进行时,有两个以上的键同时断裂或形成,是多中心一步反应。
③反应时作用物的变化有突出的立体选择性。
④在反应过渡态中原子排列是高度有序的。
二. 分子轨道理论几个原子轨道线性组合,形成几个分子轨道,比原子轨道能量低的为成键轨道,比原子轨道能量高的为反键轨道。
其电子填充符合Pauli原理和Hund规则。
σ轨道:Л轨道:丁二烯的分子轨道:镜面节面直链共轭多烯烃分子轨道特点:①节面数:若共轭多烯烃有几个原子,它的n个轨道就有n-1个节面。
②轨道的节面越多,能量越高。
③高一能级的轨道和低一能级的轨道的对称性是相反的。
④图中的共轭多烯烃的对称性都是指类顺型(像顺型)的。
三.前线轨道.福井认为最高的已占分子轨道(HOMO)上的电子被束缚得最松弛,最容易激发到能量最低的空轨道(LUMO)中去。
这些轨道是处于前线轨道(FMO),前线轨道理论认为:化学键的形成主要是由FMO的相互作用决定的。
分子的HOMO与LUMO 能量接近,容易组成新轨道。
第二节电环化反应1.定义:在n个Л电子的线型共轭体系中,在其两端点之间生成一个单键的反应及其逆过程称为电环化反应。
电环化反应中,多烯烃的一个Л键变成环烯烃里的一个σ键。
如:(Z,E)2,4-己二烯根据微观可逆性原则,正反应和逆反应所经过的途径是相同的。