2013-第三章--配合物的化学键理论解析
- 格式:ppt
- 大小:2.30 MB
- 文档页数:93








配合物的化学键理论The Chemical Bond Theories of Complexes配合物的化学键理论处理中心原子(或离子)与配体之间的键合本质问题,用以阐明中心原子的配位数、配位化合物的立体结构以及配合物的热力学性质、动力学性质、光谱性质和磁性质等。
几十年来,提出来的化学键理论有: 静电理论(EST) Electrostatic Theory 价键理论(VBT) Valence Bond Theory 晶体场理论(CFT) Crystal Field Theory分子轨道理论(MOT) Molecular Orbital Theory 角重叠模型(AOM) Angular Overlap Model在这一节中,我们讲授配合物的价键理论和晶体场理论。
分子轨道理论和角重叠模型在后续课程中学习。
一、价键理论(Valence Bond Theory )L .Pauling 等人在二十世纪30年代初提出了杂化轨道理论,首先用此理论来处理配合物的形成、配合物的几何构型、配合物的磁性等问题,建立了配合物的价键理论,在配合物的化学键理论的领域内占统治地位达二十多年之久。
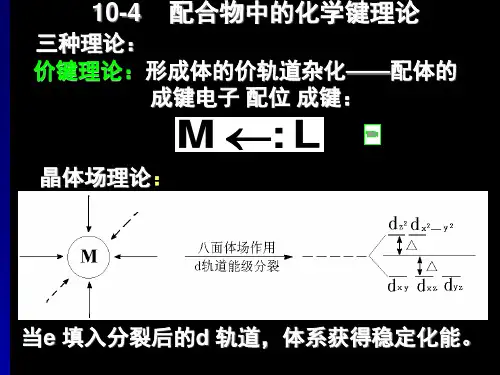
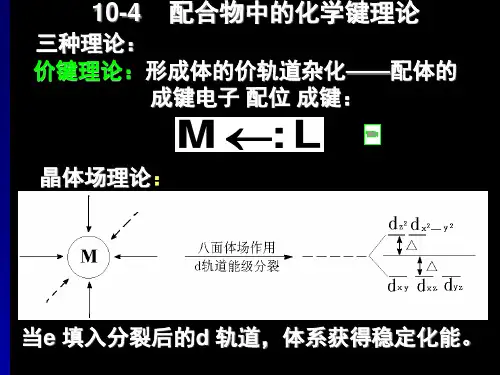
1.价键理论的基本内容:(1) 配合物的中心体M 与配体L 之间的结合,一般是靠配体单方面提供孤对电子对与M 共用,形成配键M ←∶L ,这种键的本质是共价性质的,称为σ配键。
(2) 形成配位键的必要条件是:配体L 至少含有一对孤对电子对,而中心体M必须有空的价轨道。
(3) 在形成配合物(或配离子)时,中心体所提供的空轨道(s 、p ,d 、s 、p 或s 、p 、d)必须首先进行杂化,形成能量相同的与配位原子数目相等的新的杂化轨道。
2.实例:(1) 主族元素配合物 Be 4O(CH 3COO)6:每个Be 原子都采取sp 3杂化-4BF :B 原子为sp 3杂化,正四面体构型 -36AlF :-3][ Al 3+周围共有12个价电子 Al 3+采取sp 3d 2杂化 (2) 过渡元素配合物a .(n - 1)d 10电子构型中心体+243)Zn(NH sp 3杂化 正四面体-3HgI sp 2杂化 平面三角形b .(n - 1)d 8电子构型中心体F Al F F F FF+243])[Ni(NH sp 3杂化 正四面体 -24]Ni(CN)[ dsp 2杂化 平面四方-24PtCl dsp 2杂化 平面四方c .(n - 1)d x (x <8)电子构型中心体-36Fe(CN) d 2sp 3杂化 正八面体+363])[Co(NH d 2sp 3杂化 正八面体 +263])[Co(NH sp 3d 2杂化 正八面体-36FeF sp 3d 2杂化 正八面体3.讨论:(1) 配合物中的中心体可以使用两种杂化形式来形成共价键:一种杂化形式为(n - 1)d 、n s 、n p 杂化,称为内轨型杂化。
配合物的化学键理论摘要:化学键理论在配位化学中有着重要的运用,它现在主要有三大流派。
本文就回顾化学键的发展历程,并对三大化学键理论做出仔细的阐述。
关键字:化学键价键理论分子轨道理论晶体场理论配位场理论化学键的发展历程最早化学家假设原子和原子之间是用一个神秘的钩钩住的,这种设想至今仍留下痕迹,化学键的键字就有钩的意思。
1916年,德国科学家柯塞尔考察大量的事实后得出结论:任何元素的原子都要使最外层满足8 电子稳定结构。
柯塞尔的理论能解释许多离子化合物的形成,但无法解释非离子型化合物。
1923 年,美国化学家路易斯发展了柯塞尔的理论,提出共价键的电子理论:两种元素的原子可以相互共用一对或多对电子,以便达到稀有气体原子的电子结构,这样形成的化学健叫做共价健。
柯塞尔和路易斯的理论常叫原子价电子理论。
它只能定性地描述分子的形成,化学家更需要对化学键做定量阐述。
1927 年,海特勒和伦敦用量子力学处理氢分子,用近似方法计算出氢分子体系的波函数和能量获得成功,这是用量子力学解决共价键问题的首例。
1930 年,鲍林更提出原子成键的杂化理论(杂化轨道理论),洪德把单键、多键分成δ和∏键两类。
δ健是指在沿着连接两个原子核的直线(对称轴)上电子云有最大重叠的共价键,这种键比较稳定。
∏键是指沿电子云垂直于这条直线方向上结合而成的键,这种键比较活泼。
这就使价键理论进一步系统化,使经典的化合价和化学键有机地结合在一起了。
由于上述的价键理论对共扼分子、氧气分子的顺磁性等事实不能有效解释,因此本世纪30 年代后又产生一种新的理论——分子轨道理论。
分子轨道理论在1932 年首先由美国化学家马利肯提出。
他用的方法跟经典化学相距很远,一时不被化学界接受,后经密立根、洪德、休克尔、伦纳德等人努力,使分子轨道理论得到充实和完善。
它把分子看作一个整体,原子化合成分子时,由原子轨道组合成分子轨道,原子的电子属于分子整体。
分子轨道就是电子云占据间,它们可相互重叠成键。