有机设计实验报告
- 格式:doc
- 大小:499.00 KB
- 文档页数:17

实验报告一、实验名称:有机混合物的分离分析——气相色谱法的应用二、实验目的:1.了解气相色谱分离分析方法。
2.初步了解气相色谱仪的基本工作原理及气相色谱流程。
3.学习气相色谱仪的使用操作技术,以及用微量注射器进样的技术。
4.学习应用保留值法进行定性分析。
三、实验原理:在一定的色谱条件(色谱柱和温度、流速等操作条件)下,物质均有各自确定不变的保留值(保留时间或保留体积)。
对于较简单的多组份混合物,若其色谱峰均能互相分开,则可将各个峰的保留值,与各相应的标准样品在同一条件所测的保留值一一进行对照,确定各色谱峰所代表的物质,籍以定性。
四、实验用品:SC-200型气相色谱仪、微量注射器1μL 1支、滴管及磨口塞试管若干、氮气钢瓶、正戊烷、正己烷、正庚烷、正辛烷、环己烷、苯。
五、实验步骤:1.取正戊烷10滴,正己烷15滴,正庚烷、正辛烷各10滴于磨口塞试管A中混合均匀。
2.取环己烷、苯各10滴于磨口塞试管B中混合均匀。
3.取出1μL的微量注射器,用试管A中的溶液洗涤5次,然后吸取1μL试管A中的溶液。
将注射器垂直插入气相色谱仪的进样口中,迅速注入试样,同时点击屏幕上的采集数据按钮。
待屏幕上出现完整的4个峰的时候停止采集,并记录每个峰对应的保留值。
4.用试管B中的溶液洗涤微量注射器5次,然后吸取1μL试管B中的溶液。
将注射器垂直插入气相色谱仪的进样口中,迅速注入试样,同时点击屏幕上的采集数据按钮。
待屏幕上出现完整的2个峰的时候停止采集,并记录每个峰对应的保留值。
5.用未知试样洗涤微量注射器5次,然后吸取1μL未知试样。
将注射器垂直插入气相色谱仪的进样口中,迅速注入试样,同时点击屏幕上的采集数据按钮。
待采集时间超过前两步中的最长保留值后停止采集,并记录每个峰对应的保留值。
6.整理器材,分析实验数据,判定未知试样的成分。
六、实验数据及处理:1.试管A中各物质的保留值:正戊烷0.657min,正己烷1.073min,正庚烷1.998min,正辛烷3.948min。
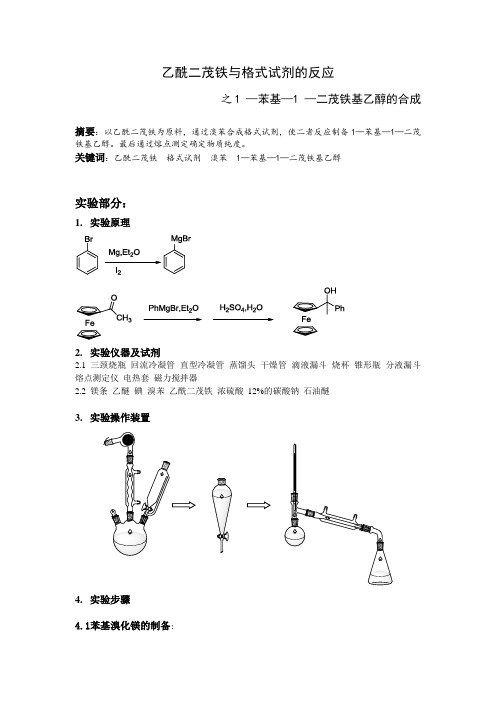
乙酰二茂铁与格式试剂的反应之1 —苯基—1 —二茂铁基乙醇的合成摘要:以乙酰二茂铁为原料,通过溴苯合成格式试剂,使二者反应制备1—苯基—1—二茂铁基乙醇。
最后通过熔点测定确定物质纯度。
关键词:乙酰二茂铁格式试剂溴苯 1—苯基—1—二茂铁基乙醇实验部分:1.实验原理2.实验仪器及试剂2.1三颈烧瓶回流冷凝管直型冷凝管蒸馏头干燥管滴液漏斗烧杯锥形瓶分液漏斗熔点测定仪电热套磁力搅拌器2.2 镁条乙醚碘溴苯乙酰二茂铁浓硫酸12%的碳酸钠石油醚3.实验操作装置4.实验步骤4.1苯基溴化镁的制备:4.2 1 —苯基—1 —二茂铁基乙醇的制备:5.实验产率及产品鉴定5.1产品由石油醚析出得到。
由于纯化难以进行,所以推测可能含有杂质。
实际得量0.28g。
产率=0.28/0.674*100% =41.54%5.2熔点测定:当温度到达110℃时可以看到开始融化,但具体确实接近150,在148℃时完全融化。
所以分析110℃时是杂质乙酰二茂铁的的影响。
6.实验结果与讨论本实验旨在掌握乙酰二茂铁与格式试剂的反应及相关性质。
但是实验具体操作时有很多值得我们讨论分析的地方,结果也不是很令人满意。
首先,对于格式试剂的制备,虽然可能遇到引发不了的情况,但注意操作还是可以比避免的。
如,本次实验我预先加入了一点点碘,实验引发的相当迅速。
当进入1—苯基—1—二茂铁基乙醇的制备时,我们遇到过一点问题。
首先反应并没有像我们方案上预想的一样反应得到橙黄色溶液,而是红棕色液体。
特别是在后来蒸馏了乙醚后,对于除去溴苯,没有非常合适的方法。
最后我采用直接用石油醚使其析出,虽然析出的物质还是比较多,先不管产率的损失,但却不可避免的含有一些杂质。
所以,本实验还需有所改进。
参考文献:[1].张首才.松辽学刊,1—苯基—1—二茂铁基乙醇[J] .2001, (3):73-74[2].武汉大学化学与分子科学学院实验中心.有机化学实验,武汉大学出版社。

实验名称:有机合成实验——苯甲酸的制备一、实验目的1. 学习有机合成的基本原理和方法。
2. 掌握苯甲酸的制备方法。
3. 培养实验操作技能,提高实验观察和记录能力。
二、实验原理苯甲酸是一种重要的有机酸,广泛应用于食品、医药、化工等领域。
本实验采用硝化法合成苯甲酸,其反应原理如下:C6H5CH3 + HNO3 → C6H5COOH + H2O + NO2↑三、实验仪器与试剂1. 仪器:烧瓶、冷凝管、滴液漏斗、烧杯、锥形瓶、铁架台、酒精灯、温度计、玻璃棒、试管等。
2. 试剂:苯、浓硝酸、浓硫酸、氢氧化钠溶液、冰水混合物、乙醇、蒸馏水等。
四、实验步骤1. 准备反应液:将苯和浓硫酸按体积比1:1混合,加入烧瓶中,冷却至室温。
2. 硝化反应:在烧瓶中加入适量的浓硝酸,用玻璃棒搅拌,控制反应温度在50℃左右,反应时间约为1小时。
3. 冷却反应液:将反应液冷却至室温,过滤掉生成的硝基苯,用蒸馏水洗涤沉淀,直至滤液呈中性。
4. 中和反应:将沉淀转移至烧杯中,加入适量的氢氧化钠溶液,搅拌至沉淀完全溶解。
5. 分离提纯:将反应液转移至锥形瓶中,加入适量的乙醇,加热蒸发,冷却结晶,过滤,干燥,得到苯甲酸。
五、实验数据记录与处理1. 反应时间:1小时2. 反应温度:50℃3. 沉淀质量:0.5g4. 理论产量:0.6g5. 实际产量:0.5g六、实验结果与讨论1. 实验结果:本实验成功制备了苯甲酸,实际产量为0.5g,理论产量为0.6g,产率为83.3%。
2. 讨论:在本实验中,苯甲酸的制备过程中,反应温度的控制对产率有较大影响。
实验过程中,反应温度控制在50℃左右,产率较高。
此外,实验过程中,沉淀的过滤和洗涤对苯甲酸的纯度也有一定影响。
七、实验总结1. 本实验成功制备了苯甲酸,掌握了有机合成的基本原理和方法。
2. 在实验过程中,应注意反应温度的控制,以及沉淀的过滤和洗涤,以提高产率和纯度。
3. 本实验培养了实验操作技能,提高了实验观察和记录能力。

乙酸异戊酯制备实验报告乙酸异戊酯制备实验报告引言:乙酸异戊酯是一种常见的有机化合物,常用于食品香料和溶剂制备等领域。
本实验旨在通过酯化反应制备乙酸异戊酯,并对反应条件进行优化。
实验步骤:1. 实验前准备首先,准备所需的实验器材和试剂,包括乙酸、异戊醇、硫酸、酸化石墨、冷却水等。
2. 反应体系的搭建将酸化石墨加入反应瓶中,加入适量的乙酸和异戊醇,然后加入少量的硫酸作为催化剂。
3. 反应条件的优化为了得到较高的产率和纯度,我们需要对反应条件进行优化。
首先是温度的选择,我们将反应瓶放入恒温水浴中,控制温度在60℃左右。
然后是反应时间的控制,反应进行2小时后,取样检测产物纯度。
如果纯度不够高,可以延长反应时间。
4. 产物的提取和纯化反应结束后,将反应瓶取出,加入适量的冷却水进行冷却。
然后,用饱和氯化钠溶液洗涤产物,将有机相收集。
最后,用无水硫酸钠干燥有机相,并用旋转蒸发仪去除溶剂,得到纯净的乙酸异戊酯。
结果与讨论:经过优化后,我们成功制备了乙酸异戊酯。
通过红外光谱和质谱分析,确认了产物的结构和纯度。
实验结果显示,乙酸异戊酯的产率达到了90%以上,纯度超过99%。
这表明我们所选择的反应条件和催化剂是合适的。
结论:本实验通过乙酸异戊酯的制备,展示了酯化反应的基本原理和实验操作。
通过对反应条件的优化,我们成功地制备了高产率和高纯度的乙酸异戊酯。
这对于相关领域的研究和应用具有重要意义。
总结:乙酸异戊酯是一种重要的有机化合物,本实验通过酯化反应制备了乙酸异戊酯,并对反应条件进行了优化。
实验结果显示,我们成功地制备了高产率和高纯度的乙酸异戊酯。
这为相关领域的研究和应用提供了可靠的实验基础。
通过本实验,我们不仅掌握了酯化反应的操作技巧,还深入了解了反应条件对产物纯度和产率的影响。
这对于我们今后的科研工作和实验设计具有重要的指导意义。

实验一有机化学实验基本操作实验目的:1、使学生明白进入有机化学实验学习,必须阅读有机化学实验的一般知识的内容及安全实验是有机化学实验的基本要求;2、仪器的清点和玻璃仪器的清洗、安装。
教学内容:一、实验室的安全、事故的预防与处理1、实验室的一般注意事项2、火灾、爆炸、中毒及触电事故的预防3、事故的处理和急救二、有机化学实验常用仪器、设备和应用范围1、玻璃仪器2、金属用具3、其它仪器设备三、有机实验常用装置的安装练习1、回流装置2、蒸馏装置3、气体吸收装置4、搅拌装置四、仪器的清洗、干燥和塞子的配置1、仪器的清洗2、仪器的干燥3、塞子的配置和钻孔五、实验预习、记录和实验报告六、实验产率的计算实验二萃取和洗涤实验目的:1、学习萃取法的基本原理和方法;2、学习分液漏斗的使用方法。
实验原理:萃取和洗涤是利用物质在不同溶剂中的溶解度不同来进行分离的操作。
萃取和洗涤在原理上是一样的,只是目的不同。
从混合物中抽取的物质,如果是我们需要的,这种操作叫做萃取或提取;如果是我们不要的,这种操作叫做洗涤。
萃取是利用物质在两种不互溶(或微溶)溶剂中溶解度或分配比的不同来达到分离、提取或纯化目的的一种操作。
实验仪器及药品:仪器:分液漏斗、试管药品:0.01%I2—CCl4溶液、1%KI—H2O溶液实验操作步骤:(本次实验为间歇多次萃取操作)一、多次萃取操作步骤及注意事项1、选择容积较液体体积大一倍以上的分液漏斗,把活塞擦干,在活塞上均匀涂上一层润滑脂,使润滑脂均匀分布,看上去透明即可。
2、检查分液漏斗的顶塞与活塞处是否渗漏(用水检验),确认不漏水时方可使用。
3、将被萃取液和萃取剂依次从上口倒入漏斗中,塞紧顶塞(顶塞不能涂润滑脂)。
4、取下分液漏斗,并前后振荡,然后再将漏斗放回铁圈中静置。
5、待两层液体完全分开后,打开顶塞,再将下层液体自活塞放出至接受瓶:6、将所有的萃取液合并,加入过量的干燥剂干燥。
7、然后蒸去溶剂,根据化合物的性质利用蒸馏、重结晶等方法纯化。

萃取和分液实验报告一、实验目的:(1)了解萃取分液的基本原理。
(2)熟练掌握分液漏斗的选择及各项操作。
二、实验原理:利用某溶质在互不相溶的溶剂中的溶解度不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,在利用分液的原理和方法将它们分离开来。
三、实验仪器和药品:药品:碘水、ccl4器材:分液漏斗、100ml烧杯、带铁圈的铁架台、20ml四、实验步骤:1、分液漏斗的选择和检验:验分液漏斗是否漏水,检查完毕将分液漏斗置于铁架台上;2、振荡萃取:用量筒量取10 ml碘水,倒入分液漏斗,再量取5 ml萃取剂ccl4加入分液漏斗,盖好玻璃塞,振荡、放气;需要重复几次振荡放气。
3、静置分层:将振荡后的分液漏斗放于铁架台上,漏斗下端管口紧靠烧怀内壁;4、分液:调整瓶塞凹槽对着瓶颈小孔,使漏斗内外空气相通,轻轻旋动活塞,按“上走上,下走下”的原则分离液体;五、实验室制备图:(见右图)六、实验总结(注意事项):1、分液漏斗一般选择梨形漏斗,需要查漏。
方法为:关闭活塞,在漏斗中加少量水,盖好盖子,用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来用力振荡,看是否漏水。
2、将溶液注入分液漏斗中,溶液总量不超过其容积的3/4;3、振荡操作要领:右手顶住玻璃塞,左手握住活塞,倒置振荡;振荡过程中要放气2-3次,让分液漏斗仍保持倾斜状态,旋开旋塞,放出蒸气或产生的气体,使内外压力平衡;4、要及时记录萃取前后的液面情况及颜色变化;振荡前,上层为黄色,下层为无色;振荡静置后,上层为无色(或淡黄色),下层为紫色;5、萃取剂的选择a.溶质在萃取剂的溶解度要比在原溶剂(水)大。
b.萃取剂与原溶剂(水)不互溶。
c.萃取剂与溶液不发生发应。
6、按“上走上,下走下”的原则分离液体是为了防止上层液体混带有下层液体。
七、问题:1、如果将萃取剂换成苯,实验现象是否相同?使用哪种有机溶剂做萃取剂更好些?为什么?篇二:有机实验报告五华南师范大学实验报告学生姓名学号专业年级、班级课程名称近代有机分析实验 11 实验项目固相微萃取气相色谱法用于挥发性有机化合物混合物的分离分析实验类型□验证□设计□综合实验时间 2012 年10 月 31日实验指导老师实验评分实验五:固相微萃取气相色谱法用于挥发性有机化合物混合物的分离分析一、实验目的1、了解固相微萃取及气相色谱仪的基本结构和分离分析的基本原理2、了解影响分离效果的因素3、掌握定性分析与测定二、实验原理固相微萃取 (spme) 是20世纪90年代初发展的一种集萃取、浓缩、解吸于一体的样品前处理技术。
有机化学实验总结(五篇范文)第一篇:有机化学实验总结有机化学实验总结转眼间,短短五周的实验课已经结束了。
现在回想起来,在有机化学实验课上,真的收获了很多。
这些收获也不仅仅是学会了一些基本的化学实验操作,对很多反应和有机物的性质有了更深的理解,更重要的是学会了严谨,学会了提前准备,学会了思考……这些都将在我以后的学习和生活中有很重要的意义。
最重要的一点是严谨,做实验时要做到一丝不苟。
还记得第一次进入实验室看到的情景,整齐的仪器、药品摆放,一尘不染的桌面,还有处理的器材……我深深意识在这个实验室里是不容许有一点马虎的。
做有机实验是要严格按照标准操作来的。
蒸馏、过滤、萃取、干燥……每一个地方都要足够细心,足够严谨,很多时候会做得慢,如果有时候追求速度,就很容易出现反应进行不充分、生成物产率低的情况。
还记得第一次做酯化反应实验时,由于没有注意控制水位,导致无法分析反应是否已经达到限度,加热了很长时间,还没能准确测出生成的水量。
我深深体会到了做有机实验时是一点也马虎不得的。
任何一个失误都有可能对实验结果造成很大的影响。
当然做有机实验时也需要足够的耐心。
还记得做呋喃甲酸和呋喃甲醇合成实验的时候,总共用了三十分钟搅拌反应物,萃取又做了三次,还有每次蒸馏的时候都要时刻注意温度的变化和烧瓶里的变化,不能走神。
这些过程都需要足够的耐心。
当看到自己制备的晶体长的很“好看”时,当得到的产物量“很足”的时候,觉得一切等待都是值得的。
还有很多实验操作是需要慢工出细活的,如果没有足够的耐心,很难做出理想的实验结果。
做有机实验时要提前准备,事先有预习是非常重要的,如果预习了,就会对这个实验有一个初步的了解,知道了实验的一些具体步骤,要准备哪些药品和器材,实验过程中又要注意一些什么问题,只有预习好了,在做实验时才能够得心应手。
当然,在预习中,我们也可能会发现一些问题,有一些不懂的地方,而这些我们都可以把它们标记下来,在老师讲解的时候认真搞懂,或者是带着疑惑去实验探究,这对加深知识点的理解是很有帮助的。
有机化学实验报告(菁选最新6篇在现实生活中,报告使用的频率越来越高,报告成为了一种新兴产业。
相信很多朋友都对写报告感到非常苦恼吧,下面是精心为大家整理的6篇《有机化学实验报告(菁选》,希望能够对困扰您的问题有一定的启迪作用。
有机化学实验报告篇一实验名称组装实验室制取氧气的装置实验目的正确地组装一套实验室制取氧气的装置,并做好排水集气的准备实验器材、药品大试管(Ф32mm×200mm)、带导管的橡皮塞(与试管配套)、酒精灯、铁架台(带铁夹)、木质垫若干块、集气瓶(125mL)、毛玻璃片、水槽(装好水)、烧杯(100mL)。
实验步骤1. 检查仪器、药品。
2. 组装气体发生装置。
3. 检查气体发生装置的气密性。
4. 按照实验室制取氧气的要求装配好气体发生装置。
5. 在水槽中用烧杯向集气瓶中注满水,盖好毛玻璃片,将集气瓶倒置在水槽中。
6. 拆除装置,整理复位。
有机化学实验报告篇二一、实验目的1.了解熔点的意义,掌握测定熔点的操作2.了解沸点的测定,掌握沸点测定的操作二、实验原理1.熔点:每一个晶体有机化合物都有一定的熔点,利用测定熔点,可以估计出有机化合物纯度。
2.沸点:每一个晶体有机化合物都有一定的沸点,利用测定沸点,可以估计出有机化合物纯度。
三、主要试剂及物理性质1.尿素(熔点132.7℃左右)苯甲酸(熔点122.4℃左右)未知固体2.无水乙醇(沸点较低72℃左右)环己醇(沸点较高160℃左右)未知液体四、试剂用量规格五、仪器装置温度计玻璃管毛细管Thiele管等六、实验步骤及现象1.测定熔点步骤:1装样2加热(开始快,低于15摄氏度是慢,1-2度每分钟,快到-熔点时0.2-0.5摄氏度每分钟)3记录2.熔点测定现象:1某温度开始萎缩,蹋落2之后有液滴出现3全熔3.沸点测定步骤:1装样(0.5cm左右)2加热(先快速加热,接近沸点时略慢,当有连续汽泡时停止加热,冷却)3记录(当最后一个气泡不冒出而缩进是为沸点)沸点测定现象:刚开始有气泡后来又连续气泡冒出,最后一个气泡不冒而缩进。
最新有机化学实验实验报告实验目的:本实验旨在通过合成一种简单的有机化合物,加深对有机反应机理的理解,并熟悉有机化学实验的基本操作技能。
实验原理:本次实验选择合成乙酸乙酯(ethyl acetate),这是一种广泛应用的有机溶剂和合成中间体。
反应通过乙醇(ethanol)和醋酸(acetic acid)在酸性催化剂(如浓硫酸)的作用下进行酯化反应。
反应方程式如下:CH3COOH + C2H5OH → CH3COOC2H5 + H2O实验材料与仪器:1. 乙醇(C2H5OH)2. 醋酸(CH3COOH)3. 浓硫酸(H2SO4)4. 饱和食盐水(NaCl溶液)5. 无水硫酸钠(Na2SO4)6. 滴定管、分液漏斗、圆底烧瓶、冷凝管、加热套、磁力搅拌器、真空旋转蒸发仪实验步骤:1. 在通风橱内,将50毫升乙醇和25毫升醋酸加入圆底烧瓶中。
2. 缓慢滴加5毫升浓硫酸作为催化剂,并装上冷凝管和磁力搅拌器。
3. 使用加热套缓慢加热混合液至回流状态,维持反应1-2小时。
4. 反应完成后,让反应混合物自然冷却至室温。
5. 将反应混合物转移到分液漏斗中,加入饱和食盐水和无水硫酸钠,静置分层。
6. 打开分液漏斗的开关,放出下层液体,收集上层有机相。
7. 将收集的有机相转移到旋转蒸发仪中,旋转蒸发去除溶剂,得到乙酸乙酯产物。
实验结果:通过观察和闻气味,确认产物为乙酸乙酯。
产物的收率约为70%,通过核磁共振(NMR)和红外光谱(IR)分析,进一步验证了产物的结构。
实验讨论:本次实验中,酯化反应的收率受多种因素影响,包括反应时间、温度、催化剂的用量等。
实验过程中应注意控制反应条件,以提高产物的纯度和收率。
同时,实验过程中应严格遵守安全操作规程,避免使用有毒有害的化学品造成伤害。
结论:通过本次实验,成功合成了乙酸乙酯,并对有机化学中的酯化反应有了更深入的理解。
实验过程中的操作技巧和注意事项对于提高实验效率和安全性至关重要。
化学与环境学院有机化学实验报告实验名称以苯胺为起始原料合成对溴苯胺专业化学教育班级12化一姓名黄冰如学号20122401055 指导老师杨定乔实验分组第一组日期2014年5月30日以苯胺为起始原料合成对溴苯胺摘要:以苯胺为起始原料设计合成了对溴苯胺,不能直接通过卤代反应实现合成过程,由于氨基是强给电子基,和溴反应很难停留在一元取代的阶段,因此,要制备对溴苯胺,必须先将苯环的活性降低,在本实验中,先将苯胺乙酰化再进行溴代反应,当溴代完毕再水解将乙酰基除去,这其中要合成二个中间体,分别为乙酰苯胺、对溴乙酰苯胺,通过本实验的合成步骤,能较为有效和便捷地合成对溴苯胺。
关键词:苯胺;乙酰苯胺;对溴乙酰苯胺;对溴苯胺Study on the Synthesis of 4 - BromoanilinesAbstract: Aniline as starting materials synthesized Bromoaniline not directly implement the synthesis reaction by a halo, as is a strong electron-donating group, and bromine is difficult to stay in one dollar replaced the stage, so be prepared for Bromoaniline must first reduce the activity of the phenyl ring, in this experiment, the first bromo aniline then acetylation reaction is complete when the bromide of acetyl group is removed by hydrolysis, to which two synthetic intermediates, namely, acetanilide on Bromoacetanilide through synthesis step of the experiment, can be more effective and convenient synthesis of bromoaniline.Keywords: Aniline;Acetanilide;Bromoacetanilide;4 - Bromoanilines;1.前言1.1对溴苯胺的制备或来源方法(1) 对溴苯胺的传统的工业制法如下:NH 2NO 2NaNO 2H 2SO 4N=NOSO 3HNO 2Cu 2Br 2HBrBrNO 2Fe HBrBrNH 2可以看出,该方法虽成本较低,但是污染环境严重,不符合绿色化学的宗旨,不利于可持续发展。
(2) 现代化学家都致力于开发无毒无污染的一步制备方法,主要方法有:固体溴化试剂,比如PyHBr3、DBUHBr3、Me4NBr3、用金属羰基合成催化剂氧化原子溴;以W-4型Raney-Ni 为催化剂,双氰胺为脱溴抑制剂(助催化剂),甲醇为溶剂,以对溴硝基苯为原料用催化加氢法还原制备对溴苯胺等等。
但由于成本过高,暂未在工业上应用。
(3) 本实验以苯胺为起始原料合成对溴苯胺的方法如下:本实验选取硝基苯还原为苯胺,苯胺加乙酰基保护氨基再加入溴进行亲电取代,最后在酸性下水解得到目标产物的方法,虽然毒性大,对环境污染大,但是成本低,进行这种方法的探究有利于我们理解传统工业制备对溴苯胺的方法。
第一个中间体乙酰苯胺为无色晶体,具有退热镇痛作用,是较早使用的解热镇痛药,因此俗称“退热冰”。
乙酰苯胺也是磺胺类药物合成中重要的中间体。
胺的酰基化在有机合成中有着重要作用。
作为一种保护措施,一级和二级芳胺在合成中通常被转化为它们的乙酰基衍生物,以降低胺对氧化降解的敏感性,使其不被反应试剂破坏;同时氨基酰化后降低了氨基在亲电取代反应(特别是卤化)中的活化能力,使其由很强的第I 类定位基变为中等强度的第II 类定位基,使反应由多元取代变为有用的一元取代,由于乙酰基的空间位阻很大,往往选择性地生成对位取代物。
伯胺、仲胺可用酰氯、酸酐或与冰醋酸加热来进行酰化,使用冰醋酸试剂易得,价格便宜,但需要较长的反应时间,适合于规模较大的制备。
酸酐一般来说是比酰氯更好的酰化试剂。
如果在醋酸-醋酸钠的缓冲溶液中进行酰化,由于酸酐的水解速率比酰化速率慢得多,可以得到高纯度的产物。
乙酰苯胺可由苯胺与乙酰化试剂,如乙酰氯、乙酐或乙酸等直接作用来制备。
反应活性是乙酰氯>乙酸酐>乙酸。
由于乙酰氯和乙酸酐的价格较贵,本实验采用纯的乙酸作为乙酰化试剂。
反应式如下:冰乙酸与苯胺的反应速率较慢且可逆,可采用冰乙酸过量和利用分馏柱移去反应生成的水的方式提高产率。
加入锌粉的目的是防止苯胺在反应过程中被氧化。
第二个中间体对溴乙酰苯胺是通过苯环卤代反应合成的,卤素对苯环上的取代属于亲电取代反应,常用的催化剂有铁、铝、磷及其卤化物等。
苯环上有乙酰氨基,乙酰氨基是邻对位取代基团,由于空间位阻大,主要产物是对溴乙酰苯胺。
乙酰氨基酸性条件下不稳定,可在酸性条件下去保护,生成对溴苯胺。
1.2对溴苯胺的物化性质结构式HN Br2英文名称4-BromoanilinesCAS号106-40-1熔点66.4 ℃沸点沸点时分解相对分子质量172.03密度 1.4970(液体,99.6℃)溶解情况不溶于水,易溶于乙醇和乙醚性状从60%乙醇中析出者为正交晶系双锥体针状结晶毒性LD50(mg/kg) 有毒,其毒性较氯苯胺类更严重,可经表皮吸收,具有溶血性、能引起膀胱癌。
1.3 对溴苯胺的应用对溴苯胺是很重要的化工中间体,广泛应用于医药、染料、颜料等精细化工产品的合成,它在精细化工生产中处于不可替代的地位。
(1)在医药中:对溴苯胺作为医药中间体的作用是无可匹敌的,所合成的药物可用于治疗气喘、肾炎、增生病、神经紊乱、帕金森等疾病。
(2)在染料中:用对溴苯胺作为原料能够制备传统的硫化和偶氮染料,同时还可以制备香豆素类荧光染料,这类染料是高档荧光染料,具有发射强度高,色光鲜艳,荧光强烈等优点。
(3)在农药中:主要制备草酞替苯胺类药物,有利于小麦属植物授粉。
(4)其它:对溴苯胺还用于制备抗污剂,抗氧剂,稳定剂,石油添加剂等。
在材料方面,对溴苯胺能制备氰基联苯型液晶材料,性能好,对光、热的稳定性最好,还具有良好的防湿性能。
1.4使用试剂及产物的物理常数名称分子量状态熔点(℃)沸点(℃)相对密度苯胺93.12 无色液体-6.3 184 1.022冰醋酸60.05 无色液体117.9 1.0492 活性炭12.00 黑色固体对溴乙酰苯胺214.06 白色固体167~169 353.4 1.717 乙酰苯胺135.16 白色晶体114.3 304 1.2190液溴159.80红棕色液体-7.2 58.78 3.119 95%乙醇46.07 无色液体-114.3 78.4 0.789 氢氧化钠40.01 无色液体318 1390 2.130浓盐酸36.47 无色液体无固定 1.179 亚硫酸氢钠104.6 无色液体150 1.48 锌粉65.39 固体419.5 908 7.142.实验部分2.1 中间体乙酰苯胺的制备【试剂和仪器】仪器:50ml圆底烧瓶;刺形冷凝管;直形冷凝管;接液管;量筒;温度计;100ml烧杯;吸滤瓶;布氏漏斗;小水泵;保温漏斗;电热套。
试剂:苯胺;冰醋酸;锌粉;活性炭。
【实验装置】【实验步骤及实验现象】实验步骤实验现象注意事项1.在50ml圆底烧瓶中,放置10mL新蒸馏过的苯胺、15mL 冰乙酸及少许锌粒,如反应装置所示,用小火加热回流,保持温度计读数于105℃1h,当温度下降时表明反应已完全。
加入苯胺、冰乙酸、锌粒后,溶液呈淡黄色,圆底烧瓶瓶壁发烫。
加热,气泡增多,温度一直变化,没有超过100℃,当移开石棉网,温度大于100℃,开始有液体蒸出,液体沸腾,黄色液体逐渐变澄清。
1.玻璃仪器必须干燥。
2.苯胺因为氧化而颜色较深,使用前要重新蒸馏。
因为苯胺的沸点较高,蒸馏时选用空气冷凝管冷凝,或采用减压蒸馏。
3. 冰醋酸具有强烈刺激性,要在通风橱内取用。
4. 由于苯胺易氧化,锌粉的作用是防止苯胺氧化,只要少量即可。
加得过多,会出现不溶于水的氢氧化锌。
5. 反应时分馏温度不能太高,保持馏出速度为1 d/2~3 秒,以免大量乙酸蒸出而降低产率和有二取代产物生成。
6.加入活性炭的目的是脱色;不能在沸腾的溶液中加入活性炭,以免引起暴沸,要等溶液稍冷却;活性炭不宜加多,以免吸附部分产品。
7. 趁热过滤时,布氏漏斗和吸滤瓶一定要预热。
滤纸大小要合适,抽滤过程要快,避免产品在布氏漏斗中结晶。
8. 若让反应液冷却,则乙酰苯胺固体析出,沾在烧瓶壁上不易倒出。
2.在搅拌下趁热将反应物倒入盛有100mL冷水的烧杯中,冷却后抽滤,用冷水洗涤粗产品。
将反应物移入盛有500mL烧杯中,加入300ml 水,在石棉网上加热溶解,稍冷后,加入少量活性炭(约0.5克),在搅拌下再次加热煮沸10分钟,趁热过滤除去活性炭,滤液冷却,结晶,抽滤,晾干后称量并计算产率。
趁热将圆底烧瓶内的溶液倒入盛冷水的烧杯中,有乳白色悬浮物产生。
重结晶中有少量油滴,溶解后加活性炭,热过滤,得到白色晶体,冷却结晶,抽滤后得白色片状晶体。
2.2中间体对溴乙酰苯胺的制备【试剂和仪器】仪器:电动搅拌器;水浴锅;250ml三口烧瓶;恒压滴液漏斗;200度温度计2根;烧杯;抽滤瓶;布氏漏斗;刮刀。
试剂:乙酰苯胺;溴;乙醇;冰醋酸;亚硫酸氢钠。
【实验装置】【实验步骤及实验现象】实验步骤实验现象注意事项1.在250ml三口烧瓶上配制电动搅拌器、温度计、恒压在搅拌的过程中,乙酰苯胺固体溶解,且溶液变为浅黄色。
1. 搅拌器与三口烧瓶连接处的密封性要好,以防止溴化氢滴液漏斗,并在恒压滴液漏斗上连接气体吸收装置,以吸收反应中产生的溴化氢。
在100ml锥形瓶中,将3.5g 乙酰苯胺中溶解于15ml乙醇中,将 1.31g溴溶解于3ml 冰醋酸,一边搅拌一边慢慢地将溴-冰醋酸溶液滴加至乙酰苯胺的醇溶液中,滴加速度以溶液的棕红色较快褪去为宜。
滴加溴时,棕红色溶液退去较快,45℃水浴加热,溶液颜色变浅。
升温至60℃,溶液变成淡黄色,没有红棕色蒸气产生。
溶液最终呈现很浅的黄色。
从瓶口逸出。
2. 溴具有强腐蚀性和刺激性,必须在通风橱中量取,操作时应带上乳胶手套。
3. 因为反应会生成HBr气体,会污染空气和对人体有害,所以要用一盛有NaOH溶液的烧杯作为气体吸收装置来吸收HBr,防止其逸出。