新人教版高一化学必修一第一章第三节第一节 氧化还原反应
- 格式:pptx
- 大小:4.30 MB
- 文档页数:51






人教版高一化学第一章第三节氧化还原反应一、内容概括本节主要介绍了氧化还原反应的基本概念,包括氧化数(氧化态)、氧化剂与还原剂的定义、氧化还原反应的特征以及如何通过电子转移来识别和配平氧化还原反应。
通过学习这些基础知识,学生能够理解物质在化学反应中的电子得失过程,并掌握氧化还原反应方程式的书写方法。
二、重点归纳1.氧化数:表示一个原子在一个化合物中所带的电荷数,用于描述元素的氧化状态。
2.氧化剂与还原剂:1.氧化剂:获得电子的物质,其氧化数降低。
2.还原剂:失去电子的物质,其氧化数升高。
3.氧化还原反应的特征:1.反应过程中存在电子的转移。
2.氧化数发生变化。
4.氧化还原反应的配平:1.使用氧化数法或离子-电子法配平氧化还原反应方程式。
5.常见的氧化还原反应类型:1.金属与非金属的直接反应。
2.酸碱反应中的氧化还原过程。
3.溶液中的离子反应。
三、练习题讲解及举一反三题目练习题1:下列哪个选项正确描述了氧化剂?• A. 失去电子的物质• B. 获得电子的物质• C. 保持电子不变的物质• D. 提供质子的物质答案:B解析:氧化剂是获得电子的物质,在反应过程中其氧化数降低。
举一反三题目:下列哪个选项正确描述了还原剂?• A. 失去电子的物质• B. 获得电子的物质• C. 保持电子不变的物质• D. 接受质子的物质答案:A解析:还原剂是失去电子的物质,在反应过程中其氧化数升高。
练习题2:写出并配平以下反应的化学方程式:锌与稀硫酸反应生成硫酸锌和氢气。
•答案:Zn + H₂SO₄→ ZnSO₄ + H₂•解析:锌(Zn)与稀硫酸(H₂SO₄)反应生成硫酸锌(ZnSO₄)和氢气(H₂)。
这是一个典型的置换反应,也是氧化还原反应,其中锌作为还原剂,硫酸作为氧化剂。
举一反三题目:写出并配平以下反应的化学方程式:铁与稀盐酸反应生成氯化亚铁和氢气。
•答案:Fe + 2 HCl → FeCl₂ + H₂•解析:铁(Fe)与稀盐酸(HCl)反应生成氯化亚铁(FeCl₂)和氢气(H₂)。


第1课时氧化还原反应核心微网络素养新要求1.了解氧化还原反应的概念。
2.从化合价升降、电子得失或电子对偏移角度理解氧化还原反应。
3.培养由宏观到微观的科学探究意识。
学业基础——自学·思记·尝试一、氧化还原反应概念发展1.从得氧、失氧的角度认识氧化还原反应(1)得氧、失氧的分析(2)从得氧、失氧的角度分析氧化反应和还原反应(3)结论:氧化还原反应是反应过程中有氧得失的化学反应。
(4)模型2.从化合价变化的角度认识氧化还原反应(1)化合价变化的分析(2)从化合价变化的角度分析氧化反应和还原反应(3)结论:氧化还原反应是反应过程中有元素化合价升降的化学反应。
(4)模型特别提醒(1)在氧化还原反应中,并不是所有元素的化合价都发生改变。
(2)并非只有得氧、失氧的反应才是氧化还原反应。
凡是有元素化合价升降的化学反应都是氧化还原反应。
化合价变化是氧化还原反应的外在特征,是判断氧化还原反应的依据。
(3)任何氧化还原反应中,元素化合价升高与元素化合价降低一定同时发生,且化合价升高总数=化合价降低总数。
3.从电子转移的角度认识氧化还原反应(1)电子转移的分析a.电子得失的分析Na原子失去1个电子→Na元素化合价升高→Na被氧化→Na发生氧化反应;Cl原子得到1个电子→Cl元素化合价降低→Cl2被还原→Cl2发生还原反应。
b.电子对偏移的分析Ⅰ.氯原子对共用电子对的吸引力稍强,共用电子对偏向氯原子,发生还原反应。
Ⅱ.氢原子对共用电子对的吸引力稍弱,共用电子对偏离氢原子,发生氧化反应。
特别提醒元素原子间通过共用电子对形成化合物时,共用电子对偏向哪种元素的原子,哪种元素就显负价;共用电子对偏离哪种元素的原子,哪种元素就显正价。
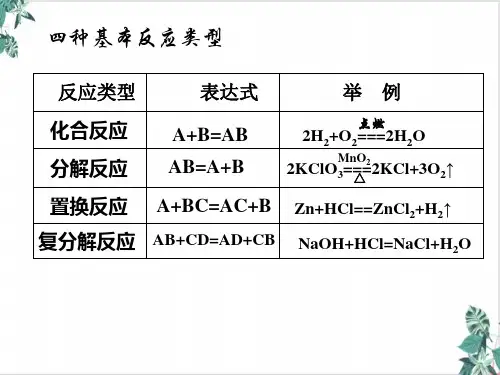
(2)从电子转移的角度分析氧化反应和还原反应(3)结论氧化还原反应是反应过程中有电子转移(电子得失或共用电子对偏移)的化学反应。
(4)模型二、氧化还原反应的特征和本质归纳总结近几年高考中一些特殊物质的元素的化合价:三、氧化还原反应与四种基本反应类型的关系C+O2CO22H2O2H2↑+O2↑以上关系可用以下图示表示:(1)交叉分类图(2)集合图[即学即练]1.判断正误,正确的打“√”,错误的打“×”(1)氧化还原反应中一定有氧元素参加。

