无机合成化学第四章习题
- 格式:doc
- 大小:139.50 KB
- 文档页数:4

第一章概论1现代无机合成的容和方法与旧时代相比有哪些变化?答:2为什么说无机合成化学往往是一个国家工业发展水平的标志?无机合成化学与国民经济的发展息息相关,在国民经济中占有重要的地位。
工业中广泛使用的三酸两破”,农业生产中必不可少的化肥、农药,基础建设中使用的水泥、玻璃、瓷,涂料工业中使用的大量无机料等无一不与无机合成有关。
这些产品的产量和质量几乎代表着一个国家的工业水平。
3.为什么说合成化学是化学学科的核心,是化学家改造世界、创造社会財富的最有力的手段?答:作为化学学科中当之无愧的核心,合成化学已成为化学家改造世界创造未来最有力的工具。
合成化学领域的每一次进步都会带动产业的一次革命。
发展合成化学,不断创造和开发新的物种,不仅是研究结构、性能及其相互关系,揭示新的规律与原理的基础,也成为推动化学学科与相关学科发展的主要动力。
4您能举出几种由p区元素合成的无机材料吗?碳纳米管、5为什么从某种意义上讲,合成化学的发展史就是化学的发展史?6.无机合成有哪些热点领域?(1)特种结构无机材料的制备(2)软化学合成(3)极端条件下的合成(4)无机功能材料的制备(5)特殊聚集态材料的合成(6)特种功能材料的分子设计(7)仿生合成(8)纳米粉体材料的制备(9)组合化学(10)绿色化学。
7.什么是极端条件下的合成?能否举一例说明。
极端条件是指极限情况,即超高温、超高压、超真空及接近绝对零度、强磁场与电场、激光等离子体等。
例如,在模拟宇宙空间的情况下,可能合成出没有位错的高纯度品体。
8查阅文献,找出一例绿色合成原理在无机合成化学中的应用。
9何谓软化学合成方法?与所谓的“硬化学法”相比有什么特点?软化学是相对于硬化学而言的。
它是指在较温和条件下实现的化学反应过程。
特点:1.不需用高纯金属作原料2.制得的合金是有一定颗粒度的粉末,不需在使用时再磨碎3.产品本身具有高活性4.产品具有良好的表面性质和优良的吸放氢性能5.合成方法简单6.有可能降低成本7.为废旧储氢合金的回收再生开辟了新途径第二章低温合成1温度与物性有怎样的关系?什么是物质的第五态?温度与物性的关系:对于一般液体来说,随着温度降低,密度会逐渐增加。

无机化学习题参考答案第一章1.4.解:〔1〕H 2O 22C〔2〕S 2O 32- 3v C 〔3〕N 2O (N -N -O 方式) v C ∞〔4〕Hg 2Cl 2h D ∞〔5〕H 2C=C=CH 2 2d D 〔6〕UOF 4 C 5v 〔7〕BF 4-d T 〔8〕SClF 54v C〔9〕反-Pt(NH 3)2Cl 22h D〔10〕PtCl 3(C 2H 4)- 2v C1.B(CH 3)3和BCl 3相比,哪一个的Lewis 酸性强,为什么?一般来说,CH 3为推电子基团,Cl 为吸电子基团,因此的Lewis 酸性强。
〔BCl 3易水解;B(CH 3)3不溶于水,在空气中易燃〕2.BH 3和BF 3都可和(CH 3)2NPF 2生成加合物,在一种加合物中,B 原子和N 相连,另一种则和P 相连,绘出两种结构式,并说明形成两种结构的原因。
PFFH 3CH 3PF F H 3CH 3B BH 3F 3(该题可参考史启桢等翻译的"无机化学",作者Shriver 等,由高教社出版, 其中关于热力学酸度参数的部分,p.190-191; 或者该书的英文原版第5章的相关内容)3. 无水AlCl 3可作为傅-克烷基化反应的催化剂, 而吸水后则失效, 原因何在? 配位饱和〔6配位〕,失去Lewis 酸性4. 吸水后失效 的AlCl 3有什么方法可以脱水?因为Al 3+是典型的硬酸,与氧的亲合力很强,因此实验室不能在HCl ,NH 4Cl ,SOCl 2等气氛下加热脱水。
〔只能加强热生成 Al 2O 3后,用高温下用加C 和Cl 2用复原氯化法制备,这就不是脱水方法了〕。
第二章2.1 解:Ni 2+ d 8组态Pt 2+ d 8组态 第四周期〔分裂能小〕第六周期〔分裂能大〕P Ni ClP ClClCl P Ptrans cis四面体构型 平面四方形构型〔两种构型〕 只有一种结构 〔P 代表PPh 3〕2.2 解 〔1〕MA 2B 4〔2〕MA 3B 3M A ABB M ABA BM ABAB M A AA Btrans cis fac(面式) mer(经式) D 4h C 2v C 3v C 2v μ=0 μ≠0 μ≠0 μ≠0μfac >μmer2.3 Co(en)2Cl 2+D 2hC 2 光活异构体 C 2Co(en)2(NH 3)Cl 2+33Htrans cisCo(en)(NH3)2Cl2+3Cl333NHNH33trans(1) trans(2)cis2.4 Co(en)33+Ru(bipy)32+手性分子D3D3PtCl(dien)+dienHNCH2CH2CH2NH2NH2CH2基本上为平面分子,无手性2.5 (1) 分别用BaCl2溶液滴入,有白色沉液出现的为[Co(NH3)5Br]SO4,或分别加入AgNO3溶液,产生浅黄色沉淀的为[Co(NH3)5SO4]Br。

第四版无机化学习题及答案第一章原子结构和原子周期系1-1根据原子序数给出下列元素的基态原子的核外电子组态:(a)K (b)Al (c)Cl (d)Ti(Z=22)(e)Zn(Z=30)(f)As(Z=33)答:(a)[Ar]4s1(b)[Ne]3s23p1(c)[Ne]3s23p5(d)[Ar]3d54s2(e)[Ar] 3d104s1(f)[Ar]4s24p31-2给出下列原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的电子用箭头表示。
(a)Be (b)N (c)F (d)Cl-(e)Ne+(f)Fe3+(g)As3+1-3 Li+、Na+、K+、Rb+、Cs+的基态的最外层电子组态与次外层电子组态分别如何?1-4以下+3价离子那些具有8电子外壳?Al3+、Ga3+、Bi3+、Mn3+、Sc3+答:Al3+和Sc3+具有8电子外壳。
1-5已知电中性的基态原子的价电子层电子组态分别为:(a)3s23p5(b)3d64s2(c)5s2(d)4f96s2(e)5d106s1 试根据这个信息确定它们在周期表中属于那个区、哪个族、哪个周期。
答:(a)p区,ⅦA族,第三周期(b)d区,Ⅷ族,第四周期(c)s区,ⅡA族,第五周期(d)f区,ⅢB族,第六周期(e)ds 区,ⅠB族,第六周期1-6根据Ti、Ge、Ag、Rb、Ne在周期表中的位置,推出它们的基态原子的电子组态。
答:Ti位于第四周期ⅣB族,它的基态原子的电子组态为[Ar]3d24s2;Ge位于第四周期ⅣA族,它的基态原子的电子组态为[Ar]3d104s24p2;Ag位于第五周期ⅠB族,它的基态原子的电子组态为[Kr] 4d105s1;Rb位于第五周期ⅠA族,它的基态原子的电子组态为[Kr] 5s1;Ne位于第二周期0族,它的基态原子的电子组态为[He] 2s22p6。
1-7某元素的基态价层电子构型为5d36s2,给出比该元素的原子序数小4的元素的基态原子电子组态。
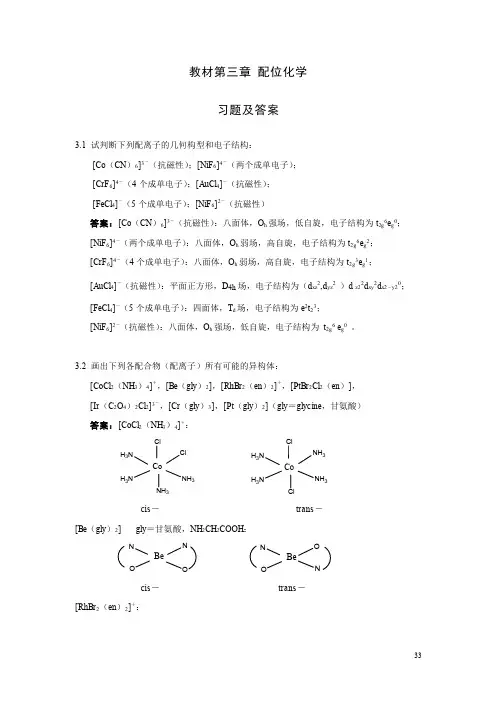
教材第三章 配位化学习题及答案3.1 试判断下列配离子的几何构型和电子结构:[Co (CN )6]3-(抗磁性);[NiF 6]4-(两个成单电子); [CrF 6]4-(4个成单电子);[AuCl 4]-(抗磁性); [FeCl 4]-(5个成单电子);[NiF 6]2-(抗磁性)答案:[Co (CN )6]3-(抗磁性):八面体,O h 强场,低自旋,电子结构为t 2g 6e g 0; [NiF 6]4-(两个成单电子):八面体,O h 弱场,高自旋,电子结构为t 2g 6e g 2; [CrF 6]4-(4个成单电子):八面体,O h 弱场,高自旋,电子结构为t 2g 3e g 1; [AuCl 4]-(抗磁性):平面正方形,D 4h 场,电子结构为(d xz 2,d yz 2 )d z22d xy 2d x2-y20; [FeCl 4]-(5个成单电子):四面体,T d 场,电子结构为e 2t 23; [NiF 6]2-(抗磁性):八面体,O h 强场,低自旋,电子结构为 t 2g 6 e g 0 。
3.2 画出下列各配合物(配离子)所有可能的异构体:[CoCl 2(NH 3)4]+,[Be (gly )2],[RhBr 2(en )2]+,[PtBr 2Cl 2(en )], [Ir (C 2O 4)2Cl 2]3-,[Cr (gly )3],[Pt (gly )2](gly =glycine ,甘氨酸) 答案:[CoCl 2(NH 3)4]+:ClNH 3H 3NH 3NCoClNH 3NH 3NH 3H 3NH 3NCoClClcis - trans -[Be (gly )2] gly =甘氨酸,NH 2CH 2COOH :NONOBeONN O Becis - trans - [RhBr 2(en )2]+:NNNNRhBrBrNBrNNRhNBrNNNBrRhNBrtrans - cis - cis - [PtBr 2Cl 2(en )]:BrBrNNPtClClClClNNPtBrBrBrClNNPtBrClBrClNNPtBrCl[Ir (C 2O 4)2Cl 2]3-:OOOIrClClOClOOIrOClOClOOIrOCltrans - cis - cis - [Cr (gly )3]:NOONCrNONOONCrNON ON OCrNON ON OCrNOmer - mer - fac - fac - [Pt (gly )2]:NNOPtONNO Ptcis - trans -3.3 (a )已知配合物[M (A -B )2]和[M (A -B )2X 2]型的配合物都是旋光活性的,请分别画出它们的几何结构。

第一章习题:1.现代无机合成的内容和方法与旧时代相比有哪些变化?2。
为什么说无机合成化学往往是一个国家工业发展水平的标志?3.为什么说合成化学是化学学科的核心,是化学家改造世界、创造社会财富的最有力的手段?4.您能举出几种由p区元素合成的无机材料吗?5。
为什么从某种意义上讲,合成化学的发展史就是化学的发展史?6。
您或您的朋友的研究课题属于无机合成领域?如果是,属于哪个热点领域?举例说。
7. 什么是极端条件下的合成?能否举一例说明。
8. 查阅文献,找出一例绿色合成原理在无机合成化学中的应用。
9。
何谓软化学合成方法?与所谓的“硬化学法"相比有什么特点?10.在研究工作中,您最喜欢利用哪种工具查阅化合物的合成方法?第二章习题:1。
化学热力学在无机合成中的起着什么样的重要的作用?2。
Bartlett是怎样从吉布斯-亥姆霍兹方程分,确立稀有气体第一个化合物制备的热力学根据?3。
Ellingham 图建立的依据是什么?4。
查阅Ellingham 图,看MnO被C还原为金属的最低温度是多少?写出该温度下的总反应方程式。
5。
偶合反应在无机合成中应用的原理何在?请举例说明。
6. 10。
Pourbaix图(pH-E)的实质是什么?它都有哪些方面的应用?第三章习题:1。
温度与物性有怎样的关系?什么是物质的第五态?2。
实验室中,获得低温的方法或低温源装置有哪几种?各举一例.3。
为什么任何碱金属与液氨反应后溶液都具有同一吸收波长的蓝光?核心物种是什么?如何证明?4. 什么是金属陶瓷?有什么特殊性质?用在哪些方面?它们是如何在高温下制备的?5。
获得高温有哪些手段?高温合成技术有哪些广泛应用?6。
何谓高温下的化学转移反应?它主要应用在无机合成的哪些方面?7.什么是等离子体超高温合成?它主要有哪些方面的用途?8.什么是自蔓延高温合成?该法有什么特点?其关键技术是什么?9.从物理化学原理说明高温高压合成的机理。
10.什么是超导体?超导体具有什么突出的性质?哪些元素是超导元素?第四章习题1.什么是水热—溶剂热合成?该法有什么特点?有无不足?2。
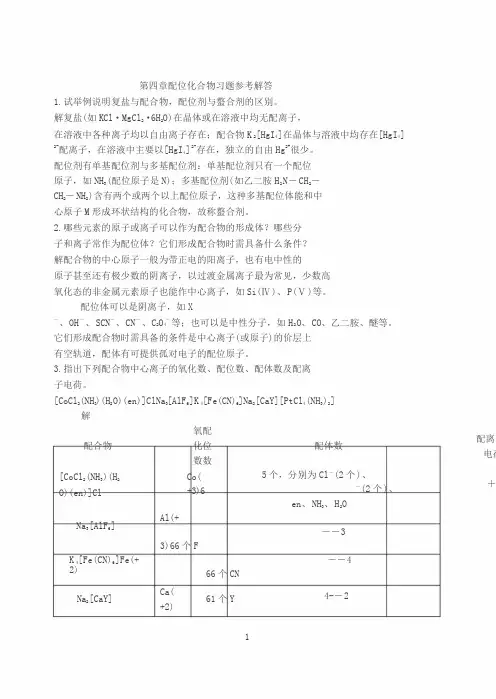
第四章配位化合物习题参考解答1.试举例说明复盐与配合物,配位剂与螯合剂的区别。
解复盐(如KCl ·MgCl 2·6H 2O)在晶体或在溶液中均无配离子,在溶液中各种离子均以自由离子存在;配合物K 2[HgI 4]在晶体与溶液中均存在[HgI 4]2-配离子,在溶液中主要以[HgI 4]2-存在,独立的自由Hg 2+很少。
配位剂有单基配位剂与多基配位剂:单基配位剂只有一个配位 原子,如NH 3(配位原子是N);多基配位剂(如乙二胺H 2N -CH 2- CH 2-NH 2)含有两个或两个以上配位原子,这种多基配位体能和中 心原子M 形成环状结构的化合物,故称螯合剂。
2.哪些元素的原子或离子可以作为配合物的形成体?哪些分 子和离子常作为配位体?它们形成配合物时需具备什么条件? 解配合物的中心原子一般为带正电的阳离子,也有电中性的 原子甚至还有极少数的阴离子,以过渡金属离子最为常见,少数高 氧化态的非金属元素原子也能作中心离子,如Si(Ⅳ)、P(Ⅴ)等。
配位体可以是阴离子,如X-、OH -、SCN -、CN -、C 2O 4-等;也可以是中性分子,如H 2O 、CO 、乙二胺、醚等。
它们形成配合物时需具备的条件是中心离子(或原子)的价层上 有空轨道,配体有可提供孤对电子的配位原子。
3.指出下列配合物中心离子的氧化数、配位数、配体数及配离 子电荷。
[CoCl 2(NH 3)(H 2O)(en)]ClNa 3[AlF 6]K 4[Fe(CN)6]Na 2[CaY][PtCl 4(NH 3)2]解配合物 [CoCl 2(NH 3)(H 2 O)(en)]Cl 氧配 化位 数数 Co( +3)6配体数5个,分别为Cl -(2个)、-(2个)、en 、NH 3、H 2O配离子电荷+Na 3[AlF 6]A l(+--33)66个FK 4[Fe(CN)6]Fe(+2) --466个CNNa 2[CaY]C a( +2)61个Y4--2 1[PtCl4(NH3)2] P t(+4)66个,4个Cl -,2个NH304.命名下列配合物,指出中心离子的氧化数和配位数。

第四章(p.96)1. 下列说法是否正确?说明理由。
(1) 凡是盐都是强电解质;(2) BaS04, AgCI难溶于水,水溶液导电不显著,故为弱电解质;(3) 氨水冲稀一倍,溶液中[0H-]就减为原来的一半;(4) 由公式;-K c可推得,溶液越稀,「就越大,即解离出来的离子浓度就越大。
(5) 溶度积大的沉淀都容易转化为溶度积小的沉淀。
(6) 两种难溶盐比较,K sP较大者其溶解度也较大。
答:(1)不正确。
强电解质应在水溶液中能够百分之百的离解。
但有些盐,女口:HgCl2在水溶液中的离解度远达不到百分之百,所以不是强电解质。
(2) 不正确。
溶解在水溶液中的BaSO4, AgCl可以百分之百地离解,所以它们是强电解质。
只是由于它们的溶解度非常小,所以其水溶液的导电性不显著。
(3) 不正确。
氨水在水溶液中产生碱离解平衡:NH3 + H 2O = NH 4+ + OH -当氨水被稀释时,离解平衡将向氨离解度增加的方向移动,所以达到平衡时,溶液中的[OH -]将高于原平衡浓度的1/2。
(4) 不正确。
溶液越稀,离解度:•就越大,但溶液中相应离子的浓度是弱电解质的浓度c和离解度:•的乘积,所以离子的浓度还是会随着c的降低而降低的。
(5) 不正确。
对于不同类型的难溶盐而言,溶度积大的物质未必是溶解度大的物质,严格的讲,应该是溶解度大的物质易于转化溶解度小的物质。
(6) 不正确。
对于相同类型的难溶盐,K sp较大者其溶解度也较大。
对于不同类型的难溶盐,不能直接用溶度积的大小来比较它们的溶解度。
学习参2. 指出下列碱的共轭酸:SO42-, S2-, H2PO4-, HSO「NH3;指出下列酸的共轭碱:NH4+,HCI, HClO 4, HCN, H 2O2。
答:SO42-, S2-, H2PO4-, HSO 4-, NH 3 的共轭酸分别是:HSO,, HS-, H 3PO4, H 2SO4, NH 4+;NH4+, HCI, HCIO 4, HCN, H 2O2 的共轭碱分别是:NH 3, Cl-, CIO4-, CN-, HO 2-。

无机合成参考题无机合成化学参考题1.进行无机合成时,选择溶剂应遵循什么样的原则答:有利于反应进行对人毒性较小对环境污染小不是很贵2.分子筛可以用于纯化与催化反应的原理是什么答:原理:分子筛中有均匀的空隙结构当物质大小与分子筛空隙大小相近时就会透过分子筛进而阻挡一部分物质,达到纯化的目的;分子筛中有许许多多的空腔,空腔内又有许多直径相同的微孔相连,这些微孔能将极性不同,沸点不同,饱和程度不同的分子分离开来就可以达到纯化的作用;分子筛经过质子交换处理后,表面具有丰富的质子酸位,可以在酸催化反应中可以提供很高的催化活性,其孔道结构形成选择性也可催化炼油反应;3.以1 : 1摩尔比的MgO和Al2O3的混合物反应生成尖晶石为例来讨论固体反应过程的影响因素;并解释为什么在实际实验中反应生成两界面以1 : 的比例移动4.精细陶瓷与传统陶瓷有什么区别答:原料:前者使用粘土为主要原料,后者则使用可以在化学组成、形态、粒度和分布精确控制的氧化物、氮化物、硅化物、硼化物、碳化物等为主要原料;成分:前者由粘土产地决定,后者因为是纯化合物由人工配比决定;定制工艺:前者主要是手工来制坯,上釉工艺,以炉窑来生产,后者主要用等静压,注射成型和气相沉积来获得相对精确的和较大密度的坯体,以真空烧结等先进烧结手段;性能:前者主要用来观赏,生活使用,后者则具有高强度、高硬度、耐腐蚀、导电、绝缘以及在磁、电、光、声、生物工程各方面具有的特殊功能在高温机械等领域得到广泛的应用;5.什么叫水热与溶剂热合成,影响水热反应的因素有哪些答:概念:水热与溶剂热合成指在一定温度下100—1000°C和压强1-100MPa条件下利用溶液中物质化学反应来合成材料,重点研究高温和密闭或高压条件下溶液中的化学行为与规律一般在特定类型的密闭容器活高压釜中进行的一类有效的合成方法;影响因素:溶液中的溶剂种类,如水或者非水反应物本身性质温度一般是较低温度压力,pH等反应时间,添加剂,6.溶胶—凝胶合成的原理是什么该合成方法有哪些特点答:原理:一般以无机物或者金属醇盐做前驱体,在液相将这些原料均匀混合,并进行水解,缩合化学反应,在溶液中形成稳定的透明溶胶体系,溶胶经过陈化,胶粒间缓慢聚合,形成三维空间网络结构的凝胶,形成凝胶,再经过干燥,烧结固化制备出分子乃至纳米亚结构的材料;特点:优点:因为起始原料首先被分散在溶剂中形成低粘度溶液所以可以均匀混合得到均匀的材料所制备的原料具有较高的纯度材料组成组分较好控制反应时温度比较低具有流变特性可以控制孔隙度缺点:原料成本较高存在残留小空洞较长反应时间有机溶剂对人有一定的危害性7.离子液体的含义,与传统溶剂相比有哪些优点答:含义:指没有电中心且100%有阴离子和阳离子组成,室温下为液体的物质;优点:有着优异的化学和热力学稳定性,较宽的温度范围,对有机及无机化合物有很好的溶解性,室温下几乎没有蒸汽压,具有良好的导电性,较高的离子迁移和扩散速度,不燃烧,是一种强极性,低配位能力的溶剂;与传统有机溶剂比是一种“绿色溶剂”;8.固,液相反应的主要区别答:固相是非均相的反应,物质之间是直接接触进行反应,反应温度一般低于系统的共熔温度,反应较慢,工艺较简单选择性高;反应分子距离较大;液相反应则是均相反应,反应物质在溶剂中相互作用,溶剂效应,盐效应等物理作用;9.无机膜分离的原理是什么制备无机膜的方法有哪些答:原理:膜两边的物质粒子由于尺寸大小的差异、扩散系数的差异或溶解度的差异等等,在一定的压力差、浓度差、电位差或电化学位差的驱动下发生传质过程,由于传质速率的不同因而造成选择性透过,导致混合物的分离;方法:固态粒子烧结法:无机粉料分散在溶剂中形成悬浮液然后制成有湿粉堆积的膜层,燥和高温焙烧最后得出;溶胶-凝胶法:以金属醇盐及其化合物为原料,在一定条件下进行水解-缩聚反应成凝胶,在干燥,热处理得到材料;相分离法:使用三元相图经温度热处理形成两厢,然后用侵蚀的方法即可得到另一相;化学蒸汽沉积法:是成膜物质以气态进行化学反应,从而在载体上沉积下来;合成法:在多孔载体的孔口合成分子筛膜;10.什么是自蔓延高温合成SHS,关键技术有哪些该方法有什么优点答:概念:利用反应物之间高的化学反应热的自加热和自传导做用来合成材料的一种合成方法;关键技术:制备技术,分为化合法和还原化合法烧结技术,指在燃烧中发生固相烧结致密化技术,包含加压法,挤压法,等静法熔铸技术利用高热性反应物来制备超过产物熔点的燃烧温度焊接技术:在两块材料之间填进合适的燃料进行反应图层技术:熔铸涂层,气相传输涂层优点:节省时间,能源利用充分、设备,工艺简单、产品纯度高产量高、可以很快用于工业生产、能产生新产品11.熔盐有哪些特性熔盐在无机合成中有哪些主要应用答:特征:离子熔体具有很高的导电性使用温度范围比较广泛,较高的热稳定性较低的蒸汽压对物质有较高的溶解能力较大的热容量和热传导值具有化学稳定性主要应用:金属Nd和Nd-Fe合金的制造半导体的制备制造高温超导体单晶及铌酸锂单晶12.试从材料结构方面比较测量纳米材料的XRD小角度XRD与一般块材XRD较高角度的差异在哪里13.铜铬黑CuCr2O4是一种性能优异的无机颜料,先欲获得高质量的铜铬黑粉末,请给出合理的实验方案并说明理由;答:实验方案:采用均匀沉淀法;以尿素为沉淀剂,将硝酸铜硝酸铬加入混合溶液然后沉淀出前驱体,接着抽滤,洗涤,干燥,煅烧成成品;理由:此方法可以使得反应物充分混合,且达到分子级或原子级的混合,使得反应进行比较完全,而且由于这种方法中的缑构晶离子是缓慢的释放出来所以粒子的生长速度可以方便的控制,从而制备的粉体粒度均匀分散性好;14.什么是冷冻干燥法其原理是什么给出一个无机合成的实例,并指出其优缺点;答:概念:将含水物料冷冻懂啊冰点以下,使水转变为冰,然后再较高真空下使冰升华的干燥方法,原理:主要是在水的相律作用下让其冷却升华干燥;实例:制备纳米TiO2多孔材料评价:优点:设备简单,安全性高,成品热稳定性好,热耗较少,缺点:操作关键点不易控制;15.化学热力学,化学动力学以及物质结构等理论对无机合成起怎样的作用请通过具体实例说明;答:化学热力学,主要研究化学反应方向和反应进行程度;如在无机合成中可以判断从理论上反应能否进行;化学动力学,主要研究物质性质随时间变化的非平衡的动态体系;在无机合成中可以加快或减缓反应速率;物质结构理论,主要研究物质组成以及与物质性质的关系;在无机合成中可以指导我们得到物质性质要从组成物质的微观粒子入手;16.高温合成反应实验室中获得高温的方法有哪些答:方法:电阻炉,发热材料有石墨,金属,氧化物等发热材料感应炉,主要是通过感应线圈来涡流发热电弧炉,利用电极电弧产生的高温17.化学气相沉积法有哪些反应类型该法对反应体系有什么要求在热解反应中,用金属烷基化物和金属烷基氧化物作为源物质时,得到的沉积层分别为什么物质如何解释答:类型:热分解反应,化学合成,化学输运反应要求:在沉积温度下反应物应保证足够的压力,除需要的沉积物外,其他反应物应是挥发性的,沉积薄膜本身必须具有足够的蒸汽压;18.微波的概念,微波加热有什么特别之处答:概念:微波指波长足够短,能在发射和接收过程中实际应用波导和谐振技术的电磁波,波长范围为1-1000mm之间;特点:及时性,加热迅速整体性,微波穿透力强选择性,微波只可加热部分材料能量利用高效性,安全无污染,具有杀菌能力19.高压合成反应中获得高压的方法高压合成有哪些优点答:方法:利用外界机械加载方式来获得、利用爆炸来获得优点:合成迅速拓宽了现有物质的相空间可以更快更准确的优化物质性质20.影响晶体生长的外部因素有哪些如何影响答:影响因素:涡流,会使溶液物质供给不均匀,导致形态特征不同温度,生长速度的差异导致形状不同杂质,改变晶体上不同面网表面能,影响晶体形态粘度,粘度增大减少涡流,晶体结晶规则结晶速度,速度快成针状且易引入杂志21.纳米粒子有哪些特性如何防止纳米粒子的团聚答:特性:小尺寸效应,非晶态纳米微粒的颗粒表面层附近原子密度减小,导致声,光等特性出现小尺寸效应表面效应,表面能较高,会使颗粒表面原子数相对增多从而使这些表面原子有较高活性且极不稳定;量子尺寸效应,随着尺寸的减小导致费米能级附近的电子能级有连续变为离散能级,导致纳米晶体材料的光,热等有着显着不同宏观量子隧道效应22.简述低温固相反应的过程及影响因素有哪些答:过程:具有四个过程即扩散-反应-成核-产物结晶粒生长;影响因素:反应物颗粒细度,反应温度,是否添加催化剂,研磨时间等;23.请谈一谈什么是非晶态材料,以及其主要制备方法及应用;答:非晶态材料:是亚稳材料中的一个重要分支,一般通过急冷方式得到,真实的固体且具有固态的基本属性;内部原子排列是及其无序且没有周期性,又称为金属玻璃;主要制备方法:熔液急冷法,熔液碰到金属冷表面而快速凝固;乳化液滴法,可以提高过冷度进而加快冷却速度;固态反应法,利用不同金属固态互相扩散反应来制备非晶材料;主要应用:非晶材料有着很好的各种性能和磁性;主要有非晶催化材料,非晶结构材料, 非晶耐蚀合金;24.在高压下无机化合物会发生哪些变化高压在合成中的作用;答:变化:一种是产物组成成分保持不变,发生了晶体结构的多型相转变,形成了新相物质一种是某种物质体系发生了元素间或不同物质间的化合形成了新化合物,新物质;作用:可以提高反应速率和产物转化率,降低合成温度,缩短合成时间较容易获得单相物质,可以提高结晶度增加物质密度,对称性,配位数的作用一定条件下,促进化合物的分解25.什么是等离子体它有什么特点有几种获得方法等离子合成技术有哪些广泛应用答:等离子体:又叫做电浆,是有部分电子被剥夺后的原子及原子团被电离后产生的正负离子组成的离子化气体状物质;特点:较高的导电率包含两三种不同的粒子,粒子之间相互作用较大具有表面等离激元效应获得方法:北极光,闪电等自然获得;直流弧光放电法,交流工频放点法,高频感应放点法,低气压放电法,燃烧法应用:特征类金刚石表面制造,毫米级厚金刚石片制备研究,合成无机化合物,超纯超细耐高温精细陶瓷材料的合成,金属冶炼,金属材料的表面处理;26.采用重力分离式自蔓延高温合成制备陶瓷内衬复合铜管是一种新型制备方法,简要叙述该方法制备陶瓷内衬铜管的原理及过程;答:原理:利用铝热反应3CuO + 2Al → 3Cu + Al2O 3此反应为放热反应,产生的大量的热可使生成物成液态,在后续冷却过程中,由Al2O3先于Cu凝固,生成物就变为这两者的固体混合物,在离心力的作用下,Cu层紧靠铜管表面,Al2O3在最里层,冷却之后形成了Al2O3陶瓷内衬复合铜管,Cu形成过渡层;过程:将原料混合物化学纯Al,CuO注入铜管,启动离心机并在适当时刻进行燃烧合成,反应结束后停机进行后处理即可得到陶瓷内衬复合铜管;。

无机合成与制备化学习题一,填空题1.等离子体中主要基元反应过程包括、、、2.主族金属有机化合物中金属利用n和np轨道形成构型,由于不同,同周期两端元素易形成,非金属或类金属则形成3.纳米粒子呈现出许多奇异的特性,目前归结于,,,四方面效应。
4.根据固体中连续的化学键作用的分布范围,可将固体分为和两种。
5.制备各种各样的稀土固体材料,常采用和两种方式。
6.固相化学反应种类繁多,经研究发现低热固相化学具有,,,和等独有的规律。
7.真空泵通常采用,,和四个参量来表征其工作特性。
8.高压一般是指压力在0.1-500GPa或者500GPa以上的压力,根据压力作用的时间可将高压分为和两类9.金属有机配合物可采用,,,和等光化学反应进行合成。
10.高温是无机合成的重要手段,实验室中常采用,,等获得高温。
11.金属有机化合物通常指含有的化合物,可分为和两类。
12.凡是有固相参与的化学反应都可称为固相反应。
固相反应可分为,,,和四个阶段。
13.化学转移反应中常采用,和等作为传输剂。
14.光化学反应中反应物分子需要吸收的光子才能激发到激发态,所以光化学反应的比热反应的强15.1946年由于发明超高压装置和在高压物理学领域的突出贡献获得第四十六届物理学奖。
16.晶体的形成是在一定条件下发生的物质相变过程,它可分为和生长两个阶段。
17.粉体的表面修饰和改性常采用,,,和来改变粒子表面的物理化学性质。
18.实际上,沸石的晶体结构并不十分完美,普遍存在和,这两种缺陷可以在合成中得到控制。
19.按反应历程划分,沸石生长过程可以分为,和几个阶段,但在实际情况下这几个阶段并没有十分清楚的界限,是相互重叠的。
20.高温是无机合成的重要手段,为了进行高温无机合成,就需要、、等一些符合不同要求的产生高温的设备和手段。
21.低温技术的发展对推动许多尖端科学技术与学科的发展起到重要作用,在实验室中常采用等作为低温热源。
22.光化学反应的初级反应过程是反应分子吸收光子被激发的过程,其速率只与有关,与无关,表现为零级反应。

第四章(p.96)1.下列说法是否正确?说明理由。
(1)凡是盐都是强电解质;(2)BaSO4, AgCl难溶于水,水溶液导电不显著,故为弱电解质;(3)氨水冲稀一倍,溶液中[OH-]就减为原来的一半;(4)由公式cα可推得,溶液越稀,就越大,即解离出来的离子浓度就越大。
=K aθ(5)溶度积大的沉淀都容易转化为溶度积小的沉淀。
(6)两种难溶盐比较,θK较大者其溶解度也较大。
sp答:(1) 不正确。
强电解质应在水溶液中能够百分之百的离解。
但有些盐,如:HgCl2在水溶液中的离解度远达不到百分之百,所以不是强电解质。
(2)不正确。
溶解在水溶液中的BaSO4, AgCl可以百分之百地离解,所以它们是强电解质。
只是由于它们的溶解度非常小,所以其水溶液的导电性不显著。
(3)不正确。
氨水在水溶液中产生碱离解平衡:NH3 + H2O = NH4+ + OH-当氨水被稀释时,离解平衡将向氨离解度增加的方向移动,所以达到平衡时,溶液中的[OH-]将高于原平衡浓度的1/2。
(4) 不正确。
溶液越稀,离解度就越大,但溶液中相应离子的浓度是弱电解质的浓度c和离解度的乘积,所以离子的浓度还是会随着c的降低而降低的。
(5) 不正确。
对于不同类型的难溶盐而言,溶度积大的物质未必是溶解度大的物质,严格的讲,应该是溶解度大的物质易于转化溶解度小的物质。
(6) 不正确。
对于相同类型的难溶盐,θK较大者其溶解度也较大。
对于不同类型的难sp溶盐,不能直接用溶度积的大小来比较它们的溶解度。
2. 指出下列碱的共轭酸:SO42-, S2-, H2PO4-, HSO4-, NH3;指出下列酸的共轭碱:NH4+, HCl,HClO4, HCN, H2O2。
答:SO42-, S2-, H2PO4-, HSO4-, NH3的共轭酸分别是:HSO4-, HS-, H3PO4, H2SO4, NH4+;NH4+, HCl, HClO4, HCN, H2O2的共轭碱分别是:NH3, Cl-, ClO4-, CN-, HO2-。

第一章概论1现代无机合成的内容和方法与旧时代相比有哪些变化?答:2为什么说无机合成化学往往是一个国家工业发展水平的标志?无机合成化学与国民经济的发展息息相关,在国民经济中占有重要的地位。
工业中广泛使用的三酸两破”,农业生产中必不可少的化肥、农药,基础建设中使用的水泥、玻璃、陶瓷,涂料工业中使用的大量无机料等无一不与无机合成有关。
这些产品的产量和质量几乎代表着一个国家的工业水平。
3.为什么说合成化学是化学学科的核心,是化学家改造世界、创造社会財富的最有力的手段?答:作为化学学科中当之无愧的核心,合成化学已成为化学家改造世界创造未来最有力的工具。
合成化学领域的每一次进步都会带动产业的一次革命。
发展合成化学,不断创造和开发新的物种,不仅是研究结构、性能及其相互关系,揭示新的规律与原理的基础,也成为推动化学学科与相关学科发展的主要动力。
4您能举出几种由p区元素合成的无机材料吗?碳纳米管、5为什么从某种意义上讲,合成化学的发展史就是化学的发展史?6.无机合成有哪些热点领域?(1)特种结构无机材料的制备(2)软化学合成(3)极端条件下的合成(4)无机功能材料的制备(5)特殊聚集态材料的合成(6)特种功能材料的分子设计(7)仿生合成(8)纳米粉体材料的制备(9)组合化学(10)绿色化学。
7.什么是极端条件下的合成?能否举一例说明。
极端条件是指极限情况,即超高温、超高压、超真空及接近绝对零度、强磁场与电场、激光等离子体等。
例如,在模拟宇宙空间的情况下,可能合成出没有位错的高纯度品体。
8查阅文献,找出一例绿色合成原理在无机合成化学中的应用。
9何谓软化学合成方法?与所谓的“硬化学法”相比有什么特点?软化学是相对于硬化学而言的。
它是指在较温和条件下实现的化学反应过程。
特点:1.不需用高纯金属作原料2.制得的合金是有一定颗粒度的粉末,不需在使用时再磨碎3.产品本身具有高活性4.产品具有良好的表面性质和优良的吸放氢性能5.合成方法简单6.有可能降低成本7.为废旧储氢合金的回收再生开辟了新途径第二章低温合成1温度与物性有怎样的关系?什么是物质的第五态?温度与物性的关系:对于一般液体来说,随着温度降低,密度会逐渐增加。
第四章化学键与分子构造增补习题【选择题】1.以下卤化物中,离子键成分大小次序正确的选项是()。
A.CsF>RbCl>KBr>NaI B.CsF>RbBr>KCl>NaFC.RbBr>CsI>NaF>KCl D.KCl>NaF>CsI>RbBr2.以下物质中沸点高低次序正确的选项是()。
A.H2Te>H2Se>H2S>H2O B.H2Se>H2S>H2O>H2Te;C.H2O>H2S>H2Se>H2Te D.H2O>H2Te>H2Se>H2S3.既能权衡元素金属性强弱,又能权衡其非金属性强弱的物理量是()。
A.电负性B.电离能C.电子亲和能D.偶极矩4.Pb2+、Bi3+离子均属何种电子构型()。
A.18B.18+2C.8D.9~175.以下离子型化合物熔点最低的是()。
A.NaF B.BaO C.SrO D.MgO 6.以下各化学键中极性最大的是()。
A.B-Cl B.Ba-Cl C.Be-Cl D.Br-Cl7.以下分子中属于非极性分子的是()。
A.CHCl3B.PCI3C.CO2D.HCl8.以下分子中,空间构型不是直线的是()。
A.CO B.H2O C.CO D.HgCI229.以下说法中错误的选项是()。
A.杂化轨道有益于形成σ键B.杂化轨道均参加成键C.采纳杂化轨道成键,更能知足轨道最大重迭原理D.采纳杂化轨道成键,能提升原子成键能力10.BF4-离子中,B原子采纳的杂化轨道是()。
A.spB.sp2C.sp3D.不等性sp3 11.以下分子中,构型是平面三角形的分子是(A.CO2 B.PCl3)。
C.BCl3D.NH312.以下分子中键角最大的是()。
A.PCl3 B.NH3C.SiCl4D.CO2 13.以下对于杂化轨道理论的说法中正确的选项是()。
第四章1.什么是水热-溶剂热合成?该法有什么特点?有无不足?水热-溶剂热合成是指温度为100~1000 ℃、压力为1MPa~1GPa 条件下利用水溶液中物质化学反应所进行的合成。
水热-溶剂热合成的特点:⑴水热-溶剂热条件下,由于反应物处于临界状态,反应活性会有大大提高,有可能代替固相反应以及难于进行的合成反应;⑵在水热-溶剂热条件下中间态、介稳态及特殊物相易于生成,可用于特种介稳结构、特种凝聚态的新合成产物;⑶能够使低熔点化合物、高蒸气压且不能在融体中生成的物质、高温分解相在此条件下晶化生成;⑷有利于生长极少缺陷、取向好、完美的晶体,且合成产物结晶度高以及易于控制产物晶体的粒度;⑸易于反应的环境气氛,有利于低价态、中间价态与特殊价态化台物的生成,并能均匀地进行掺杂。
不足:⑴由于反应在密闭容器中进行,无法观察生长过程,不直观,难以说明反应机理;⑵设备要求高(耐高温高压的钢材,耐腐蚀的内衬)、技术难度大(温压控制严格)、成本高;⑶安全性能差(我国已有实验室发生“炮弹”冲透楼顶的事故)。
2. 水热-溶剂热合成都有哪些反应类型?⑴合成反应(2)热处理反应(3)转晶反应⑷离子交换反应⑸单晶培育⑹脱水反应⑺分解反应⑻提取反应⑼沉淀反应⑽氧化反应⑾晶化反应⑿烧结反应⒀反应烧结⒁水热热压反应3. 影响水热-溶剂热合成的因素有哪些?反应介质对反应的影响:①压强-温度②填充度③合成溶剂性质的改变4. 水热-溶剂热合成有哪些具体应用?⑴微孔材料的水热-溶剂热合成①沸石与分子筛的骨架结构②几种典型沸石分子筛的合成③空心纳米笼及纳米管制备研究取得新进展⑵纳米粉料的水热-溶剂热合成①纳米氧化物的水热合成②陶瓷纳米材料的水热合成③溶胶-水热合成纳米粉料④有机溶剂热合成纳米粉料⑤特殊结构材料的水热-溶剂热合成⑥无机-有机复合材料的水热-溶剂热合成5. 什么是“空气敏感化合物”?无水无氧操作主要应用在哪些方面?由于许多化合物对于空气中的O2、湿气(水蒸气)和CO2敏感,易与其反应,因此将这些化合物称为“空气敏感化合物”大多数使用该操作手段的是制备金属有机化合物(organometallic compounds),它们是指至少含有一个碳-金属(C-M)键的化合物。
.何谓软化学?他有什么特征?答:通常将在温和条件下进行地反应如先驱物法,水热法,溶胶凝胶法,局部化学反应,流变相反应,低热固相反应称之为软化学.文档来自于网络搜索特点:反应常在交温和地条件下进行.反应过程路径机制易于控制..绿色化学是在什么背景下提出地?它有什么内涵和特点?答:化学物质大规模地生产和广泛使用,使得全球性地生态环境问题日趋严重.在经过千方百计地末端治理效果不佳地情况下,国际社会重新审视已经走过地环保历程,提出了绿色化学地概念.所谓绿色化学又称环境无害化学,环境友好化学,清洁化学,在绿色化学基础上发展地技术称环境友好技术.它地主要特点是“原子经济型”.即在获取新物质地转换过程中充分利用原料中地每个原子,实现化学反应中废物地零排放.文档来自于网络搜索.软化学和绿色化学有哪些异同点?答:绿色化学和软化学关系密切.但又有区别.软化学强调地是反应条件地温和与反应设备地简单.从而达到节能高效地目地.在某些情况下这也是经济洁净地,这与绿色化学是一致地.但在有些情况下,它并没有解决经济洁净地问题.绿色化学是全方位地要求达到高效节能经济洁净,可以预见,软化学和绿色化学将会逐渐统一.文档来自于网络搜索.分别叙述先驱物法和溶胶凝胶法地定义和特点.在何种情况下不宜用先驱物法?( )文档来自于网络搜索答:先驱物法:先驱物法是为了解决高温固相反应中产物地组成均匀性和反应物地传质扩散所发展起来地节能地合成方法.其基本思路是:首先通过准确地分子设计,合成出具有预期组分、结构和化学性质地先驱物,再在软环境下对先驱物进行处理,进而得到预期地材料.先驱物法特点:()混合地均一化程度高()阳离子地摩尔比准确()反应温度低下种情况不宜使用先驱物法:()两种反应物在水中溶解度相差很大()生成物不是以相同地速度产生结晶()常生成过饱和溶液溶胶凝胶法:胶体分散系是分散程度很高地多相体系.溶胶地粒子半径在~间,具有很大地相界面,表面能高,吸附性能强,许多胶体溶液之所以能长期保存,就是由于胶粒表面吸附了相同电荷地离子.由于同性相持使胶粒不易聚沉,因而胶体溶液是一热力学不稳定而动力学稳定地体系.如果在胶体溶液中加入电解质或者两种带相反电荷地胶体溶液相互作用,这种动力学上地稳定性立即受到破坏,胶体溶液就会发生聚沉,成为凝胶.这种制备无机化合物地方法叫做溶胶凝胶法.溶胶凝胶法特点:()通过混合个反应物地溶液,可获得所需要地均相多组分体系()可大幅度降低制备材料和固体化合物地温度,从而可在比较温和地条件下制备陶瓷、玻璃等功能材料.() 利用溶胶或凝胶地流动性,通过某种技术如喷射、浸涂等合成出特殊形态地材料如薄膜、纤维、沉积材料.文档来自于网络搜索.溶胶有什么特点?如何使溶胶成为凝胶?为什么说溶胶体系是热力学上不稳定而动力学上稳定地体系?答:溶胶分散系是分散程度很高地多相体系.溶胶粒子半径在到之间,具有很大地相界面.表面能高,吸附性强,许多胶体溶液之所以能长期保存,就是由于胶粒表面吸附了相同电荷地离子.由于同性相斥使得胶粒不易聚成,因为胶体溶液是一个热力学不稳定而动力学稳定地体系.如果在胶体溶液中加入电解质或者两种相反电荷地胶体溶液相互作用,这种动力学上地稳定性立即受到破坏,胶体溶液就会发生聚沉,成为凝胶.这种制备无机化合物地方法就叫做溶胶凝胶法.文档来自于网络搜索.试述局部化学反应地意义和类型.(答案)意义:局部化学反应也成为拓扑反应或规整化反应.局部化学反应通过反应物地结构来控制反应性,反应前后主体结构大体上或基本上保持不变.类型:脱水反应、分解反应、氧化还原反应、嵌入反应、离子交换反应、同晶置换反应.文档来自于网络搜索.试述低热固相反应地机理、规律和应用.(答案)机理:固相反应地发生起始于两个反应物分子地扩散接触,接着发生键地断裂和重组等化学作用,生成新地化学物分子.此时地生成物分子分散在源反应物中,只有当产物分子聚积形成一定大小地粒子,才能出现产物地晶核,从而完成成核过程.随着晶核地长大,达到一定地大小后出现产物地独立晶相.这就是固相反应经历地扩散、反应、成核、生长四个阶段.规律:潜伏期无化学平衡拓扑化学控制原理分布反应嵌入反应应用:低热固相反应在合成化学中地应用,如在原子簇、新地多酸化合物、新地配合物等方面地应用. 低热固相反应在生产中地应用:低热固相反应在颜料制造业中地应用低热固相反应在制药业中地应用其他地应用,如工业上采用加热苯胺磺酸盐制备对氨基苯磺酸等文档来自于网络搜索.什么叫水热合成法?按反应温度可分为几类?水热合成法有哪些优点和应用前景?高温高压下水热合成法有哪些特征?说明用水热合成法合成水晶地必然性.文档来自于网络搜索(答案)水热合成法:水热法是指在密闭体系中,以水为溶剂,在一定地温度下,在水地自生压强下,反应混合物进行反应地一种方法.按反应温度分类:低温水热法.在100℃以下进行地水热反应中温水热法.在~300℃下进行地水热反应高温高压水热法.在300℃以上,下进行地水热反应优点及前景:该法可制得许多其他方法不能或难以得到地化合物.众多地介稳相可通过水热反应加以合成.这在硅酸盐、硅铝酸盐地合成中是相当常见地,为新相地开发提供了广阔地前景.用这个方法可以开发出更多更好地无机功能材料和各种新型无机化合物.高温高压下水热合成特征:使复杂离子间地反应加速使水解反应加剧使其氧化还原反应电势发生明显变化.用水热合成法合成水晶地必然性:从各种原料要想得到水晶,按一般地思路无非两种方法:一是从水溶液中生长水晶体.由于不溶于水,故此法行不通.二是从熔体中生长水晶体.熔体冷去后一般生成了非晶态固体玻璃,故此法得不到水晶,所以只有用水热法了,这就是用水热法合成水晶地必然性.水晶生长地速度和质量受下列因素地影响:()碱溶液地种类(,)、浓度及原料地填充度.矿化剂一般浓度为~()填充度%~%()生成区地温度~350℃()生成区与溶解区地温度差~80℃()挡板地开孔度()籽晶地结晶方向总地来说,在高温下相应提高填充度和溶液碱浓度可提高晶体地完整性.文档来自于网络搜索.何谓流变态?它涉及哪些领域?答:流变学是研究物质地流动和形变地科学,它是一门介于力学化学物理和工程之间地新兴交叉边缘科学.这里所说地物质既包括流体形态,也包括固体形态地物质.涉及生物流变学,高聚物流变学,食品流变学,土流变学,悬浮体流变学,高分子流变学等分支.文档来自于网络搜索.流变相反应有哪些优点?有哪些应用?答:.在流变相体系中,固体微粒在流体中分布均匀,紧密接触,其表面能够得到有效地利用,反应能够进行地更加充分..能得到纯净单一地化合物,产物和反应容器地体积比非常高.还可以避免大量废弃物地产生,有利于环保,是一种高效节能经济地绿色化学反应..流变热交换良好,传热稳定..在流变相体系中,很多物质会表现出超浓度现象和新地反应特征,甚至可以通过自组装得到一些新型结构和特异功能地化合物..用流变相发硬技术很容易活地纳米材料和非晶态功能材料..采用流变相发应法还可以得到大地单晶.文档来自于网络搜索应用:.用流变相反应法制备芳香酸盐发光材料..用流变相反应法制备复合氧化物..用流变相反应发制备纳米材料..用流变相反应法生长单晶.文档来自于网络搜索第五章(答案在).讨论理论分解电压,超电压,实际分解电压,槽电压之间地关系.答:当外加电源对电池两极所加电压低于这个反电压数值时,电流不能正常通过,电解过程就不能进行.这个最低电压地数值成为理论分解电压.理论分解电压等于反向电压,而实际开始分解地电压往往要比理论分解电压大一些,两者之差为超电压.而实际分解电压高海英包括电解池内溶液电阻产生地电压降.文档来自于网络搜索.试述熔盐地特性,举例说明熔盐在无机合成中地应用:特性:()高温离子熔盐对其他物质具有非凡地溶解能力,一些矿石、难容氧化物、高温难容物质,可望在高温熔盐中进行处理.()熔盐中地离子浓度高,粘度低,扩散快,导电率大,从而使高温化学反应过程中传质、传热速率快,效率高.()金属熔盐离子电极界面间地交流电流特别高,达到~10A(而金属水溶液离子电极界面间地只有~-1A),使电解过程中地阳极氧化和阴极还原不仅可在高温高速下进行,而且能耗低;动力学迟缓过程引起地活化过电位和扩散过程引起地浓差过电位都较低,熔盐电解生产合金时,往往伴随去极化作用.()常用熔盐作为溶剂,用于电解制备金属(水溶液中,电解无法得到).()大多数熔盐在一定温度范围内,具有良好地热稳定性.()熔盐地热容量大,贮热和导热性能好,可用作蓄热剂、载热剂和冷却剂.()熔盐耐辐射,在核工业受到重视和广泛应用.无机合成中地应用:合成新材料()熔盐法或提拉法生长激光晶体.()单晶薄膜磁光材料地制备.()玻璃激光材料地制备.()稀土发光材料地制备.()阴极发射材料和超硬材料地制备.()合成超低损耗地氟化物玻璃光纤预制棒. 非金属元素,地制取在熔盐中合成氟化物合成非常规价态化合物文档来自于网络搜索.说明光化学反应地原理和配位化合物光化学合成地类型.答:光化学合成是指那些用热化学反应难以或者必须在苛刻条件下才能合成地化合物用光化学容易合成地光化学反应.文档来自于网络搜索配位化合物光化学地类型:.光取代反应..光异构化反应..光致电子转移反应..光敏化反应. .说明微波地概念和微波加热地特点.答:微波是哟中频率在到地电磁波.位于电磁波谱地红外辐射和无线电波之间,微波是特殊地电磁波段.不能用在无线电和高频技术中普遍使用地器件来产生.文档来自于网络搜索特点;可以在被加热物体地不同深度同时产生热.也正是这种“体加热作用”,是地加热速度快而且加热均匀.缩短了处理材料需要地时间,节省了能源.文档来自于网络搜索简述自蔓延高温合成地意义和类型.自蔓延高温合成()是材料与工程领域地研究热点之一,也称为燃烧合成.意义(特点):()节能()高效()合成产品纯度高()合成产品成本低()易于从实验转入规模生产()可控制合成产品冷却速率类型直接合成法()热、热合成法:—体系地合成碳化钨地合成陶瓷内衬复合钢管地制备文档来自于网络搜索。
第四章氧化和还原1、在下列两种物质中,分别按Mn,N元素的氧化值由低到高的顺序将各物质进行排列:(1)MnO, MnSO4, KMnO4, MnO(OH), K2MnO4, Mn(2) N2, NO2, N2O5, N2O, NH3, N2H42、指出下列反应中的氧化剂,还原剂以及它们相应的还原,氧化产物。
(1)SO2+ I2 + 2H2O →H2SO4 + 2HI(2)SnCl2 + 2HgCl2→SnCl4 + Hg2Cl2(3) 3I2 + 6NaOH →5NaI + NaIO3 + 3H2O3、用氧化值法配平下列氧化还原反应方程式:(1)Cu + H2SO4 (浓)→CuSO4 + SO2 + H2O(2)KMnO4 + S →MnO2 + K2SO4(3) As2S3+ HNO3 + H2O →H3AsO4 + H2SO4 + NO(4) (NH4)2Cr2O7→N2 + Cr2O3 + H2O(5) P4 + NaOH →PH3+ NaH2PO24、用离子-电子法配平下列氧化还原反应方程式:(1)Cr2O72-+ SO32+ + H+→Cr3+ + SO42-(2) PbO2(s) + Cl- + H+→Pb2+ (实际是PbCl42-) + Cl2(3) H2S + I2→I- + S(4) CrO2- + H2O2 + OH-→CrO42-(5) ClO3- + S2-→Cl- + S + OH-(6) KMnO4+ FeSO4+ H2SO4→MnSO4+ Fe2(SO4)3+ K2SO4 + H2O(7) KI + KIO3 + H2SO4→I2+ K2SO4(8) Ca(OH)2 + Cl2→Ca(ClO) 2 + CaCl2(9) Fe(OH)2 + H2O2→Fe(OH)3(10) Al + NO3-→[Al(OH) 4] - + NH3(11) ClO- + Fe(OH)3→Cl- + FeO42-(12) P + CuSO4→Cu3P + H3PO4 + H2SO45、把镁片和铁片分别放入浓度均为1 mol .L-1的镁盐和亚铁盐的溶液中,并组成一个原电池。
(叶芬霞)无机化学教材习题解答第一章习题一、填空题1.稀溶液的依数性包括蒸气压下降,沸点升高,凝固点降低,渗透现象。
2.引起溶胶聚沉的诸多因素中,最重要的是电解质的聚沉作用。
3.在15℃和97 kPa压力下,15 g氮气所占有的体积为13升。
4.在20℃和97 kPa压力下,0.842 g某气体的体积是0.400 L,这气体的摩尔质量是52.89 g•mol-1。
5.试比较下列溶液的沸点:0.1 mol•L-1蔗糖水溶液= 0.1 mol•L-1NaCl 水溶液= 0.1 mol•L-1Na2SO4水溶液。
6.试比较下列溶液的凝固点:0.1 mol•L-1蔗糖水溶液=0.1 mol•L-1甲醇水溶液= 0.1 mol•L-1苯甲醇水溶液。
7.试比较下列溶液的渗透压:0.1 mol•L-1蔗糖水溶液=0.1 mol•L-1NaCl 水溶液= 0.1 mol•L-1Na2SO4水溶液。
二、选择题1.下列溶液性质中哪一种不是依数性?(D)A. 凝固点B. 沸点C. 渗透压D. 颜色2.在容易聚沉的溶胶中加入适量的大分子物质溶液,以使溶胶的稳定性大大增加,这叫做什么作用?(B)A. 敏化作用B. 保护作用C. 加聚作用D. 聚沉作用3.等体积:0.1 mol•L-1KI和:0.1 mol•L-1AgNO3溶液混合制成的AgI溶胶,下列电解质中,聚沉能力最强的是( C )A. Na2SO4B. MgSO4C. FeCl3D. K3[Fe(CN)6]4.溶胶的基本特征之一是(D)A. 热力学上和动力学上皆稳定的系统B. 热力学上和动力学上皆不稳定的系统C. 热力学上稳定而动力学上不稳定的系统D. 热力学上不稳定和动力学上稳定的系统5.25℃时,0.01mol•kg-1的糖水的渗透压为∏1,而0.01mol•kg-1的尿素水溶液的渗透压为∏2,则(C)A. ∏1<∏2B. ∏1>∏2C. ∏1=∏2D. 无法确定6.当AgNO3的稀溶液与KI的稀溶液作用时,若AgNO3过量时,此溶胶( B )A. 不带电B. 带正电C. 带负电D. 无法确定7.加入下列哪一种溶液,能使As2S3胶体溶液凝聚最快(A)A. Al2(SO4)2B. CaCl2C. Na3PO4D. MgCl28.当不挥发性溶质溶于溶剂形成稀溶液后,则(A )A. 溶剂蒸气压降低B. 溶液的蒸气压升高C. 溶液的蒸气压不变D. 溶液的蒸气压可能升高也可能降低三、是非题1.真实气体在低温高压下可以近似地看作理想气体。
第四章
1.什么是水热-溶剂热合成?该法有什么特点?有无不足?
水热-溶剂热合成是指温度为100~1000 ℃、压力为1MPa~1GPa 条件下利用水溶液中物质化学反应所进行的合成。
水热-溶剂热合成的特点:
⑴水热-溶剂热条件下,由于反应物处于临界状态,反应活性会有大大提高,有可能代替固相反应以及难于进行的合成反应;
⑵在水热-溶剂热条件下中间态、介稳态及特殊物相易于生成,可用于特种介稳结构、特种凝聚态的新合成产物;
⑶能够使低熔点化合物、高蒸气压且不能在融体中生成的物质、高温分解相在此条件下晶化生成;
⑷有利于生长极少缺陷、取向好、完美的晶体,且合成产物结晶度高以及易于控制产物晶体的粒度;
⑸易于反应的环境气氛,有利于低价态、中间价态与特殊价态化台物的生成,并能均匀地进行掺杂。
不足:
⑴由于反应在密闭容器中进行,无法观察生长过程,不直观,难以说明反应机理;
⑵设备要求高(耐高温高压的钢材,耐腐蚀的内衬)、技术难
度大(温压控制严格)、成本高;
⑶安全性能差(我国已有实验室发生“炮弹”冲透楼顶的事故)。
2. 水热-溶剂热合成都有哪些反应类型?
⑴合成反应(2)热处理反应(3)转晶反应⑷离子交换反应⑸单晶培育⑹脱水反应⑺分解反应⑻提取反应⑼沉淀反应⑽氧化反应⑾晶化反应⑿烧结反应⒀反应烧结⒁水热热压反应
3. 影响水热-溶剂热合成的因素有哪些?
反应介质对反应的影响:①压强-温度②填充度③合成溶剂性质的改变
4. 水热-溶剂热合成有哪些具体应用?
⑴微孔材料的水热-溶剂热合成
①沸石与分子筛的骨架结构②几种典型沸石分子筛的
合成③空心纳米笼及纳米管制备研究取得新进展
⑵纳米粉料的水热-溶剂热合成
①纳米氧化物的水热合成②陶瓷纳米材料的水热合
成③溶胶-水热合成纳米粉料④有机溶剂热合成纳米
粉料⑤特殊结构材料的水热-溶剂热合成⑥无机-有机复合材料的水热-溶剂热合成
5. 什么是“空气敏感化合物”?无水无氧操作主要应用在哪些方面?
由于许多化合物对于空气中的O2、湿气(水蒸气)和CO2敏感,易与其反应,因此将这些化合物称为“空气敏感化合物”
大多数使用该操作手段的是制备金属有机化合物(organometallic compounds),它们是指至少含有一个碳-金属(C-M)键的化合物。
6. 无水无氧操作有哪几种具体技术?相比各有什么特点?
7.何谓电解合成?无机化合物的电解合成,有哪些其他合成方法所不及的优点?
电解合成指通过电氧化或电还原过程,在水溶液、熔盐和非
水溶液中的合成。
优点:1.在电解中能提供高电子转移的功能,可以使之达到一般化学试剂所不具有的氧化还原能力;2.合成反应体系及其产物不会被还原剂(或氧化剂)及其相应的氧化产物(或还原产物)所污染;3.由于能方便地控制电极电势和电极的材质,因而可选择性地进行氧化或还原,从而制备出许多特定价态的化合物;4.由于电氧化还原过程的持殊性,因而能制备出其他方法不能制备的许多物质和聚集态。
8.有哪些电解条件影响理想的电解合成?电流效率和能量效率,电流-电压曲线,氢和氧的超电压,电极材料的影响,电极电势的影响,浓度的影响,温度的影响以及金属的电沉积等。
9.电解合成技术有哪些广泛应用?
⑴获得高纯金属⑵新工艺合成碘酸钙的研究⑶电化学合成无机纳米材料⑷特殊价态化合物合成⑸熔盐体系的电化学无机合成⑹非水溶剂中无机化合物的电解合成。