发展甲醇化工的意义及工艺路线分析
- 格式:doc
- 大小:25.00 KB
- 文档页数:5

甲醇生产技术介绍了当前国内外甲醇的主要生产工艺甲醇是一种用途广泛的有机化工产品及重要的基本有机化工原料,应用于有机合成、农药、医药、涂料、染料和国防工业等领域。
随着社会经济的快速增长,能源、环境问题日益突出,甲醇作为燃料应用的比例越来越大。
近20年来,甲醇生产发展很快,技术不断提高,生产规模逐年扩大,生产工艺逐步成熟,各项技术指标不断完善,特别是近年来甲醇汽、柴油的开发和应用,使其作为代用燃料,从技术性、经济性上具有了很强的竞争力。
一、甲醇生产技术发展概况甲醇是传统的化工产品,其生产技术、生产工艺经过几十年的试验研究,特别是近20年来不断发展和创新,在原料路线、生产规模、节能降耗、过程控制与优化及与其他化工产品联合生产等方面都有新的突破和进展。
(一)原料路线甲醇生产的原料大致有煤、石油、天然气、生物秸杆和含H2、CO (或CO2)的工业废气等。
从50年代开始,天然气逐步成为制造甲醇的主要原料,但是,随着能源的紧张,有效地开发煤炭资源,以煤制甲醇的煤气化技术发展迅速,除传统的固定床UGI炉外,固定床鲁奇化炉、流化床温克勒气化炉、气流床K-T炉、气流床德士古气化炉的开发均取得进展,并都在工业上得到使用。
从长远的战略观点来看,世界江的贮藏量远远超过天然气和石油,我国情况更是如此,经过不断的发展和创新,我国已处于世界领先地位。
为适应不同的原料、工艺及规模,我国已开发了多种多样的拥有自主知识产权的系列化技术,可适应无烟煤、烟煤、高硫煤、焦炉气、煤层气等不同原料和中小化肥厂联产、单产和煤矿坑口大型化的不同规模。
(二)生产规模甲醇生产技术发展趋势之一是单系列、大型化。
由于高压设备尺寸的限制,50年代以前,甲醇合成塔的单塔生产能力一般不超过100-200吨/日,60年代不超过200-300吨/日。
但近十几年来,单系列大型甲醇合成塔不断被开发,并在工业生产中使用。
Lurgi管壳型甲醇合成塔单塔能力何达1000-1500吨/日,ICI多段冷激型甲醇合成塔单塔生产能力可达2500吨/日。

甲醇合成的工艺方法发展路线介绍2012-05-12 11:39:02| 分类:煤化工资料|字号订阅甲醇合成是可逆的强放热反应,受热力学和动力学控制,通常在单程反应器中,CO 和CO2的单程转化率达不到100%,反应器出口气体中,甲醇含量仅为6~12%,未反应的CO、CO2和H2需与甲醇分离,然后被压缩到反应器中进入一步合成。
为了保证反应器出口气体中有较高的甲醇含量,一般采用较高的反应压力。
根据采用的压力不同可分为高压法、中压法和低压法三种方法。
自1923年开始工业化生产以来,甲醇合成的原料路线经历了很大变化。
按反应压力分,甲醇合成方法分为:高压法、中压法、低压法。
一、高压法即用一氧化碳和氢在高温(340~420℃)高压(30.0~50.0MPa)下使用锌-铬氧化物作催化剂合成甲醇。
这是八十年代以前世界各国生产甲醇的主要方法。
缺点:高压法生产压力过高、动力消耗大,设备复杂、产品质量较差。
一、低压法即用一氧化碳和氢气为原料在低压(5.0MPa)和275℃左右的温度下,采用铜基催化剂(Cu-Zn-Cr)合成甲醇。
这种方法是70年代实现工业化的合成甲醇方法。
低压法成功的关键是采用了铜基催化剂,铜基催化剂比锌-铬催化剂活性好得多,使甲醇合成反应能在较低的压力和温度下进行。
优点是:铜基催化剂的选择性比锌-铬催化剂好,因此,消耗在副反应中的原料气和粗甲醇中的杂质都比较少。
缺点是:设备体积庞大,生产能力较小,且甲醇合成收率较低。
低压法,目前世界上工业化比较成功的主要有:I.C.I.法合成工艺和鲁奇合成工艺。
三、中压法随着甲醇合成工业的迅速发展,新建厂的规模也日趋大型化,目前已建成投产的装置有日产超过5000吨的。
如果采用低压法搞这样的大型工厂,由于处理气量大,会出现设备庞大而一次性投资高的弊病,以及带来设备制作和运输的困难。
因此在70年代出现了中压法合成甲醇的工艺流程,它是在低压法基础上开发的在5-10MPa压力下合成甲醇的方法,该法成功地解决了高压法的压力过高对设备、操作所带来的问题,同时也解决了低压法生产甲醇所需生产设备体积过大、生产能力小、不能进行大型化生产的困惑,有效降低了建设费用和甲醇生产成本。

甲醇工艺流程
《甲醇工艺流程》
甲醇是一种重要的工业化学品,广泛用于合成化学制品、溶剂、清洁燃料等领域。
甲醇的重要性使得其生产工艺流程备受关注。
甲醇的生产主要通过合成气裂解来实现,合成气由一定比例的一氧化碳和氢气组成,通常由天然气、煤炭或生物质通过气化等方法制备。
合成气经过一系列反应转化成甲醇,工艺流程包括催化裂解、催化合成等环节。
工艺流程的第一步是催化裂解,将一氧化碳和氢气通过催化剂进行转化,生成甲醛和水。
接下来,甲醛再进行加氢反应,生成甲醇。
这两个步骤都是在一定温度、压力和催化剂条件下进行的。
在催化合成环节中,选择合适的催化剂是至关重要的一环。
通常采用的催化剂包括氧化锌、铜、铬等金属氧化物和过渡金属催化剂。
这些催化剂能够促进甲醛和水的加氢反应,有效提高甲醇的产率和纯度。
除了催化裂解和催化合成外,还需要进行一系列的精馏、脱水、除硫等过程,以提高甲醇的纯度和质量。
这些过程也是甲醇工艺流程中不可或缺的一部分。
总的来说,甲醇的工艺流程复杂而严谨,需要精密的控制和高效的催化剂,才能实现高产量、高纯度的甲醇生产。
随着工业
技术的不断发展,甲醇工艺流程也在不断完善和优化,以满足市场需求和环境保护的要求。


化工工艺过程开发及工艺路线选择摘要:化工工艺开发和工艺路线是化工生产的重要组成部分,关系到化工企业的安全生产和连续生产。
本文首先介绍了工艺开发所涉及的程序,然后讨论了化工工艺开发和工艺路线选择。
关键词:化工工艺;过程开发;工艺路线选择引言由于选择原材料的选项、工艺开发的方向和产品的类型非常多样,且有丰富的多样性要素,因此在确定最终工艺开发的方向和路线时,应考虑多方面的各种要素。
在建造一套完整的生产设备时,只要确定其功能方向,就必须在下一个工作流程中仔细考虑如何实现与投资成本和相关方案设计密切相关的工艺开发路线。
所有这些都是为了确保设备的整体效益和效果能够得到优化。
一、工艺开发过程中涉及到的程序一般来说,这项工作的生产过程需要由几个过程组成,如预处理、生成化学反应和物理化学处理。
预处理一般由机械操作、传热等过程组成。
在特定的反应期间,温度和压力值需要保持在一个稳定的水平内。
后续处理包括传质、相分离等过程。
通过选择不同的化学加工方法,可以获得相同的化学产品。
这是由于科学技术的不断发展和进步,使得可以挖掘不同的方案。
在这些计划中,有隐含的社会经济损益,反映了社会效益中的成就,直观地展示了环境保护的水平。
通过此过程,新技术可以在工作期间顺利集成到项目中。
化工技术发展研究的最终结果是基础设计,基础设计是整个项目开发设计的主要参考。
在具体的开发设计过程中,没有完全固定的步骤形式。
二、化工工艺过程开发及工艺路线选择在化工生产中,同一产品有时可以用不同的原料加工。
例如,乙醇可以通过发酵或乙烯水制备;甲烷(天然气)氯化或甲醇和HCl氯化可获得氯甲烷。
同一原料经过不同的加工可以得到不同的产品。
即使使用相同的原材料和相同的工艺,也可以在不同的工艺条件下获得不同的产品。
由于原料路线、工艺路线和产品品种的多样性,在选择工艺路线和确定设计方案时需要考虑许多因素。
在准备投资建设生产工厂时,一旦确定了工厂的生产能力,就必须确定与工厂投资和产品生产成本密切相关的工艺路线和工艺设计条件,以优化工厂的整体经济效益。


解析化工工艺过程开发及工艺路线选择身份证号:摘要:在科学技术不断发展的背景下,化学工业也日益发展。
在化工企业的工作过程中,化工工艺及工艺路线的选择是保证最终生产结果的重要因素。
相关人员应了解化工企业实际情况,积极优化调整化工工艺,开发新工艺路线,更好的保障化工企业的生产安全,实现化工企业可持续发展。
关键词:化工工艺;工艺路线;过程开发引言:由于原材料的选择、工艺发展方向、产品类型非常多样且丰富,因此在选择最终的化工工艺发展方向和路线时必须考虑很多因素。
在建设成套生产设备的过程中,确定了成套生产设备的功能方向后,接下来就必须确定与投资成本和相关方案设计密切相关的工艺发展路径,所有这些都是为了优化工厂的整体效益和效率。
1 工艺开发过程的工作程序一般来说,在化工工艺开发过程中,会涉及到以下工作流程方面,如预处理、化学反应的发生、物理以及化学处理等。
预处理主要包括传热、机械操作等相关工作过程。
在具体的反应过程中,相关人员需要及时调整温度和压力值,保证这些数值在科学合适的范围内。
后续处理主要包括相分离、传质等相关工作流程。
通过选择科学、精密的化学加工方法,可以获得功能齐全的化学产品。
在科技不断进步的背景下,相关技术人员需要制定不同的计划,对不同化学品的生产计划发挥主导作用。
在化工行业的发展规划中,隐含着一定的经济效益,这也直接体现了环境保护的主体作用。
在新技术的实施过程中,要全面开展基础设计工作,积极开展项目开发设计工作,用完整的流程保证产业发展的有效性。
2 工艺技术路线选择的基本原则2.1 可靠性原则一般来说,化工项目工艺技术路线的可靠性需要从工作过程的可行性、可靠、生产安全性、工艺稳定性、生产能力和三废排放能力等多方面因素进行评估。
在可行性研究过程中,相关人员必须充分了解工艺技术线的可靠性,收集相关生产数据,通过对已投入使用的同类产品进行一系列调查分析,从而做出一系列判断,不能仅仅以来根据相关文件或数据。

甲醇的工业生产工艺路线甲醇是一种重要的化工原料和能源之一,广泛应用于合成六氢呋喃、甜味剂、染料、抗凝剂、溶剂、燃料等领域。
其工业生产工艺路线主要分为煤制气法、天然气制气法和生物质加气法三种。
煤制气法是甲醇工业生产的传统工艺路线之一。
其原料为燃烧煤炭后产生的合成气(Syngas),合成气主要由一氧化碳(CO)、二氧化碳(CO2)和氢气(H2)组成。
煤制气工艺主要包括煤气化、气体净化、变换反应和甲醇合成四个步骤。
煤气化是将煤炭等碳质物料在高温下与氧气或蒸汽反应得到合成气的过程。
一般采用固定床气化、流化床气化和煤水浆气化等不同气化方式。
气体净化是将煤气中的硫化物、烟尘和重金属等杂质去除,通常采用吸附和冷凝等方法。
变换反应是将合成气中的一氧化碳和二氧化碳经过催化剂的作用,转化为一氧化碳和水蒸汽再与催化剂反应生成甲醇。
甲醇合成即通过催化剂反应生成甲醇的过程。
天然气制气法以天然气作为原料,通过蒸汽重整、催化裂化或部分氧化等方式得到合成气。
天然气制气工艺与煤制气工艺类似,但相比之下,天然气制气工艺更加简化和高效。
天然气制气法的优点在于天然气资源丰富、气化反应过程较为简单、不会产生固体废弃物等。
生物质加气法是将生物质材料(如植物秸秆、木材废料等)经过碳滴水热解或气化反应得到合成气。
生物质加气工艺具有可再生性和环境友好性的优点,能有效减少温室气体的排放。
此外,生物质加气技术还能实现资源综合利用,如通过副产物的分离和提取制取生物质炭等。
无论是煤制气法、天然气制气法还是生物质加气法,其合成气的组成都需要经过气体净化步骤,以清除杂质对催化剂的毒化作用。
合成气中的一氧化碳和二氧化碳与催化剂经过变换反应,生成甲醇。
而甲醇的合成反应通常在高温和高压下进行,催化剂的选择也对产率和选择性具有重要影响。
目前,常用的催化剂主要为氧化铜催化剂和氧化锌锆催化剂。
总之,甲醇的工业生产工艺路线主要包括煤制气法、天然气制气法和生物质加气法三种。

20万吨/年甲醇的生产技术01生产工艺路线选择1)原料来源生产甲醇的原料为合成气,是指主要成分为H2和CO的气体混合物主要有以下三种制取方式1、天然气制甲醇天然气是制造甲醇的主要原料。
天然气的主要成分是甲烷,还含有少量的其他烷烃、烯烃与氮气。
以天然气生产甲醇原料气有蒸汽转化、催化部分氧化、非催化部分氧化等方法,其中蒸汽转化法应用最广泛。
但是由于天然气大多作为民用燃料,且资源量越来越少,政府已经在07年出台相关规定禁止使用以天燃气为原料生产甲醇。
2、煤、焦炭制甲醇煤与焦炭是制造甲醇粗原料的主要固体燃料。
用煤和焦炭制甲醇的工艺路线包括燃料的气化、气体的脱硫、变换、脱碳及甲醇合成与精制。
用蒸汽与氧气对煤、焦炭进行气化,气化所得可燃性气体即为制造甲醇的初始原料气。
3、油制甲醇油制甲醇主要包括石脑油和重油。
,石石脑油生产甲醇原料气的主要方法是加压蒸汽转化法;以重油为原料制取甲醇原料气有部分氧化法与高温裂解法两种途径。
由于近年来石油消费的不断增长,油供应日趋紧张,石油价格不断上涨,采用石油产品生产大宗化工产品面临着原料枯竭、成本上涨等矛盾。
综上,由于能源结构为缺油、少气、富煤,世界煤资源远远超过天然气和石油储量,随着科技进步,煤制气中的净化手段日益提高以及甲醇需求量的大幅度增加,煤将成为甲醇生产的主要原料。
因此,从长远角度分析,我组决定选用煤制甲醇原料气。
2)催化剂性能,安全丶环保分析,经济分析甲醇的生产方法介绍1、高压法用一氧化碳与氢在高温(340~420℃)高压(30.0~50.0MPa)下用锌-铬氧化物作催化剂合成甲醇。
2、低压法一氧化碳与氢气为原料在低压(5.0MPa)和275℃左右的温度下,采用铜基催化剂合成甲醇。
低压法成功的关键是采用了铜基催化剂,铜基催化剂比锌-铬催化剂活性好得多,是甲醇合成反应能在较低的压力和温度下进行。
3、中压法中压法合成甲醇的工艺流程中,操作压力范围为10.0~27.0MPa,温度为235~315℃。
段落一:引言甲醇是一种重要的有机化工原料和清洁燃料,也是工业生产中广泛应用的化学品之一。
煤制甲醇作为一种非石化甲醇生产方式,具有资源丰富、技术成熟、环保节能等优势,是未来甲醇工业发展的重要方向之一。
本文将从煤制甲醇的原理、技术路线、优缺点、发展趋势、挑战与机遇等多角度对其进行详细介绍。
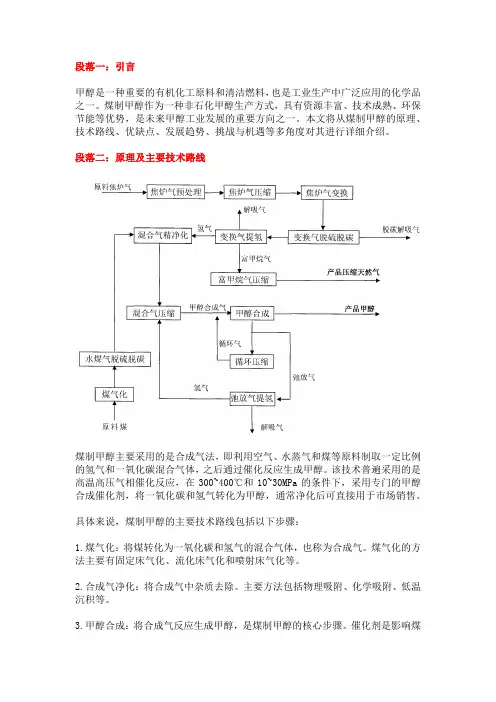
段落二:原理及主要技术路线煤制甲醇主要采用的是合成气法,即利用空气、水蒸气和煤等原料制取一定比例的氢气和一氧化碳混合气体,之后通过催化反应生成甲醇。
该技术普遍采用的是高温高压气相催化反应,在300~400℃和10~30MPa的条件下,采用专门的甲醇合成催化剂,将一氧化碳和氢气转化为甲醇,通常净化后可直接用于市场销售。
具体来说,煤制甲醇的主要技术路线包括以下步骤:1.煤气化:将煤转化为一氧化碳和氢气的混合气体,也称为合成气。
煤气化的方法主要有固定床气化、流化床气化和喷射床气化等。
2.合成气净化:将合成气中杂质去除。
主要方法包括物理吸附、化学吸附、低温沉积等。
3.甲醇合成:将合成气反应生成甲醇,是煤制甲醇的核心步骤。
催化剂是影响煤制甲醇产率和选择性的关键因素,主要包括铜基、锌基和铬基等。
4.甲醇精馏:从合成的混合物中将甲醇纯化出来的过程。
经过2~3级分馏后,可以得到高纯度的甲醇。
总之,煤制甲醇技术路线相对成熟,具有较为明确的分离纯化工艺和催化剂合成技术。
未来,随着科技不断进步,煤制甲醇的生产工艺也会不断创新和完善,以更好地满足市场需求和环保要求。
段落三:优点与传统石化甲醇生产方式相比,煤制甲醇具有以下优点:1.资源丰富:煤作为我国的主要能源来源之一,具有储量丰富、分布广泛的特点,可以为煤制甲醇提供充足的原料保障。
2.技术成熟:煤制甲醇技术在国内外已经经历了数十年的发展和实践,技术路线已经相对成熟,可以提供稳定高效的甲醇生产工艺。
3.环保节能:煤制甲醇生产不仅能够节约石油等化石能源的消耗,还可以降低CO2等温室气体的排放,具有更好的环保效益。

甲醇的生产工艺及其发展现状引言甲醇是一种重要的有机化学品,广泛应用于化工、医药、能源等领域。
本文将探讨甲醇的生产工艺以及其发展现状。
甲醇的生产工艺甲醇的生产主要有两种工艺路线:合成气法和天然气水蒸气重整法。
合成气法合成气法是通过将一定比例的二氧化碳和氢气在催化剂存在下进行反应,生成甲醇。
该工艺需要用到合成气,即一定比例的一氧化碳和二氧化碳混合而成的混合气体。
原料主要来自煤炭、天然气或生物质等资源。
该工艺主要包括以下步骤: 1. 生成合成气:将原料经过预处理后,进入转化器,通过催化剂反应生成合成气。
2. 合成甲醇:将合成气进入甲醇合成塔,在高压和适当温度下,通过催化剂反应生成液态甲醇。
3. 分离纯化:通过蒸馏等工艺,将产物中的杂质和水分去除,得到纯度较高的甲醇。
天然气水蒸气重整法天然气水蒸气重整法是利用天然气中的甲烷进行反应,生成合成气,再通过合成气法制取甲醇。
该工艺相对于合成气法来说,使用的原料更为单一。
该工艺主要包括以下步骤: 1. 水蒸气重整:将天然气经过预处理后,进入重整炉,在催化剂存在下与水蒸气反应生成合成气。
2. 合成甲醇:将合成气进入甲醇合成塔,在高压和适当温度下,通过催化剂反应生成液态甲醇。
3. 分离纯化:通过蒸馏等工艺,将产物中的杂质和水分去除,得到纯度较高的甲醇。
甲醇生产工艺的发展现状随着科技的不断进步和工艺技术的不断创新,在甲醇生产工艺方面也取得了一些进展。
催化剂技术的改进催化剂是甲醇生产中至关重要的一部分,直接影响到反应速率和产物质量。
近年来,研究人员不断改进催化剂的制备方法和组成,以提高甲醇合成反应的效率和选择性。
例如,采用新型催化剂可以降低反应温度和压力,减少能耗,并提高甲醇的纯度。
新工艺的开发除了传统的合成气法和天然气水蒸气重整法外,还出现了一些新型的甲醇生产工艺。
例如,光催化法利用太阳能进行甲醇合成,具有环保、可再生等优点;电催化法利用电能进行甲醇合成,可以实现碳资源高效利用。
甲醇工业的发展方向及应用前景一、简介甲醇是一种重要的有机化工原料,应用广泛,可以用来生产甲醛、合成橡胶、甲胺、对苯二甲酸二甲脂、甲基丙烯酸甲脂、氯甲烷、醋酸、甲基叔丁基醚等一系列有机化工产品,而且还可以加入汽油掺烧或代替汽油作为动力燃料以及用来合成甲醇蛋白。
随着当今世界石油资源的日益减少和甲醇单位成本的降低,用甲醇作为新的石化原料来源已经成为一种趋势。
尽管目前全球甲醇生产能力相对过剩,并且不排除由于某种原因而引起甲醇市场的波动,但是对于有着丰富的煤、石油、天然气资源的地区,除了研究开发新技术降低成本,还要不断开拓甲醇应用领域,大力生产和发展甲醇下游产品,从而促进整个甲醇工业的发展。
二、甲醇下游产品甲醇下游产品种类很多,结合市场需求,发展国内市场紧缺,特别是可以替代石油化工产品的甲醇下游产品,是未来大规模发展甲醇生产,提高市场竞争能力的重要方向。
1、甲醛甲醛是甲醇最重要的下游产品之一,也是最重要的基本有机化工原料之一。
它最大的用途是生产酚醛树脂、黏合剂及其它有机化学晶。
近年来,随着我国经济建设的迅速发展,甲醛产量每年以 4.5%的速度增长,年需原料甲醇100万吨以上。
为满足化工市场的需求,应大力开发以甲醇为原料的生产甲醛的新工艺,以满足优质工程塑料(酚醛树脂)和乌洛托品等合成的需要。
2、甲酸甲酯甲酸甲酯(MF)被誉为万能的中间体,由它衍生出的化学品达几十种。
它是当前C1化学发展的热点,目前国内外广泛采用的大规模生产方法是甲醇羰基化法租甲醇脱氢法。
甲醇羰基化法制甲酸甲酯成本仅为传统酯化法的1/3。
甲酸甲酯可用于生产甲酸、甲酰胺和其他精细化工产品,还可直接用作杀虫剂、杀菌剂、熏蒸剂、烟草处理剂和汽油添加剂,它的需求量将以每年10%的速度递增。
随着环保要求的不断提高,由甲醇、C02和H2合成工艺甲酸甲酯值得关注。
3、甲胺甲胺是一种重要的脂肪胺,以液氨和甲醇为原料,在催化条件下,通过加压精馏分离不同结构的系列产品(一甲胺、二甲胺、三甲胺),是基本的有机化工原料之一,目前全世界年生产能力为112万吨,国内年生产能力为25万吨,全球年消费量为165万吨,年消费递增率为12%。
毕业设计说明书设计题目:年产6万吨甲醇合成工艺设计学院:化学工程学院专业:化学工程与工艺目录第1章概述 (3)1.1甲醇性质 (3)1.2甲醇用途 (3)1. 4甲醇生产原料 (4)第2章工艺流程设计 (5)2.1合成甲醇工艺的选择 (5)2.1.1甲醇合成塔的选择 (6)2.1.2催化剂的选用 (6)2.1.3合成工序工艺操作条件的确定与论证 (6)2.2粗甲醇的精馏 (7)2.2.1精馏原理 (7)2.2.2精馏工艺和精馏塔的选择 (7)2.2.3精馏塔的选择 (8)2.2.4生产工艺参数 (8)第3章 6万吨甲醇工艺的计算 (9)3.1工艺计算 (9)3.2计算基准 (9)3.3 计算过程 (9)第4章6万吨甲醇合成工艺的分析 (10)4.1甲醇合成热力学分析 (10)4.2平衡常数 (11)4.3副反应 (12)4.4甲醇合成催化剂及反应条件 (12)4.1.1催化剂---------------------------------------------------------------12 4.1.2反应条件--------------------------------------------12第5章 6万吨甲醇合成装置物料和能量衡算 (14)5.1甲醇合成回路设计 (14)5.2合成系统物料衡算 (14)5.3合成反应器热量衡算条件-------------------------------16 5.4中间换热器热量衡算-------------------------------------18第6章结论 (20)参考文献 (22)第1章概述1.1甲醇性质甲醇俗称木醇、木精,英文名为methanol,分子式CH3OH。
是一种无色、透明、易燃、有毒、易挥发的液体,略带酒精味;分子量32.04,相对密度0.7914(d420),蒸气相对密度1.11(空气=1),熔点-97.8℃,沸点64.7℃,闪点(开杯)16℃,自燃点473℃,折射率(20℃)1.3287,表面张力(25℃)45.05mN/m,蒸气压(20℃)12.265kPa,粘度(20℃)0.5945mPa•s。
甲醇工艺技术路线甲醇是一种重要的有机化工产品,广泛应用于燃料、化工、医药等领域。
甲醇工艺技术路线主要有两种,一种是自然气甲醇工艺路线,另一种是煤制甲醇工艺路线。
自然气甲醇工艺路线是利用天然气作为原料生产甲醇。
首先,天然气经过脱硫、脱氮等预处理工序,去除杂质。
然后,将净化后的天然气经过催化重整反应转化为合成气,即一氧化碳和氢气。
接着,将合成气经过低温变换催化剂反应生成甲醇。
最后,通过蒸馏、脱水等工序,提纯得到甲醇产品。
煤制甲醇工艺路线是利用煤炭作为原料生产甲醇。
首先,煤炭经过破碎、干燥等预处理工序,使其适于反应。
然后,将煤炭与空气、蒸汽等进行气化反应,产生合成气。
接着,合成气经过一系列的催化反应,如气体净化、变换反应等,生成甲醇。
最后,通过蒸馏、脱水等工序,提纯得到甲醇产品。
这两种甲醇工艺技术路线各有优缺点。
自然气甲醇工艺路线的优点是原料资源丰富,制程技术成熟,产品质量稳定。
然而,它的缺点是生产成本相对较高,对能源消耗较大。
而煤制甲醇工艺路线的优点是原料资源丰富,对能源消耗较少。
但是,它的缺点是煤气化工艺复杂,催化剂寿命较短,设备投资大。
甲醇工艺技术路线的选择主要受原料资源、能源消耗、产品需求等因素的影响。
在天然气资源丰富、价格低廉的情况下,自然气甲醇工艺路线是较为适合的选择。
而在煤炭资源丰富、天然气资源有限的情况下,煤制甲醇工艺路线是较为适合的选择。
未来,随着能源环境的变化,甲醇工艺技术路线也会有所调整和改进。
在绿色、低碳的背景下,绿色甲醇工艺路线将得到更多的关注和发展。
这种工艺路线一般采用生物质、生物制氢等方式生产合成气,进而合成甲醇,具有较小的环境和能源消耗。
未来的甲醇工艺技术路线将更加注重资源循环利用和环境友好性,推动甲醇业的可持续发展。
第一章概述甲醇的用途及在化学工业中的地位甲醇俗称“木精”,是重要的有机化工产品,也是重要的有机化工原料,其分子式为CHOH,是碳化工的基础;甲醇产品除少量直接用于溶剂,抗凝剂和燃料外,绝大多数被用于3生产甲醛,农药,纤维,医药,涂料等;长期以来,人们一直把甲醇作为农药、染料、医药等工业的原料;随着科学技术的不断发展与进步,突破了甲醇只作传统原料的范围,甲醇的应用领域不断地被开发出来,广度与深度正在发生深刻变化;随着甲醛等下游产品的不断开发,甲醇在化学工业中的作用必将越来越重要1;甲醇市场的状况及建厂的可行性近几十年来,由于传统加工工业的发展和世界能源结构的变化,以甲醇为原料的新产品的不断开发,世界对甲醇的生产和需求量都大幅增加,表是世界甲醇市场状况,表是国内甲醇市场状况;表世界甲醇生产能力及消耗量及开工率Table World methyl alcohol productivity and consumption, utilization of capacity 年度1987 1991 1993 1995 2000 2020 生产能力万T/年1999 2300 2470 2600 5000 20000总消耗量万T/年1718 2010 2141 2390开工率 % 86 87 92表国内甲醇生产能力及消耗量Table Domestic methyl alcohol productivity and consumption年度1985 1987 1990 1994 1995 2000 生产能力万T/年69生产量万T/年100消耗量120 200 根据预测,世界范围内的生产与需求将持续发展,主要原因是:甲醇下游产品市场的扩大、甲醇作为燃料的使用将大大增加2;甲醇的性质1.3.1一般性状甲醇蒸汽在空气中的浓度随温度的升高而迅速增大;空气中甲醇蒸汽的最高允许浓度为L;甲醇具有明显的麻醉性,甲醇对呼吸道和粘膜有强烈的刺激作用,流经皮肤也能使人发生中毒迹象3;常温常压下,甲醇是易挥发,易燃的无色液体,具有类似酒精的气味;甲醇能与水任意比混溶,但不能形成共沸物,故可用分馏的方法分离甲醇和水;甲醇是良好的有机溶剂,能溶解多种树脂,但不能溶解脂肪;甲醇蒸汽能与空气形成爆炸性混合物,爆炸极限为~%V,燃烧时为蓝色火焰;甲醇比水轻,有很强的毒性,误饮能导致眼睛失明,甚至死亡;1.3.2甲醇的物理性质①甲醇的物理常数如下表所示表甲醇的物理常数Table Thephysicsdateofmethanol项目数值项目数值沸点64.5℃~64.7℃膨胀系数1/℃凝固点-97℃~-97.8℃表面张力0.00221kg/m20 ℃自燃点473℃~461℃蒸汽压力-44℃相对密度20℃-20℃闪点12℃~16℃0℃粘度液体:20℃气体:65℃10℃ 64.5℃折光系数20 ℃100℃ ②甲醇的热力学常数如下表所示表甲醇的热力学常数Table Thethermo-dynamice date of methanol1.3.3甲醇的化学性质甲醇不具酸性,也不具碱性,对酚酞和石蕊试液均呈中性;分子式CH3OH,分子量;项目数值项目数值临界压力蒸发潜热kg 临界温度240℃液体热容-25℃燃烧热mol25℃气体热容kg77℃①氧化反应完全氧化:CH3OH+23O2→CO2+2H2O+mol不完全氧化:CH3OH+21O2→HCHO+H2O+159kJ/mol②脱氢反应CH3OH→HCHO+mol ③与有机酸反应CH3OH+CH3COOH→CH3COOCH3+H2O④与无机酸反应CH3OH+HCl→CH3Cl+H2OCH3OH+H2SO4→CH3SO2OH+H2O⑤与氨反应生成甲胺CH3OH+NH3→CH3NH2+H2O+mol2CH3OH+NH3→CH32NH+2H2O+mol3CH3OH+NH3→CH33N+3H2O+mol⑥与苯作用生成甲苯CH3OH+C6H6→C6H5CH3+H2O⑦与CO 作用生成醋酸CH3OH+CO→CH3COOH⑧与乙炔作用CH3OH+C2H2→CH3OCHCH2⑨与金属Na作用2CH3OH+2Na→2CH3ONa+H2⑩与苯胺作用,生成二甲基苯胺2CH3OH+C6H5NH2→C6H5NCH32+2H2O甲醇发展历史1661年英国玻义耳BoyIe首次从木材干馏的液体产品中发现了甲醇,木材干馏成了制取甲醇最古老的方法,至今甲醇仍称木醇或木精;1834年,杜马Dumas和彼利哥Peligot 制得甲醇纯品;1857年法国贝特洛Berthelot用一氯甲烷为原料水解制得甲醇;化学合成法生产甲醇开始于1923年;德国巴登苯胺纯碱BASF公司首先建成了一套以为原料、年产300吨的高压法甲醇合成装置,在全世界开拓乐意合成气作为一种CO和H2工业合成原料的生产史;从20世纪20年代到60年代中期,世界各国甲醇合成装置都用高压法,采用锌铬催化剂;合成甲醇的原料路线在几十年中经历了很大变化;20世纪50年代前,甲醇生产多以煤和焦炭为原料,采用固定床气化的方法生产水煤气作为甲醇原料气;50年代以来,天然气和石油资源大量开采,由于天然气便于输送,适合于加压操作,可降低甲醇装置的投资与成本,在蒸汽转化技术发展的基础上,以煤为原料的甲醇生产流程被广泛采用,至今仍为甲醇生产的最主要原料;估计今后在相当长一段时间中,国外的甲醇仍以烃类原料为主;从发展趋势来看,今后以煤炭为原料生产甲醇的比例会上升,这是因为从世界能源结构分析,固体燃料的贮藏量远多于液体与气体,而煤又不能直接用作汽车、柴油机的燃料,必须通过加工为甲醇才能成为汽车、柴油机燃料;煤制甲醇作为液体燃料颇具吸引力,将成为其主要用途之一;由煤生成甲醇被称为煤的间接液化,是煤炭利用的重要方向;生产中的醇/氮比;90年代,上海焦化厂三联供工程中年产20万吨低压甲醇装置的建设和一些省市年产3~10万吨低压甲醇装置的建设,以及许多中、小氮肥厂联醇装且的投产,使我国甲醇生产跃上新的台阶;目前我国有甲醇生产企业200多家,主要集中在几个较大的生产企业,其产能均在10万吨/年左右;2005年1~11月,我国甲醇产量已达到万吨,同比增长%;进口量为万吨,同比增长%,出口量万吨,同比增长%;1~11月国内甲醇表观消费量已达到万吨,同比增长%;照此增长速度,预计全年甲醇产量有望达到570万吨,表观消费量将达到620万吨左右,产量和表观消费量仍呈稳步增加的趋势1;甲醇的生产方法合成甲醇1.5.1由CO和H2在加热压力下,在催化剂作用下合成甲醇;其中包括高压法340~用CO和H2420℃,30~50MPa,用Zn-Cr催化剂;中压法235~275℃,5MPa左右,用Cu-Zn-Al催化剂;低压法220~280℃,5MPa左右,用Cu-Zn-Cr催化剂及联醇220~270℃,10~13MPa;1.5.2其他合成方法①甲烷直接氧化法:在催化剂作用下发生,2CH4+O2→2CH3OH②液化石油气氧化法③煤气氧化法甲醇生产技术的发展趋势近年来,国外甲醇生产技术发展有以下几个趋向:原料路线多样化、生产规模大型化、合成压力从高压转为低压、多采用铜基催化剂、节能降耗,充分利用余热,降低能耗、过程控制自动、联合生产普遍化1第二章低压鲁奇法制甲醇的原理方法及流程反应方程式合成工段,5MPa下铜基催化剂作用下发生一系列反应主反应: CO+2H2→CH3OH+kmol副反应: 2CO+4H2→CH32O+H2O+kmolCO+3H2→CH4+ H2O+kmol4CO+8H2→C4H9OH+3H2O+kmolCO+H2→CO+kmol除副反应中第三个外,副反应的发生,都增大了CO的消耗量,降低了产率,故应尽量减少副反应;合成法反应机理本反应采用铜基催化剂,5MPa,250℃左右反应,清华大学高森泉,朱起明等认为其机理为吸附理论,反应模式为:H2+2e˙→2H˙CO+H→HCO˙HCO˙+H˙→H2CO˙˙H 2CO˙˙+2H˙→CH3OH+3e˙CH3OH˙→ CH3OH+ e˙前两个反应为控制,即吸附控制;由一氧化碳加氢合成甲醇,是一个可逆反应CO+2H2=CH3OH气反应物中有二氧化碳存在时,亦可发生下列反应CO2+3H2= CH3OH+H2O反应热效应:一氧化碳加氢合成甲醇是放热反应,在25℃时反应热△HT=h 常压下不同温度的反应热可按下式进行计算:△HT =+××10-6T3其中△HT—常压下合成甲醇的反应热,J/molT—开氏温度,K由上式计算得到不同温度下的反应表温度与焓值表Table and enthalpy value tables温度 K 298 573 473 573 673 773△H T97平衡常数由一氧化碳加氢合成甲醇的平衡常数Kf 与标准自由焓△θG T关系如下表示:K f =fCH3OH/ fco×fH22 =exp-△θG T/RT其中:△θG T-----标准自由焓T-----反应温度f----- 逸度由上式可以看出平衡常数Kf 只是温度的函数,当反应温度一定时,可以由△θG T值直接求出Kf 值;不同温度的△θG T与K f 值如下表:表温度的△θG T与K f 值表Table Temperatures △θG T and K f value table温度K △θG T J/mol K f温度K △θG T J/mol K f273 -29917 527450 623 51906 ×10-5373 -7367 673 63958 ×10-5473 16166 ×10-3 723 75967 ×10-6523 27925 ×10-2 773 88002 ×10-6573 39892 ×10-4结论:由上表中可以看出,随着温度的升高,自由焓△θG T增大,平衡常数变小,就说明在低温下反应对甲醇合成有用;由一氧化碳加氢合成甲醇,是一个可逆反应CO+2H2=CH3OH气对反应有KP =PCH3OH/PCO×PH22式中PCH3OH、PCO、PH2分别是CH3OH、CO及H2的分压 KN=NCH3OH/NCO×N H22,式中N CH3OH 、N CO 及N H 分别是CH 3OH 、CO 及H 2的摩尔分率 K Y =Y CH3OH /Y CO ×Y H2 ,式中Y CH3OH 、Y CO 及Y H2分别为CH 3OH 、CO 及H 2的逸度;表甲醇合成反应的平衡常数表Table Methyl alcohol building-up reactions balanced chart从表中可以看出不同温度下的平衡常数值,以及不同压力下的K P 和 K N 值,由表中K N 数据可以看出在同一温度下,压力越大K N 值越大,即甲醇平衡产率越高;在同一压力下,温度越高K N 值越小;所以从热力学观点来看,低温高压对甲醇合成有利;若反应温度高,则必须采用高压,才能有足够大的K N 值;降低反应温度,则所需的压力就可相应的降低;但是实际上还要考虑催化剂的活性温度及耐受程度6;铜基催化剂CuO 、ZnO 、Al 2O 3的组合铜基催化剂大多数采用共沉淀法制备,使用需进行还原,使用温度在280℃左右;温度过高会造成其失活;因此使用中应防止温度过大的波动;目前,国内有C-207系,C-301系和CNJ-202系;国外有英国的51-1型,前苏联的CHM-1型和BASF 等;资料显示,每吨催化剂约能生产500~600吨粗甲醇,催化剂成本中,催化剂占5~7%8;温度℃MPaY CH3OH Y CO Y H2 K f K Y K P K N 200×10-2×10-2×10-2×10-2×10-226 97 234 300×10-4×10-4×10-4×10-4×10-4 400×10-5×10-5 ×10-5×10-5×10-52.3.1造气工段 ①对甲醇原料气的要求 合理的氢碳比例要求f=H 2—CO 2/CO+CO 2=~用半水煤气为原料,氢过量,需要补加CO 2以适应以上要求;经脱硫、变换后,尚含有相当量的二氧化碳,CO CO 2之比太高,气体组成不符合=+-222CO CO CO H ~;甲醇合成的要求,而且经变换后,COS 、CS 2等有机硫转化为H 2S,也需在送往甲醇合成工序前预以清除;因此在甲醇生产总流程中必须设置脱除二氧化碳同时也可脱除残余硫化氢的工序,简称脱碳工序;合理的CO 和CO 2比例合成甲醇原料气中应保持一定量的CO 2,能促进铜基催化剂上甲醇合成的反应速率,使用铜基催化剂时原料气中CO 2应大于5%;CO/CO 2>2摩尔比,使放热减少,从而保持铜基催化剂,延长其寿命;原料气对毒物与杂质的要求原料气需净化,除去油,水,尘粒,羰基铁,氯化物,硫化物;其中主要是硫化物的危害较大,其危害大致有造成催化剂中毒、造成管道设备的羰基腐蚀、造成粗甲醇质量下降等,Lurgi 法要求原料气中硫的含量小于10;②造气的工艺流程普遍采用加压操作,同时水蒸气过量,以提高甲烷的转化率,反应温度为 800℃,压力2~3MPa,水/碳摩尔比为 ~;③原料气的净化以煤为原料制甲醇,原料气的净化实际就是一个脱硫的问题,脱硫的方法很多,本设计采用钴钼催化加氢和ZnO 吸收串联脱硫;钴钼催化加氢就是使有机硫化物转变为可被吸收的H 2S ;ZnO 吸收脱硫的实质为: H 2S+ZnO →ZnS+H 2O2.3.2甲醇合成工段 ①甲醇的合成合成工序配置:经过净化的原料气,经预热加压,于5Mpa 、220℃下,从上到下进入Lurgi 反应器,在铜基催化剂的作用下发生反应,出口温度为250℃左右,甲醇7%左右,因此,原料气必须循环,则合成工序配置原则为图;粗甲醇驰放气图合成合序配置原则The Figure Syntheses gathers the foreword disposition principle②甲醇的分离甲醇在高压下容易冷凝,基于这个原理,甲醇的分离采用冷凝分离法,高压下与液相甲醇呈平衡的气相甲醇含量随温度降低,压力增加而下降,表为不同温度下气相甲醇的饱和含量11;表 5MPa下不同温度气相甲醇的饱和含量%Table 5MPa different temperature gas phase methyl alcohol saturated content%T ℃0 10 20 30Y %由表可见,通过水冷水冷后气体温度为30℃左右,可以使气相甲醇含量下降到%5MPa,补充新鲜气后可使这一值下降到%以下,故分离甲醇只要水冷已足够,不需要氨冷,水冷后设分离器,并定期将冷凝下来的甲醇排入粗甲醇贮槽;③气体的循环气体在合成系统内的循环是依靠联合压缩机提供动力以克服流动阻力;④新鲜气的补充和惰性气的排放新鲜气在粗甲醇分离后补充,一般在联合压缩机出口处加入;在合成过程中,未反应的惰性气体累集在系统中,需要进行排放,该气体一般在压缩机前,甲醇分离器后排放6;图甲醇合成的工艺流程Figure Methyl alcohol synthesis technical process1.透平压缩机2.热交换器3.锅炉水预热器4.水冷却器5.甲醇合成塔6.汽包7.甲醇分离器8.粗甲醇贮槽这个流程是德国Lurgi公司开发的甲醇合成工艺,流程采用管壳式反应器,催化剂装在管内,反应热由管间沸腾水放走,并副产高压蒸汽,甲醇合成原料在离心式透平压缩机内加压到以1:5的比例混合循环,混合气体在进反应器前先与反应后气体换热,升温到220℃左右,然后进入管壳式反应器反应,反应热传给壳程中的水,产生的蒸汽进入汽包,出塔气温度约为250℃,含甲醇7%左右,经过换热冷却到40℃,冷凝的粗甲醇经分离器分离;分离粗甲醇后的气体适当放空,控制系统中的惰性气体含量;这部分空气作为燃料,大部分气体进入透平压缩机加压返回合成塔,合成塔副产的蒸汽及外部补充的高压蒸汽一起进入过热器加热到50℃,带动透平压缩机,透平后的低压蒸汽作为甲醇精馏工段所需热源13;第三章 甲醇合成生产工艺计算工艺计算作为化工工艺设计,工艺管道,设备的选择及生产管理,工艺条件选择的主要依据,对平衡原料,产品质量,选择最佳工艺条件,确定操作控制指标,合理利用生产的废料,废气,废热都有重要作用;3.1甲醇合成工艺流程概要合成系统是甲醇厂的核心车间,因为上游的很多工序一长串流程制取的新鲜合成气都是为合成反应要求而配备的,合成技术的变化必然影响全局;若在合成不能充分利用制取甲醇,不论是在物料和能量上都是巨大的损失;合成系统的设备和管路都是在高压下操作,为了安全,防漏,防爆, 对设备的设计和制造,以及生产操作都有很高的要求12;3.1.1甲醇合成流程主线因CO 、H 2 、CO 2在合成塔内反应不能达到平衡且单程转化率很低,出塔气体有大量为未反应的CO 、H 2 、CO 2,甲醇必须分离出系统才可以继续参与循环反应;甲醇合成流程主线方框图如下所示:图甲醇合成流程主线方框图合成分离循环机粗甲醇循环气新鲜气弛放气Figure Methyl alcohol synthesis flow master line block diagram 从图中可以看出主要合成工艺主要是合成,分离,及循环气压缩,三大核心过程组成,更进一步的过程都是在此基础上附加的反应辅助及维持系统的稳定而配备的,例如出塔气换热分离弛放气排放等过程组成;再进一步精细的过程即在此系统附加的仪表监控管道配制等;甲醇合成流程有很多种,但是最基本的步骤单元过程是共同具备的;3.1.2 原则流程简介新鲜气进入新鲜气压缩机,循环气进入循环气压缩机,生至所需压力,两股气体混合后进入塔外换热器与出合成塔的气体进行换热,换热至所需的压力进入甲醇合成塔进行反应,出塔的气体经换热后进入水冷却器,降至醇分所需的温度,并在醇分器中分离出粗甲醇,未反应的气体再次经过排放部分弛放气后,再次进入循环气压缩机增压后再次进行循环操作;由此可见:①甲醇合成流程采用的是循环流程,即分离出产品,未反应的气体再次参与反应,这一点与其他流程不同;②合成系统主要由两部分组成,即甲醇的合成与甲醇分离,前者在合成塔中完成,后者在一系列的传热与汽液分离设备中完成;③合成气流经过设备时,必有阻力,存在压降,使其压力逐渐降低,要其循环必须设循环压缩机升压;3.1.3流程探讨分析①采用循环流程的原因由于平衡和速率的限制,甲醇合成单程转化率很低,约4﹪ ~ 7﹪导致未反应的原料气较多;对甲醇合成而言较好的办法是,分离出甲醇后把未反应的气体返回合成塔重新利用;循环流程之所以必要是有“合成率低”与要求“原料气利用高”二者之间的矛盾是共同决定的;②关于新鲜气补入的位置最有利的位置是在合成塔的进口处,而不宜在合成塔出口或甲醇分离之前,以免甲醇分压降低,减少甲醇收率;循环机放在合成塔之前是最有利的因为在整个循环中,循环机出口压力最大,压力高对合成反应有利;③关于弛放气排放的位置采用循环流程的一个必然结果是惰性气体在系统中的积累;为了维持系统稳定必须排放部分弛放气,因为惰性气体不参与反应 但积累在系统中会降低有效合成气的分压,降低了甲醇合成速率,为此应该设放空管线,防空时应避免尽可能减少有效成分的损失,因此放空位置应选择循环中惰性气体浓度最大的地方,即醇分后应该是合适的9;甲醇生产的物料平衡计算已知 新鲜气中惰性气体含量8%出塔气中惰性气体含量%不含粗甲醇入塔气组分:CO CO 2 H 2 惰性气体% 3% % %粗醇组分摩尔百分比: 甲醇 二甲醚 丁醇 水分 93% % % % 设入塔气2n =100kmol合成塔中:副反应 4CO+8H 2→CH 32CHCH 2OH +3H 2O 2CO+4H 2→CH 32O+H 2O 主反应 CO+2H 2→CH 3OH CO 2+3H 2→CH 3OH+H 2O 以惰性成分为基准:解得 3n =设生成的甲醇为p n kmol,则粗甲醇中其他组分为: 异丁醇CH 32CHCH 2OH二甲醚CH 32O 水份H 2OCO 2生成的水份=p n p n p n p n 生成的甲醇=p n CO 生成的甲醇=p n对进出合成塔的各气体组分列物料平衡方程:则有100×%=3CO x +p n +4×p n +2×p n ①100×3%=23co x +p n ②23H 10061.7%=92.27x 80.003440.008620.9630.044np np np np ⨯+⨯+⨯+⨯+⨯③2233co 3123.3%H CO x xx ++=-④联立①、②、③、④解得p n =,3CO x =%,23co x =%,23H x =%甲醇产量3万吨/年,以8000小时计,则甲醇时产量为h 则入塔气量 V 2=100×3750/32×/=1033463/Nm h 出塔气量 V 3=×V 2=953573/Nm h 令V 1为新鲜气,V 4为循环气以惰性成分为基准:103346×﹪=﹪×V 4 + V 1 ×8﹪ ⑤ 以总物料为基准:103346= V 4 + V 1 ⑥ 联立⑤、⑥,解得 V 1=120823/Nm h V 4=912643/Nm h 驰放气、循环气组分与出塔气的相同,则有: 驰放气V 5=V 3-V 4=95357-91264=40933/Nm h103346×﹪= 91264×﹪+120823CO x ⑦103346×3﹪= 91264×﹪+1208221CO x ⑧103346×﹪= 91264×﹪+ 1208221H x ⑨联立解得:21H x =64%,21CO x =%,3CO x =%水煤气净化过程中,惰性组分流量不变,即V 0惰=V 1惰=V 1×8﹪=9673/Nm h 水煤气 V 0=967/﹪=125303/Nm h V 0 H2S =12530×﹪=3/Nm h 变换反应方程式:CO+H 2O →CO 2+H 2脱碳反应方程式:K 2CO 3+CO 2+H 2O →2KHCO 3 脱碳反应掉的CO2 V co 2脱==3/Nm h0CO V 3129=773220H V ①20CO V +7732-20H V = ② 2210.2%7.72%co co H x x x ++=-- ③12530×20H x = 20H V ④ 12530×0co x =0CO V ⑤ 12530×20co x =20CO V ⑥联立①、②、③、④、⑤、⑥,解得20H V =133103/Nm h 0CO V =47823/Nm h 20CO V =10993/Nm h 20H x =% 0co x =% 20co x =%年产3万吨甲醇物料平衡结果如下表年产3万吨甲醇物料平衡表Table Yearly produces 30,000 ton methyl alcohol balance sheet of materials物料单位组分合计COCO 2 H 2 惰性成分H 2S 水煤气V%100 Nm 3/h96712530 新鲜气V%64 8 100 Nm 3/h12082入塔气V% 3 100Nm3/h 103346 出塔气V% 100Nm3/h 95357 循环气V% 100Nm3/h 91264 驰放气V% 100Nm3/h 4093甲醇h甲醇的能量平衡计算已知:合成塔入塔气为220℃,出塔气为250℃,热损失以5%计,壳层走4MPa的沸水;查化工工艺设计手册得13,4MPa下水的气化潜热为kg,即kg,密度799.0kg/m3,水蒸气密度为19.18kg/m3,温度为250℃;入塔气热容见;表 5MPa,220℃下入塔气除CH3OH热容Table 5MPa,220℃ under enters the tower gas to eliminate CH3OH heat capacity组分流量:Nm3比热:kJ/kmol℃热量:kJ/℃COCO2H2N2ArCH4合计查得220℃时甲醇的焓值为kmol,流量为;所以:Q入=⨯4.2257.1537+⨯==kJ出塔气热容除CH3OH见表表 5MPa,220℃下出塔气除CH3OH热容Table 5MPa,220℃ under tower gas eliminate CH3OH heat capacity 组分流量:Nm3比热:kJ/kmol℃热量:kJ/℃COCO2H2N2ArCH4CH32O合计查得250℃时甲醇的焓值为kmol,流量为 Nm3所以:Q出=⨯4.229.19766+⨯= kJ由反应式得:Q反应=4.2233.18229⨯+4.2262.25⨯+4.22568.211⨯+4.2220204⨯+4.221.2116⨯⨯1000=+++⨯ kJQ热损失=Q入+Q出⨯5%= ⨯5%= kJ所以:壳程热水带走热量Q传= Q入+Q反应-Q出-Q热损失=+= kJ又:Q传=G热水r热水所以:G热水=99.171408.37462156=21843.8 kg/h即时产蒸气:18.198.21843=1138.88 m3第四章主要设备的选型设备是化工工艺运作的载体,选择合适的设备,对于提高生产率,降低原料,能量的消耗有着重要的作用;甲醇合成塔甲醇合成塔是合成甲醇最重要的核心设备,合成工序的“心脏”设备,它的设计好坏直接决定了合成的工艺水平;甲醇合成塔的内件的形式有很多种,在很长一段时间内甲醇合成塔和氨合成塔是共用的;因为二者在反应放热形式是一样的,只是甲醇合成放热量比合成氨大,温度的控制较为不易;下图是典型的三套管甲醇合成塔基本的构成:由简体、催化剂支承装置、换热构件和气体分布器等组成;甲醇合成反应是强放热过程,反应温度较高,可用高压、中压和低压不同的工艺;由于工艺及反应热的移出方法不同,有不同形式的合成塔1;图甲醇合成塔10Figure methyl alcohol synthetic tower1-催化剂 2-筒体 3-冷却管 4-换热器 5-分布器 6-环隙按冷却方法分为直接冷却的冷激式和间接冷却的冷管式及列管式合成塔;冷激式合成塔内部无换热构件,其反应床层分为若干绝热段,两段之间加入冷的原料气使反应气体直接冷却;冷管式合成塔的内部有换热构件,并把双套管置于催化剂层内,由原料气通过管壁间接带走反应热;列管式合成塔的结构类似管壳式换热器,反应热由管外的锅炉给水带走,同时产生高压蒸汽;不管何种类形式的合成塔内件,它的核心是催化剂框,它的设计好坏直接影响了合成塔的产量和消耗定额1;一个好的合成塔内件催化床的设计应有如下的要求:①能有效的移走反应热,合理的控制催化剂床层的温度分布,使其逼近最佳操作温度线,提高醇净值和催化剂的使用寿命②能保证气体均匀地通过催化剂层,阻力小,气体的处理量较大;③充分的利用高压空间,尽可能多装催化剂,提高容积利用系数;④操作稳定灵活,调节方便,能使用各种操作条件的变化;⑤能保证催化剂在升温,还原过程中操作正常,还原充分,尽可能提高催化反应的活性,达到最大的生产强度;⑥结构简单,运转可靠,装卸催化剂方便;甲醇合成塔的形式有很多种,有ICI四段冷激式,Lurgi 型管壳副产蒸汽式,托普索全径向合成塔,国内亦有多种合成塔,GC型轴径冷激式,Lindar均温型合成塔等1;出塔气冷凝器出塔气中含甲醇%加其它未反应气体,通过冷凝器可使出塔气中大部分甲醇和其它产物冷凝下来,以利分离,一般有喷淋式和壳管式,由设计采用管壳式冷凝器15;甲醇分离器甲醇分离器的作用是将经过冷凝器冷凝下来的液体甲醇和未反应气体进行气液分离,分离出的甲醇在液面控制下在分离器底部减压送粗甲醇贮槽;粗甲醇贮槽贮槽的工作压力为,液体以5MPa减压后,溶于粗甲醇中的气体释放出来,以贮罐气的形式在压力控制下经气体排出口排出,贮槽液体出口管上装有液体控制装置;压缩机压缩机的任务是把合成塔来反应的气体送回甲醇合成塔,其动力由高压蒸汽透平提供.结论甲醇合成工艺,流程采用管壳式反应器,催化剂装在管内,反应热由管间沸腾水放走,并副产高压蒸汽,甲醇合成原料在离心式透平压缩机内加压到以1:5的比例混合循环,混合气体在进反应器前先与反应后气体换热,升温到220℃左右,然后进入管壳式反应器反应,反应热传给壳程中的水,产生的蒸汽进入汽包,出塔气温度约为 250 ℃,含甲醇7%左右,经过换热冷却到40℃,冷凝的粗甲醇经分离器分离;分离粗甲醇后的气体适当放空,控制系统中的惰性气体含量;整个设计所采用的低压法Lurgi甲醇合成技术不仅先进而且成熟,投资和操作费用低,操作简便;通过对年产三万吨甲醇整个合成工段的物料衡算、能量衡算;依据所得的计算结果可以对整个合成工段的主要设备进行选型,以确定最后的设备型号,为更好的完成生产任务创造了条件;。
甲醇行业分析报告2022年甲醇行业发展前景及规模分析_智研瞻产业研究院甲醇,甲醇行业分析报告,甲醇市场规模,甲醇行业发展前景相关报告:《中国甲醇行业发展前景与投资战略规划分析报告》中国甲醇行业发展与宏观经济相关性分析甲醇作为清洁燃料,肩负着促进宏观经济可持续发展和提高人民生活质量的重任。
甲醇经济的发展可以带动1万亿以上的GDP,是中国在经济新常态下走向低碳环保社会的最佳路径。
能源是工业命脉,中国石油对外依存度已达70%,远高于50%的能源安全门槛。
中国还向世界承诺减少碳排放。
面对能源短缺和环境压力的双重困难,一方面,相对于含7-13碳的汽油和含14-22碳的柴油,甲醇作为燃料只含1碳,是典型的清洁能源;另一方面,中国利用丰富的煤炭资源开发甲醇替代石油燃料,可以有效保障国家能源安全。
此外,甲醇还具有以下优点。
首先,液体能源具有很大的运输优势,并且拥有最广泛的加氢基础设施。
液态甲醇能很好地与现有的加油站系统兼容,这种平稳过渡的特点,与建设充电站和加氢站相比,投资和难度更低。
此外,既能完美继承现有燃油动力汽车续航里程长、加油方便等优点,又符合绿色环保的发展方向。
其次,甲醇的价格远低于汽油和柴油,并且具有大规模的工业生产能力。
此外,中国的原材料煤炭储量充足,可以减少对外部能源的依赖。
此外,还可以通过可再生生物质制备甲醇,且技术日趋成熟。
微甲醇重整制氢系统再次以甲醇为燃料,与氢燃料电池高度集成,直接发电。
水氢发动机可以作为电动汽车的动力,具有能量转换效率和灵活性。
其转化方式为纯电化学反应,转化效率和环保性均高于直接燃料甲醇。
这是氢能源和燃料电池的有效落地方案。
综上所述,在经济新常态下,甲醇对经济发展的拉动作用尤为重要。
着力拓展甲醇经济新增长点,形成新的发展动力。
因此,建议各级有关部门采取更加有力的措施,促进甲醇经济的发展,带动经济复苏。
中国甲醇行业发展历程上世纪50年代,中国甲醇工业在东北地区诞生。
甲醇工业经过60多年的发展,已成为中国煤化工和精细化工不可缺少的组成部分。
发展甲醇化工的意义及工艺路线分析
【摘要】我们国家的有机化工行业在最近几年来的发展势头非常之好,而甲醇作为煤炭化工当中非常重要的产品,其需求量不但增大,在世界基础有机化工原料的需求排名当中已经位居第四,正是因为这样,就有必要在认识现状的前提之下控制好行业内的发展速度。
【关键词】甲醇行业化工原料工艺路线
1 我们国家发展甲醇化工的意义分析
在我们国家较长的一段时间内,以石油为基础的石油化工及其相应的产品都是国家现代文明发展和进步的重要物质基础,但可以看到的是,地球上的石油资源非常有限,且随着石油资源的大量消耗,到目前为止,在整个世界范围内都已经出现了多次石油危机,使得石油及其制品的价格持续上涨,并较大程度的影响到其他相关行业的健康发展。
基于此,我们开始从能源多元化以及可持续发展的角度来进行思考和分析,认为应当对煤和天然气能源的化工原料技术进行开发和推进,以此来开辟出能源发展的新天地,但考虑到我们国家缺油、少气但煤炭资源丰富,因此就应当集中精力大力发展煤化工,而甲醇正是煤炭化工生产所需要的产品之一。
甲醇是一种非常重要的有机化工原料,在较多行业内都有着广泛的用途和出色的功能,我们国家在石油、天然气的储量上并不突出,煤炭资源相当丰富,与此同时,煤炭行业的下游行业对于甲醇的需求量在最近几年以来始终不断攀升,这甚至在我们国家内掀起了一
股甲醇装置建设的大热潮。
但需要认识到的是,虽然我们国家在甲醇的生产以及应用当中都有着非常好的市场,但还是非常有必要对其行业的长期稳定发展予以适当的控制,在这其中,首先需要做的就是弄清楚我们国家甲醇行业长期发展的经济效应和发展条件,以此来适度发展甲醇工业的重要战略意义。
2 我们国家甲醇行业发展的现状分析
相比于石油或者是天然气,我们国家在煤炭资源的储量上更有优势,且大多数资源都集中在我们国家的西南西北地区,因此这样一些位置也是我们国家化工甲醇企业比较集中的地方。
早在上世纪初期,国外就有公司发明出了高压状态下生产甲醇的方法,随后中压甚至是低压状态下的生产方法也被找到,我们国家是在上世纪中期引入了甲醇的生产方法,并在上述资源丰富地区基于合成氨工业开发出了联产法生产甲醇的工艺,一方面是在工艺路线上有了新的突破,另一方面也较大程度的降低了甲醇生产的成本。
甲醇的合成原料随着我们国家经济条件的发展发生了较大的变化,从原有的煤炭以及焦炭转变成为天然气和重油,这样一种转变最为主要的原因就是因为天然气和重油的使用能够在甲醇合成的环节当中较大程度的降低对环境的污染,并能够相应提高煤炭洁净的利用程度。
事实上,甲醇不仅仅是非常重要的化工原料,同时也是非常理想的能源和车用燃料,在世界能源危机的背景之下,采用甲醇作为替代燃料就能够表现出显著的优势,不仅安全、廉价、燃烧充分,而且在环保方面也有着非常好的表现,正是因为这样,在
汽车能源方面的应用已经在我们国家进行的非常好。
3 我们国家甲醇行业发展过程当中所存在的问题分析
我们国家甲醇行业正在如火如荼的发展,但在此过程当中表现出两个非常重要也是非常关键的问题:一方面就是甲醇行业本身的发展过于迅猛,但可以看到的是,我们国家对于甲醇的需求并没有这样迅猛的势头,更多的是趋近于一种平稳的增长状态。
最近几年来,全世界能源价格都处于上升的状态,相应的化工甲醇项目也处于非常良好的循环趋势之内,但即便是这样,如果只是一味的进行盲目的投资建设就很有可能为企业将来的发展埋下不良隐患,总之,在当前环境条件下,我们仍然要高度关注和重视一些潜在的不利因素。
另一方面就是甲醇成本的不断增加,我们国家在最近几年较短的时间内就相继开发建设了多个甲醇项目,使得甲醇产量节节攀升,而对外的出口数量反而是逐年减少的,正是因为这样,我们国家的甲醇市场主要还是对内,而我们国家甲醇的产地集中在西南西北等地区,经过生产加工之后还需要运输到东北相对发达的市场内,加之甲醇在运输过程当中容易出现挥发、燃烧等问题,就使得甲醇产业不仅增大了风险,还加大了其实际的成本,使得其长期经营的效益都不高。
4 我们国家甲醇行业发展的工艺路线分析
4.1 减少甲醇运输量
甲醇运输量的减少应当同时伴随甲醇行业建设量的增大,甲醇行业内的长途运输确实造成了行业效益的大幅下降,加之中西部地区
内的甲醇消费市场比较局限,因此有必要在减少产品运输量的同时将中西部的甲醇行业迁向下游的延伸产品量,与下游企业建立起长期为稳定的价格协调机制来,这样就能够较大程度避免甲醇生产项目的重复性建设,在避免大起大落造成的不良影响之外较大程度的提高甲醇行业项目的附加价值。
4.2 加强甲醇生产装置的研究
我们国家的甲醇行业在较短的时间内都还很难避免和摆脱国外甲醇行业的冲击,这主要就是因为国外的甲醇生产装置要比我们国家所使用的好的多,而在我们国家甲醇生产装置的条件下,生产规模的增大往往就伴随着能耗率的不断提高,到目前为止,我们国家已经研制出了传统的低压生产装置,与此同时正在进行对液相甲醇装置及工艺的进一步研究,基于此,大的方面有二:一是不断进取面向大型的甲醇装置,二是不断追求国际化最高水平来发展。
4.3 不断提高生产技术水平
随着科学技术的不断发展和经济水平的不断提高,我们国家的甲醇行业在技术以及设备上都已经有了非常可观的进步。
在科学技术上的进步主要表现在多喷嘴对置式水煤浆气化技术和经济型气流床分级气化技术,除此之外还包括精脱硫技术和煤粉加压气化技术,而在装置方面的显著进步则主要体现在甲醇低压合成装置上。
在这样两个方面的不断发展和显著进步之上,我们国家更是实现了甲醇精馏技术和信息自动互化管理技术的完美结合,这样一种技术上的结合,不仅仅极大程度的提高和保证了精馏甲醇的产出质量,
还大大提高了生产过程当中各个环节的实际工作效率。
而煤炭、天然气作为原料的甲醇装置的大型化,同样也是极大程度的提升了我们国家甲醇行业的整体水平和先进程度,使其在发展过程当中越来越接近于世界先进水平。
5 结语
总而言之,我们国家科学技术的不断进步和国民经济的不断发展,确实使得甲醇行业在我们国家有非常好的市场和前景,但同时需要认识到的就是我们国家煤炭石油紧缺所造成的甲醇行业内的问题。
我们所需要做的,就是在认识到甲醇行业所存在问题的基础之上,结合上文当中所提出的分析和建议来尽力改善之,尽可能使得我们国家能够在收获经济效益的同时建设良好社会。
参考文献
[1] 魏双绍.甲醇化工新进展[j].天然气化工,2005(1)
[2] 杨绍斌,王继仁,王志宏.中国煤制甲醇的现状及发展[j].洁净煤技术,2001(4)
[3] 杨恒俊.我国化工甲醇行业现状与发展建议[j].科技资讯,2012(20)。