共轭效应和电子效应
- 格式:ppt
- 大小:4.81 MB
- 文档页数:96

有机化学中的电子效应与取代效应有机化学作为化学的一个重要分支,主要研究碳原子及其化合物的结构、性质和变化规律。
而有机化学中的电子效应与取代效应则是研究有机分子中电子分布和取代基对化合物性质的影响。
本文将着重探讨有机化学中的电子效应和取代效应的特点和应用。
一、电子效应在有机化学中,电子效应是指共轭体系中电子运动或电子密度改变所引起的化学性质变化。
常见的电子效应有共轭效应、杂化效应和亲电性与亲核性。
1. 共轭效应共轭效应是指当有机化合物中存在共轭体系时,电子的运动会影响到整个共轭体系中的化学性质。
一般来说,共轭体系中的π电子可在整个分子上运动,从而引起分子的共轭稳定性和共轭异构体的形成。
典型的共轭体系包括芳香性化合物和共轭双烯等。
共轭效应可以对有机化合物的稳定性、反应性和光学性质产生显著影响。
2. 杂化效应杂化效应是指由于原子轨道杂化的改变,使得有机化合物中的C—C和C—H键的键能、键长和键角等性质发生变化。
杂化效应的经典案例是烷烃和烯烃分子中的σ键和π键的性质差异。
杂化效应对于有机化合物的化学性质和反应机理具有重要的影响。
3. 亲电性与亲核性亲电性和亲核性是指有机化合物中的一种电子云相对于另一种电子云的相对亲和性。
一般来说,具有富电子云的基团属于亲电性较强,而具有亏电子云的基团属于亲核性较强。
亲电性与亲核性的大小决定了基团之间的化学反应类型,如亲电取代反应和亲核取代反应等。
二、取代效应取代效应是指取代基对有机化合物的性质产生的影响。
取代效应可以使分子的稳定性、反应性、溶解度和光学性质发生明显变化。
1. 取代基的电子效应取代基的电子效应主要分为活化效应和稳定效应两种。
活化效应是指取代基提供电子给反应部分,使其具有更强的亲电性或更强的亲核性,从而增强反应活性。
稳定效应则是指取代基通过吸引或推挤电子云,使化合物更加稳定。
2. 取代基的空间效应除了电子效应外,取代基的空间效应对有机化合物的性质也有一定影响。

有机化学中的电子效应电子效应是影响有机化合物反应活性和反应规律的重要因素之一,深入理解有机化学中的电子效应,可以对有机化学的认识由感性向理性方向发展。
电子效应包括诱导效应、共轭效应和超共轭效应;有时三种效应同时存在,表现共同作用的综合结果。
一、诱导效应(Inductive effect )诱导效应是电子效应的一种,是由路易斯(Lewis )首先提出。
路易斯认为,对于有机化合物,诱导效应是由一个电负性较强的原子X 取代了碳原子上的氢原子后,在C -X 键上产生一个极性分布,这个极性分布通过电性诱导作用,在分子中其它键上引起一系列的极性变化,结果在整个分子中产生一个向着X 原子方向的较大范围的电子运动,这种电子运动称为诱导效应:CCδ-电负性比碳弱的元素原子也可以在分子中引起一系列的极性变化,只是所产生的诱导效应的方向刚好相反。
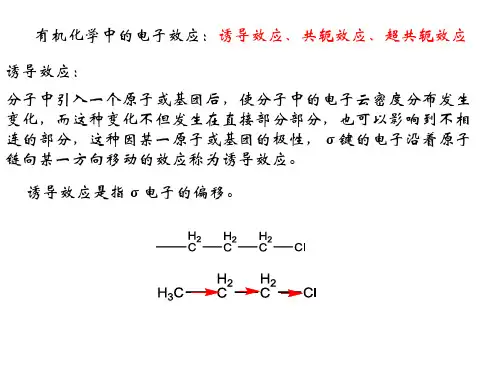
诱导效应是指在有机化合物分子中引入一个基团或原子后,由于原子的电负性差异,导致σ键电子的移动,使分子中的电子云密度分布发生变化,而这种变化不但发生在直接相连的部分,也可以影响到不直接相连的部分。
这种因某一原子或基团的极性而引起电子沿碳链向某一方向移动的效应,称为诱导效应。
如氯丙烷分子中,取代在碳上的氯原子的电负性较强, C -Cl 键产生偶极,使与氯原子连接的第一个碳原子(α-碳原子)产生部分正电荷(δ+),也使第二个碳原子带有部分正电荷,第三个碳原子带有更少的正电荷,依次影响下去。
这种影响的特征是沿着碳链传递,并随着碳链的增长而迅速减弱或消失,一般传递到第三个碳原子就可忽略不计。
诱导效应是一种静电作用,共用电子并不能完全转移到另一原子,只是电子云密度分布发生变化,亦即键的极性发生变化。
δ+ δ+ δ+ δ- CH 3—CH 2—CH 2→Cl1.静态诱导效应(I s )诱导效应分为静态诱导效应和动态诱导效应。
静态诱导效应是由分子本身结构决定的,是分子本身所固有的极化效应,与由极性溶剂或反应试剂等产生的外电场无关。

共轭效应的四种类型
共轭效应是有机化学中的一种重要的电子效应,是指由于共轭系
统的存在而影响周围原子或团的化学性质的现象。
共轭效应通常是由
连续的π键或π键与非共价键相互作用所引起的。
共轭效应有四种类型,分别为:
1.电子给体共轭效应
电子给体共轭效应指含有孤对电子或负离子的官能团对周围π键
的电子密度会产生吸引作用,提高周围π键的电子密度。
例如,酮中
的羰基、酯中的羰基和伯胺中的氨基等都是电子给体共轭效应的典型
例子。
2.电子吸引剂共轭效应
电子吸引剂共轭效应是指对周围π键的电子产生推托作用,使π键的电子密度降低。
例如,苯环上的硝基和甲基等就可以通过电子吸
引剂共轭效应来增强苯环上π键的电子亏损程度。
3.氧自由基共轭效应
氧自由基共轭效应是指氧分子通过与π键的共价键形成氧自由基,从而影响周围π键的电子密度。
例如,芳香醛和苯酚中的-OH官能团
均可以通过氧自由基共轭效应来增强其相邻的π键中的电子亏损程度。
4.碳自由基共轭效应
碳自由基共轭效应是指碳自由基与周围π键形成相互作用,并影响周围π键的电子密度。
例如烯烃中的π键可以通过碳自由基共轭效应来提高自由基的稳定性。


六、电子效应
1共轭效应:单双键交替出现的体系称为共轭体系。
在共轭体系中,由于原子间的相互影响而使体系内的π电子(或P电子)分布发生变化的一种电子效应称为共轭效应。
凡共轭体系上的取代基能降低体系的π电子密度,则这些基团有吸电子的共轭效应,用-C表示。
凡共轭体系上的取代基能增高共轭体系的π电子云密度,则这些基团有给电子的共轭效应,用+C表示。
共轭效应只能在共轭体系中传递,但无论共轭体系有多大,共轭效应能贯穿于整个共轭体系中。
2场效应:取代基在空间可以产生一个电场,对另一头的反应中心有影响,这种空间的静电作用称为场效应,
3诱导效应:因分子中原子或基团的极性(电负性)不同而引起成键电子云沿着原子链向某一方向移动的效应称为诱导效应。
诱导效应的电子云是沿着原子链传递的,其作用随着距离的增长迅速下降,一般只考虑三根键的影响。
诱导效应一般以氢为比较标准,如果取代基的吸电子能力比氢强,则称其具有吸电子诱导作用,用-I表示。
如果取代基的给电子能力比氢强,则称其具有给电子诱导效应,用+I表示。
4超共轭效应:当C-H σ键与π键(或P轨道)处于共轭位置时,也会产生电子的离域现象,这种C-H键σ-电子的离域现象叫做超共轭效应。
在超共轭体系中电子转移的趋向可用弧形箭头表示:超共轭效应的大小,与p轨道或π轨道相邻碳上的C-H键多少有关,C-H键愈多,超共轭效应愈大。

有机反应中的电子效应——有机反应机理作业班级:应用化学101班姓名:祖广权学号:2010014032在有机化学中,分子间中原子间的相互影响一般可以用电子效应和立体效应来描述,其中电子效应主要包括诱导效应和共轭效应。
所谓的电子效应顾名思义,就是通过改变分子中电子云密度的分布来影响分子的理化性质的。
下面我们将对两种相应进行讨论。
一、诱导效应当两个原子形成共价键时,由于原子的电负性不同,使成键电子云偏向于电负性较大的一方,从而形成极性共价键。
而这种极性共价键产生的电场将引起临近价键电荷的偏移。
如:C—F键形成的电场使第二个碳原子也带上部分的正电荷(σσ+),而第三个碳原子带有更小的正电荷(σσσ+)。
在分子中引入一个原子或原子团后,可使分子中电子云密度发生变化,这种变化不仅发生在直接相连的部分,而且沿着分子链影响整个分子的电子云密度分布。
这种因某一原子或原子团的电负性,而引起分子中σ键电子云分布发生变化,进而引起分子性质发生变化的效应叫做诱导效应(inductive effect),通常用I来表示。
例如:溴乙酸的酸性比乙酸的酸性要强,我们可以利用溴原子的诱导效应来解释。
我们知道溴原子的电负性比氢原子的电负性大,吸电子能力比氢原子强,所以在溴乙酸分子中,Br—C键上σ电子向 Br原子方向“偏移”,使C2原子变得带正电性,C2原子再通过C2原子影响O原子,结果在溴乙酸分子中O—H键的σ电子“偏向”O原子,加大了O—H键的极化度,从而有利于氢原子的电离,使酸性较乙酸增强。
显然溴原子的诱导效应是吸电子的。
甲酸的酸性比乙酸强,说明甲基的诱导效应与溴原子是相反的,是推电子的。
我们现在知道,诱导效应有拉电子和推电子之分,那么我们该如何判断一个原子或原子团是拉电子诱导效应还是推电子诱导效应呢?在讨论原子或原子团的诱导效应方向时,我们都以H原子作为比较标准,我们将饱和的H—C键的诱导效应规定为零。
当一个原子或原子团X取代了H—Cabc分子中的H以后,若X—Cabc分子中的Cabc 部分带了部分正电荷(常用σ+来表示)或正电荷增大,则X的诱导效应就是吸电子诱导效应或拉电子诱导效应,用-I表示。
![第3章电子效应[1]](https://uimg.taocdn.com/7f14d8c65fbfc77da269b1fe.webp)

电⼦效应电⼦效应:共轭效应、诱导效应、超共轭效应。
⼀、共轭效应共轭体系: π-π共轭:π键 + π键(双键/三键 + 单键 + 双键/三键)。
例: CH2=CH-CH=CH2(1,3-丁⼆烯):C=C(碳碳双键) + C=C(碳碳双键)π-π共轭。
CH2=CH-CHO(丙烯醛):C=C(碳碳双键) + C=O(碳氧双键)π-π共轭。
CH2=CH-CN(丙烯腈):C=C(碳碳双键) + C≡N(碳氮三键)π-π共轭。
p-π共轭:p轨道 + π键。
多电⼦p-π共轭: 例:CH2=CH-Cl(氯⼄烯):3原⼦4电⼦。
等电⼦p-π共轭: 例:CH2=CH-CH2·(烯丙基⾃由基):3原⼦3电⼦。
缺电⼦p-π共轭: 例:CH2=CH-CH2+(烯丙基碳正离⼦):3原⼦2电⼦。
p-p共轭:p轨道 + p轨道。
例:C=O(羰基)。
共轭效应: 正效应(推电⼦效应/+C效应): 例:C=C(碳碳双键)、-CH3(甲基)。
负效应(吸电⼦效应/-C效应): 例:C=O(碳氧双键)、-CN(氰基)、-NO2(硝基)。
性质: ①共平⾯(sp2)。
②体系能量降低(共轭能/离域能)。
③键长趋于平均化(单键变短,双键变长)。
④正负电荷交替出现。
⑤沿共轭链传递,⼤⼩不变。
⼆、诱导效应共价键:极性共价键(同种元素)、⾮极性共价键(不同种元素)。
元素电负性差越⼤,极性越⼤。
电负性:s > sp > sp2 > sp3。
偶极矩:键偶极矩(键矩)、分⼦偶极矩。
物理意义:描述共价键/分⼦极性⼤⼩的物理量。
定义:电荷中⼼的电荷量与电荷中⼼之间的距离之积。
标⽮性:⽮量。
⼤⼩:µ = qd。
µ:偶极矩。
q:电荷中⼼的电荷量。
d:电荷中⼼之间的距离。
分⼦偶极矩 = 键偶极矩(键矩)的⽮量和。
单位: 国际单位:库·⽶(C·m)。
常⽤单位:德拜(德,D)。

有机化学基础知识点有机物的电子效应和共轭效应有机化学是研究碳元素及其化合物的科学,其中有机物的电子效应和共轭效应是基础知识点之一。
电子效应指的是有机分子中原子轨道电子自身或与其它原子间的相互作用产生的效应,而共轭效应则是指相邻多个π键在共同作用下形成一组共轭体系后的效应。
本文将从电子效应和共轭效应两方面进行讨论。
一、电子效应1. 取代基效应在有机化合物中,原子或基团的取代会对分子的性质产生显著影响。
电子给体(电子供应基团)对有机分子具有+I效应(电子效应),使分子带有正电荷;而电子受体(电子吸引基团)则对有机分子具有-I效应(电子效应),使分子带有负电荷。
举例来说,甲醇(CH3OH)中的羟基(-OH)是一个电子给体,在碳原子上提供了一个富电子密度。
而甲酸(HCOOH)中的羧基(-COOH)是一个电子受体,导致碳原子上的电子云向自身集中,并带有负电荷。
2. 形成共轭体系的电子效应当共轭体系中的π键数量增加时,分子的稳定性和共轭效应会增强。
共轭体系可以通过增加共轭双键、共轭三键或环状结构来形成。
例如,苯(C6H6)是一个具有共轭体系的芳香烃,由6个碳原子和6个氢原子构成的六角形结构。
苯环中的π键相互作用形成了一个共轭体系,使苯分子的稳定性增强。
二、共轭效应1. 共轭体系的形成共轭体系指的是由相邻的不同杂化态碳原子上的π键组成的体系。
这些π键在共轭作用下共享电子,并通过共享电子来稳定整个体系。
共轭体系可以由多个碳原子形成的烯烃类物质、芳香族化合物以及其他具有共轭结构的有机分子中找到。
2. 共轭体系的效应共轭体系的形成影响了分子的反应性、吸收光谱和电子结构等性质。
共轭体系的存在使分子的能带结构发生变化,导致电子能级分布宽度增加,从而使分子的稳定性增强。
共轭体系对于有机分子的化学性质具有重要影响。
例如,共轭体系可以使有机分子的吸收光谱发生位移,使其吸收特定波长的光线。
此外,共轭体系也可以影响有机分子的反应性,使其更容易参与一些特定的反应。

电子效应电子效应分为:诱导效应、共轭效应、超共轭效应 一、诱导效应1概念:有机物分子中,由电负性不同的取代基的影响沿着键链传递,使分子中电子云密度而偏移的效应,用I 表示。
2分类:吸电子诱导效应:电负性大的原子或原子团使分子其余部分的电子云密度降低推电子诱导效应:电负性小的原子或原子团使分子其余部分的电子云密度升高3注意(1)与分子结构有关,永久性的(2)只能沿着σ键传递,随距离增加而迅速减小,一般超过3个σ键不再考虑 (3)只涉及电子云密度的改变,并不造成共用电子对单独属于某一原子的情况 (4)引起键极性的改变,键的极性改变一般是单一方向的,不会产生极性交替的现象 4相对强度(1)通过测定取代酸解离常数确定 (2)测定偶极矩确定 (3)NMR 化学位移确定(化学位移越大,电子云密度越低) ☆5影响取代基诱导效应相对强度的因素 (1)周期律→电负性①同一周期吸电子诱导效应从左向右增加 例 ―CR 3< ―NR 2< ―OR < ―F②同族吸电子诱导效应从上而下降低 例 ―F > ―Cl > ―Br > ―I (2)电荷带正电荷的基团比同类型的不带电荷的基团吸电子能力强得多X C δδδδδδYC C δδδδ带负电荷的基团比同类型的不带电荷的基团给电子能力强得多(3)价键饱和程度不饱和程度高的同种原子吸电子能力强(s 成分越多,碳的电负性越强) 吸电子诱导效应:二、共轭效应 1概念三个或三个以上相邻原子P 轨道相互平行重叠,形成一个大π键,称为共轭体系。
π电子围绕三个或更多的原子运动,称为离域。
电子通过共轭体系传递并引起体系性质改变的效应称为共轭效应,用C 表示。
2基本类型(1)π−π共轭体系 多个饱和键之间的共轭体系(单间与不饱和键相间)(2)p −π共轭体系 不饱和键与相邻原子p 轨道之间的共轭体系3注意(1)共轭效应起源于共轭体系中π电子的高度活动性 例 聚乙炔导电 (2)传到距离:从共轭体系的一端,沿共轭键传递到另一端(3)传递方式:沿着共轭键传递→共轭键电子云密度平均化(键长平均化) (4)极性交替 电子在共轭链中传递时,出现电荷密度高低不同的交替现象C CR CR CR CR CR >>222CH 2CH CH CH 2CH 2CH CHNH CH 2CHCHO CCCH CH 2CCCH CHCCH 2CHN CH 2CHCl 2CH CH 2CHCH 2CHCH 2COX O CO(R)(5)共轭体系中,电子的运动范围扩大,体系的能量降低;共轭体系越大,体系越稳定;共轭结构有利于分子整体结构的稳定。
电子效应:诱导效应、共轭效应、场效应等一.诱导效应1.基础知识存在于不同的原子形成的极性共价键中如:X d- ←A d+在多原子分子中,这种极性还可以沿着分子链进行传递X d- ←A d+ ←B dd+ ←C ddd+Y d+→A d- →B dd- →C ddd-由于原子或原子团电负性的影响,引起分子中电子云沿σ键传递的效应称为诱导效应。
这种效应经过三个原子后其影响就很小诱导效应的方向,是以氢原子作为标准。
用-I表示Y d+ →d-CR3H—CR3 X d- ←d+CR3+I效应比较标准-I 效应+I诱导效应与-I诱导效应相反。
具有+I效应的原子或原子团与碳原子成键后,可使电子云偏向该碳原子。
正诱导效应用+I表示。
例:C H3C H3C CH H常见的具有+I 效应的基团有:―O―>(CH3)3C―>(CH3)2CH―>CH3CH2―>CH3―>D―常见的具有-I效应的基团有:―CN,―NO2>―F >―Cl >―Br >―I >RO―>C6H5―>CH2=CH―一般来说,诱导效应的强弱变化有以下规律:A.同一族的元素随着原子层的增加而吸电子诱导效应降低。
如:—F > —Cl > —Br > —I—OR > —SR—NR2 > —PR2B.同一周期的元素从左到右吸电子诱导效应增加。
如:—F > —OR > —NR2 > —CR3C.不同杂化状态的碳原子以s轨道成分多者吸电子能力强。
(sp>sp2>sp3)反映在基团方向时,如:D.带正电荷的基团具有吸电子诱导效应,带负电荷的基团具有给电子诱导效应。
与硫直接相连的原子,具有共价键,有强的吸电子诱导效应。
上面为静态分子中所表现出来的诱导效应,称静态诱导效应,它仅与键本身的极性有关。
另外,在化学反应中,由于分子受到许多外界条件的影响,例另一分子的影响,其它进攻试剂的影响,溶剂的影响等等。
在外界电场的作用下,分子会发生诱导极化,这种在外界电场影响下在化学反应时才表现出来的诱导效应称为动态诱导效应。
电子效应与有机反应机理导语:有机化学作为化学领域的重要分支,研究有机化合物的合成、性质及其反应机理。
电子效应作为有机反应机理的重要一环,对有机化学的发展起着至关重要的作用。
本文将探讨电子效应在有机反应机理中的应用及其背后的原理。
一、电子效应的基本概念在有机化学中,电子效应描述了电子在有机分子中的分布和运动对反应过程的影响。
具体来说,电子效应可以分为两类:极化效应和共轭效应。
1. 极化效应极化效应是指由于化学键的极性引起的分子内电子密度的不均一分布。
常见的极化效应有电子给体效应和电子受体效应。
电子给体效应是指通过一个原子或官能团将电子提供给另一个原子或官能团,使得其电子密度增加。
例如,氨基官能团中的孤对电子可以提供给邻近的双键碳原子,增加其亲电性,促进亲电性反应的进行。
电子受体效应与电子给体效应相反,是指通过一个原子或官能团吸收周围的电子,使得其电子密度减少。
典型的例子是硝基官能团,它可以通过共轭效应吸引邻近双键碳原子附近的电子,增加其亲核性。
2. 共轭效应共轭效应是指通过共轭体系中的π键和非相邻原子或官能团之间的电荷分布的相互作用产生的电子效应。
通过共轭作用,π键附近的电子可以在共轭体系中自由传递,使得反应更容易进行。
共轭体系由相邻的多个双键或芳香环组成。
典型的共轭体系有共轭二烯、芳香环、烯醇体系等。
共轭效应可以显著影响分子的稳定性、反应速率以及反应产物的形成。
二、电子效应在有机反应中的应用电子效应作为有机反应机理中的基础理论,广泛应用于有机合成和反应设计中。
1. 亲电取代反应亲电取代反应是有机化学中最为常见的反应之一,对于该类反应,电子给体效应和电子受体效应起着关键作用。
以亲电取代反应中的酯化反应为例,酯基中的羰基碳在反应过程中会受到来自亲电试剂的进攻,而电子给体效应将增加酯基碳的亲电性,促进反应的进行。
2. 共轭加成反应共轭加成反应是指在共轭体系中,双键或多键附近的π电子参与到反应中,从而引发新的键形成。