浙教版八下科学第二章知识梳理(部分·精华)
- 格式:xlsx
- 大小:13.15 KB
- 文档页数:1

八下第二章1-3节知识点+练习1.1节模型、符号的建立与作用1、符号:速度v、时间t等,厕所符号、电源符号志等。
符号的作用和意义:用符号能简单明了地表示事物2、模型:一个模型可以是、或,也可以是一个的示意。
模型可以表示很或很的事物,有些模型可以是形象的,而有的模型则是的(如一个数学或科学的)。
运用模型法的科学方法:研究磁感线、光线。
1.2物质与微观粒子模型1、分子在化学变化中是的,而原子是的。
2、物质的构成:在由分子构成的物质中,是保持物质化学性质的最小粒子。
在由原子构成的物质中,是保持物质化学性质的最小粒子。
原子直接构成的物质:、、。
例如:铁的性质是由保持的。
氦气的化学性质是由保持的。
氢气的化学性质由保持3、①构成分子的原子可以是同种原子,也可以是不同种原子。
②同种原子构成不同物质时结构是不一样的,如。
4.粒子的大小与质量组成某个分子的原子,肯定比分子更小,如氢分子由2个氢原子构成,氢原子比氢分子小。
但并不能说原子一定比分子小,某些原子比某些分子大,如铁原子比氢分子大。
1.3原子结构的模型1、原子模型的建立:原子内部结构模型的建立是一个不断完善、不断修正的过程。
历程:道尔顿原子模型(1803年)――模型汤姆生原子模型(1904年)――模型(汤姆生发现原子中有,带负电)卢瑟福原子模型(1911年)―模型(实验:原子核的的很小,很大,带电)波尔原子模型(1913年)――模型电子云模型(1927年—1935年)――电子云模型2、物质构成:原子核的秘密:数= 荷数= 数= 数 所以整个原子不显电性(显电中性) 质量数(A )=质子数(Z )+中子数(N ) 符号表示:R AZ4、原子的质量主要集中在 上,原子核所占的质量很大,但占据的体积很小。
核内质子和中子的质量接近,电子的质量所占的比重极小,几乎可忽略。
5、科学家认为质子和中子是由更小的粒子 构成 8、 的原子――离子:氯化钠是由 构成的。
项目 原子离子表示方法用元素符号表示 钠原子:Na2个钠原子:2Na在元素符号右上角先写电荷数,后标出电性(+,—),例如:氧离子O 2— 2个氧离子2 O 2—数量关系核内质子数 = 核外电子数阳离子:核内质子数 核外电子数 阴离子:核内质子数 核外电子数写出下列符号的含义:Na H Na + 原子的最外层电子数决定了元素的 性质。

第一章粒子的模型与符号1.1节模型、符号的建立与作用1、符号:在生活中,我们经常会用到一些如录音机、随身听上类似的符号来表示事物,我们曾经用过的符号有:速度v、时间t、质量m、密度ρ、压强p、电流I、电压U、电阻R、冷锋、暖锋等,你可以对以前的知识进行归纳总结。
我们生活中,用过的符号有:厕所符号、电源符号、交通标志等。
符号的作用和意义:用符号能简单明了地表示事物用符号可避免由于外形不同引起的混乱用符号可避免表达的文字语言不同而引起的混乱2、模型:建构模型常常可以帮助人们认识和理解一些不能直接观察的到的事物。
一个模型可以是一幅图、一张表或计算机图像,也可以是一个复杂的对象或过程的示意。
模型可以表示很大或很小的事物,有些模型可以是具体形象的,而有的模型则是抽象的(如一个数学或科学的公式)。
1.2物质与微观粒子模型1、分子:分子是保持物质化学性质的一种微粒。
分子在化学变化中是可分的,而原子是不可分的。
2、物质的构成:如右图由原子直接构成的物质:金属、稀有气体、少数非金属的固体如碳、硅。
3、①原子的种类比较多,现在已知的有几百种原子。
不同种类和不同数量的原子就能构成各种不同的分子,从而使自然界中有种类繁多的物质。
它们之间的互相组合就好比是26个英文字母可组合成无数个英文单词一样。
②构成分子的原子可以是同种原子,也可以是不同种原子。
③同种原子构成不同物质时结构是不一样的,如金刚石和石墨。
④原子是一种微粒,具有一定的质量和体积,通常原子半径一般在10-10米数量极,不同种类的原子质量不同,体积也不同。
1.3原子结构的模型1、原子模型的建立:原子内部结构模型的建立是一个不断完善、不断修正的过程。
②历程:道尔顿原子模型(1803年)――实心球模型汤姆生原子模型(1904年)――西瓜模型(汤姆生发现原子中有电子,带负电)卢瑟福原子模型(1911年)―行星绕太阳模型(α粒子散射实验:原子核的存在)波尔原子模型(1913年)――分层模型电子云模型(1927年—1935年)――电子云模型2、物质构成:3、原子核的秘密:质子数=核电荷数=核外电子数所以整个原子不显电性(显电中性)4、原子的质量主要集中在原子核上,原子核所占的质量很大,但占据的体积很小。

(完整版)浙江科学⼋年级下册第⼆章知识点第⼆章微粒的模型与符号⼀、模型、符号的建⽴与作⽤1、模型(1)定义:通过⼀定的科学⽅法,建⽴⼀个适当的模型来反映和代替客观对象,并通过研究这个模型来解释客观对象的形态、特征和本质,这就是模型⽅法。
(2)作⽤:可以帮助⼈们认识和理解⼀些不能直接观察到的或复杂的事物。
模型可以是⼀幅图、⼀张表或计算机图象,也可以是⼀个复杂的对象或过程的⽰意。
2、符号:(1)代表事物的标记(2)符号的作⽤:(1)简单明了地表⽰事物(2)可避免由于事物形态不同引起的混乱(3)可避免由于表达的⽂字语⾔不同引起的混乱注:模型与符号的区分:模型可以反映或代替客观对象;符号只能简单明了的表⽰事物。
⼆、物质与微观粒⼦模型1、分⼦与原⼦的区别和联系1、卢瑟福的α粒⼦轰击⾦箔实验:1、⼤多数α粒⼦穿透⾦箔,且不改变前进⽅向,说明原⼦核很⼩,原⼦中有很⼤的空间2、有⼀⼩部分α粒⼦改变了原来的运动路径,说明原⼦核带正电3、有极少数的α粒⼦好像碰到了坚硬不可穿透的质点⽽被弹了回来,说明原⼦的质量集中在原⼦核上2、第⼀个提出原⼦概念的⼈是道尔顿;第⼀个发现电⼦的⼈是汤姆⽣。
3、原⼦的结构核外电⼦:带负电荷原⼦质⼦:带正电荷原⼦核质⼦数+中⼦数=相对原⼦质量中⼦:不带电荷注:(1)核电荷数=质⼦数=核外电⼦数(2)根据核电荷数(即质⼦数)区分原⼦和元素;(3)在⼀个原⼦核中⼀定含有质⼦不⼀定含有中⼦(如氢元素)(4)同位素:原⼦中核内质⼦数相同,中⼦数不相等的同类原⼦的总称。
四、组成物质的元素1、元素:具有相同核电荷数(即质⼦数)的⼀类原⼦的总称。
注:元素和原⼦的区别2、元素的分类1、⾦属元素2、⾮⾦属元素(包括稀有元素)注:稀有元素:性质⾮常稳定,在通常情况下很难与其他元素或物质发⽣化学反应,在⾃然界的含量稀少的元素3、混合物、纯净物(单质、化合物)混合物:由两种或两种以上物质组成的物质。
(空⽓、海⽔、盐酸)物质单质:由⼀种元素组成的纯净物。


第二章粒子的模型与符号第一节:模型,符号的建立与作用1、使用能简单明了地表示事物,建立可以帮助人们认识和理解一些不能直接观察到的事物。
★下列所出示的代表符号的是,代表模型的是A、地球仪;B、 t;C、ρ;D、细胞模式图;E、地图;F、S=vt;G、W.C;H、 O2★读图:书本P37图2-3液态水与气态水的模型,从中可得:(1)水在状态变化中,水分子其本身(有或没有)发生变化,发生变化的只是分子之间的;(2)态水的水分子之间间隔最大;第二节:物质的微观粒子模型1、英国科学家提出了原子的概念。
利用水分子的电解模型回答下列问题:(1)发现一个水分子通电分裂为个氧原子和个氢原子。
个氧原子重新组合变1个氧分子,个氢原子重新组合变成1个氢分子;(2)化学反应从分子这个角度看,是分子为原子,原子再变成其它新的分子;反应前后分子的种类(发生或不发生)变化,而原子的种类(发生或不发生)变化;(3)从微观角度看,可再分,而不可再分,★所以是化学反应中的最小微粒。
(4)水通电时,水分子最终变成了氢分子和氧分子,它们的化学性质与水分子的化学性质(不同或相同),★所以是保持物质化学性质的最小粒子。
(注:当物质直接由原子构成时,保持物质化学性质的最小粒子就是原子。
)(5)电解水最终变成氢气和氧气,它们的体积比约为,质量比为,这是个变化。
★保持氧气化学性质的最小微粒是,保持铁的化学性质的最小微粒是,保持金刚石化学性质的最小微粒是。
2、物质通常由构成,分子由构成,但有些物质也可以由直接构成的,如、、等。
(注:物质也可能由另一种粒子——离子构成,所以构成物质的微粒有、、三大类)3、自然界中分子种类繁多,分子的种类是由和决定的。
不同种类和不同数量的原子经过不同的组合能构成千万种分子。
构成分子的原子可以是同种原子,如分子,也可以是由不同种原子,如分子;由碳原子直接构成的物质种类有、等,这些由同种原子构成的不同物质性质是不同的,主要原因是构成物质时原子的不同的。


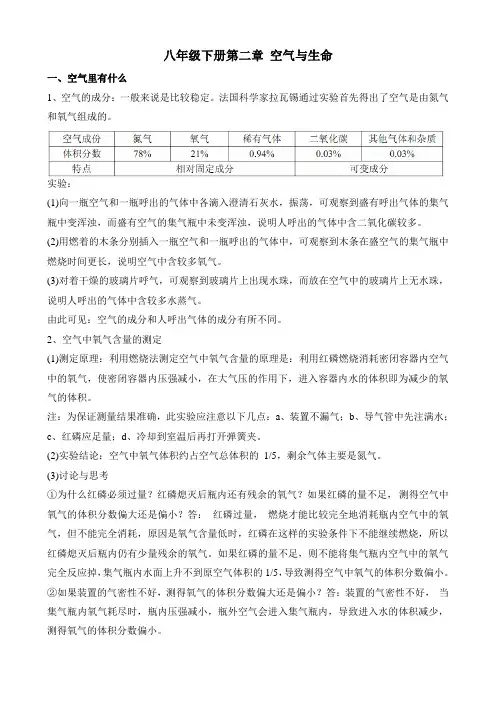
浙江省八年级下册科学第二章知识点总结第2章知识要点:一、空气1、空气是由几种单质和几种化合物组成的混合物。
2、空气的组成:(体积比)氮气:78% 二氧化碳:0.03% 3 、空气的利用。
(1)氮气的用途氮是构成生命体蛋白质的主要元素。
灯泡、食品中作保护气制化肥、炸药、染料等液态氮可作冷冻剂(2)氧气与人类的关系最密切。
氧气的用途:提供呼吸、急救病人、登山、潜水等支持燃烧、气焊、气割、炼钢等(3)用途二、氧气和氧化1、氧气的物理性质:通常情况下是一种无色、无味气体密度比空气大不易溶于水(或难溶于水)三态变化,液态氧、固态氧呈淡蓝色。
_______________________________________ __ _________________________________________ 2、氧气的化学性质:供呼吸、支持燃烧、化学性质较活泼、具有氧化性。
(1)硫在氧气中燃烧:在氧气中燃烧时发岀明亮的蓝紫色火焰,放岀大量的热,生成一种有刺激性气味的(2 )S + 02===SO2 (3 )铁在氧气中燃烧:3Fe+2O2 ==== Fe 304 色固体(注意:铁丝燃烧时要绑一燃烧时火星四射,放岀大量的热,生成一种黑3、氧化反应:物质与氧发生的化学反应。
燃烧:发光发热的剧烈的氧化反应,可引起爆炸缓慢氧化:速率缓慢的氧化反应,可引起自燃4、氧气的制取(1 )①实验室制取实验室常用分解过氧化氢或加热高锰酸钾或加热氯酸钾和二氧化锰混合的方法来制取,反应的化学方程式分别为:稀有气体:化学性质很稳定,通电时能发岀各种有色光。
制作保护气制成各种电光源用于激光技术氧气:21%稀有气体:0.94% 其他气体和杂质0.03% 气体。
(在空气中燃烧时发岀淡蓝色的火焰)根火柴来引燃,瓶底要放点水或细砂防止炸裂瓶底)2H 202 ====2H2O +02 2KMnO 4====K2 MnO4 + MnO2 +02 2KC1O3=======2KCI +302 ②③收集方法(2 )5、催化剂。

第1节模型、符号的建立与作用A.模型1.模型:帮助人们认识和理解一些不能直接观察到的或复杂的事物。
一个模型可以是一幅图、一张表或计算机图像,也可以是一个复杂的对象或过程的示意2.模型方法:通过一定的科学方法,建立一个适当的模型来代替和反映客观对象,并通过研究这个模型来揭示客观对象的形态、特征和本质的方法3.作用:帮助人们认识和理解一些不能直接观察到的或复杂的事物4.水的状态模型:由右侧模型可直接地得出水在状态变化中,没有变成其他物质,构成水的水分子也没有变成其他分子。
在液态水变成气态水的变化中,水分子之间的距离发生了变化B.符号1.定义:代表事物的标记2.意义:简单明了地表示事物,可避免由于事物外形不同和表达的文字语言不同而引起的混乱第2节物质的微观粒子模型A.构成物质的粒子模型1.分子的构成1)一般常用模型来表示分子由原子构成篮球表示氧原子,白球表示氢原子,黑球表示碳原子,棕球表示氮原子,黄球表示硫原子2)构成分子的原子可以是同种原子,也可以是不同种原子2.分子构成物质:在由分子构成的物质中,分子是保持物质化学性质的最小粒子。
例如:水的性质是由水分子保持的。
电解水时,水分子变成了氢分子和氧分子,它们不再保持水的化学性质3.有些物质是直接由原子构成的。
例如:金属铝由铝原子构成、铅笔芯内的石墨由碳原子构成等B.粒子的大小与质量1.分子和原子都有一定的质量和体积1)原子的体积很小,原子半径一般在10—10m数量级2)分子和原子的质量也非常小。
氢分子是最轻的分子,其分子质量的数量级是—27图示2.不同种类的分子和原子质量不同,体积也不同组成某个分子的原子,肯定比分子更小,如氢分子由2个氢原子构成,氢原子比氢分子小。
但并不能说原子一定比分子小,某些原子比某些分子大,如铁原子比氢分子大第3节原子结构的模型A.原子结构模型的建立2.原子的构成原子核(带正电荷)原子核外电子(带负电荷)1)原子呈电中性,原因是原子核与核外电子所带的电量——大小相等,电性相反2)原子核在原子中所占的体积极小,其半径大约是原子半径的十万分之一,但它几乎集中了原子全部的质量3)核外电子在核外空间做高速运动B.揭开原子核的秘密1.原子核的构成1)核电荷数:原子核所带的电荷数2)原子中:核电荷数= 质子数= 核外电子数2.夸克1)质子和中子都是由更微小的基本粒子——夸克构成的2)夸克还可以再分C.带电的原子——离子1.离子1)离子:带电的原子或原子团。
八年级下册第二章空气与生命一、空气里有什么1、空气的成分:一般来说是比较稳定。
法国科学家拉瓦锡通过实验首先得出了空气是由氮气和氧气组成的。
实验:(1)向一瓶空气和一瓶呼出的气体中各滴入澄清石灰水,振荡,可观察到盛有呼出气体的集气瓶中变浑浊,而盛有空气的集气瓶中未变浑浊,说明人呼出的气体中含二氧化碳较多。
(2)用燃着的木条分别插入一瓶空气和一瓶呼出的气体中,可观察到木条在盛空气的集气瓶中燃烧时间更长,说明空气中含较多氧气。
(3)对着干燥的玻璃片呼气,可观察到玻璃片上出现水珠,而放在空气中的玻璃片上无水珠,说明人呼出的气体中含较多水蒸气。
由此可见:空气的成分和人呼出气体的成分有所不同。
2、空气中氧气含量的测定(1)测定原理:利用燃烧法测定空气中氧气含量的原理是:利用红磷燃烧消耗密闭容器内空气中的氧气,使密闭容器内压强减小,在大气压的作用下,进入容器内水的体积即为减少的氧气的体积。
注:为保证测量结果准确,此实验应注意以下几点:a、装置不漏气;b、导气管中先注满水;c、红磷应足量;d、冷却到室温后再打开弹簧夹。
(2)实验结论:空气中氧气体积约占空气总体积的1/5,剩余气体主要是氮气。
(3)讨论与思考①为什么红磷必须过量?红磷熄灭后瓶内还有残余的氧气?如果红磷的量不足,测得空气中氧气的体积分数偏大还是偏小?答:红磷过量,燃烧才能比较完全地消耗瓶内空气中的氧气,但不能完全消耗,原因是氧气含量低时,红磷在这样的实验条件下不能继续燃烧,所以红磷熄灭后瓶内仍有少量残余的氧气。
如果红磷的量不足,则不能将集气瓶内空气中的氧气完全反应掉,集气瓶内水面上升不到原空气体积的1/5,导致测得空气中氧气的体积分数偏小。
②如果装置的气密性不好,测得氧气的体积分数偏大还是偏小?答:装置的气密性不好,当集气瓶内氧气耗尽时,瓶内压强减小,瓶外空气会进入集气瓶内,导致进入水的体积减少,测得氧气的体积分数偏小。
③导管事先未注满水,会引起测量结果如何改变?答:导管未注满水,燃烧冷却后进入的水有一部分留在导管中,所以集气瓶内水的体积减少,故测得氧气的体积减少,测量结果偏低。

第二章微粒的模型与符号一、模型、符号的建立与作用1、模型(1)定义:通过一定的科学方法,建立一个适当的模型来反映和代替客观对象,并通过研究这个模型来解释客观对象的形态、特征和本质,这就是模型方法。
(2)作用:可以帮助人们认识和理解一些不能直接观察到的或复杂的事物。
模型可以是一幅图、一张表或计算机图象,也可以是一个复杂的对象或过程的示意。
2、符号:( 1)代表事物的标记(2)符号的作用:(1)简单明了地表示事物(2)可避免由于事物形态不同引起的混乱(3)可避免由于表达的文字语言不同引起的混乱注:模型与符号的区分:模型可以反映或代替客观对象;符号只能简单明了的表示事物。
二、物质与微观粒子模型1、分子与原子的区别和联系原子分子定义化学变化中的最小粒子在由分子构成的物质中,分子是保持物质化学性质的最小粒子本质区别在化学变化中,原子不可以再分在化学变化中,分子可以再分相同点( 1)质量和体积都很小;( 2)都在不停地做无规则运动 - 分子的扩散运动;( 3)微粒间都有空隙 - 可压缩;( 4)同种微粒性质相同,不同种微粒性质不同;( 5)都能直接构成物质联系原子可以构成分子,分子可以分裂成原子组成物质金属、稀有气体、非金属固体碳、硅氧气、二氧化硫、二氧化碳三氧化铁三、原子结构的模型1、卢瑟福的α 粒子轰击金箔实验:1 、大多数α粒子穿透金箔,且不改变前进方向,说明原子核很小,原子中有很大的空间2 、有一小部分α粒子改变了原来的运动路径,说明原子核带正电3 、有极少数的α粒子好像碰到了坚硬不可穿透的质点而被弹了回来,说明原子的质量集中在原子核上2、第一个提出原子概念的人是道尔顿;第一个发现电子的人是汤姆生。
3、原子的结构核外电子:带负电荷原子质子:带正电荷原子核质子数 +中子数 =相对原子质量注:( 1)核电荷数 =质子数 =核外电子数(2)根据核电荷数(即质子数)区分原子和元素;(3)在一个原子核中一定含有质子不一定含有中子(如氢元素)(4)同位素:原子中核内质子数相同,中子数不相等的同类原子的总称。

八年级下科学知识点整理第一章电与磁1、奥斯特实验:通电导线的周围存在磁场,称为电流的磁效应。
该现象在1820年被丹麦的物理学家奥斯特发现。
该现象说明:通电导线的周围存在磁场,且磁场与电流的方向有关。
2、通电螺线管的磁场:通电螺线管的磁场和条形磁铁的磁场一样。
其两端的极性跟电流方向有关,电流方向与磁极间的关系可由安培定则(也叫右手螺旋定则)来判断。
判断通电直导线周围磁感线环绕方向的方法:A:通电直导线中的安培定则(安培定则一):用右手握住通电直导线,让大拇指指向电流的方向,那么四指的指向就是磁感线的环绕方向;它同样也适用于判断通电螺线管的南北极;B:通电螺线管中的安培定则(安培定则二):用右手握住通电螺线管,使四指弯曲与电流方向一致,那么大拇指所指的那一端是通电螺线管的N极。
通过比较我们可以得出,这两种安培定则的话实际上都可以说成是右手螺旋定则,只不过四指环绕方向分别代表磁感线方向和电流方向;而拇指方向则代表电流方向和通电螺线管的N极方向。
为了方便理解,我们可以总结为:四指弯曲方向为环绕方向,大拇指所指方向为通电直导线中的电流方向或者通电螺线管的N极方向。
3、电磁铁:带铁芯的通电螺线管就是电磁铁。
原理:利用电流来控制电磁铁的磁性。
接通螺线管中的电流,电磁铁产生磁性;断开电磁铁中的电流,电磁铁就没有磁性。
应用:电铃、电磁继电器、电磁选矿机、电磁起重机、磁悬浮列车等。
4、电磁继电器:由电磁铁控制的自由开关。
作用:利用电磁继电器可用低电压和弱电流来控制高电压和强电流。
实质:利用一个接低压电源的通电螺线管(控制电铃)控制由磁铁制成的开关的断开与闭合,从而达到控制高压电路(工作电路)的目的。
5、直流电动机:【问题】怎样使线圈在转过平衡位置后继续沿原来的方向转动下去?1. 直流电动机靠直流电源供电,是利用通电线圈在磁场里受到力的作用而转动的现象制成的,是把电能转化为机械能的装置。
2. 直流电动机主要由磁铁和线圈组成,此外还有换向器、电刷等。
浙教版八年级科学下册思维导图(全册)第1章电和磁思维导图目录电和磁节节节节节节一P1 2 3 4 56 7M H指南针为什么能指方向 电生磁 电磁铁的应用 电动机 磁生电 家庭电路 电的安全使用编十"*0 ■< ■J — * "恤 f勁电动机Cg ]电GR 铁的应用圖1BE休上磁性最强的部位H If理N祀険决淇*同名拠相互抖E斥异名磁极相互啪引衙极间的作用f使没有谨性的物体得到遊性的过程-晦念用蛊箱在钢棒上沿同一方向摩擦十第次「方法磁现象附地暉场地理南极是地磁场的北饭,地理北饭是地磁场的南扱指南针南极指南(地磁场北极)小谨针北极所着的方向为磁场方向百箭头義顽磁场方向;磁感红密磁场强r疏磁场弱夕HE场:从N到S内部逑场:从5到N底屯导件同围存在葩场-冥斯桔实殓醯场电导融中心的同「匕圍「吕通电导録垂亘「向夕曲场逐渐林电生蹿调节R,比较A喙弓I大头针的雰少-赳施大<1、探究电晞铁r-晡性强弱的影响因索羽右手:如图大拇指方向为电磴方向,0 指环毙方向为磁场方向咏变,血中有无枝芯比较大头針旁少自无扶苗用右手:四指坯绕庁叵为电踰方向「大拇指戶鬥旨万向为电竝铁N战方向fVF变B下面大淘+的雰少-戒圏降电遵扶的磁场廿在卑条形磁铁相似通过目隔的佔无殛制歯钳肖无电珮趙重机电拎:随温度上升接通担制宙源,产生魏生吸引衔铁,电铃咂电徳蹩电器具悴应用来垃自动控制:随着水上升,达到嘗戒水位时接11控制电懑「产生磁性吸引衔铁,红XJ亮电訖夭小至化的叫輯电隹号匣过电主v彖決听-> 生兀同的逑注,丛而校薄全屋版产生石同'吃(転訪來圧愿肖电詛专提哥輕=挖制电番工柞乜毒廩理:挖制电勝幵驻整通衔誹吸下,每灯亮,览制电痒幵爻断幵「匚弹蚩吸引D与与惑ftawcr亮臓:低电庄翦电舷制茗电压强电渝r 并巨可以实验巨商咼制通电导体在磁场中受力运动。
运动方向与电漩方向、磁场方向有芙基本原理运动方向判断(左手定律)如图磁感纯穿过手心,四指方向为电流方电‘大拇拒方向国受力运动的方向电动机画电动机廈理通电注昌在金场牛受巧转动,乙圏中线困受力转动,转到甲厘所示位置* 田于二力平衡「不能继绽转动。
XX教版八年级下册-科学知识点归纳XX教版八年级下册科学知识点归纳第一章电与磁一、磁现象:1、磁性:能够吸引铁、钴、镍等物质的性质2、磁体:具有磁性的物质(磁铁:铁质的磁体)3、磁极:定义:磁体上磁性最强的部分叫磁极,任何磁体都有两个磁极。
种类:如果磁体能自由转动,指南的磁极叫南极(S),指北的磁极叫北极(N)相互作用规律:同名磁极相互排斥,异名磁极相互吸引。
4、磁化:①定义:使原来没有磁性的物体得到磁性的过程。
磁铁吸引铁钉的原因是因为铁钉被磁化后,铁钉与磁铁的接触部分间形成异名磁极,异名磁极相互吸引的结果。
②钢和软铁的磁化:软铁被磁化后,磁性容易消逝,称为软磁材料。
钢被磁化后,磁性能长期保持,称为硬磁性材料。
所以制造永磁体使用钢,制造电磁铁的铁芯使用软铁。
二、磁场:1、定义:磁体周围存在着的物质,它是一种看不见、摸不着的特别物质。
磁场看不见、摸不着我们可以根据它所产生的作用来认识它。
这里使用的是转换法。
2、基本性质:磁场对放入其中的磁体产生力的作用,磁极间的相互作用是通过磁场而发生的。
3、方向规定:小磁针静止时北极所指的方向就是该点磁场的方向。
4、磁感线:在磁场中一些带箭头的曲线。
①方向:磁体周围的磁感线都是从磁体的北极出来,回到磁体的南极。
②说明:、磁感线是为了直观、形象地描述磁场而引入的曲线,不是客观存在的。
B、用磁感线描述磁场的方法叫模型法。
C、磁感线是封闭的曲线。
D、磁感线立体的分布在磁体周围,而不是平面的。
E、磁感线不相交。
F、磁感线的疏密程度表示磁场的强弱。
③熟练掌握条形磁铁磁感线的画法。
三、地磁场:①定义:在地球产生的磁场,磁针指南北是因为受到地磁场的作用。
②磁极:地磁北极在地理南极附近,地磁南极在地理北极附近。
③磁偏角:首先由我国宋代的沈括发现,地磁南北极与地理南北极不重合。
四、电生磁:1.奥斯特实验:通电导线的周围存在磁场,称为电流的磁效应。
直线电流周围的磁感线是围绕导线的同心圆,距离直线电流越近,磁场越强。
浙教版科学八年级下册重要知识点第1章粒子的模型与符号第1节模型、符号的建立与作用1、符号: 用符号能简单明了地表示事物,可避免由于事物外形不同和表达地文字语言不同而引起地混乱。
2、水在三态变化分子没有发生变化水在三态变化中,分子间的距离发生了变化。
3、建立模型的意义:可以帮助人们认识和理解一些不能直接观察到的事物。
模型可以是一幅图、一张表格、或一个公式。
第2节物质与微观粒子模型1、分子和原子的区别:在化学变化中,分子可分,原子不可再分。
2、化学变化的实质:分子分割成原子,原子重新组合成新的原子。
3、化学变化和物理变化的本质区别:在变化中,物质的分子变成了其它物质的分子,就是化学变化。
在变化中,物质的分子还是原来的分子,只是分子间的距离发生了变化,就是物理变化。
4、分子是由原子构成的。
一些气体、液体主要由分子构成5、原子直接构成的物质:金属和固体非金属及稀有气体6、金刚石和石墨物理性质不同是由于原子排列不同。
7、粒子的大小与质量(1)分子和原子都有一定的质量和体积。
原子的体积很小,半径的数量级在10-10米。
原子的质量也非常小,数量级在10-26千克。
(2)不同质量的原子质量不同,体积也不同。
第3节原子结构的模型一、原子结构模型的建立与修正1、道尔顿--实心球原子结构--发现原子2、汤姆森--“汤姆森模型”:原子是一个平均分布着正电荷的球体,带负电荷的电子嵌在中间。
--发现电子3、卢瑟福--“卢瑟福模型”:电子绕原子核运行4、波尔--“分层模型”:电子在固定的轨道上运动 5、“电子云模型质子(带正电) 夸克二、原子的结构:1、原子:原子核 (带正电) 中子(不带电) 夸克(不显电性)核外电子 (带负电)(1)核电荷数=质子数=核外电子数(2)中子数不一定等于质子数。
(3)原子内可以没有中子。
(4)质子不同,原子种类一定不同。
电子质量很小,在整个原子的质量中所占的比例极小,可忽略不计。
原子的质量主要集中在原子核上。
第一节模型、符号的建立与作用1.模型的概念:模型是依照实物的现状和结构按比例制成的物品,是用来显示复杂事物或过程的表现手段,如图表、图画、计算机图像、计算公式等。
2.符号的概念:代表事物的标记。
如数学符号、物理符号、天气符号、警示标志等。
注意点:(1)“公式”属于模型,如s=vt,而其中的s、v、t都代表一种符号。
(2)模型可以是抽象的,也可以是具体的。
第二节物质的微观粒子模型一、分子1.分子的定义:分子是由原子构成的,分子可以构成物质。
由分子构成的物质中,分子是保持物质化学性质的最小微粒。
2.分子的性质:(1)分子很小;(2)分子在永不停息的做无规则运动;(3)分之之间有间隙;(4)同种物质的分子化学性质相同,不同种物质的分子化学性质不同。
3.用分子的观点来解释由分子构成的物质发生的物理变化和化学变化。
(1)物理变化:分子本身不变,只是构成物质的分子间的距离发生了变化,比如水的三态变化。
(2)化学变化:分子本身发生变化,变成更小的微粒------原子,而原子又重新组合成新的分子,如电解水实验。
注意点:(1)(2)(3)(4)物理变化与化学变化区别:化学变化中产生了“新的物质”,而物理变化没有。
二、原子1.原子的定义:原子是化学变化中的最小微粒(在化学变化中原子不能再分)。
原子也可以直接构成物质。
2.注意点:(1)原子也是构成物质的基本粒子之一,如金属、多数固态非金属(碳、硅等)、稀有气体由原子直接构成;(2) 在化学变化中原子不可再分,但是脱离“化学反应”这一前提,原子仍可以分成更小的微粒。
三、不同的分子组成1.分子种类繁多的原因:原子种类和原子数量的搭配构成了丰富多彩的分子世界。
2.分子构成的方式:(1)同种原子,不同的原子数量,可以组成不同的分子。
如1个氧分子(O2)由2个氧原子组成,1个臭氧分子(O3)由3个氧原子组成;(2)不同种原子,不同的原子数量,可以组成不同的分子。
如1个水分子(H2O)由2个氢原子和1个氧原子组成,1个过氧化氢分子(H2O2)由2个氢原子和2个氧原子组成。