有机化学:氨基酸、多肽和蛋白质
- 格式:ppt
- 大小:2.09 MB
- 文档页数:18

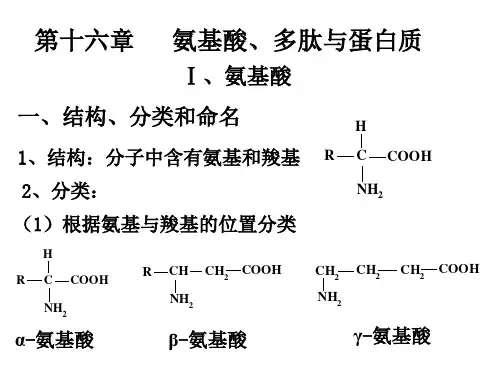
第22章氨基酸多肽蛋白质酶和核酸22.1 复习笔记一、氨基酸1.氨基酸的结构与名称(1)羧酸分子中烃基上的一个或几个氢原子被氨基取代后生成的化合物称为氨基酸。
(2)根据氨基和羧基的相对位置,氨基酸可以分为α-氨基酸、β-氨基酸、γ-氨基酸等。
α-氨基酸β-氨基酸γ-氨基酸根据氨基酸分子中羧基与氨基的相对数目,氨基酸可以分为中性氨基酸、酸性氨基酸和碱性氨基酸。
(3)组成蛋白质的氨基酸主要是α-氨基酸,可用通式RCH(NH2)COOH表示。
除R—H外,α-氨基酸中的α碳原子都是手性碳原子。
(4)将α-氨基酸用Fischer投影式表示,羧基写在竖线的上方,R基写在竖线的下方,氨基和氢写在横线的两侧,若氨基的位置与L-甘油醛中羟基的位置一致,就定义是L-氨基酸,与D-甘油醛中羟基的位置一致,就定义为D-氨基酸。
天然的氨基酸多数是L-构型的。
L一氨基酸L一甘油醛D一氨基酸D一甘油醛(5)氨基酸的名称一般都用俗名。
2.氨基酸的物理性质氨基酸分子中既有碱性基团——氨基,又有酸性基团——羧基,所以分子以内盐(internal salt)的形式存在,即氨基酸以两性离子的形式存在,例如:丙氨酸谷氨酸组氨酸alanine,Ala glutamic acid,Glu histidine,His 氨基酸在水中有一定的溶解度,但不溶于有机溶剂。
氨基酸的偶极矩数值都很大,熔点很高,多数氨基酸受热分解而不熔融。
二、氨基酸的反应1.氨基酸的等电点和酸碱反应(1)等电点氨基酸是一个两性分子(amphoteric molecular),既能与酸发生反应,又能与碱发生反应,在有H+和HO-的溶液中存在着如下的平衡:通过调节溶液的酸碱性找到一个合适的pH值,在该pH下正、负离子的浓度完全相等,此时向阳极移动和向阴极移动的离子彼此抵消,即电场中没有净电荷的迁移。
此时的pH即为该氨基酸的等电点(isoelectric point)。
中性氨基酸的等电点pH=6.2~6.8,酸性氨基酸的等电点pH=2.8~3.2,碱性氨基酸的等电点pH=7.6~10.8。





多肽和蛋白质的化学合成过程多肽和蛋白质是构成生命体的基础。
多肽是由数个氨基酸结合而成的化合物,而蛋白质则是由数个多肽链组成的复杂有机物。
它们在生化反应、细胞信号传递、免疫系统等方面都发挥着至关重要的作用。
原本只存在于生物体内的多肽和蛋白质,现在已经得到了人工的化学合成方法,为科学和医学研究提供了巨大的便利。
在多肽和蛋白质的化学合成过程中,最重要的步骤就是氨基酸的连接。
氨基酸是多肽和蛋白质的组成单元,每个氨基酸分子都包含有一个氨基基团(NH2)、一个羧基团(COOH)和一个侧链。
在化学合成时,我们需要将氨基酸的羧基和氨基通过化学键连接起来,形成肽链。
这个过程被称为“肽键形成”。
实现肽键形成的难度主要在于,连接两个氨基酸的反应需要在合适的条件下进行,避免受到空气、水和温度等外在因素的干扰而导致反应失败。
因此,化学家们在肽合成反应的过程中,必须选用适合的方法来控制反应条件,使其保持在理想的状态下进行。
一种常用的合成方法是固相合成法。
这种方法先将第一个氨基酸通过其中的侧链和选择性化学反应物连接在固相合成介质上生成支架,然后再依次加入接下来的氨基酸。
反应的过程可以通过依靠不同的化学反应物来控制反应条件,从而避免了其他因素的影响。
除了固相合成法,在溶液中的合成法也是一种常见的方法。
这种方法需要通过不同的溶剂、反应物和温度等条件来控制反应过程。
反应层次多、选择性差和带有多种副反应是这种方法的主要难点。
化学家们还在不断改进这些方法,近年来也发展出了新的多肽和蛋白质化学合成技术。
其中,化学合成的核心原理是通过对氨基酸结构的改变,在不改变氨基酸序列的情况下,增加和改变功能基团的数量和分布,从而解决肽链性质差异的问题。
另一种技术是利用天然的酵素做反应催化剂,通过营造特定的条件来加速反应,提高合成效率。
通过以上方法可以合成不同类型和数量的多肽和蛋白质,从而进行真正意义上的生命科学研究。
这些研究为疾病治疗、药物发现、功能化学和新材料等领域的发展提供了重要的支持。

多肽与蛋白质的区别多肽和蛋白质都是人体内重要的生物分子,它们在生物学中扮演着重要的角色。
因为两者具有相似的化学结构和生物学功能,在很多情况下会被混淆。
但在化学和生物学上,多肽和蛋白质之间有许多明显的区别。
本文旨在介绍多肽和蛋白质的区别。
化学结构多肽是由氨基酸通过肽键构成的分子。
氨基酸是一种具有2个基本结构的分子:一端是胺基(NH2),另一端是羧基(COOH)。
在氨基酸之间,羧基的酸性羰基与胺基的碱性氮原子结合形成肽键。
两个氨基酸的肽键称为二肽。
当氨基酸连接到一起时,便形成多肽。
在多肽中,氨基酸数目通常小于100,而且它们不会形成二级及二级以上的结构。
蛋白质是由一组氨基酸通过肽键构成的大分子。
蛋白质分子通常比多肽大,氨基酸数目可能多达数百到数千个。
蛋白质分子通过一个特殊的过程被折叠成特定的三维结构,这种结构是由分子中的氨基酸序列确定的。
生物学功能生物体内的多肽和蛋白质的生物学功能存在差异。
多肽在体内扮演的角色很多。
它们可以被用作荷尔蒙(如促甲状腺激素)、细胞凋亡调节剂(如Bcl-2)和其他诸如抗生素和毒素的生物分子。
蛋白质在体内的功能已经被研究得更深入。
蛋白质的功能包括:构建组成体,如细胞膜和细胞骨架,调节细胞机体的基本生物过程,如代谢、生长和分裂,以及承担免疫系统的协调作用。
此外,酶和激素都是蛋白质,因此,生命体内的所有生物反应都依赖于一定数目的酶催化过程,激素会在整个机体内起到调节功能。
在生物化学上,多肽和蛋白质之间是有很多明显区别的。
多肽由较少的氨基酸组成而不具备折叠成三维大分子的条件,因此,它通常是线性的。
蛋白质由更多的氨基酸组成,因此有足够的条件形成三级及以上的结构,从而获得其特定的生物活性。
多肽在体内扮演的角色也有很大差异,它们通常是调节剂和表观基因调节剂。
而蛋白质在体内发挥着更全面的功能,被视为生物有机分子中的重要代表。
总之,多肽和蛋白质在化学结构和生物学功能上都有明显的区别。
了解这些区别有助于我们更好地理解生命的本质,为生命科学的发展提供指导。


侯英健核心笔记生物化学内容如下:
1. 氨基酸和多肽:氨基酸是蛋白质的基本单位。
有8种氨基酸的异构体在生物化学上最重要,且合成蛋白质的酶很稳定。
通过肽键作用,两个氨基酸形成多肽,进一步聚合形成蛋白质。
氨基酸和多肽有重要的化学性质,如等电点。
了解氨基酸和多肽的性质有助于理解蛋白质的结构和功能。
2. 酶与生物催化:酶是一种生物催化剂,比许多无机催化剂效率更高。
酶催化反应具有选择性,这与它的三维结构有关。
生物催化是指一些生物体通过化学反应而产生的代谢或合成反应。
了解酶和生物催化对于理解生命的化学过程至关重要。
3. 核酸:核酸是所有生物体的遗传物质,包括DNA和RNA。
DNA主要存在于细胞核中,而RNA主要存在于细胞质中。
了解核酸的结构、功能以及基因表达对于理解生命的本质至关重要。
4. 糖类和脂质:糖类、脂质和蛋白质是构成生物体的主要有机化合物。
糖类和脂质在能量储存和运输、细胞膜的结构和功能等方面发挥着重要作用。
5. 蛋白质折叠与稳定:蛋白质折叠是指一个未折叠的氨基酸链如何形成一个有功能的蛋白质结构。
蛋白质的折叠和稳定受到许多因素的影响,如氨基酸序列、环境因素等。
在回答侯英健核心笔记生物化学时,可以围绕以上五个主题展开论述,详细解释每个主题的基本概念、化学性质、功能以及它们在生命过程中的作用。
同时,可以讨论蛋白质折叠问题、基因工程、蛋白质组学等前沿领域的研究进展,以帮助读者更好地理解现代生物化学的发展和应用。
总之,要确保回答清晰、准确、全面,以便帮助读者更好地理解和掌握生物化学知识。

氨基酸和多肽的关系氨基酸是构成蛋白质的基本组成单位,而多肽则是由多个氨基酸残基通过肽键连接而成的链状分子。
它们之间存在着密不可分的关系,氨基酸是多肽的构成要素,而多肽则是蛋白质的组成单元。
氨基酸是有机化合物,它由一个氨基基团、一个羧基基团和一个侧链组成。
在天然氨基酸中,氨基基团和羧基基团都与碳原子结合,形成一个碳骨架。
氨基酸的侧链决定了其特定的物化性质和生物活性。
在自然界中,已经发现了20种常见的氨基酸,它们分别是丙氨酸、甘氨酸、丝氨酸、脯氨酸、酪氨酸、色氨酸、赖氨酸、亮氨酸、异亮氨酸、苏氨酸、酸性氨基酸谷氨酸和天冬氨酸、碱性氨基酸赖氨酸和精氨酸、无极性氨基酸酮氨酸和甲硫氨酸、极性氨基酸谷氨酰胺和天冬酰胺。
这些氨基酸的不同组合和顺序决定了多肽或蛋白质的结构和功能。
多肽是由氨基酸通过肽键连接而成的链状分子。
肽键是由氨基基团和羧基基团之间的反应产生的化学键。
当两个氨基酸通过肽键连接时,其中一个氨基酸的羧基基团与另一个氨基酸的氨基基团反应,释放出一个水分子。
这个反应可以在蛋白质合成过程中重复进行,形成不同长度的多肽链。
多肽的长度可以从几个氨基酸残基到几百个氨基酸残基不等。
当多肽链中的氨基酸数目较少时,多肽通常被称为寡肽,而当氨基酸数目较多时,则被称为多肽。
当多肽的氨基酸残基数目超过100个时,就被称为蛋白质。
多肽的结构和功能取决于其氨基酸序列和空间构象。
氨基酸序列决定了多肽链的线性顺序,而空间构象则决定了多肽的立体结构。
多肽的立体结构可以分为四个级别:一级结构是指多肽链的线性序列,二级结构是指多肽链的局部折叠形式,如α-螺旋和β-折叠,三级结构是指多肽链的整体立体结构,包括各种非共价相互作用,如氢键、离子键和疏水效应,四级结构是指多个多肽链之间的相互作用,形成复合物或聚集体。
多肽具有多种生物活性和功能。
它们可以作为激素、抗体、酶、受体和传递子等生物活性分子。
例如,胰岛素是一种由两个多肽链组成的激素,它调节血糖水平;多肽抗体可以识别和结合特定的抗原,从而参与免疫反应;酶是一种具有催化作用的多肽分子,它可以加速化学反应的速率。