定量分析的一般步骤
- 格式:doc
- 大小:51.00 KB
- 文档页数:12




统计师如何进行定量和定性分析统计师是负责搜集、分析和解释数据的专业人士。
在统计学领域中,常见的分析方法包括定量分析和定性分析。
本文将介绍统计师在进行定量和定性分析时所需的步骤和技巧。
一、定量分析定量分析是一种利用数学和统计方法来处理数值和量化数据的分析方法。
下面是进行定量分析的主要步骤:1. 提出问题和假设: 首先,统计师需要明确需要回答的问题,并根据问题提出相应的假设。
例如,如果我们想分析某产品的销售额是否受到广告费用的影响,我们可以假设广告费用对销售额有正向影响。
2. 数据收集: 接下来,统计师需要搜集相关的定量数据。
数据可以通过问卷调查、实验设计、观察等方式获取。
确保数据的可靠性和有效性至关重要。
3. 数据清理和整理: 在进行分析之前,统计师需要对数据进行清理和整理,包括剔除异常值、填补缺失值、对数据进行标准化等。
这样可以保证数据的准确性和可比性。
4. 变量选择和描述统计: 统计师需要选择适当的变量来分析,并进行描述统计统计,例如计算平均值、标准差、相关系数等。
这些统计量可以提供数据的集中趋势、变异程度和变量之间的关系。
5. 假设检验和回归分析: 在定量分析中,假设检验和回归分析是常用的统计方法。
通过假设检验可以判断样本的差异是否具有统计显著性。
而回归分析可以用来确定变量之间的因果关系。
6. 结果解释和报告: 最后,统计师需要将分析结果进行解释和报告。
结果的解释要清晰明了,包括具体的数值、图表和相应的结论。
二、定性分析定性分析是一种用来研究非结构化、主观性数据的分析方法。
下面是进行定性分析的主要步骤:1. 研究问题和目标: 首先,统计师需要明确研究的问题和目标,例如探索人们对某一产品的满意度或者了解不同年龄段对政治观点的不同理解等。
2. 数据收集: 定性数据可以通过访谈、焦点小组讨论、观察等方式收集。
在数据收集过程中,需要保持中立和客观的态度。
3. 数据整理和分类: 统计师需要将收集到的数据整理和分类。
一、简答题:
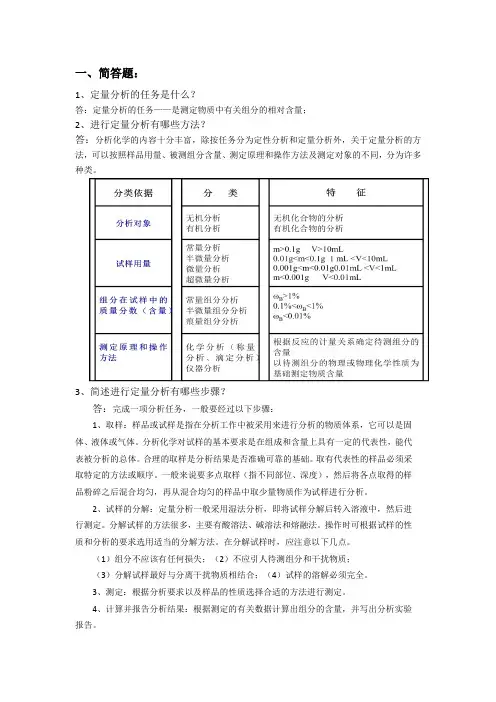
1、定量分析的任务是什么?
答:定量分析的任务——是测定物质中有关组分的相对含量;
2、进行定量分析有哪些方法?
答:分析化学的内容十分丰富,除按任务分为定性分析和定量分析外,关于定量分析的方法,可以按照样品用量、被测组分含量、测定原理和操作方法及测定对象的不同,分为许多种类。
3、简述进行定量分析有哪些步骤?
答:完成一项分析任务,一般要经过以下步骤:
1、取样:样品或试样是指在分析工作中被采用来进行分析的物质体系,它可以是固体、液体或气体。
分析化学对试样的基本要求是在组成和含量上具有一定的代表性,能代表被分析的总体。
合理的取样是分析结果是否准确可靠的基础。
取有代表性的样品必须采取特定的方法或顺序。
一般来说要多点取样(指不同部位、深度),然后将各点取得的样品粉碎之后混合均匀,再从混合均匀的样品中取少量物质作为试样进行分析。
2、试样的分解:定量分析一般采用湿法分析,即将试样分解后转入溶液中,然后进行测定。
分解试样的方法很多,主要有酸溶法、碱溶法和熔融法。
操作时可根据试样的性质和分析的要求选用适当的分解方法。
在分解试样时,应注意以下几点。
(1)组分不应该有任何损失;(2)不应引人待测组分和干扰物质;
(3)分解试样最好与分离干扰物质相结合;(4)试样的溶解必须完全。
3、测定:根据分析要求以及样品的性质选择合适的方法进行测定。
4、计算并报告分析结果:根据测定的有关数据计算出组分的含量,并写出分析实验报告。

第二章定量分析的一般步骤一、分析试样的采集与制备1.试样的采集与制备:是指从大批物料中采取少量的样本作为原始试样,然后再制备成供分析用的最终式样。
采样的基本原则:均匀、合理、具有代表性试样的形态:气体、液体、固体2.取样方法:气体样品:集气法(eg.工厂废气中有毒气体的分析)、富集法(eg.大气污染物的测定、室内甲醛的含量测定)固体样品:抽样样品法(“四角+中央”)、圆锥四分法液体样品:混合均匀后按照上中下分层取样二、试样的分解(预处理)1.分解试样的原则:①式样分解必须完全,处理后的溶液中不得残留原试样的细屑或粉末②式样分解过程中待测组分不应挥发③不应引入待测组分和干扰物质2.分解方法:溶解法、熔融法、消解法(1)溶解法:水:例(NH4)2SO4中含氮量的测定酸:HCl、H2SO4、HNO3、HF等及混合酸分解金属、合金、矿石等碱:例:NaOH溶解铝合金分析Fe、Mn、Ni含量有机溶剂:相似相溶原理(2)熔融法:酸溶:K2S2O7、KHSO4溶解氧化物矿石碱溶:Na2CO3、NaOH、Na2O2溶解酸性矿物质(3) 消解法——测定有机物中的无机元素湿法消解:通常用硝酸和硫酸混合物与试样一起置于克氏烧瓶中,一定温度下分解,属于氧化分解法常用试剂:HNO3、H2SO4、HClO4、H2O2和KMnO4等。
干法灰化:待测物质加热或燃烧后灰化、分解,余留残渣用适当的溶剂溶解。
适用范围:有机物和生物试样中金属元素、硫、卤素等无机元素。
常用方法:坩埚灰化法、氧瓶燃烧法和低温灰化法。
三、常用的分离、富集方法1. 分离:让试样中的各组分互相分开的过程(纯化)分离的作用:提高方法的选择性、提高方法的灵敏度、准确度分离方法:沉淀分离、萃取分离、挥发分离、色谱分离2. 富集:待测组分含量低于测定方法的检测限时,在分离时将其浓缩使其能被测定富集方法:萃取富集、吸附富集、共沉淀富集四、测定方法的选择分析对象(样品性质、组分含量、干扰情况)→分析方法(准确度、灵敏度、选择性、适用范围)→用户(用户对分析结果的要求和对分析费用的承受度)→成本(时间、人力、设备、消耗品)五、分析结果的计算与评价1. 分析结果的计算及评价的目的:判断分析结果的准确度、灵敏度、选择性等是否达到要求2. 含量计算方法:根据分析过程中有关反应的化学计量关系及分析测量所得数据进行计算3. 测定结果及误差分布情况的分析:可采取统计学方法进行评价,如平均值、相对标准偏差、置信度、显著性检查等。





定量分析的一般步骤试样的分析过程,一般包括下列步骤:试样的采取和制备、称量和试样的分解、干扰组分的掩蔽和分离、定量测定和分析结果的计算和评价等。
§12-1 试样的采取和制备要求分析试样的组成必须能代表全部物料的平均组成,即试样应具有高度的代表性。
否则分析结果再准确也是毫无意义的。
一、气体试样的采取对于气体试样的采取,亦需按具体情况,采用相应的方法。
例如大气样品的采取,通常选择距地面50-180厘米的高度采样、使与人的呼吸空气相同。
对于烟道气、废气中某些有毒污染物的分析,可将气体样品采入空瓶或大型注射器中。
大气污染物的测定是使空气通过适当吸收剂,由吸收剂吸收浓缩之后再进行分析。
在采取液体或气体试样时,必须先把容器及通路洗涤,再用要采取的液体或气体冲洗数次或使之干燥,然后取样以免混入杂质。
二、液体试样的采取装在大容器里的物料,只要在贮槽的不同深度取样后混合均匀即可作为分析试样。
对于分装在小容器里的液体物料,应从每个容器里取样,然后混匀作为分析试样。
如采取水样时,应根据具体情况,采用不同的方法。
当采取水管中或有泵水井中的水样时取样前需将水龙头或泵打开,先放水10-15分钟,然后再用干净瓶子收集水样至满瓶即可。
采取池、江、河中的水样时,可将干净的空瓶盖上塞子,塞上系一根绳,瓶底系一铁铊或石头,沉入离水面一定深处,然后拉绳拔塞,让水流满瓶后取出,如此方法在不同深度取几份水样混合后,作为分析试样。
三、固体试样的采取和制备固体试样种类繁多,经常遇到的有矿石、合金和盐类等,它们的采样方法如下:(一) 矿石试样在取样时要根据堆放情况,从不同的部位和深度选取多个取样点。
采取的份数越多越有代表性。
但是,取量过大处理反而麻烦。
一般而言应取试样的量与矿石的均匀程度、颗粒大小等因素有关。
通常试样的采取可按下面的经验公式(亦称采样公式)计算:m =Kda式中:m-----为采取拭样的最低重量(公斤);d------为试样中最大颗粒的直径(毫米);K-----为经验常数,可由实验求得,通常K值在0.02-1之间,d<0.1mm-----------------K=0.2.0.1mm<d< 0.6mm------K= 0.4d>0.6mm------------=0.8-1。
原子荧光光谱法定量
原子荧光光谱法(Atomic Fluorescence Spectroscopy,AFS)是一种用于定量分析的光谱技术,通常用于检测和测定液体样品中的金属元素。
下面是使用原子荧光光谱法进行定量分析的一般步骤:
1.样品制备:收集待测样品,必要时对样品进行前处理,以确保
合适的样品状态和浓度范围。
2.原子化:将样品中的金属元素原子化。
这通常通过火焰、电感
耦合等离子体(ICP)、石墨炉等手段来实现。
原子化的目的是将金属元素从其化合物中转化为自由的原子态。
3.激发和发射:通过使用激发源(通常是辐射源,如光源或激光)
激发原子的电子,导致金属原子发射荧光辐射。
每个金属元素都有独特的光谱线,这些光谱线可以用于唯一地识别和测定该元素。
4.分析光谱:通过使用荧光光谱仪测量发射的荧光光谱。
光谱中
的荧光峰的强度与样品中金属元素的浓度成正比。
5.制备标准曲线:使用一系列已知浓度的金属元素标准溶液,绘
制标准曲线。
这将用于将光谱信号转换为元素浓度。
6.定量分析:将样品中的光谱信号与标准曲线进行比较,从而确
定样品中金属元素的浓度。
7.质量控制:进行质量控制,确保分析的准确性和可靠性。
这包
括使用质控样品、重复分析等。
原子荧光光谱法的优势在于其高灵敏度、选择性和多元素分析能
力。
然而,需要注意的是,对于不同元素,可能需要调整光谱测量条件,并考虑矩阵效应等因素。
第二章分析试样的采取和预处理方法教学要求:1、掌握定量分析的一般步骤;2、掌握试样采取得一般原则、无机和有机试样的分解方法;3、了解试样的制备和保存方法试样的分析过程,一般包括下列步骤:试样的采取和制备、试样的预处理、干扰组分的掩蔽和分离、定量测定、分析结果的计算和评价。
§2-1 分析试样的采取和制备试样采取得重要性和意义:分析试样的采集: 指从大批物料中采取少量样本作为原始试样,所采试样应具有高度的代表性,采取的试样的组成能代表全部物料的平均组成,否则分析结果再准确也是毫无意义的。
一、采取试样的一般原则1、现场勘察并收集资料;2、代表性;3、采用量符合要求;4、合理保存二、固体试样的采取(一)矿石试样1、采样点的布设(汽车、火车、轮船、矿堆、传送带等)2、湿存水的去除(100-105o C烘干)3、制备制备试样分为破碎,过筛,混匀和缩分四个步骤。
粗碎(过4-6号筛)、缩分、中碎(过20号筛)、缩分、碾磨、缩分、分析试样。
大块矿样先用压碎机破碎成小的颗粒,再进行缩分。
常用的缩分方法为“四分法”,将试样粉碎之后混合均匀,堆成锥形,然后略为压平,通过中心分为四等分把任何相对的两份弃去,其余相对的两份收集在一起混匀,这样试样便缩减了一半,称为缩分一次。
每次缩分后的最低重量也应符合采样公式的要求。
如果缩分后试样的重量大于按计算公式算得的重量较多,则可连续进行缩分直至所剩试样稍大于或等于最低重量为止。
然后再进行粉碎、缩分,最后制成100-300克左右的分析试样,装入瓶中,贴上标签供分析之用。
通常试样的取样量可按下面的经验公式(亦称采样公式)计算:m = Kd a式中:m为采取拭样的最低重量(公斤);d为试样中最大颗粒的直径(毫米);K和a为经验常数,可由实验求得,通常K值在0.02-1之间,a值在1.8—2.5之间。
地质部门规定a值为2,则上式为:m=Kd2筛号(网目) 20 40 60 80 100 120 200筛孔大小/mm 0.83 0.42 0.25 0.177 0.149 0.125 0.074一般要求通过100-200目筛。
(二)土壤试样(了解)1、采样点的布设:根据地形地貌和地块大小决定。
有梅花形、棋盘式、蛇形布点法等。
2、采样时间:根据分析内容确定3、采样深度:根据作物的根系确定:农作物0-20,水果0-604、采用量:每点采1-2kg,经压碎、风干、粉碎、过筛、缩分等步骤,取粒径小于0.5 mm的样品作分析试样。
5、保存:根据测定项目,对挥发酚、氨氮、氰化物等不稳定组分需要新鲜土壤,其他多数需要风干土壤。
风干时注意阳光直射和尘土落入,保存在玻璃或聚四氟乙烯塑料容器中。
(三)金属或金属制品(了解)由于金属经过高温熔炼,组成比较均匀,因此,对于片状或丝状试样,剪取一部分即可进行分析。
但对于钢锭和铸铁,由于表面和内部的凝固时间不同,铁和杂质的凝固温度也不一样,因此,表面和内部的组成是不很均匀的。
取样时应先将表面清理,然后用钢钻在不同部位、不同深度钻取碎屑混合均匀,作为分析试样。
对于那些极硬的样品如白口铁、硅钢等,无法钻取,可用铜锤砸碎之,再放入钢钵内捣碎,然后再取其一部分作为分析试样。
(四) 粉状或松散物料试样(了解)常见的粉状或松散物料如盐类、化肥、农药和精矿等,其组成比较均匀,因此取样点可少一些,每点所取之量也不必太多。
各点所取试样混匀即可作为分析样品。
三、液体试样的采取与保存(了解)1、采样点的布设:液体试样一般比较均匀,取样单元可以较少,但对河流、湖泊和海洋等水质监测时,应考虑可能的不均匀性。
应从不同的位置和深度分别采样,混合均匀后作为分析试样,以保证它的代表性装在大容器里的物料,只要在贮槽的不同深度取样后混合均匀即可作为分析试样。
对于分装在小容器里的液体物料,应从每个容器里取样,然后混匀作为分析试样。
如采取水样时,应根据具体情况,采用不同的方法。
当采取水管中或有泵水井中的水样时取样前需将水龙头或泵打开,先放水10-15分钟,然后再用干净瓶子收集水样至满瓶即可。
水质监测采用位置根据水种类:天然水(河、湖、海、地下);用水(引用、工业用、灌溉);排放水(工业废水、城市污水)采样多变性:河水—上、中、下(大河:左右两岸和中心线;中小河:三等分,距岸1/3处);湖水---从四周入口、湖心和出口采样;海水---粗分为近岸和远岸;生活污水---与作息时间和季节性食物种类有关;工业废水---与产品和工艺过程及排放时间有关详见教材第14-15页。
2、采样设备:地表水样可用水桶等,深层水样常用采样器,常用的是单层采样器。
可将干净的空瓶盖上塞子,塞上系一根绳,瓶底系一铁铊或石头,沉入离水面一定深处,然后拉绳拔塞,让水流满瓶后取出,如此方法在不同深度取几份水样混合后,作为分析试样。
3、水样的保存:保存的容器:聚乙烯容器用于保存测定金属和无机物的水样,玻璃容器用于保存测定有机物和生物组分的水样,石英和聚四氟乙烯容器存放特殊测定项目的水样。
存储时间:用于一般清洁水样存放时间不应超过72小时,轻度污染水样不超过48小时,严重污染水样存放时间不超过12小时。
保存方法:控制溶液的pH值、加入化学稳定试剂、冷藏和冷冻、避光和密封等四、气体试样的采取1、采样点的布设原则:大气污染物试样应在监测区同时进行多点布设,人口、工业、交通密集地区多布点,研究大气污染对人体的影响,通常选择距地面50-180厘米的高度采样、使与人的呼吸空气相同。
对于烟道气、废气中某些有毒污染物的分析,可将气体样品采入空瓶或大型注射器中。
2、采样方法:(1)直接采样法,用注射器,塑料袋和采样管等。
静态气体试样直接采样,用换气或减压的方法将气体试样直接装入玻璃瓶或塑料瓶中或者直接与气体分析仪连接动态气体试样采用取样管取管道中气体,应插入管道1/3直径处,面对气流方向---常压,打开取样管旋塞即可取样。
若为负压,连接抽气泵,抽气取样。
(2)浓缩采样法:溶液吸收法,固体阻留法及低温冷凝法。
五、生物试样的采取与制备生物试样包括:植物试样(花、叶、茎、根、种子),动物试样(体液、组织器官、肌肉、毛发等)待分析的组分:植物体内的营养成分、农药残留,动物体内的药物和代谢产物等。
(一)植物试样的采集与制备1、采样点的布设:梅花形布点法、平行交叉布点法。
2、采样量:干重1kg,湿重5kg。
3、植物试样的制备:新鲜的洗净,捣碎或剪碎,风干或40-60o C烘干,过40-60目筛,与广口瓶中保存。
(二)动物试样的采集与制备1、血液:全血、血清、血浆。
2、尿液3、毛发和指甲§2-2 试样的预处理在一般分析工作中,通常先要将试样分解,制成溶液。
试样的分解工作是分析工作的重要步骤之一。
在分解试样时必须注意:一、试样分解必须完全,处理后的溶液中不得残留原试样的细屑或粉末,二、试样分解过程中待测组分不应挥发,三、不应引入被测组分和干扰物质。
由于试样的性质不同,分解的方法也有所不同。
方法有溶解和熔融两种。
一、无机试样的分解(一)溶解法采用适当的溶剂将试样溶解制成溶液,这种方法比较简单、快速。
常用的溶剂有水、酸和碱等。
溶于水的试样一般称为可溶性盐类,如硝酸盐、醋酸盐、铵盐、绝大部分的碱金属化合物和大部分的氯化物、硫酸盐等。
对于不溶于水的试样,则采用酸或碱作溶剂的酸溶法或碱溶法进行溶解,以制备分析试液。
1. 水溶法可溶性的无机盐直接用水制成试液。
2. 酸溶法酸溶法是利用酸的酸性、氧化还原性和形成络合物的作用,使试样溶解。
钢铁、合金、部分氧化物、硫化物、碳酸盐矿物和磷酸盐矿物等常采用此法溶解。
常用的酸溶剂如下:酸溶(盐酸、硫酸、硝酸、高氯酸、氢氟酸、磷酸;混酸有王水、硝酸+高氯酸,HF+硫酸、HF+硝酸等分解金属、合金、矿石等)3. 碱溶法碱溶法的溶剂主要为NaOH和KOH。
碱溶法常用来溶解两性金属铝、锌及其合金,以及它们的氧化物、氢氧化物等。
在测定铝合金中的硅时,用碱溶解使Si以SiO32-形式转到溶液中。
如果用酸溶解则Si可能以SiH4的形式挥发损失,影响测定结果。
(二)熔融法1. 酸熔法碱性试样宜采用酸性熔剂。
常用的酸性熔剂有K2S2O7(熔点419℃)和KHSO4(熔点219℃),后者经灼烧后亦生成K2S2O7,所以两者的作用是一样的。
这类熔剂在300℃以上可与碱或中性氧化物作用,生成可溶性的硫酸盐。
如分解金红石的反应是:TiO2 + 2 K2S2O7= Ti(SO4)2 + 2K2SO4这种方法常用于分解A12O3、 Cr2O3、Fe3O4、ZrO2、钛铁矿、铬矿、中性耐火材料(如铝砂、高铝砖)及磁性耐火材料(如镁砂、镁砖)等。
2. 碱熔法酸性试样宜采用碱熔法,如酸性矿渣、酸性炉渣和酸不溶试样均可采用碱熔法,使它们转化为易溶于酸的氧化物或碳酸盐。
常用的碱性熔剂有Na2CO3(熔点853℃)、 K2CO3(熔点89l℃)、NaOH(熔点318℃)、Na2O2(熔点460℃)和它们的混合熔剂等。
这些溶剂除具碱性外,在高温下均可起氧化作用(本身的氧化性或空气氧化),可以把一些元素氧化成高价(Cr3+、Mn2+可以氧化成Cr(ⅤI)、Mn(VII),从而增强了试样的分解作用。
有时为了增强氧化作用还加入KNO3或KClO3,使氧化作用更为完全。
(1) Na2CO3或K2CO3常用来分解硅酸盐和硫酸盐等。
分解反应如下:A12O3•2SiO2 + 3Na2CO3 = 2NaAlO2 +2Na2SiO3 + 3CO2↑BaSO4 + Na2CO3 = BaCO3 + Na2SO4(2) Na2O2常用来分解含Se、Sb、Cr、Mo、V和Sn的矿石及其合金。
由于Na2O2是强氧化剂,能把其中大部分元素氧化成高价状态。
例如铬铁矿的分解反应为:2FeO•Cr2O3+7Na2O2=2NaFeO2+4Na2CrO4+2Na2O熔块用水处理,溶出Na2CrO4,同时NaFeO2水解而生成Fe(OH)3沉淀:NaFeO2+2H2O=NaOH+Fe(OH)3↓然后利用Na2CrO4溶液和Fe(OH)3沉淀分别测定铬和铁的含量。
(3) NaOH(KOH)常用来分解硅酸盐、磷酸盐矿物、钼矿和耐火材料等。
(三) 烧结法此法是将试样与熔剂混合,小心加热至熔块(半熔物收缩成整块),而不是全熔,故称为半熔融法又称烧结法。
常用的半熔混合熔剂为:2份MgO+3 Na2CO3;1份MgO+ Na2CO3; 1份ZnO+ Na2CO3此法广泛地用来分解铁矿及煤中的硫。
其中MgO、ZnO的作用在于其熔点高,可以预防Na2CO3在灼烧时熔合,保持松散状态,使矿石氧化得以更快更完全反应产生的气体容易逸出。
此法不易损坏钳锅,因此可以在瓷钳锅中进行熔融,不需要贵重器皿。