卡波姆第四版药典
- 格式:docx
- 大小:215.41 KB
- 文档页数:6
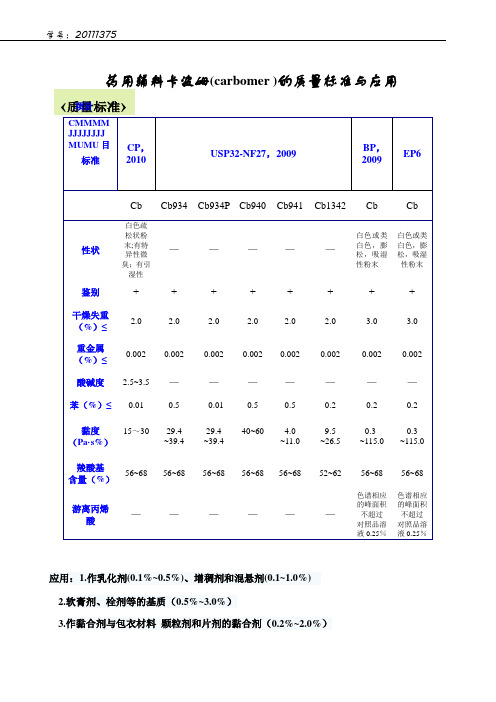
药用辅料卡波姆(carbomer )的质量标准与应用应用:1.作乳化剂(0.1%~0.5%)、增稠剂和混悬剂(0.1~1.0%) 2.软膏剂、栓剂等的基质(0.5%~3.0%)3.作黏合剂与包衣材料 颗粒剂和片剂的黏合剂(0.2%~2.0%)CMMMM JJJJJJJJ MUMU 目 标准CP ,2010USP32-NF27,2009BP ,2009EP6CbCb934 Cb934P Cb940 Cb941 Cb1342 CbCb性状 白色疏松状粉末;有特异性微臭;有引湿性— — — — —白色或类白色,膨松,吸湿性粉末白色或类白色,膨松,吸湿性粉末鉴别 ++++++++干燥失重(%)≤ 2.02.02.02.02.02.03.03.0重金属(%)≤ 0.002 0.0020.002 0.002 0.002 0.002 0.002 0.002酸碱度 2.5~3.5 ———————苯(%)≤0.010.5 0.01 0.5 0.5 0.2 0.2 0.2 黏度(Pa·s%) 15~3029.4 ~39.4 29.4 ~39.4 40~604.0 ~11.0 9.5 ~26.50.3 ~115.00.3 ~115.0羧酸基含量(%) 56~6856~6856~6856~68 56~6852~62 56~6856~68游离丙烯酸— — — — — —色谱相应的峰面积不超过 对照品溶液0.25%色谱相应的峰面积不超过 对照品溶液0.25%‹质量标准›项目4.作缓控释材料(6.0%~10.0%)5.还可与羟丙基纤维素合用作粘膜贴剂的基质。

卡波姆第四版药典
卡波姆(Capomulin)是一种针对小鼠肺癌的化学治疗药物,在许多动物试验和人体试验中都显示出良好的疗效。
第四版的卡波姆药典是对以前版本的完善和更新。
药物介绍
卡波姆是一种针对小鼠肺癌的化学治疗药物,通常通过腹腔注射的方式给予。
它可以破坏癌细胞的结构,阻止癌细胞的增殖,从而起到抑制癌症的作用。
卡波姆也能增加小鼠造血干细胞的浓度,使其更能够抵抗癌症。
第四版药典中的变化
第四版药典中,卡波姆的工艺得到了更加严格的控制,以确保每一批药物的质量和效果。
新的成分分析技术和成分检测方法的引入,使得药品的纯度更高,更加精确。
另外,第四版药典中,对卡波姆的毒性和副作用也进行了详细的调查和研究。
这些研究结果表明,卡波姆对小鼠的毒性较小,副作用也比较轻微。
药品的使用
在使用卡波姆时,需要按照药品说明书上的剂量和使用方法正确地给药,以获得最佳的治疗效果。
在实验室动物中使用时,建议选择与小鼠体重相当的剂量,并在一段时间内进行治疗。
在临床应用中,需要确保患者的身体状况和病情符合使用卡波姆的条件。
第四版卡波姆药典的发布,为研究和治疗小鼠肺癌提供了更精确,更高效和更安全的药物选择。
但是,在使用卡波姆时需要注意,药品的质量和使用方法对于治疗效果和副作用都有着重要的影响。
因此,使用前需要做好充分的准备和了解,并遵循正确的使用方法。

卡波姆Carbomer1 通用名BP:CarbomersPhEur:CarbomeraUSPNF:Carbomer注意:USPNF 20收载几个单独的卡波姆品目。
见第4项、第9项。
2 异名Acritamer;acrylic acid polymer;Carbopol;carboxy polymethylene,polyacrylic acid;car-boxyvinyl polymer;Permulen;Ultrez.3 化学名和CAS注册号carbomer[9003-01-4](卡波姆)注意,卡波姆910,934,934P,940,941,971P和974P共用一个CAS注册号9003-01-4。
卡波姆1342是一种共聚物,CAS注册号不同。
4分子式与分子量卡波姆是合成的丙烯酸与烯丙基蔗糖或与烯丙基季戊四醇醚交联的高分子聚合物。
以干品计算,含56%~68%的羧酸基团。
BP 2001版和PhEur 2002版有单独品目描述卡波姆。
USPNF20用几个品目描述了不同水溶液黏度和用于口服或非口服级别的卡波姆。
卡波姆树脂的分子量理论上估计在7X105到4X106之间。
在一项测量交联分子量的研究工作中,研究人员将弹性网状结构理论应用于溶胀的凝胶,而且建立了弹性模量和交联分子量之间的逆函数关系[1~3]。
已有报道,卡波姆941的交联分子量估计值为237 600g/mol,卡波姆941的交联分子量为104 400g/mol[4]。
一般来说,低黏度和低硬度的卡波姆树脂有较高的交联分子量值,相反高黏度和较高硬度的卡波姆有较低的交联分子量值。
5 结构式卡波姆聚合物是由丙烯酸的重复单元构成的。
单元结构如下图所示。
聚合物链与烯丙基蔗糖或烯丙基季戊四醇交联。
见第4项。
卡波姆的丙烯酸单体6 类别生物黏附剂;乳化剂;释放调节剂;助悬剂;片剂黏合剂;增黏剂。
7 在药物制剂或制剂工艺中的应用卡波姆主要作为助悬剂或增黏剂应用于液体或半固体的药物剂型。

附件:卡波姆均聚物(曾用名:卡波姆)Kabomu JunjuwuCarbomer Homopolymer本品系以非苯溶剂为聚合溶剂的丙烯酸键合多元醇烯丙基醚的高分子聚合物。
按干燥品计,含羧酸基(-COOH)应为56.0%~68.0%。
乙酸乙酯与环己烷(生产工艺中使用时测定)置顶空瓶中,精密加人二甲基亚砜5ml,密封,作为供试品溶液;分别取乙酸乙酯和环己烷适量,精密称定,用二甲基亚砜定量稀释成每1ml 中含乙酸乙酯0.2mg 和环己烷0.12mg 的混合溶液,精密量取5ml ,置顶空瓶中,密封,作为对照品溶液。
照残留溶剂测定法(通则0861 第二法)测定,用100%二甲基聚硅氧烷为固定液(或极性相近的固定液)的毛细管柱,程序升温,起始温度为40℃,维持3 分钟,以每分钟5℃的速率升温至120℃,维持20 分钟,再以每分钟20 ℃的速率升温至220℃,维持3 分钟,再以每分钟20℃的速率升温至240℃,维持8 分钟;进样口温度260℃,检测器温度260℃;顶空瓶平衡温度为85°C ,平衡时间为90 分钟。
取对照品溶液与供试品溶液分别顶空进样。
按外标法以峰面积计算,含乙酸乙酯不得过0.5% ,环己烷不得过0.3%。
苯取苯适量,精密称定,用二甲基亚砜定量稀释制成每1ml 中含苯1.0mg 的溶液。
精密量取该溶液适量,加水定量稀释制成每1ml 中含苯0.5μg 的溶液,作为苯储备液。
取本品约炽灼残渣取本品1.0g,依法检查(通则0841),遗留残渣不得过2.0%。
重金属取炽灼残渣项下遗留的残渣,依法检查(通则0821 第二法),含重金属不得过百万分之二十。
【含量测定】取本品约0.4g,精密称定,加水400ml,充分溶胀后加氯化钾2g,照电位滴定法(通则0701),用氢氧化钠滴定液(0.25mol/L)滴定。
每1ml 氢氧化钠滴定液(0.25mol/L)相当于11.25mg 的-COOH。
【类别】药用辅料,软膏基质和释放阻滞剂。

复方痤疮凝胶50%乙醇30ml,红霉素0.75g氯霉素0.5苦参总碱0.4g雌二醇4mg丙二醇10ml,卡波姆1g,三乙醇胺1.5g,注射用水适量.取卡波姆撒入水中使溶胀后,加入丙二醇搅匀,缓慢加入三乙醇胺,边加边搅拌得透明状凝胶基质.另将苦参碱,红霉素,氯霉素,雌二醇溶于乙醇中,再与凝胶基质混合加水至100g,搅拌均匀即得.痤疮凝胶剂克林霉素10g,维甲酸0.25g,卡波姆940:10g,丙二醇200g,月桂氮卓酮10g,三乙醇胺10g,吐温-80:10g,加蒸馏水至1000g.将卡波姆撒于适量的蒸馏水中,充分溶胀,加入甘油,丙二醇100g,月桂氮卓酮研磨使润湿,加三乙醇胺研磨成透明凝胶基质,水浴至70℃.取克林霉素,维甲酸,丙二醇100g,吐温-80混合加热溶解后,将上述药液加入到基质中,慢加快搅,加蒸馏水至1000g,继续搅拌均匀,得金黄色透明凝胶剂.1%盐酸麻黄素凝胶剂盐酸麻黄素10g,尼泊金乙酯0.3g,氯化钠9g,三乙醇胺10g,卡波姆940 5g,蒸馏水加至1000g (1)取适量蒸馏水,在高速搅拌下将卡波姆940粉末撒入,继续搅拌直至粉末完全分散到溶媒中,在低速搅拌下加入三乙醇胺,使成凝胶基质,备用.(2)将尼泊金乙酯溶于适量热蒸馏水中,放至室温备用.(3)将盐酸麻黄素,氯化钠溶于少量蒸馏水中,在搅拌下将此溶液加入凝胶基质中,加入尼泊金乙酯溶液,加水至全量,搅匀即得.丙酸氯倍他索凝胶剂CBT0.05g,卡波姆941 1.0g,丙二醇10.0g,甘油10.0g,三乙醇胺1.5g,乙醇10.0ml,加水至100.0g. 取卡波姆941,加少量水溶胀.另取CBT0.05g,用乙醇溶解后,依次加入丙二醇和甘油,将此液缓慢加入卡波姆基质中,边加边搅拌,再滴加三乙醇胺,最后加纯化水至100.0g,搅匀,即得白色CBT半透明凝胶剂.呋喃西林凝胶剂呋喃西林10g,硼酸10g,Carbopol934 10g,甘油100g,无水乙醇200ml,碘酸钾,薄荷脑,三乙醇胺适量,蒸馏水加至1000g.取Carbopol934分次撒入适量蒸馏水中,使其缓慢溶胀,加入甘油,搅拌,使成透明凝胶基质.另取薄荷脑溶于乙醇,碘酸钾,硼酸溶于适量水中,三项合并,搅匀.边搅拌边撒入呋喃西林粉,以三乙醇胺调PH,加水至足量,搅匀,分装.成品pH为4.5~5.5.氟尿嘧啶凝胶剂①妇科用的处方为:氟尿嘧啶2g,卡波普2g,丙二醇12g,苯甲酸钠0.5g,月桂氮 酮2ml,NaOH 试液调pH至8,加水至100g.②皮肤科用的处方为:各药剂量均为妇科用药的1倍.称取卡波普2g,撒于60ml水的液面上溶化,加丙二醇12g,放置48h,搅拌成透明凝胶,加苯甲酸钠0.5g,月桂氮 酮2ml,氟尿嘧啶2g,用NaOH试液调pH至8,加水至100g,搅拌均匀即可.复方氯霉素凝胶氯霉素1.0g,己烯雌酚10mg,硫酸锌0.2g,卡泊姆940 1.0g,甘油10.0g,三乙醇胺1.5g,95%乙醇20mL,氮酮2.0g,蒸馏水加至100g.将硫酸锌溶于适量水中,取卡泊姆在适量的蒸馏水中充分溶胀,加入甘油和硫酸锌溶液,搅匀.滴加三乙醇胺,搅拌至透明凝胶.将氯霉素,己烯雌酚溶于乙醇后加至凝胶中,加入氮酮,用蒸馏水加至全量,搅匀,即得.复方马来酸氯苯那敏凝胶剂马来酸氯苯那敏1g,盐酸麻黄碱1g,95%乙醇24g,丙二醇10g,三乙醇胺1.5g,卡波姆-940 1.0g,蒸馏水加至100g.将卡波姆-940配制成4%的浓溶液静置过夜,让其充分溶胀,取蒸馏水适量,溶解丙二醇,并与上述卡波姆溶液混合均匀后,边搅拌边加入三乙醇胺,使成凝胶基质(a),将马来酸氯苯那敏,盐酸麻黄碱溶于乙醇中(b),在搅拌下将(b)缓慢加入(a)中,最后加蒸馏水至足量,即得.卡波姆为高分子量丙烯酸交联聚合物,它在水中溶胀后成为pH为3.0左右的胶体溶液,再用碱中和后其粘度迅速增高.制备凝胶时应注意三乙醇胺的滴加速度不宜过快,同时要充分搅拌,以免局部凝胶形成过快产生结块.复方替硝唑凝胶剂替硝唑1g,盐酸丁卡因0.5g,卡波姆3g,甘油20mL,三乙醇胺适量,蒸馏水加至100g.取卡波姆3g加适量水溶胀后,加入甘油,研磨使润湿,加三乙醇胺研磨成透明凝胶基质.另取替硝唑,丁卡因用适量水溶解,搅匀.将上述药液加入凝胶基质中,边加边研磨,加蒸馏水至100g,继续搅拌均匀,得透明凝胶剂.复方替硝唑凝胶剂替硝唑10g,氯霉素15g,升华硫30g,丙二醇100g,三乙醇胺18g,3%卡巴甫-940 250g,95%乙醇240g,蒸馏水加至1000g.用95%乙醇将替硝唑溶解得A液.用丙二醇将氯霉素溶解,升华硫过80目筛加入丙二醇溶液中得B液.3%卡巴甫-940与蒸馏水均匀混合,在搅拌下缓慢加入三乙醇胺使成凝胶基质,pH控制在6~8.将A,B液在搅拌下加入凝胶基质中,再加入蒸馏水至全量即得.更昔洛韦凝胶剂更昔洛韦3g,丙二醇10g,氮酮2g,卡波普1g,0.1mol/LNaOH溶液20ml,蒸馏水加至100g.取卡波普加蒸馏水约50ml,浸泡,搅拌使溶解,另取更昔洛韦,加0.1mol/LNaOH20ml,加热使更昔洛韦溶解,在不断搅拌下将其加入到上述液体中,调pH=7左右,再加入丙二醇,氮酮蒸馏水至全量搅拌均匀,即得.更昔洛韦水溶性差,溶解度为1.5mg/ml,其钠盐易溶于水,5%的水溶液pH=11,pH值下降可析出沉淀.故先将更昔洛韦用0.1mol/LNaOH溶解,再加入到凝胶中.环丙沙星凝胶剂环丙沙星0.3g,聚羧乙烯941 0.5g,乙醇3g,甘油5g,三氯叔丁醇0.1g,三乙醇胺适量,蒸馏水加至100g.按处方称取各组分,将三氯叔丁醇用乙醇溶解,然后将环丙沙星加入,并加适量蒸馏水搅拌使溶解,备用.另取容器,加适量蒸馏水,将聚羧乙烯941加入,让其自然溶胀后,将备用液及甘油一并加入该容器中,同时添加蒸馏水至约90g,充分搅拌的同时,滴加三乙醇胺适量,使成凝胶状,最后补加蒸馏水至全量,搅拌均匀,得pH为6.8,透明,粘稠的溶解型环丙沙星凝胶剂,分装于塑料软膏袋中,每袋10g,即得.苦参凝胶苦参总碱70g,CMC-Na30g,甘油100g,蒸馏水加至1000ml.取苦参总碱置于烧杯中,加水约600ml,加热至完全溶解,以稀盐酸调节pH值至4~5,得A液.取CMC-Na置于烧杯中,加甘油充分混匀,放置约30min后缓慢加入A液,边加边搅至均匀,再放置1~2h后加水至全量,搅匀后置输液瓶中,封盖,于100℃流通蒸气灭菌30min,分装即得. pH值调至4~5,与阴道内固有酸度相一致,从而减小了原苦参栓的刺激性;CMC-Na溶解时易形成包块,影响其进一步溶胀,我们加入甘油可有效地解决这一问题,同时甘油可滋润阴道粘膜,促进药物渗透.凝胶的粘滞度可随气候变化而调节.夏季应加大CMC-Na的投量,以占总量的3%为宜,过高则不易灌装;冬季可稍低一些,但亦不低于2.5%.硫磺凝胶剂升华硫200.0g 甘油100.0g 卡波姆-940 10.0g 三乙醇胺10.0g 聚山梨醇-80 10.0g 对羟基苯甲酸乙酯0.5g 95%乙醇适量纯化水加至1000.0g取甘油置乳钵中,加卡波姆-940,充分研磨使湿润,再加纯化水约600ml,研磨,使其充分溶胀后,加聚山梨醇-80及溶于适量乙醇的对羟基苯甲酸乙酯,研匀;再将升华硫(80目粉)分次加入,边加边研磨,待升华硫分散均匀后,加三乙醇胺,边加边搅,使成凝胶,加纯化水至全量,搅匀,分装,即得.马来酸氯苯那敏凝胶剂马来酸氯苯那敏1g,乙醇24g,丙二醇10g,三乙醇胺1.8g,卡波姆940 1g,蒸馏水加至100g.制备方法将卡波姆940配成4%的浓溶液,静置过夜,使其充分溶胀;取蒸馏水适量溶解丙二醇并与上述卡波姆溶液混合均匀后,边搅拌边加入三乙醇胺,使成凝胶基质(Ⅰ);将马来酸氯苯那敏溶于乙醇中(Ⅱ);在搅拌下将Ⅱ加入Ⅰ中,加蒸馏水至足量,即得.美洛昔康凝胶剂分别将聚乙烯醇(PV A),卡波普,HPMC用蒸馏水浸泡,三乙醇胺调节卡波普溶液的pH至5~6,加入PV A适量,卡波普与HPMC以2:1混合均匀,加入适量保湿剂,透皮促进剂,置乳钵中研磨均匀得凝胶基质.称取ME适量用乙醇溶解,与上述凝胶基质混匀.尼美舒利透明质酸凝胶尼美舒利1g,透明质酸2.5g,卡波姆941 0.5g,苯甲醇0.5g,丙二醇5g,乙醇20ml,三乙醇胺0.5g,蒸馏水加至100g.将适量蒸馏水煮沸,加入丙二醇混匀,冷却至50~60℃后,在搅拌下加入透明质酸,卡波姆941,静置24h(充分溶胀)(A);在另一容器中用乙醇溶解尼美舒利,加入苯甲醇混匀(B);将(B)加入到(A)中,滴入三乙醇胺中和(至pH6左右),加蒸馏水至足量,搅拌至均匀即得.处方中苯甲醇为防腐剂,丙二醇为保湿剂,乙醇为溶剂,三乙醇胺调节pH(pH主要影响凝胶的粘度).青藤碱凝胶青藤碱2g,卡波姆971 2g,丙二醇15ml,EDTA0.02g,氮酮适量,NaHSO30.4g,无水乙醇30ml,三乙醇胺3g,加蒸馏水至100g.将卡波姆均匀撒于适量蒸馏水面上,静置,使之充分溶胀;将青藤碱,NaHSO3和EDTA用适量蒸馏水溶解;将氮酮,丙二醇和无水乙醇混合均匀.将上述组分混合,搅匀,缓慢滴加三乙醇胺,边加边搅拌,控制pH6.0~6.5,分装即可.塞克硝唑凝胶剂塞克硝唑8g,聚羧乙烯941 0.5g,甘油8g,乙醇3g,三氯叔丁醇0.15g,三乙醇胺适量,蒸馏水加至100g.按处方称取各组分,将三氯叔丁醇用乙醇溶解备用.另取容器,加适量蒸馏水,将聚羧乙烯941加入,让其自然溶胀后,将备用液及甘油一并加入该容器中,同时添加蒸馏水至80g,将塞克硝唑细粉(过120目筛)加入,在充分搅拌的同时,滴加三乙醇胺适量,使成凝胶状,最后补加蒸馏水至全量,搅拌均匀,得pH为6.8,微白粘稠的塞克硝唑凝胶剂,分装于塑料软膏袋中,每袋10g,并配以给药器即得.双氯芬酸钠凝胶双氯芬酸钠15.0g,卡波姆-940 10g,甘油50g,10%三乙醇胺xg,无水乙醇200ml,桉叶油xg,冬青油xg,蒸馏水加至于1000g.取卡波姆和甘油,置250ml蒸馏水中自然溶胀24h,得(Ⅰ):另取双氯芬酸钠溶于350ml热蒸馏水中,不断搅拌下加入(Ⅰ)中,即得(Ⅱ);取桉叶油,冬青油,无水乙醇混匀后加入(Ⅲ)中,加入10%三乙醇胺,再加水至全量,搅匀后分装于密闭避光容器中,贮于凉暗处.双氯芬酸凝胶双氯芬酸1g,Carbopol-940 1g,丙二醇10g,三乙醇胺1.5g,95%乙醇30ml,尼泊金乙酯0.1g,蒸馏水加至100g.将Carbopol-940溶于适量蒸馏水中,于搅拌下加入三乙醇胺,制成凝胶基质.另取双氯芬酸,尼泊金乙酯溶于丙二醇及95%的乙醇中,于搅拌下缓缓加至凝胶基质中,加蒸馏水至足量,继续搅匀至凝胶状.双氯灭痛凝胶剂双氯灭痛5g,95%乙醇120g,丙二醇50g,三乙醇胺9g,4%卡巴甫-940水溶液125g,蒸馏水适量,制成约500g.a.在搅拌下将双氯灭痛溶于95%乙醇中;b.将丙二醇,4%卡巴甫-940水溶液,蒸馏水均匀地混合,然后边搅拌边加入三乙醇胺使成凝胶基质;c.在搅拌下将a加入b中,再加入剩余蒸馏水,制得约500g双氯灭痛凝胶剂.双氯灭痛的溶剂由蒸馏水,乙醇和丙二醇组成,其中乙醇和丙二醇兼有促进药物经皮吸收作用,但用量宜分别控制在40%和30%(重量比)以内,否则会发生树脂化,凝胶化,主药易析出结晶.此外在制备时,还需注意随加随搅拌,以免局部浓度过高,发生上述现象.另外加入适量三乙醇胺,以控制pH在7.0~7.2之间.双嘧达莫凝胶剂双嘧达莫5.0g,丙二醇10.0g,卡波姆934 1.0g,三乙醇胺2.0g,30%乙醇加至100g.取30%乙醇50g与卡波姆混合,充分搅拌后放置,使卡波姆充分溶胀;另取双嘧达莫溶于10g丙二醇与30%乙醇20g的混合液中,在不断搅拌下,倒入已充分溶胀的卡波姆凝胶中,加入三乙醇胺,搅匀,将剩余的30%乙醇加至全量,搅匀即得.据文献报道,皮肤局部用制剂的理想黏度约为20Pa s,所以设定卡波姆浓度为1%,在实际使用中,该凝胶易于从包装管中挤出,患者使用简便易行.酮康唑凝胶剂酮康唑20g,无水亚硫酸钠2g,95%乙醇350g,丙二醇100g,三乙醇胺18g,4%卡波姆-940水溶液250g,蒸馏水适量,制成1000g.在搅拌下将酮康唑溶于95%乙醇中;b.将无水亚硫酸钠溶于蒸馏水中,与丙二醇,4%卡波姆-940水溶液均匀混合,然后边搅拌边加入三乙醇胺使成凝胶基质;c.在搅拌下将a加入b中,再加入剩余蒸馏水,制得2%酮康唑凝胶剂1000g.硝酸咪康唑凝胶剂卡波姆940 2.0g,甘油5.0g,硝酸咪康唑1.8g,聚乙二醇4000 1.6g,无水乙醇30ml,三乙醇胺2.7g,加蒸馏水至100g.取卡波姆940加适量蒸馏水于研钵中研磨均匀,滴加三乙醇胺调节使成凝胶状,再加入甘油,研匀.另取MCZ, 聚乙二醇4000水浴加热溶于无水乙醇中.将上述药液缓缓加入上述基质中研匀.加蒸馏水至足量并继续研磨至均匀,得到MCZ凝胶.MCZ难溶于水,溶于乙醇,故在本实验中,用PEG作分散剂和助溶剂与MCZ混合溶于乙醇制备1.8%的MCZ凝胶剂,分散均匀,效果理想.盐酸达克罗宁凝胶盐酸达克罗宁2g,卡波姆940 2g,95%乙醇20g,甘油15g,聚山梨酯80 0.4g,羟苯乙酯0.2g,三乙醇胺2.7g,月桂氮 酮2g,蒸馏水加至200g.将卡波姆940与聚山梨酯80及60g蒸馏水混合,三乙醇胺溶于20g蒸馏水后加入上液搅匀,再将羟苯乙酯和月桂氮 酮溶于95%乙醇4g后逐渐加入上液中搅匀,再加入甘油搅匀,即得基质.取盐酸达克罗宁溶于蒸馏水50g和95%乙醇16g的混合溶剂中,全溶后加入上述基质中,加水至全量,搅拌均匀,除去气泡,即得.盐酸达克罗宁凝胶剂盐酸达克罗宁1g,卡波沫1g,聚山梨酯80 5g,三乙醇胺1.35g,甘油10g,山梨酸2.5g,糖精钠和薄荷脑适量,去离子水加至100g.处方依据:凝胶剂要求药物要溶解在基质中,本制剂选择常用的水凝胶基质卡波沫,而1%的盐酸达克罗宁在水中不能完全溶解,因此需要采取有效的方法增加药物的水中溶解度.通过上述药物在制剂中常用溶剂和增溶剂中溶解度的测定结果可知,在软膏剂中上述溶剂和增溶剂的加入量范围内,只有乙醇和5%的聚山梨酯80水溶液可满足制备要求.但乙醇易于挥发,不利于制剂的长期储存,因此本处方选择5%的聚山梨酯80为增溶剂.同时由于本品为口唇用软膏剂,又加入了糖精钠,薄荷脑作为矫味剂,山梨酸为防腐剂.取甘油,薄荷脑,糖精钠,山梨酸溶于适量水中,加入卡波沫充分溶胀后,加入三乙醇胺形成凝胶基质.聚山梨酯80加入处方量40%的去离子水再加入盐酸达克罗宁搅拌溶解后,加入到上述凝胶基质中,混合均匀,脱泡,即得.盐酸丁卡因凝胶剂盐酸丁卡因4g,CMC-Na3g,丙二醇20g,乙醇26g,蒸馏水加至100g.取CMC-Na分散于乙醇中,加入适量蒸馏水,放置过夜使其充分溶胀,将盐酸丁卡因溶于丙二醇和适量蒸馏水中,分次加入CMC-Na中,边加边搅拌,研磨,加蒸馏水至足量,研匀,分装于密闭避光的容器中,贮存于凉处.盐酸萘替芬凝胶剂盐酸萘替芬2g,卡波姆1.5g,甘油10g,三乙醇胺1.5g,吐温-80 lg,医用乙醇20ml,蒸馏水加至100g.取甘油10g置乳钵中,加卡波姆1.5g,充分研磨使润湿并加蒸馏水适量,另取盐酸萘替芬2g,加吐温-80 lg,三乙醇胺1.5g,乙醇20ml,适量蒸馏水使溶解,加入到上述乳钵中,边加边搅使成凝胶状;加蒸馏水至100g,研匀,即得.盐酸赛庚啶凝胶剂盐酸赛庚啶5g,甘油100g,三乙醇胺18g,月桂氮 酮10g,丙二醇100g,2%卡波普940水溶液500g,蒸馏水至1000g.取盐酸赛庚啶加甘油混合;再将2%卡波普940水溶液,丙二醇及月桂氮 酮均匀混合研磨使成基质,在搅拌下,将赛庚啶甘油混合液加入到上述卡波普940基质中混合,慢慢滴加三乙醇胺,边加边搅拌使成凝胶,加蒸馏水至全量,搅匀,分装即得.盐酸万乃洛韦凝胶剂盐酸万乃洛韦,氧化锌各5g,丙二醇10g,氮酮,三乙醇胺各2g,卡波姆1g,蒸馏水加至100g.取卡波姆加蒸馏水约50mL,浸泡,搅拌使溶解,滴加三乙醇胺pH调至7,用蒸馏水溶解盐酸万乃洛韦,加入上液中,再加入氧化锌,丙二醇,氮酮,加蒸馏水至100g,搅匀即得.右旋布洛芬凝胶右旋布洛芬,卡波姆940各1g,乙醇30mL,丙二醇15g,三乙醇胺1.5g,蒸馏水加至100g.称取卡波姆940干粉分次撒于适量蒸馏水中,放置过夜,使充分溶胀,备用.取右旋布洛芬,加入丙二醇研匀,再加乙醇和适量蒸馏水,水浴加热使完全溶解,待冷后,缓缓加入上述备用基质中,充分搅拌的同时,滴加三乙醇胺使成凝胶状态,再补加蒸馏水至全量,搅匀,分装即得.。

卡波姆痔疮凝胶技术要求概述及解释说明1. 引言1.1 概述卡波姆痔疮凝胶是一种常用于治疗痔疮的药物制剂,通过其特殊的成分和配方,在临床上广泛应用。
该凝胶具有良好的渗透性和舒缓作用,能够有效缓解痔疮引起的不适感和炎症反应。
本文将对卡波姆痔疮凝胶的技术要求进行深入探讨,并详细解释其使用方法及临床应用案例。
1.2 文章结构本文分为五个主要部分:引言、卡波姆痔疮凝胶技术要求、卡波姆痔疮凝胶使用方法解释说明、卡波姆痔疮凝胶的临床应用案例分析以及结论与展望。
1.3 目的本文旨在全面介绍卡波姆痔疮凝胶的技术要求,并对其使用方法进行详细说明和解释。
同时,通过实际案例的分析,评估该凝胶在临床应用中的效果,并探讨着眼未来发展趋势。
通过本文的阐述,希望能够给痔疮患者和医生提供一些有益的参考和指导。
以上是“1. 引言”部分内容的详细清晰撰写,希望对你的长文写作有所帮助。
2. 卡波姆痔疮凝胶技术要求2.1 定义和背景知识卡波姆痔疮凝胶是一种用于治疗痔疮的药物凝胶。
它是以卡波姆(carbomer)为主要成分,经过特定配方制备而成。
卡波姆具有黏稠度高、与水混合良好的特点,能够在皮肤或黏膜表面形成一层保护层,起到止血、镇痛、消肿等作用。
2.2 成分和配方要求卡波姆痔疮凝胶的主要成分为卡波姆,在制备过程中可能还会添加其他药物成分,如利多卡因、酞丁安等。
配方应根据临床需求进行调整,以达到最佳的治疗效果。
此外,凝胶中所使用的成分应符合相关药典规定的质量标准,并确保无任何污染物和有害物质。
2.3 制备和质量控制要点制备卡波姆痔疮凝胶需要遵循一定的工艺流程和质量控制要求。
首先,应保证制备设备和容器的清洁无菌,并严格按照配方比例将成分加入。
在搅拌过程中,需控制好温度、搅拌速度等参数,确保凝胶的均匀性和稳定性。
最后,凝胶应进行质量检验,检测指标包括外观、黏度、PH值等,并且需要进行细菌限度、纯度和微生物检测,确保产品符合质量标准。
这些技术要求对于卡波姆痔疮凝胶的制备工艺和质量控制至关重要。
0114 凝胶剂凝胶剂系指原料药物与能形成凝胶的辅料制成的具凝胶特性的稠厚液体或半固体制剂。
除另有规定外,凝胶剂限局部用于皮肤及体腔,如鼻腔、阴道和直肠等。
乳状液型凝胶剂又称为乳胶剂。
由高分子基质如西黄蓍胶制成的凝胶剂也可称为胶浆剂。
小分子无机原料药物如氢氧化铝凝胶剂是由分散的药物小粒子以网状结构存在于液体中,属两相分散系统,也称混悬型凝胶剂。
混悬型凝胶剂可有触变性,静止时形成半固体而搅拌或振摇时成为液体。
凝胶剂基质属单相分散系统,有水性与油性之分。
水性凝胶基质一般由水、甘油或丙二醇与纤维素衍生物、卡波姆和海藻酸盐、西黄蓍胶、明胶、淀粉等构成;油性凝胶基质由液状石蜡与聚乙烯或脂肪油与胶体硅或铝皂、锌皂等构成。
凝胶剂在生产与贮藏期间应符合下列有关规定。
一、混悬型凝胶剂中胶粒应分散均匀,不应下沉、结块。
二、凝胶剂应均匀、细腻,在常温时保待胶状,不干涸或液化。
三、凝胶剂根据需要可加入保湿剂、抑菌剂、抗氧剂、乳化剂、增稠剂和透皮促进剂等。
除另有规定外,在制剂确定处方时,该处方的抑菌效力应符合抑菌效力检查法(通则1121)的规定。
四、凝胶剂一般应检查pH值。
五、除另有规定外,凝胶剂应避光、密闭贮存,并应防冻。
六、凝胶剂用于烧伤治疗如为非无菌制剂的,应在标签上标明“非无菌制剂”;产品说明书中应注明“本品为非无菌制剂”,同时在适应症下应明确“用于程度较轻的烧伤(I°或浅II°)”;注意事项下规定“应遵医嘱使用”。
除另有规定外,凝胶剂应进行以下相应检查。
【粒度】除另有规定外,混悬型凝胶剂照下述方法检查,应符合规定。
检查法:取供试品适量,置于载玻片上,涂成薄层,薄层面积相当于盖玻片面积,共涂3片,照粒度和粒度分布测定法(通则0982第一法)测定,均不得检出大于180µm的粒子。
【装量】照最低装量检查法(通则0942)检查,应符合规定。
【无菌】除另有规定外,用于烧伤[除程度较轻的烧伤(I°或浅II°)外]、严重创伤或临床必须无菌的照无菌检查法(通则1101)检查,应符合规定。
卡波姆Carbomer1 通用名BP:CarbomersPhEur:CarbomeraUSPNF:Carbomer注意:USPNF 20收载几个单独的卡波姆品目。
见第4项、第9项。
2 异名Acritamer;acrylic acid polymer;Carbopol;carboxy polymethylene,polyacrylic acid;car-boxyvinyl polymer;Permulen;Ultrez.3 化学名和CAS注册号carbomer[9003-01-4](卡波姆)注意,卡波姆910,934,934P,940,941,971P和974P共用一个CAS注册号9003-01-4。
卡波姆1342是一种共聚物,CAS注册号不同。
4分子式与分子量卡波姆是合成的丙烯酸与烯丙基蔗糖或与烯丙基季戊四醇醚交联的高分子聚合物。
以干品计算,含56%~68%的羧酸基团。
BP 2001版和PhEur 2002版有单独品目描述卡波姆。
USPNF20用几个品目5描述了不同水溶液黏度和用于口服或非口服级别的卡波姆。
卡波姆树脂的分子量理论上估计在7X106到4X10之间。
在一项测量交联分子量的研究工作中,研究人员将弹性网状结构理论应用于溶胀的凝[1~3]胶,而且建立了弹性模量和交联分子量之间的逆函数关系。
已有报道,卡波姆941的交联分子量[4]估计值为237 600g/mol,卡波姆941的交联分子量为104 400g/mol。
一般来说,低黏度和低硬度的卡波姆树脂有较高的交联分子量值,相反高黏度和较高硬度的卡波姆有较低的交联分子量值。
5 结构式卡波姆聚合物是由丙烯酸的重复单元构成的。
单元结构如下图所示。
聚合物链与烯丙基蔗糖或烯丙基季戊四醇交联。
见第4项。
卡波姆的丙烯酸单体类别6生物黏附剂;乳化剂;释放调节剂;助悬剂;片剂黏合剂;增黏剂。
7 在药物制剂或制剂工艺中的应用卡波姆主要作为助悬剂或增黏剂应用于液体或半固体的药物剂型。
卡波姆Carbomer1 通用名BP:CarbomersPhEur:CarbomeraUSPNF:Carbomer注意:USPNF 20收载几个单独的卡波姆品目。
见第4项、第9项。
2 异名Acritamer;acrylic acid polymer;Carbopol;carboxy polymethylene,polyacrylic acid;car-boxyvinyl polymer;Permulen;Ultrez.3 化学名和CAS注册号carbomer[9003-01-4](卡波姆)注意,卡波姆910,934,934P,940,941,971P和974P共用一个CAS注册号9003-01-4。
卡波姆1342是一种共聚物,CAS注册号不同。
4分子式与分子量卡波姆是合成的丙烯酸与烯丙基蔗糖或与烯丙基季戊四醇醚交联的高分子聚合物。
以干品计算,含56%~68%的羧酸基团。
BP 2001版和PhEur 2002版有单独品目描述卡波姆。
USPNF20用几个品目描述了不同水溶液黏度和用于口服或非口服级别的卡波姆。
卡波姆树脂的分子量理论上估计在7X105到4X106之间。
在一项测量交联分子量的研究工作中,研究人员将弹性网状结构理论应用于溶胀的凝胶,而且建立了弹性模量和交联分子量之间的逆函数关系[1~3]。
已有报道,卡波姆941的交联分子量估计值为237 600g/mol,卡波姆941的交联分子量为104 400g/mol[4]。
一般来说,低黏度和低硬度的卡波姆树脂有较高的交联分子量值,相反高黏度和较高硬度的卡波姆有较低的交联分子量值。
5 结构式卡波姆聚合物是由丙烯酸的重复单元构成的。
单元结构如下图所示。
聚合物链与烯丙基蔗糖或烯丙基季戊四醇交联。
见第4项。
卡波姆的丙烯酸单体6 类别生物黏附剂;乳化剂;释放调节剂;助悬剂;片剂黏合剂;增黏剂。
7 在药物制剂或制剂工艺中的应用卡波姆主要作为助悬剂或增黏剂应用于液体或半固体的药物剂型。
剂型包括乳膏,凝胶,眼用软膏[5~7],直肠[8,9]局部制剂:[10~12]。
即使只有低残留的苯的卡波姆型号如卡波姆934P,欧洲药典2002版已不再收载。
然而,含有低残留的除ICH规定的“第一类OVI溶剂”之外的其他溶剂可以在欧洲应用。
只含低残留的乙酸乙酯的卡波姆,如卡波姆971P或974P,可以用于口服制剂,混悬剂、片剂、或缓释片剂[13~17]。
在片剂中卡波姆用作干或湿的黏合剂以及作为释放速度控制辅料。
在湿法制粒工艺中,水或乙醇-水的混合物可用作润湿剂。
加入聚合物黏合剂的无水有机溶剂也可以应用。
湿物料的黏性随着在制粒液体中加入某些阳离子物质而降低[18]。
有水时,在处方中加入滑石粉也可降低黏性。
卡波姆树脂已研究用于制备缓释骨架微丸[18],在含有多肽的制剂中用作肠蛋白酶的酶抑制剂[19,20],作为子宫颈贴 (cervical patch)[21]的黏胶剂和鼻腔给药的微球[22],以及定位药物传递到食道的磁性颗粒(magnetic granules)[23].卡波姆也作为乳化剂用于外用的O/ W型的乳剂。
为了这个目的,卡波姆部分用氢氧化钠,部分用长链脂肪胺如硬脂胺中和。
卡波姆951作为增黏剂也用于复乳微球的制备[24]。
卡波姆也常用于化妆品中。
见表Ⅰ。
表Ⅰ卡波姆的用途卡波姆是一种白色、“绒毛状”、酸性、吸水性、微具轻微特殊气味的粉末。
扫描电镜照片1辅料名:Carbomer 971P(商品;Carbopol 971P)生产厂家:BF Goodrich放大倍数:2000X电压:25kV扫描电镜照片2辅料名:Carbomer 971P(商品:Carbopol 971P)生产厂家:BF Goodrich放大倍数:6000X电压:25kV9 药典标准见表Ⅱ。
注意,不同的卡波姆级别在USPNF 20中有几个品目,BP 2001和PhEur 2002只有一个品目。
其他级别的卡波姆都应符合USPNF所规定的标准。
卡波姆974P包含在USPNF 20卡波姆934P的品目中。
同样,卡波姆980应符合卡波姆940的标准,卡波姆971P和981应符合卡波姆941品目的限度。
其他国家药典收载的卡波姆树脂有的是单一品种,有的是一个品目包括几个品种。
除另有说明之外,本品所列的测试限量适用于所有级别的卡波姆。
10 一般性质酸碱度:pH=2.7~3.5[0.5%(W/V)水分散液]pH=2.5~3.0[1%(W/V)水分散液]松密度:1.76~2.08g/cm3轻敲密度:1.4g/cm3玻璃化温度:100~105℃熔点:260℃时,30分钟内分解。
见第11项。
含水量:一般情况下,水分含量可达到2%(W/W)。
然而卡波姆具有吸水性,在25℃和相对湿度50%条件下,一般的平衡含水量为8%~10%(W/V)。
卡波姆的含水量不会影响其增黏的性能,但是含水量的增加使卡波姆更难处理,因为它更不易分散。
粒度分布:原粉颗粒平均粒径为0.2μm。
结絮的粉末颗粒平均粒径为2~7μm,并且不能粉碎成为原颗粒大小。
最近,有人介绍了一种颗粒状的卡波姆,粒径为180~425μm,其松密度和轻敲密度也比其他的卡波姆的为高。
溶解度:溶于水,中和之后溶于95%的乙醇和甘油。
卡波姆尽管被称为“可溶的”,但并不溶于水,而只是显著溶胀,形成三维交联的微凝胶。
药典的标准是不明确的,乙醇中溶胀要用长链的脂肪胺或乙氧基化的长链的脂肪胺进行中和,而甘油中溶胀则需要用水溶性的有机胺。
比重:1.41动力黏度:卡波姆分散在水中形成酸性的低黏度胶体分散液,中和之后产生高黏度的凝胶。
首先将卡波姆粉末分散在剧烈搅拌的水中,注意避免形成团块。
然后,加入碱中和。
生产厂家推荐使用商品Corbopol ETD和Ultrez 10系列的卡波姆,以帮助克服粉末分散在水性溶剂中所出现的问题。
卡波姆润湿很快,但水化缓慢,同时具有较低的未中和分散液黏度。
用于中和卡波姆树脂聚合物的物质有氨基酸、硼砂、氢氧化钾、碳酸氢钠,氢氧化钠和极性有机胺如三乙醇胺。
十二胺和硬脂胺可以用于非极性系统的胶凝剂。
1g的卡波姆被大约0.4g 的氢氧化钠所中和。
在制备凝胶的过程中,胶液应该用宽的搅拌桨缓慢的搅拌,以避免产生气泡。
中和的水凝胶pH6~11时黏度更大。
pH小于3或大于12,或有强电解质存在时,黏度显著降低[18,25]。
凝胶经紫外线照射,黏度急剧下降,但加入抗氧剂能减轻。
11 稳定性和贮藏条件卡波姆是稳定并具有吸湿性的物质,在104℃下加热2小时,不影响其增稠性。
然而,暴露于过高的温度能使变色和稳定性降低。
260℃加热30分钟完全分解。
干粉状的卡波姆不长霉。
相反,微生物在无防腐剂的水分散液中生长良好。
所以,应当加入防腐剂,如0.1%(W/V)的氯甲酚,0.18%(W/V)的羟苯甲酯0.02%(W/V)的羟苯丙酯,或0.1%(W/V)的硫柳汞。
某些抑菌剂的加入,如苯扎氯铵或苯甲酸钠,高浓度时(0.1%W/V)能够引起浑浊和卡波姆分散液黏度的降低。
水凝胶能够用热压灭菌[7],如果将混入的氧气除尽,pH和黏度只有很小的变化;也可以用γ射线灭菌,但这种技术能够增加制剂的黏度[26,27]。
室温条件下,能延长卡波姆的保存期且黏度不变。
如果在制剂中加入抗氧剂,或者分散液避光保存,在温度不断升高的情况下,分散液的黏度不变,或者有轻微的降低。
光照可引起氧化,这反映在分散液黏度的降低上。
加入0.05%~0.1%(W/V)的水溶性的紫外线吸收剂如二苯甲酮-2或二苯甲酮-4与0.05%~0.1%(W/V)的EDTA的混合物可使上述变化改善。
三乙醇胺作为中和剂也可以改善卡波姆对紫外线的稳定性。
见第10项。
卡波姆粉末应保存在阴凉,干燥的环境下,置密闭的防腐容器中。
含卡波姆的药物制剂宜用玻璃、塑料、或树脂衬里的容器盛装。
铝管包装时,要求制剂的pH小于6.5,包装在其他的金属管或容器中时pH要求高于7.7,以提高卡波姆的稳定性。
12 配伍禁忌卡波姆遇间二苯酚变色,且和苯酚,阳离子聚合物,强酸及高浓度的电解质不相容。
某些抑菌剂也应避免使用,或者以低浓度使用。
见第11项。
痕量的铁或其他过渡金属能够催化降解卡波姆分散液。
卡波姆与强碱物质如氨、氢氧化钾、氢氧化钠或强碱性有机胺接触的时候,能够产生大量的热。
某些含氨基官能团药物与卡波姆能形成水溶性的络合物。
通常这种情况可用适当的醇或多元醇调节液体的溶解度参数(solubility parameter)来防止。
卡波姆与某些聚合物辅料也能够形成pH依赖型的络合物,调节溶解度参数在这种条件下也能够起作用。
13 制法卡波姆是合成的高分子量丙烯酸交联聚合物。
由聚(丙烯酸)聚合物与烯丙基蔗糖或烯丙基季戊四醇交联制得。
聚合反应最常用的溶剂是苯。
而较新的卡波姆型号是用乙酸乙酯或环己烷-乙酸乙酯共溶剂的混合物制备的。
商品Carbopol ETD树脂是用一种专利聚合助剂在共溶剂中使树脂与聚烯基聚醚交联制得。
14 安全性卡波姆广泛应用于非注射制剂,特别是局部的液体和半固体制剂。
有某些级别可以应用于口服制剂中,见第18项。
动物急性口服毒性研究表明,卡波姆934P的口服毒性较低。
狗按照每千克体重8g的剂量给药,无死亡。
一般认为卡波姆基本上是无毒、无刺激性的辅料。
没有证据表明局部应用卡波姆有过敏反应。
人口服卡波姆1~3g的剂量可被用作强腹泻剂。
卡波姆934 LD50(豚鼠,口服):2.5g/kg[28]卡波姆934P LDb50(豚鼠,口服):2.5g/kg卡波姆940 LD50(豚鼠,口服):2.5g/kg卡波姆934P LD50(小鼠,IP):0.04g/kg卡波姆940 LD50(小鼠,IP):0.04g/kg卡波姆934P LD50(小鼠,IV):0.07g/kg卡波姆940 LD50(小鼠,IV):0.07g/kg卡波姆934P LD50(小鼠,口服):4.6g/kg卡波姆934 LD50(小鼠,口服):4.6g/kg卡波姆940 LD50(小鼠,口服):4.6g/kg卡波姆910 LD50(大鼠,口服):10.25g/kg卡波姆934P LD50(大鼠,口服):2.5g/kg卡波姆934 LD50(大鼠,口服):4.1g/kg卡波姆940 LD50(大鼠,口服):2.5g/kg卡波姆941 LD50(大鼠,口服):>1g/kg15 操作注意事项遵守材料操作的环境和数量相应的注意事项。
应尽量避免产生过多的粉末,以避免爆炸的危险。
最低爆炸浓度为100g/m3。
卡波姆粉末对眼、黏膜、呼吸道有刺激。
与眼接触时,卡波姆粉末由于形成凝胶状的膜,难以用水除去,需要用盐水冲洗。
建议在操作时使用手套,保护眼睛和防尘呼吸器。
16 法规已收载于FDA《非活性组分指南》(用于口服混悬剂和片剂,眼用制剂、直肠制剂和局部用制剂)。