—甲醇;—醇;—异丙醇;—丙酮;—正丙醇;—
- 格式:doc
- 大小:27.50 KB
- 文档页数:2

有机化学复习题一、命名或写化学结构式(有立体异构的要注明)1. 5-(1,2-二甲基丙基)壬烷2. (S)-1,6-二甲基环己烯3. 4-甲氧基-3-溴苯甲醛4. 3,3’-二氯-4,4’-联苯二胺5. (2S,3R)-3-甲基-2-己醇6. 1-硝基-6-氯萘7. (R,Z)-4-甲基-2-己烯8. 5-甲基-1,3-环己二烯甲酰氯9. N-甲基环己烷磺酰胺10. (2R,5S)-2-氯-5-溴-3-己炔11. (Z,Z)-2-溴-2,4-辛二烯12. (2R,3R)-3-氯-2-溴戊烷13. (1R,3R)-3-甲基环己醇14.N,N-二乙基间甲基苯甲酰胺15. 2-甲基-3, 3-二氯戊酸钠16. 二环[4.3.0]-壬酮17. 异丙基烯丙基酮18. 反-1-甲基-4-溴环己烷19.1-对甲苯基-2-氯丁烷20.N-甲基-N-乙基对异丙基苯甲酰胺21.二苄醚22.四氢呋喃23.3-甲氧基-1-戊醇24.苯基环氧乙烷25.(R)3-苯基-3-氯丙酸26.(E)-4-甲基-4-烯-3-己炔酮27.对苯氧基苯甲酸28.3-甲基-4-异丙基庚烷29.5-(1, 2-二甲基丙基) 壬烷30.(R)- -溴代乙苯31.2-甲基-3-乙基己烷32.顺-1, 2-二甲基环己烷(优势构象) 33.苄基氯34.5-乙基-4-辛醇35. 乙丙酐36. DMF(N, N-二甲基甲酰胺)37. (S)-2-氯丁烷(请写出Fischer投影式)38. 偶氮苯39. 吲哚40. 4-乙基-1-庚烯-5-炔41. TMS(四甲基硅烷)42. 苯并-15-冠-543. (E)-2-甲基-1-氯-2-戊烯44.(2S,3R)-1,2,3,4-丁四醇(标出R、S构型)二、选择题1. 最稳定的碳正离子是()(A)H2C CHCH2(B)H2C CHH2C CH2(C)H2C CHHC CH3(D)H2C CHC(CH3)22 . 具有顺反异构体的物质是()(A)H3C CHC COOH3(B)H3C CHC CH3CH3(C)H3C C CHH2C3CH3(D)H2C CH23. 2—氯丁烷最稳定的构象是()(A)3H3(B)3H3(C)3H3(D)3H34. 下列化合物中,具有手性的是()B. C. D.5. 下列分子或离子中,亲核性最强的是()A. H2OB. HO-C. H2N-D. NH36. 下列羰基化合物发生亲核加成反应的速度次序是()(1)HCHO (2)CH3COCH3(3)CH3CHO (4)C6H5COC6H5(A)(1)>(2)>(3)>(4) (B)(4)>(3)>(2)>(1) (C)(4)>(2)>(3)>(1) (D)(1)>(3)>(2)>(4)7. 下列羧酸酯在酸性条件下发生水解反应的速度次序是()(1)CH 33)3O(2)CH 3COCCH 2CH 3O(3)CH 3COCH(CH 3)2O (4)CH 33O(A ) (4)>(2) >(3) >(1) (B )(1)>(3) >(2) >(4) (C ) (4)>(3) >(2) >(1) (D )(1)>(2) >(4) >(4)8. 下列化合物的酸性次序正确的是 ( )(1)CH 3CH 2CNH 3O(2)ClCH 2CH 2NH 3 (3)CH 3CH 2CH 2NH 3 (4)CH 3CH 2SO 2NH 3 (A ) (4)>(1) >(2) >(3) (B )(1)>(3) >(2) >(4) (C ) (2)>(3) >(1) >(4) (D )(4)>(3) >(2) >(1) 9 . 下列化合物于NaHSO3饱和溶液反应最快的是( )A.B.C. .D.10. 下列化合物按E1机理消除HBr时,最容易的是( )A.B.C.D.11.下列碳正离子最稳定的是 ( )(A )(CH 3)2C CHCH 2 (B )CH 3CHCH 3 (C )H 2C CHCH 2 (D )12 .下列化合物酸性最强的是 ( ) (A )CH 3CH 3 (B )H 2CCH 2 (C )HCCH (D )HC CCH 313 .在下列化合物中,最容易进行亲电加成反应的是 ( ) (A )H 2C CHCH CH 2 (B )H 3C C H C HCH 3(C )H 3CC H C HCHO(D )H 2C CHCl14 .在下列化合物中,熔点最高的是 ( )(A)(B)n—C6H14(C)n—C7H1615 . 在下列化合物中,偶极矩最大的是();偶极矩最小的是()。

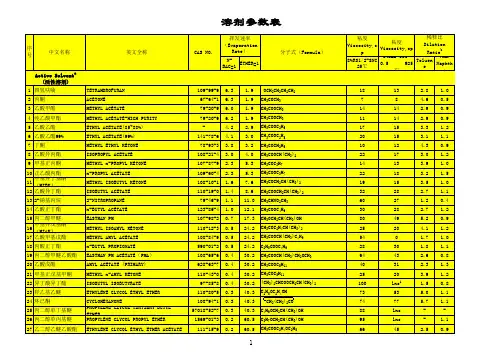
深圳市变色科技有限公司专业生产感温变色颜料Thermochromic Material 一.可逆感温变色颜料的变色原理和结构:感温变色颜料是一种随温度上升或下降而反复改变颜色的微胶囊。
可逆感温变色颜料是由电子转移型有机化合物体系制备的。
电子转移型有机化合物是一类具有特殊化学结构的有机发色体系。
在特定温度下因电子转移使该有机物的分子结构发生变化,从而实现颜色转变。
这种变色物质不仅颜色鲜艳,而且可以实现从“有色===无色”和“无色===有色”状态的颜色变化,这是重金属复盐络合物型和液晶型可逆感温变色物质所不具备的。
微胶囊化的可逆感温变色物质称为可逆感温变色颜料(俗称:温变颜料,感温粉或温变粉)。
这种颜料的颗粒呈圆球状,平均直径为2~7微米(一微米等于千分之一毫米)。
其内部是变色物质,外部是一层厚约0.2~0.5微米既不能溶解也不会融化的透明外壳,正是它保护了变色物质免受其他化学物质的侵蚀。
因此,在使用中避免破坏这层外壳是十分重要的。
二. 感温变色颜料的基本色:目前本公司生产的可逆感温变色颜料在显色状态有以下15个基本色:1、感温变色颜料之间的互配和拼色:因为可逆感温变色颜料在隐色状态时是无色的,这使得不同颜色/不同变色温度/不同系列的变色颜料之间可以互配和拼色,从而获得更加丰富多彩的变色效果。
2-1、感温变色颜料基本色之间的互配:将基本色之间按一定比例互配,可以获得许多过渡色无色的变色效果。
例如:2-2、感温变色颜料与普通颜料之间拼色:可以获得色A 色B 的变色效果。
例如:三、热敏变色颜料的类型:1、热消色型(R系列):在低温时为有色状态,当温度升至设定值时颜料从有色变为无色。
它的变色温度可根据用户需要在-20~80℃范围内设定:。
R系列变色颜料的品种最多,色谱齐全,是最常用的变色颜料系列。
其色~温关系曲线如图1所示:图 1. R系列色~温关系曲线图 2. F系列色~温关系曲线2、热发色型(F系列):其色~温特性与R系列正相反。
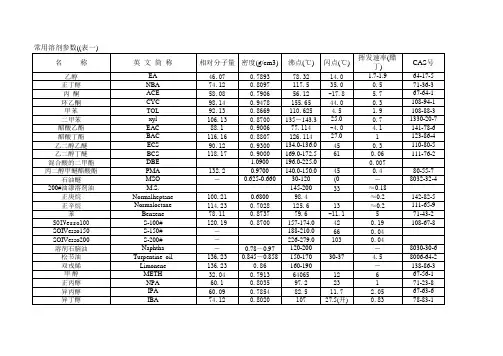

常见的共沸物共沸物水/乙醇水/正丙醇水/异丙醇水/正丁醇水/异丁醇水/叔丁醇水/异戊醇水/正戊醇水/氯乙醇水/乙醚水/乙腈水/丙烯腈水/甲酸水/丙酸水/乙酸乙酯水/二氧六环水/氯仿水/四氯化碳水/二氯乙烷水/苯水/甲苯水/二甲苯水/吡啶水/二硫化碳甲醇/二氯甲烷甲醇/氯仿甲醇/四氯化碳甲醇/丙酮甲醇/苯甲醇/甲酸甲酯/环己烷乙醇/乙酸乙酯乙醇/苯乙醇/氯仿乙醇/四氯化碳乙醇/苯/水乙酸乙酯/四氯化碳乙酸乙酯/环己烷乙酸甲酯/环己烷氯仿/丙酮组分的沸点(℃) 100/78.5 97.2 82.4 117.7 108.4 82.5 131.0 138.3 129.0 35 81.5 78.0 101 141.4 78 101.3 61.2 77.0 83.7 80.4 110.5 137-140.5 115.5 46 64.7/41 56.2 77.0 56.2 80.617.8/48.6/33.6 78.3/78.0 80.6 61.2 77.0 78.3/80.6/100 78.0/77.0 61.2/56.4 组成(w/w) 5/95 28.8/71.2 12.1/87.9 37.5/62.5 30.2/69.8 11.8/88.2 49.6/50.444.7/55.3 59.0/41.0 1.0/99.0 14.2/85.8 13.0/87 26/74 82.2/17.8 9.0/91 18/822.5/97.5 4.0/96 19.5/80.5 8.8/91.2 20/80 37.5/62.5 42/58 2.0/98.0 7.3/92.712/88 21/79 12/88 39.1/60.9 50.8 30/70 32/68 7/93 16/84 19/74/7 43/57 46/5483/17 80/20 共沸点(℃) 78.15 87.7 80.4 92.2 89.9 79.9 95.1 95.4 97.8 34 76 70.0 107 99.1 70 87.8 56.1 66.0 72.0 69.2 85.0 92.0 94.0 44 37.8 55.5 55.7 55.5 57.6 72.0 68.2 59.4 65.1 64.9 75.0 71.6 54.9 64.7 甲苯/乙酸 101.5/118.5 72/28 105.4 又称恒沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分与沸点均保持不变。
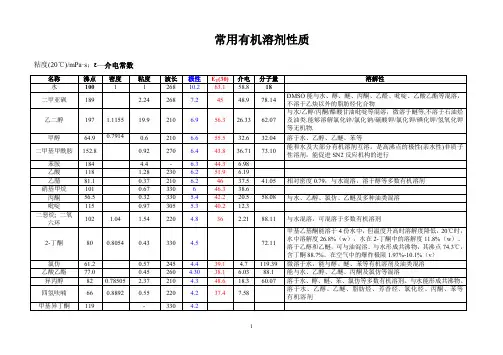
常用有机溶剂性质粘度(20℃)/mPa·s; —介电常数名称沸点密度粘度波长极性E T(30) 介电分子量溶解性水100 1 1 268 10.2 63.1 58.8 18二甲亚砜189 2.24 268 7.2 45 48.9 78.14 DMSO能与水、醇、醚、丙酮、乙醛、吡啶、乙酸乙酯等混溶,不溶于乙炔以外的脂肪烃化合物乙二醇197 1.1155 19.9 210 6.9 56.3 26.33 62.07 与水/乙醇/丙酮/醋酸甘油吡啶等混溶,微溶于醚等,不溶于石油烃及油类.能够溶解氯化锌/氯化钠/碳酸钾/氯化钾/碘化钾/氢氧化钾等无机物.甲醇64.9 0.7914 0.6 210 6.6 55.5 32.6 32.04 溶于水、乙醇、乙醚、苯等二甲基甲酰胺152.8 0.92 270 6.4 43.8 36.71 73.10 能和水及大部分有机溶剂互溶,是高沸点的极性(亲水性)非质子性溶剂,能促进SN2反应机构的进行苯胺184 4.4 - 6.3 44.3 6.98乙酸118 1.28 230 6.2 51.9 6.19乙腈81.1 0.37 210 6.2 46 37.5 41.05 相对密度0.79,与水混溶,溶于醇等多数有机溶剂硝基甲烷101 0.67 330 6 46.3 38.6丙酮56.5 0.32 330 5.4 42.2 20.5 58.08 与水、乙醇、氯仿、乙醚及多种油类混溶吡啶115 0.97 305 5.3 40.2 12.3二恶烷; 二氧六环102 1.04 1.54 220 4.8 36 2.21 88.11 与水混溶,可混溶于多数有机溶剂2-丁酮80 0.8054 0.43 330 4.5 72.11 甲基乙基酮能溶于4份水中,但温度升高时溶解度降低,20℃时,水中溶解度26.8%(w),水在2-丁酮中的溶解度11.8%(w)。
溶于乙醇和乙醚,可与油混溶。


6章思考题6.1 试解释实验中所遇到的下列问题:(1)(1)金属钠可用于除去苯中所含的痕量H2O,但不宜用于除去乙醇中所含的水。
(2)(2)为什么制备Grignard试剂时用作溶剂的乙醚不但需要除去水分,并且也必须除净乙醇(乙醇是制取乙醚的原料,常参杂于产物乙醚中)。
(3)(3)在使用LiAlH4的反应中,为什么不能用乙醇或甲醇作溶剂?6.2 叔丁基醚[(CH3)3C]2O既不能用Williamson法也不能用H2SO4脱水法制得,为什么?6.3 苯酚与甲苯相比有以下两点不同的物理性质:(a)苯酚沸点比甲苯高;(b)苯酚在水中的溶解度较甲苯大。
你能解释其原因吗?6.4 解释下列现象(1)(1)从2-戊醇所制得的2-溴戊烷中总含有3-溴戊烷。
(2)(2)用HBr处理新戊醇(CH3)2C-CH2OH时只得到(CH3)2CBrCH2CH3。
解答6.1 答(1)乙醇的活泼氢能与Na发生反应,苯与Na无反应。
(2)RMgX不仅是一种强的亲核试剂,同时又是一种强碱,可与醇羟基中的H结合,即RMgX可被具活性氢的物质所分解,如(3)LiAlH4既是一种强还原剂,又是一种强碱,它所提供H-与醇发生反应,如6.2叔丁基醚用H2SO4脱水法合成时,主要产生烯烃。
6.3 答甲苯和苯酚的相对分子质量相近,但是甲苯的沸点110.6℃,而苯酚的沸点181.8℃,这是由于苯酚可以形成分子间氢键;甲苯不溶于水,而苯酚易溶于水,是由于苯酚与水分子之间会形成氢键:6.4习题6.1比较下列各组化合物与卢卡斯试剂反应的相对速度:(1) 正戊醇, 2-甲基-2-戊醇, 二乙基甲醇(2) 苄醇, 对甲基苄醇, 对硝基苄醇(3)(3)苄醇, α-苯基乙醇, β-苯基乙醇6.26.2区别下列各组化合物:(1) CH2=CHCH2OH, CH3CH2CH2OH , CH3CH2CH2Br, (CH3)2CHI(2) CH3CH(OH)CH3, CH3CH2CH2OH , C6H5OH , (CH3)3COH , C6H5OCH3(3) α-苯基乙醇, β-苯基乙醇, 对乙基苯酚, 对甲氧基甲苯6.36.3写出下列各反应主要产物:6.4合成题:(1)(1)甲醇, 2-丁醇→ 2-甲基丁醇(2)(2)正丙醇, 异丙醇→ 2-甲基-2-戊醇(3)(3)甲醇, 乙醇→正丙醇, 异丙醇(4)(4)2-甲基丙醇, 异丙醇→ 2,4-二甲基-2-戊烯(5)(5)丙烯→ 甘油→ 三硝酸甘油酯(6)(6)苯, 乙烯, 丙烯→ 3-甲基-1-苯基-2-丁烯(7)(7)乙醇→ 2-丁醇(8)(8)叔丁醇→ 3, 3-二甲基-1-丁醇(9)(9)乙烯→ 三乙醇胺(10)(10)丙烯→ 异丙醚(11)(11)苯, 甲醇→ 2,4-二硝基苯甲醚(12)(12)乙烯→ 正丁醚(13)(13)苯→ 间苯三酚(14)(14)苯→ 对亚硝基苯酚(15)(15)苯→ 2,6-二氯苯酚(16)(16)苯→ 对苯醌二肟6.5某醇C5H12O氧化后生成酮,脱水则生成一种不饱和烃, 将此烃氧化可生成酮和羧酸两种产物的混合物, 试推测该醇的结构.6.6有一化合物(A)的分子式为C5H11Br, 和NaOH水溶液共热后生成C5H12O(B). B具有旋光性.能和钠作用放出氢气, 和浓硫酸共热生成C5H10(C). C经臭氧化和在还原剂存在下水解, 则生成丙酮和乙醛. 试推测A, B, C的结构, 并写出各步反应式.6.7新戊醇在浓硫酸存在下加热可生成不饱和烃. 将这不饱和烃经臭氧化后, 在锌粉存在下水解, 可得到一种醛和一种酮. 试写出反应历程及各步反应产物的构造式.6.8分离下列各组化合物:(1)(1)乙醚中混有少量乙醇(2)(2)戊烷, 1-戊炔和1-甲氧基-3-戊醇6.9 下列各醚和过量的浓氢碘酸反应, 可生成何种产物?(1)(1)甲丁醚(2)(2)2-甲氧基己烷(3)(3)2-甲基-1-甲氧基戊烷6.10有一化合物的分子式为C6H14O, 常温下不与金属钠反应, 和过量的浓氢碘酸共热时生成碘烷, 此碘烷与氢氧化银作用则生成丙醇. 试推测此化合物的结构, 并写出反应式.6.11 有一化合物的分子式为C7H16O, 并且:(1)(1)在常温下它不和金属钠反应;(2)(2)它和过量浓氢碘酸共热时生成C2H5I和C5H11I . 后者与氢氧化银反应生成的化合物的沸点为138℃.试推测原化合物的结构, 并写出各步反应式.6.12有一化合物的分子式为C20H21O4N, 与热的浓氢碘酸反应可生成碘甲烷. 当此化合物4.24 mg与氢碘酸反应, 所生成的碘甲烷通人硝酸银的醇溶液, 得到11.62mg碘化银. 问此化合物含有几个甲氧基?6.13 写出环氧乙烷与下列试剂反应的方程式:(1)(1)有少量硫酸存在下的甲醇(2)(2)有少量甲醇钠存在下的甲醇6.14 推测下列反应的机理。

常见的共沸物共沸物组分的沸点(度)组成(w/w) 共沸点(度)水--乙醇 100--78.5 5--95 78.15水--正丙醇--97.2 28.8--71.2 87.7水--异丙醇--82.4 12.1--87.9 80.4水--正丁醇--117.7 37.5--62.5 92.2水--异丁醇--108.4 30.2--69.8 89.9水--叔丁醇--82.5 11.8--88.2 79.9水--异戊醇--131.0 49.6--50.4 95.1水--正戊醇--138.3 44.7--55.3 95.4水--氯乙醇--129.0 59.0--41.0 97.8水--乙醚--35 1.0--99.0 34水--乙腈--81.5 14.2--85.8 76水--丙烯腈--78.0 13.0--87 70.0水--甲酸--101 26--74 107水--丙酸--141.4 82.2--17.8 99.1水--乙酸乙酯--78 9.0--91 70水--二氧六环--101.3 18--82 87.8水--氯仿--61.2 2.5--97.5 56.1水--四氯化碳--77.0 4.0--96 66.0水--二氯乙烷--83.7 19.5--80.5 72.0水--苯--80.4 8.8--91.2 69.2水--甲苯--110.5 20--80 85.0水--二甲苯--137-140.5 37.5--62.5 92.0水--吡啶--115.5 42--58 94.0水--二硫化碳--46 2.0--98.0 44甲醇--二氯甲烷 64.7--41 7.3--92.7 37.8甲醇--氯仿--56.2 12--88 55.5甲醇--四氯化碳--77.0 21--79 55.7甲醇--丙酮--56.2 12--88 55.5甲醇--苯--80.6 39.1--60.9 57.6甲醇/甲酸甲酯/环己烷 17.8/48.6/33.6 50.8乙醇--乙酸乙酯 78.3--78.0 30--70 72.0乙醇--苯--80.6 32--68 68.2乙醇--氯仿--61.2 7--93 59.4乙醇--四氯化碳--77.0 16--84 65.1乙醇/苯/水78.3/80.6/100 19/74/7 64.9乙酸乙酯--四氯化碳78.0--77.0 43--57 75.0乙酸乙酯--环己烷 46--54 71.6乙酸甲酯--环己烷83--17 54.9氯仿--丙酮 61.2--56.4 80--20 64.7甲苯--乙酸 101.5--118.5 72--28 105.4(a)与水形成的二元共沸物(水沸点100℃)(b)常见有机溶剂间的共沸混合物。

化学试剂安全操作规定按照公司实验室及生产车间常用化学试剂的种类,现制定以下几类化学试剂安全操作规定.对于同时属于几个种类的化学试剂,则在使用时必须同时遵守相应的安全操作规定。
一、易燃化学试剂我司在用的易燃化学试剂主要包括易燃液体和易燃固体,其中大多是极易挥发的液体,遇明火即可燃烧。
我司在用的易燃液体有:甲醇、乙醇、乙腈、乙醚、乙酸乙酯、丙酮、正丙醇、异丙醇、正丁醇、四氢呋喃、双乙酰、异戊醇、正己烷、正庚烷、苯等;易燃固体有:六亚甲基四胺、保险粉(低亚硫酸钠)、硼氢化钾、苊等,在使用这些化学试剂时必须严格遵守易燃化学试剂安全操作规定。
易燃化学试剂安全操作规定为:1.使用易燃化学试剂的人员,必须切实了解所用试剂的性质及危害,掌握处理这些试剂及个人防护的方法.2.在使用易燃化学试剂时,实验室和车间内设有通风柜或排气罩的,必须在通风柜内或排气罩下进行操作;没有通风柜或排气罩的,必须保持操作现场良好的通风。
3.在使用易燃化学试剂时,绝对不能使用明火,且加热时不能直接用加热器加热.4.在不慎将易燃化学试剂弄翻时,对于可溶解于水的试剂必须立即采用清水冲洗,对于不溶于水的试剂应立即用抹布、拖把等擦干或其它合适有效的方法将受污染部位进行清洁;若沾染到身体、衣物,则必须立即进行洗手、洗澡及更衣等。
5.在各实验室和车间中,易燃化学试剂应定点存放在阴凉通风处,不能存放于普通冰箱,存放数量一般应控制在1~2瓶(最小包装).当需要大量使用时,须预先与仓库保管人员联系,按当天用多少则领多少的原则领用。
二、有毒化学试剂一般的化学试剂对人体都有毒害,在使用时一定要避免大量吸入,并且在使用后,必须及时洗手、更换工作服.对于按照《剧毒化学品名录2002版》规定属于剧毒品的化学试剂,在使用时必须按照国家有关法规和公司《剧毒物品安全管理规程度》及相应的操作规定进行,其余按照《危险化学品名录2002版》规定属于毒害品的有毒化学试剂,如公司在用的硫酸铜、氯化钡、二氯甲烷、三氯甲烷、巯基乙醇、邻苯二胺、二盐酸—1—萘乙二胺、苯酚、丙烯酰胺、甲叉双丙烯酰胺、环氧氯丙烷等,在使用时必须严格遵守有毒化学试剂安全操作规定。

实验室常用毒、麻、精、放药品目录1. 毒品:西药类:金属砷、三氧化二砷(亚砷酸)、硫化砷、三硫化砷(雌黄)、五硫化钾(雄黄)、砷酸钾、亚砷酸钾、亚酸砷钠、亚砷酸钙、砷酸硼、二氧化硒、偏钒酸钠、砒石(红矾)五氧化二钒、白砒、亚砒酸、苯巴比妥(鲁米钠)巴比妥酸、硫代巴比妥酸(TBA)、巴比妥钠、巴比妥、戊巴比妥钠、苯巴比妥钠、阿米妥钠、阿片粉、去水吗啡、盐酸乙基吗啡、盐酸吗啡、盐酸吗啡针、海洛因、吗啡阿托品、氢溴酸后吗托品、磷酸可待因、盐酸可卡因、盐酸普罗卡因、硝酸士的年、马钱子碱、硝基马钱子硷、马钱子丁碱、硝酸毛果云香碱、氢溴酸东芭苍碱、Cauehaviein、Pricaine、毒毛旋花素K、箭毒、盐酸毒箭毒、氯化简箭毒、水杨酸毒扁豆碱、印防己毒素、盐酸佐旋麻黄素、红色氧化汞、黄色氧化汞、氯化汞、溴化汞、碘化汞、黄硫化汞、黑硫化汞、硝酸汞、硝酸亚汞、对氯汞苯甲酸、乙酸汞、乙酸亚汞、乙酸第二水银、水杨酸汞、流氰化汞、流氰酸汞、汞、汞碘化银、流氰酸汞铵、偏钒酸铵、氰化钾、氰化钠、氰化铜、氰化亚铜、氰氢酸、溴化氰、氯化钡、三氧化锑、三氧化二锑、饿酸。
中药类:砒石、砒霜、水银、生马钱子、生传乌、生草乌、生白附子、生附子、生半夏、生南星、生巴豆、斑蝥、青娘虫、红娘虫、生甘遂、生狼毒、生藤黄、生千金子、生天仙子、闹羊花、雪上枝蒿、白降丹、蟾酥、洋金花、红粉、轻粉、雄黄。
2.麻醉品:(1)阿片类(2)阿片生物碱类(3)可卡因(4)吗啡代用品(5)大麻类3.精神药品:吗啡、杜冷丁、强痛定、安钠咖、咖啡因、复方樟脑西丁等4.放射性药品:3H、14C、32P、35S、45Ca、51Cr、68Ga、59Fe、86Rb、125I、131I、99mTc等附件四:实验室常用易燃、易爆化学试剂目录1.苯类:苯、联苯、异丙苯、乙基苯、丁基苯、135三甲苯、碘代苯、氯苯、对二氯苯、邻二氯本、间二氯苯、对硝基氯代苯、2,4二硝基氯代苯、对硝基溴代苯、六氢代苯、邻溴氯苯、第二丁基苯、第三丁基苯、偶氮苯、聚氯羟苯、硝基苯、间二硝基苯、甲苯、二甲苯、对二甲苯、1,2,4,5四甲基苯、三氯甲苯、3,4二氯甲苯、间溴甲苯、间硝基甲苯、2,4二硝基甲苯,2,4一二硝基氟苯,二乙烯苯,过氧化羟异丙苯。
常见溶剂极性大小比较对于极性,也不是绝对的数值可以衡量的,因为作为极性大小的评判标准,有多几种参数,而不同的参数得出的有机溶剂的极性大小排序并不完全相同单一溶剂的极性大小顺序为:石油醚(小)→环己烷→四氯化碳→三氯乙烯→苯→甲苯→二氯甲烷→氯仿→乙醚→乙酸乙酯→乙酸甲酯→丙酮→正丙醇→乙醇→甲醇→吡啶→乙酸(大)水(最大)>甲酰胺>三氟乙酸>DMSO>乙腈>DMF>六甲基磷酰胺>甲醇>乙醇>乙酸>异丙醇>吡啶>四甲基乙二胺>丙酮>三乙胺>正丁醇>二氧六环>四氢呋喃>甲酸甲酯>三丁胺>甲乙酮>乙酸乙酯>三辛胺>碳酸二甲酯>乙醚> 异丙醚>正丁醚>三氯乙烯>二苯醚>二氯甲烷>氯仿>二氯乙烷>甲苯>苯>四氯化碳>二硫化碳>环己烷>己烷>煤油(石油醚)(最小)混合溶剂的极性顺序:苯∶氯仿(1+1)→环己烷∶乙酸乙酯(8+2)→氯仿∶丙酮(95+5)→苯∶丙酮(9+1)→苯∶乙酸乙酯(8+2)→氯仿∶乙醚(9+1)→苯∶甲醇(95+5)→苯∶乙醚(6+4)→环己烷∶乙酸乙酯(1+1)→氯仿∶乙醚(8+2)→氯仿∶甲醇(99+1)→苯∶甲醇(9+1)→氯仿∶丙酮(85+15)→苯∶乙醚(4+6)→苯∶乙酸乙酯(1+1)→氯仿∶甲醇(95+5)→氯仿∶丙酮(7+3)→苯∶乙酸乙酯(3+7)→苯∶乙醚(1+9)→乙醚∶甲醇(99+1)→乙酸乙酯∶甲醇(99+1)→苯∶丙酮(1+1)→氯仿∶甲醇(9+1)说明一下: 苯∶甲醇(95+5)的意思是95体积的苯混合5体积的甲醇配成混合溶剂!官能团极性大小比较:烷烃(—CH3,—CH2—)<烯烃(—CH=CH—)<醚类(—O—CH3,—O—CH2—)<硝基化合物(—NO2)<二甲胺(CH3—N—CH3)<脂类(—COOR)<酮类(—CO—)<醛类(—CHO)<硫醇(—SH)<胺类(—NH2)<酰胺(—NHCO—CH3)<醇类(—OH)<酚类(<Ar—OH)<羧酸类(—COOH)常用流动相极性:石油醚<汽油<庚烷<己烷<二硫化碳<二甲苯<甲苯<氯丙烷<苯<溴乙烷<溴化苯<二氯乙烷<三氯甲烷<异丙醚<硝基甲烷<乙酸丁酯<乙醚<乙酸乙酯<正戊烷<正丁醇<苯酚<甲乙醇<叔丁醇<四氢呋喃<二氧六环<丙酮<乙醇<乙腈<甲醇<氮氮二甲基甲酰胺<水。
《室内装饰装修材料内墙涂料中有害物质限量》GB18582-2008前言本标准代替GB 18582-2001《室内装饰装修材料内墙涂料中有害物质限量》。
本标准与GB 18582-2001相比主要技术差异:——范围中增加了水性墙面腻子,并对其规定了有害物质限量值;——水性墙面涂料中挥发性有机化合物的限量值大幅度降低,表示方法改为产品中除水后的挥发性有机化合物的含量;——游离甲醛计量单位改变,其限量值更加严格;——增加了苯、甲苯、乙苯和二甲苯总和控制项目;——增加了挥发性有机化合物的定义,测试方法由总挥发物扣除水分改为用气相色谱分析技术分离被测样品中各种挥发性有机化合物并定性鉴定和定量分析;——修改完善了游离甲醛和可溶性重金属的测试方法;——建立了苯、甲苯、乙苯和二甲苯总和的测试方法,并将其与测试挥发性有机化合物方法相结合。
本标准的附录A 、附录B 、附录C 、附录D 为规范性附录。
本标准由中国石油和化学工业协会提出。
本标准由全国涂料和颜料标准化技术委员会归口。
本标准负责起草单位:中国化工建设总公司常州涂料化工研究院(国家涂料质量监督检验中心)、北京微量化学研究所、上海市涂料研究所。
本标准参加起草单位:中国涂料工业协会、上海市建筑科学研究院、中国建筑科学研究院、立邦涂料(中国)有限公司、广东华润涂料有限公司、广东嘉宝莉化工有限公司、卜内门太古漆油(中国)有限公司、上海中南建筑材料公司、广东美涂士化工有限公司、莆田市三江化学工业有限公司、中华制漆(深圳)有限公司、南宝树脂(中国)有限公司、江苏大象东亚制漆有限公司、罗门哈斯(中国)投资有限公司、杭州油漆有限公司、南京天祥涂料有限公司、常州光辉化工有限公司、东莞大宝化工制品有限公司、上海富臣化工有限公司、广东巴德士化工有限公司。
本标准主要起草人:张俊智、赵玲、冯世芳、黄宁、于滨、尹建武、张卫群、曹海华、黄添源、杨勇、龚万森、段质美、寇辉、王代民、熊荣、王大期、李锋、彭冬华、凌萍、姜亚琴、杨少武、杨卫疆、姜方群、徐凯斌、刘琳、黄建华、叶荣森、方学平。