高中化学必修二 苯、芳香烃
- 格式:ppt
- 大小:799.00 KB
- 文档页数:29


芳香烃高考知识点在化学这门科学中,芳香烃是一个重要的知识点。
芳香烃是一类具有独特芳香气味的有机化合物,其分子结构含有若干个苯环。
芳香烃不仅在生活中广泛存在,如香水、某些草药的香味等,还在化学工业中具有重要应用,如合成某些药物、颜料、塑料等。
本文将深入探讨芳香烃的性质、分类以及在化学中的应用。
一、芳香烃的性质芳香烃分子结构中的苯环具有特殊的稳定性,这是因为苯环中的碳原子间存在着共轭π电子体系。
这种共轭π电子体系使得芳香烃具有很高的热稳定性和化学稳定性,不易被氧化或还原。
芳香烃分子的化学性质主要表现为取代反应和加成反应。
取代反应是指苯环中的一个或多个氢原子被其他官能团取代的反应。
而加成反应是指苯环中的π电子与其他物质发生加成反应,如硝化反应、烷基化反应等。
二、芳香烃的分类根据苯环的数量和结构,芳香烃可分为单环芳香烃和多环芳香烃。
单环芳香烃分子结构中只含有一个苯环,如苯、甲苯等。
多环芳香烃分子结构中含有两个以上苯环,如萘、蒽等。
多环芳香烃可以根据苯环之间的连接方式进一步细分,如连接为直链、连接为环状等。
三、芳香烃在化学中的应用芳香烃在化学领域有广泛的应用。
其中一个重要的应用领域是药物合成。
许多常用的药物都含有芳香环结构,如阿司匹林、苯巴比妥等。
芳香烃的稳定性使得它们能够在药物中起到稳定和延长作用。
此外,芳香烃还广泛应用于颜料的制备。
许多颜料都是由芳香烃化合物制成的,如甲苯红、甲基橙等。
芳香烃的稳定性和良好的颜色稳定性使得它们能够被广泛用于颜料的生产。
芳香烃还被用于塑料的制备。
其中一种常见的塑料就是聚苯乙烯,它由苯乙烯单体聚合而成。
聚苯乙烯具有良好的刚性和耐热性,因此广泛应用于家电、电子产品等领域。
综上所述,芳香烃作为化学中的重要知识点,其性质、分类和应用都具有一定的深度和广度。
了解芳香烃的知识,不仅能够拓宽化学知识的广度,还能够在实际应用中获得更多的启示和创新。
希望通过本文的介绍,读者们能对芳香烃有更深入的了解。

《芳香烃》教案一、教材分析:芳香烃》是人教版高中化学选修五《有机化学基础》第二章《烃和卤代烃》第2节的教学内容,主要学习苯和苯的同系物的结构和性质,在教材上呈现时突出了苯的分子结构和苯的同系物的构性知识,苯的化学性质是以探究实验形式给出的,苯的同系物的性质是根据苯的性质推导,并用实验验证得到基团之间的相互影响。
本节内容是对化学必修2中已经介绍的苯的化学性质的提升,重点介绍的是苯及其同系物的结构和化学性质。
二、教学目标::【知识与技能】1.了解苯结构特征,掌握苯和苯的同系物的化学性质2.了解芳香烃的来源及其应用【过程与方法】1.类比分析法:利用苯的架构的性质类比探究苯的同系物的性质…2.实验探究法:通过自主探究实验得出物质的性质,培养实验能力和逻辑思维能力【情感态度价值观】1.通过实验探究分析,培养学生勇于实验创新的思维能力2.培养学生比较、实验、探究的学习方法及事物间相互联系的观点三、教学重点:苯和苯的同系物的结构、化学性质[教学难点:制备溴苯实验方案的设计,苯的同系物的结构和化学性质四、教学方法:1.实验探究法:学生自主实验探究苯与酸性高锰酸钾溶液和溴水的作用现象甲苯与酸性高锰酸钾溶液的反应2.学案导学法:见学案}3、多媒体展示法:见课件4.类比分析法:比较苯与苯的同系物的结构和性质五、教学过程:课前准备:视频播放奇妙的芳香烃世界情景导入:奇妙的燃烧实验《我这里有两条滤纸,现在我要用他们作一组对比的燃烧实验,哪位同学来给我们展示一下[学生活动]:学生演示滤纸的燃烧实验:①一条直接点燃②一条用神奇的液体湿润再点燃[教师活动] :揭开它的面纱,这个物质就是苯!我们在必修2中已经学习了苯的性质,请同学们自主完成学案上苯的复习知识。
学生活动一:完成学案苯的相关复习知识苯分子式~结构式结构简式物理性质)色、气味的体,溶于水,密度比水,熔沸点,易 ,有化学性质)燃烧反应现象:取代反应)与液溴与浓硝酸加成反应与H2过渡:苯分子组成为C6H6(碳6氢6),从组成上看具有很大的不饱和性,根据苯的凯库勒结构式,苯分子是单键和双键相互交替,那么事实上是否为单键和双键相交替呢,根据已学知识如何验证(用哪些物质可以来验证是否存在碳碳双键)#[学生活动] 溴水、酸性高锰酸钾探究实验一:分别用溴水和酸性高锰酸钾溶液验证是否有碳碳双键的存在请一组同学展示实验现象,并解释产生该现象的原因,得出苯分子中不存在碳碳双键小结:实验表明,苯分子中不存在碳碳双键,能与氢气加成说明含有不饱和键,两者结合得出苯具有特殊的碳碳键。


高二化学芳香烃知识点芳香烃,通常指分子中含有苯环结构的碳氢化合物。
接下来店铺为你整理了高二化学芳香烃知识点,一起来看看吧。
高二化学芳香烃知识点1、亲电取代反应芳香烃图册主要包含五个方面:卤代:与卤素及铁粉或相应的三卤化铁存在的条件下,可以发生苯环上的H被取代的反应。
卤素的反应活性为:F>Cl>Br>I不同的苯的衍生物发生的活性是:烷基苯>苯>苯环上有吸电子基的衍生物。
烷基苯发生卤代的时候,如果是上述催化剂,可发生苯环上H取代的反应;如在光照条件下,可发生侧链上的H被取代的反应。
应用:鉴别。
(溴水或溴的四氯化碳溶液)如:鉴别:苯、己烷、苯乙烯。
(答案:step1:溴水;step2:溴水、Fe粉)。
硝化:与浓硫酸及浓硝酸(混酸)存在的条件下,在水浴温度为55摄氏度至60摄氏度范围内,可向苯环上引入硝基,生成硝基苯。
不同化合物发生硝化的速度同上。
磺化:与浓硫酸发生的反应,可向苯环引入磺酸基。
该反应是个可逆的反应。
在酸性水溶液中,磺酸基可脱离,故可用于基团的保护。
烷基苯的磺化产物随温度变化:高温时主要得到对位的产物,低温时主要得到邻位的产物。
F-C烷基化:条件是无水AlX3等Lewis酸存在的情况下,苯及衍生物可与RX、烯烃、醇发生烷基化反应,向苯环中引入烷基。
这是个可逆反应,常生成多元取代物,并且在反应的过程中会发生C正离子的重排,常常得不到需要的产物。
该反应当苯环上连接有吸电子基团时不能进行。
如:由苯合成甲苯、乙苯、异丙苯。
F-C酰基化:条件同上。
苯及衍生物可与RCOX、酸酐等发生反应,将RCO-基团引入苯环上。
此反应不会重排,但苯环上连接有吸电子基团时也不能发生。
如:苯合成正丙苯、苯乙酮。
亲电取代反应活性小结:连接给电子基的苯取代物反应速度大于苯,且连接的给电子基越多,活性越大;相反,连接吸电子基的苯取代物反应速度小于苯,且连接的吸电子基越多,活性越小。
2、加成反应与H2:在催化剂Pt、Pd、Ni等存在条件下,可与氢气发生加成反应,最终生成环己烷。

芳香烃【学习目标】1、认识芳香烃的组成、结构;2、了解苯的卤代、硝化及加氢的反应||,知道苯的同系物的性质、苯的同系物与苯性质的差异;3、结合生产、生活实际了解某些烃、烃的衍生物的重要作用及对环境和健康可能产生的影响||,芳香烃类物质在有机合成和有机化工中的重要作用||。
【要点梳理】要点一、苯的结构和性质分子中含有一个或多个苯环的碳氢化合物都属于芳香烃||。
我们已学习过最简单、最基本的芳香烃——苯||。
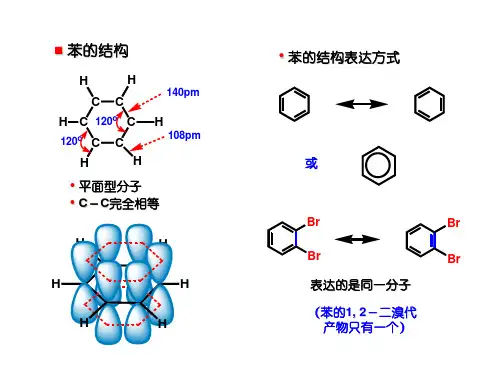
1.分子结构||。
苯的分子式为C 6H 6||,结构式为||,结构简式为 或 ||。
大量实验表明||,苯分子里6个碳原子之间的价键完全相同||,是一种介于单键和双键之间的独特的键||。
苯分子里的所有原子都在同—平面内||,具有平面正六边形结构||,键角为120°||,是非极性分子||。
2.物理性质||。
苯是无色有特殊气味的液体||,不溶于水||,密度比水小||,熔点5.5℃||,沸点80.1℃||,苯用冰冷却可凝结成无色的晶体||,苯有毒||。
3.化学性质||。
苯的化学性质比较稳定||,但在一定条件下||,如在催化剂作用下||,苯可以发生取代反应和加成反应||。
(1)取代反应||。
(溴苯是无色液体||,不溶于水||,密度比水大)(硝基苯是无色||,有苦杏仁味的油状液体||,密度比水大||,不溶于水||,有毒)(2)加成反应||。
(3)氧化反应||。
①苯在空气中燃烧发出明亮的带有浓烟的火焰:2 +15O 2−−−→点燃12CO 2+6H 2O ②苯不能使酸性KMnO 4溶液褪色;苯也不能使溴水褪色||,但苯能将溴从溴水中萃取出来||。
4.苯的用途||。
苯是一种重要的化工原料||,它广泛应用于生产合成纤维、合成橡胶、塑料、农药、医药、染料和香料等||,苯也常用作有机溶剂||。
特别提示:(1)苯的结构简式: ||,只是由于习惯才沿用至今||。
实际上苯分子中的碳碳键是完全相同的||。
(如与是同种物质)(2)由于苯环结构的特殊性||,在判断苯体现什么性质时要特别注意反应条件和反应物的状态||。

高一化学苯知识点苯是有机化合物中最简单的芳香烃,由六个碳原子和六个氢原子组成,化学式为C6H6。
苯作为一种重要的化学物质,在工业生产和实验室研究中都具有广泛的应用。
本文将介绍高一化学中关于苯的基本知识点。
一、结构和命名苯分子由一个六边形状的环组成,环上的碳原子通过共享电子形成σ键和π键。
苯的结构非常稳定,其中每个碳原子都连接了一个氢原子,分子中所有C-C键长度相等。
在命名上,苯可以称为苯环或苯基,苯基可以作为一个官能团出现在其他化合物中。
二、苯的性质1. 物理性质:苯是一种无色的液体,具有特殊的芳香气味。
它的密度低,沸点和熔点相对较低。
2. 化学性质:苯具有稳定的芳香性质,不易发生加成反应。
然而,苯可以通过取代反应引入其他基团。
常见的取代反应包括氮取代、卤素取代等。
三、苯的制备方法1. 从煤焦油中提取:苯可以从煤焦油中通过蒸馏分离得到。
煤焦油是煤转化或煤气化的副产物,其中含有苯、甲苯等芳香烃。
2. 烯烃环化:烯烃经过环化反应可以生成苯。
其中最典型的方法是费托合成,通过对甲苯进行脱甲基反应得到苯。
四、苯的用途苯是一种重要的有机溶剂,广泛应用于化工、轻工、医药等领域。
具体用途如下:1. 作为溶剂:苯作为一种极性溶剂,可溶解多种有机物,常用于溶解树脂、涂料、染料等。
2. 作为原料:苯可以作为合成其他化学品的重要原料。
例如,苯可以通过氢化反应制备环己烷,也可以通过硝化反应制备苯胺等。
3. 作为燃料:苯是一种可燃物质,可以用作燃料或气体增馏剂。
4. 医药应用:苯衍生物常用于制药工业,用于合成各种药物。
五、苯的危害性虽然苯在工业上有广泛的应用,但也存在一定的危害性。
苯蒸气具有一定的毒性,长期接触苯可能对人体造成损害,如造血系统疾病、免疫系统损害等。
因此,在使用苯时应注意安全措施,避免直接接触和长时间吸入。
总结:本文介绍了高一化学中关于苯的基本知识点,包括苯的结构和命名、性质、制备方法、用途以及危害性。
苯作为一种重要的有机化合物,在化工领域发挥着重要作用。
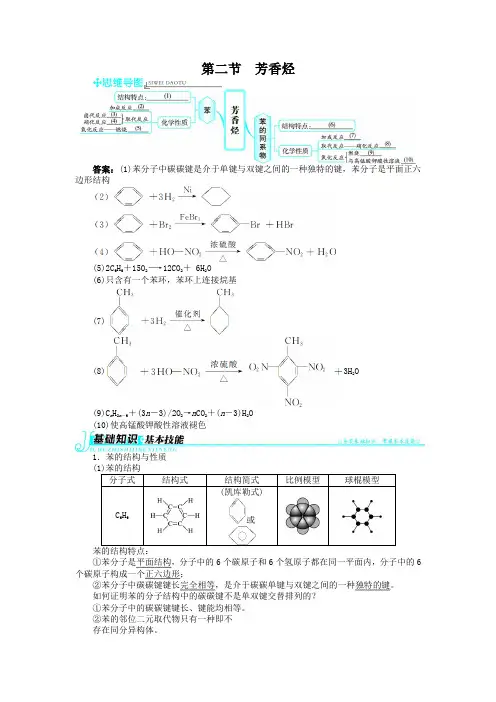

苯[知识梳理]一、苯1.苯的分子组成与结构【自主思考】1.分子中所有碳原子共平面吗?提示直接连在苯环上的原子仍在原苯环所在平面内,因此分子中所有碳原子共平面。
2.物理性质【2.如何分离苯与水的混合物?提示苯不溶于水且密度比水小,因此苯与水分层,可用分液漏斗进行分液,所得上层液体即为苯。
3.化学性质4.苯的发现及用途(1)法拉第是第一位研究苯的科学家,德国化学家凯库勒确定了苯环的结构。
(2)苯是一种重要的化工原料,也是一种重要的有机溶剂。
二、苯的同系物、芳香烃及芳香族化合物[效果自测]1.判断正误,正确的打“√”,错误的打“×”。
(1)标准状况下,22.4 L苯含有碳碳双键的数目为3N A(N A代表阿伏加德罗常数)()(2)一般用蒸馏的方法分离苯和水的混合物()(3)苯与乙烯点燃时现象相同()(4)是芳香族化合物,也是芳香烃()答案(1)×(2)×(3)×(4)×2.通常情况下,苯的化学性质较稳定,这是由于()A.苯不能使酸性KMnO4溶液褪色B.苯不与溴水发生加成反应C.苯的分子结构稳定D.苯是芳香烃答案 C3.下列有机物中,在常温、常压下为无色且密度比水小的液体是()①苯②硝基苯③溴苯④CCl4⑤环己烷A.仅②③④B.仅①⑤C.仅②③④⑤D.全部都是答案 B4.下列物质中,属于芳香化合物的是__________,属于芳香烃的是__________,属于苯的同系物的是__________(填编号)。
答案ACDEFG CDEFG DE探究一、苯的组成与结构【合作交流】1.是同一物质还是同分异构体?提示以上两种形式都是苯分子的结构简式,它们表示同一物质。
2.苯的邻位二氯代物只有一种结构,能说明苯分子中的6个碳碳键完全相同,而不是单、双键交替的形式吗?提示可以。
若苯分子为单、双键交替的结构,则其邻位二氯代物有两种结构:,若苯分子中的6个碳碳键完全相同,则其邻位二氯代物只有一种结构。
高二化学苯、芳香烃、石油的分馏【本讲主要内容】苯、芳香烃、石油的分馏苯的结构和性质,芳香烃的概念,石油分馏的原理和方法。
【知识掌握】 【知识点精析】一. 苯的物理性质和重要用途苯是一种无色的液体,有特殊气味,不溶于水,密度比水小。
熔点5.5℃,沸点为80.1℃。
有毒。
苯的重要用途:苯是一种重要的化工原料,它广泛地用于生产合成纤维、合成橡胶、塑料、农药、医药、染料和香料等,也常用作有机溶剂。
二. 苯的结构分子式:C 6H 6结构式:凯库勒式:H-C H-CCC-H C H或简写为或结构简式:或空间构型:平面正六边形的非极性分子芳香族化合物——分子里含有一个或多个苯环的有机物。
(分子中除含C 、H 元素外还可能含有O 、S 、N 、X 等。
)芳香烃——分子里含一个或多个苯环的碳氢化合物,简称芳烃。
苯环是芳香族化合物的母体,苯是最简单的芳烃。
三. 苯的化学性质 1. 氧化反应(可燃性)现象:燃烧时火焰明亮,伴有较浓的黑烟,2C 6H 6+15O 2−−→−点燃12CO 2+6H 2O 。
苯不能使酸性KMnO 4溶液褪色,也不能和溴发生加成反应,苯能将溴从溴水中萃取出来。
2. 取代反应(1)苯与溴的反应——溴化反应 反应物:苯和液溴(不能用溴水)反应条件:催化剂(Fe 粉)、温度(该反应是放热反应,常温下即可进行)。
主要生成物:溴苯(Br :无色液体,有毒,不溶于水,易溶于酒精等有机溶剂,密度大于水, )Br 2Br +催化剂+ HBr(Fe )Cl 2Cl +催化剂+ HCl(Fe )苯+液溴+Fe屑水(2)硝化反应反应物:苯和浓硝酸(HO—NO2)反应条件:催化剂浓硫酸,温度55℃~60℃主要生成物:硝基苯(NO2:无色、不溶于水、密度大于水、有苦杏仁味的油状液体。
有毒,与人体皮肤接触或其蒸气被人体吸收,都易引起中毒,易溶于酒精和乙醚,可用酒精洗去皮肤上的,它是一种制染料的重要原料。
)HO-NO++2 H2O(3)磺化反应反应物:苯和浓硫酸(HO—SO3H)反应条件:温度70℃~80℃,不必加催化剂主要生成物:苯磺酸(:无色,易溶于水,在常温下易成晶体,是一种重要的化工原料,可制烷基苯磺酸钠——洗衣粉的主要成分。
苯芳香烃一、苯的物理性质苯是无色有特殊气味的液体,密度比水小,不溶于水,苯的沸点80.1C(易挥发),熔点5.5C (结冰,无色晶体),有毒二.苯的分子结构1.分子式C6H6苯是不饱和烃。
2.苯的结构凯库勒式:苯分子是平面正六边形结构,平面形分子,12个原子共平面。
各个键的键角都是120°。
因为苯不能使酸性高锰酸钾溶液褪色,苯与溴水混合不加成。
结论:苯与一般的不饱和烃在性质上有很大的差异,苯分子中的碳碳键是介于碳碳单键与碳碳双键之间的独特的键。
用下式表示更好:既有烷烃的性质又有不饱和烃的性质3.芳香族化合物芳香族化合物:分子里含有一个或多个苯环的化合物属于芳香族化合物。
芳香烃:分子里含有一个或多个苯环的烃,苯是最简单的芳香烃。
苯的同系物:分子里含有一个苯环,侧链是烷基的烃。
三、苯的化学性质和用途易于取代,难于加成。
㈠、取代反应:①卤代用的是液溴,不是溴水,铁粉的作用:催化(真正的催化剂是FeBr3),将反应的混合物倒入水中的现象是什么?[有红褐色的油状液体沉于水底,表面有油状苯,还有红色溴]。
溴苯的物理性质如何?[比水重,不溶于水,油状]。
如何除去溴苯中的溴?[水洗,再用10%烧碱溶液洗,再干燥,蒸馏]②苯的硝化反应条件:混酸,水浴温度:50-60C;浓硫酸的作用:催化剂,吸水剂;倒入水中,硝基苯的物质性质如何?硝基苯——无色油状液体,不溶于水比水重,毒性。
③磺化反应苯磺酸:中强酸。
㈡苯的加成反应苯分子的碳碳键不是典型的双键,不容易发生加成反应,在特定条件下也能发生加成反应,注意发生加成反应的条件(1)加氢+ 3H2→环己烷(2)加氯+3Cl2→C6H6Cl6㈢、苯的氧化反应2C6H6+ 15O2→12CO2+ 6 H2O 现象:火焰明亮,有黑烟,含C% = 92.3%遇到酸性高锰酸钾四、苯的同系物1. C7H8、C8H10、C9H12用—CH3取代苯分子中的H原子,得到的分子其分子式是C7H8,其结构式是用—CH2CH3取代,得到的分子其分子式是C8H10,其结构式是,乙苯C8H10有几种同分异构体?含有苯环的同分异构体有4种:1+3用—C3H7取代,得到的分子其分子式是C9H12,其结构式是C9H12有几种同分异构体?含有苯环的同分异构体有:2+3+3它们都是苯的同系物,苯的同系物的通式是C n H2n-6。
高二化学苯和芳香烃试题答案及解析1.将浓溴水加入苯中,溴水的颜色变浅,这是由于发生了A.化学反应B.取代反应C.加成反应D.萃取过程【答案】D【解析】苯使溴水颜色变浅,是因为苯萃取了溴水中的溴,不是发生了化学反应,答案选D。
【考点】考查溴水褪色原因的判断2.下列涉及有机物的性质的说法错误的是A.苯不能使KMnO4溶液褪色,甲苯使KMnO4溶液褪色B.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝变成黑色C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了D.HNO3能与苯、甲苯、甘油、纤维素等有机物发生重要反应,常用浓硫酸作催化剂【答案】B【解析】乙醇具有还原性可以把氧化铜还原为同,因此B选项是错误的【考点】考查乙醇还原性的相关知识点3.分子式为C8H10的芳香烃的同分异构体的数目是( )A.3B.4C.5D.6【答案】B【解析】分子式为C8H10的芳香烃可能是乙苯、邻二甲苯、间二甲苯、对二甲苯四种不同的结构,因此选项是B。
【考点】考查有机物同分异构体的种类的知识。
4.下列关于苯的性质的叙述中,不正确的是A.苯是无色带有特殊气味的液体B.常温下苯是一种不溶于水但密度比水小的液体C.苯在一定条件下与溴发生取代反应D.苯不具有典型双键所具有的加成反应的性质,故不能发生加成反应【答案】D【解析】苯中的化学键是介于单键和双键之间一种特殊的键。
苯既能发生取代反应也能发生加成反应。
故D选项是错误的。
【考点】考查苯化学性质的相关知识点5.1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列事实()A.苯能发生取代反应B.能与H2发生加成反应C.溴苯没有同分异构体D.邻二溴苯只有一种【答案】D【解析】A、这种理论认为苯分子中存在单键,具有烷烃的性质,能解释苯的取代反应;B、因为是单、双键交替,存在双键,可以加成;C、溴原子连在那一个碳上,都一样;D、若是单、双键交替的话,邻二溴苯应有二种,这个现象无法解释。