九年级化学专题七 各学科交叉综合题
- 格式:doc
- 大小:649.96 KB
- 文档页数:3

【化学】九年级化学化学综合题试题(有答案和解析)含解析一、中考化学综合题1.稀硫酸是一种重要的化学试剂,现用IOg 98%的浓硫酸配制10%的稀硫酸,请回答下列问题:(1)实验的主要步骤有:计算、_______ 、配制、装瓶并贴标签。
(2)_________________________________ 由计算可知,稀释时需加水mL (水的密度为:1g∕mL),取水时选用量筒的量程最合适的是______ (填序号)。
A 25mLB 50mLC 100mLD 250mL(3)实验所需要的玻璃仪器有量筒、胶头滴管、烧杯、 _____ 和试剂瓶。
(4)某课外活动小组为测定某铜锌合金中铜的质量分数,取合金样品IOg放入烧杯,向其中逐渐加入10%的稀硫酸,所加稀硫酸与生成氢气质量的关系如图所示。
计算:*气休的两量络49加入稀硫酸的质量吕①完全反应后,产生氢气的质量为_________ g;②样品中铜的质量分数;________ (写出计算过程)【答案】量取88 C玻璃棒0.1 67.5%【解析】(1)根据浓硫酸稀释步骤解答;(2)根据计算解答需要水的体积及选择所需量筒;(3)根据浓硫酸稀释需要的仪器解答;(4)根据所加稀硫酸的质量结合反应的化学方程式计算解答。
(1)实验的主要步骤有:计算、量取、配制、装瓶并贴标签;(2)设需要加水的质量为x。
10g ×98% = (10g+x)×I0% , x=88g, 88g ×1g/ mL=88 mL。
由计算可知,稀释时需加水88 mL;取水时选用量筒的量程最合适的是100mL,故选C; (3)实验所需要的玻璃仪器有量筒、胶头滴管、烧杯、玻璃棒和试剂瓶;(4)①设完全反应后,产生氢气的质量为X,样品中锌的质量为y。
Zn+H2SO=ZnSO+H2 ↑65 98 2y 49 ×0% X65 98 2y 49g 1000 Xx=0.1gy=3.25g10g 3.25g②样品中铜的质量分数为× 10% =67.5 %10g答:①完全反应后,产生氢气的质量为0.1g ;②样品中铜的质量分数为67.5%。
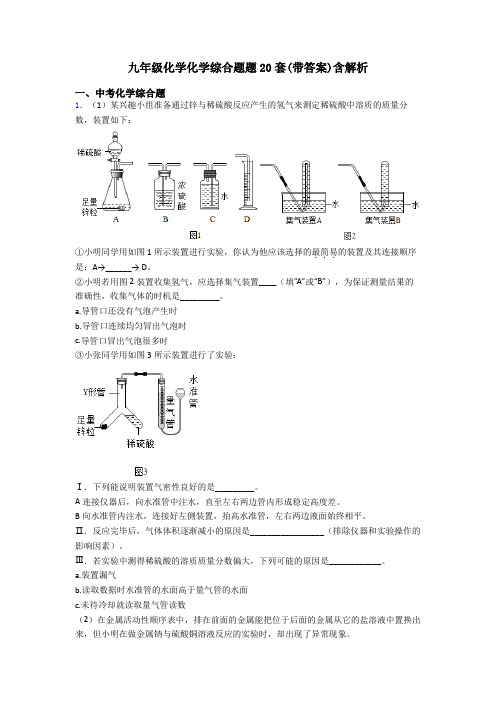
九年级化学化学综合题题20套(带答案)含解析一、中考化学综合题1.(1)某兴趣小组准备通过锌与稀硫酸反应产生的氢气来测定稀硫酸中溶质的质量分数,装置如下:①小明同学用如图1所示装置进行实验,你认为他应该选择的最简易...的装置及其连接顺序是:A→______→ D。
②小明若用图2装置收集氢气,应选择集气装置____(填“A”或“B”),为保证测量结果的准确性,收集气体的时机是_________。
a.导管口还没有气泡产生时b.导管口连续均匀冒出气泡时c.导管口冒出气泡很多时③小张同学用如图3所示装置进行了实验:Ⅰ.下列能说明装置气密性良好的是_________。
A连接仪器后,向水准管中注水,直至左右两边管内形成稳定高度差。
B向水准管内注水,连接好左侧装置,抬高水准管,左右两边液面始终相平。
Ⅱ.反应完毕后,气体体积逐渐减小的原因是_________________(排除仪器和实验操作的影响因素)。
Ⅲ.若实验中测得稀硫酸的溶质质量分数偏大,下列可能的原因是____________。
a.装置漏气b.读取数据时水准管的水面高于量气管的水面c.未待冷却就读取量气管读数(2)在金属活动性顺序表中,排在前面的金属能把位于后面的金属从它的盐溶液中置换出来,但小明在做金属钠与硫酸铜溶液反应的实验时,却出现了异常现象。
(进行实验)取一块绿豆大小的金属钠,放入盛有20毫升硫酸铜溶液的小烧杯中,发现金属钠浮在液面上不停打转,产生大量气体,烧杯发烫,溶液中出现了蓝色絮状沉淀,一会儿部分沉淀渐渐变黑,将反应后烧杯中的混合物进行过滤,得滤渣和无色滤液。
(提出问题)①生成的气体是什么?②滤渣的成分是什么?③无色滤液中的溶质是什么?(查阅资料)①钠能与水反应生成一种碱,同时放出气体。
②氢氧化铜受热至60~80℃变暗,温度再高分解为相应的金属氧化物(化合价不变)和水。
(实验探究一)探究生成的气体是什么?小明将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,把气体通入肥皂水中,将燃着的木条靠近飘起的肥皂泡,有爆鸣声。


初中化学中考各学科交叉综合题汇编及答案解析一、选择题12.(2017河北省,题号12,分值2)下列四种物质符合图4所示关系的是A.石墨B.干冰C.沥青D.陶瓷【答案】A【解析】此题考察物质的分类,物质分为纯净物和混合物,纯净物又分为单质和化合物,化合物又分为氧化物和酸、碱、盐。
A.石墨属于单质,石墨也可以导电,所以A选项正确;B.干冰是固态二氧化碳,属于晶体,但不是单质,它是化合物,所以B选项错误;C.沥青是混合物但不是晶体,所以C选项错误;D.陶瓷是混合物但不是导体,所以D选项错误;故本题选择A。
【知识点】物质的鉴别、鉴定、推断、各学科交叉综合题(2017河北省,题号10,分值2)下列科学家与他的贡献对应不正确的是A.侯德榜——联合制碱法B.门捷列夫 -----元素周期表C.阿基米德——杠杆原理:F1l1=F2l2D. 欧姆——电流通过导体产生的热量:Q=I2Rt【答案】D【解析】此题考察各科学家和相应的科学贡献。
A.侯德榜是我国制碱工业的先驱,发明了将制碱和制铵相结合的联合制碱法,选项正确,不符合题意;B.门捷列夫发现了元素周期律,并编制出元素周期表,选项正确,不符合题意;C.古希腊科学家阿基米德发现了杠杆原理,选项正确,不符合题意;D.欧姆反现了欧姆定律,通电导体产生热量是焦耳发现的焦耳定律,选项错误,符合题意;所以选择D。
【知识点】各学科交叉综合题1.(2017重庆市,题号1,分值2)下列古代文明或工艺一定包含化学变化的是:A.在甲骨上刻字B.指南针指引航海C.用泥土烧制陶瓷D 用石块修筑长城【答案】选C【解析】A.在甲骨上刻字,改变的是甲骨的外形,没有新物质生成,属于物理变化,选项错误B.指南针指引航海,指南针受到地磁场的作用指引方向,没有新物质生成,属于物理变化,选项错误C.用泥土烧制陶瓷泥土主要含有硅元素与水的混合物,而陶瓷主要成分是硅酸盐,有新物质生成,所以是化学变化。
选项正确。

九年级化学综合题题目汇编(含答案)一、 选择题1. (·连云港)下列排序正确的是( )B. 溶液的pH :――→H 2SO 4;NaCl ;NaOH由小到大C. 氮元素的化合价:――→N 2;NH 3;HNO 3由低到高D. 硫元素的质量分数:――→Na 2S ;Na 2SO 3;Na 2SO 4由小到大2. (·镇江)下列排序正确的是( ) A. 利用金属的年代:――→Al Cu Fe由先到后 B. 铁元素质量分数:――→FeO Fe 2O 3 FeS由高到低C. 碳元素的化合价:――→CH 4 CO C 60由高到低D. 物质在水中的溶解性:――→CaCl 2 CaCO 3 Ca (OH )2由大到小3. (·安徽)归纳法是学习化学的重要方法之一,下列图示正确的是( )A. 化学反应分类B. 物质分类C. 地壳中元素含量D. 金属的化学性质6. (·无锡)总结、归纳知识,有利于提升学习能力,下列知识归纳完全正确的一组是)(7. (·龙东)下列知识点归纳全部正确的是()8. (·西宁)善于梳理化学知识是学好化学的有效方法,以下梳理归纳正确的一组是()12. (·邵阳)下列图像能正确反映其对应关系的是()第12题A. ①表示向NaOH溶液中不断加水稀释B. ②表示水电解生成氢气与氧气的质量关系C. ③表示用等质量、等质量分数的过氧化氢溶液制取氧气D. ④表示分别向等质量、等质量分数的稀硫酸中加入足量的镁、铝13. (·达州)下列图像不能正确反映其对应变化关系的是()第13题A. 密闭容器中点燃红磷B. 用二氧化锰和过氧化氢溶液制氧气C. 向氯化镁和盐酸的混合溶液中,逐滴加入氢氧化钡溶液D. 分别向等质量的锌粉和铁粉中,加入足量等质量分数的稀盐酸14. (40306091)(·呼和浩特)下列四个图像不能正确反映对应变化关系的是()第14题A. 向一定量的氧化铜粉末中逐滴加入稀硫酸至过量B. 向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀盐酸至过量C. 在饱和石灰水中加入少量生石灰D. 在密闭容器中用红磷测定空气中氧气的含量15. (·岳阳)下列图像中有关量的变化趋势正确的是()第15题A. ①向一定量的盐酸和氯化钡的混合溶液中,逐渐滴加碳酸钾溶液至过量B. ②加热等质量的两份氯酸钾,一份加入二氧化锰,一份不加入二氧化锰C. ③一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应D. ④向一定量的氯化亚铁和氯化铜的混合溶液中,逐渐加入镁粉至过量16. (·南充)下列图像能正确反映对应变化关系的是()第16题A. 等质量的镁和锌中分别加入等浓度的稀H2SO4至过量B. 等质量的CaO和Ca(OH)2中分别加入等浓度的稀盐酸至过量C. CaCl2和HCl的混合溶液中加入Na2CO3溶液至过量D. AgNO3和Cu(NO3)2的混合溶液中加入锌粉至过量17. (·兰州)下列图像能正确反映相关实验过程中量的变化关系的是()第17题A. 氢氧化钠溶液加水稀释B. 一定压强下,CO2气体在水中的溶解度与温度的变化关系C. 一定温度下,向饱和的氯化钠溶液中加入氯化钠固体D. 向生锈的铁钉缓慢滴加稀盐酸18. (·新疆)下列图像能正确反映其对应变化关系的是()第18题A. 加热一定质量的KMnO4固体B. 向盛有少量H2SO4溶液的烧杯中滴加一定质量的水C. 加热一定质量KClO3和MnO2的混合物D. 向盛有一定质量NaOH和Na2CO3混合溶液的烧杯中滴加稀盐酸19. (·青岛)下列图像能正确反映其对应关系的是()第19题A. ①表示向一定量的稀硫酸中加入足量的锌粒B. ②表示向一定量稀盐酸和氯化钡的混合溶液中滴加硝酸银溶液C. ③表示向一定量的氢氧化钠溶液中滴加稀硫酸D. ④表示将等质量的大理石分别与足量的等体积等溶质质量分数的稀盐酸反应二、填空题20. (·海南)三沙市是我国位置最南、总面积最大(含海域)、陆地面积最小的地级市。

一、中考化学综合题 1. Ⅰ . 请结合下图回答问题。
( 1 )写出图中有标号仪器的名称: ______________ ① 。
( 2)用高锰酸钾制取一瓶干燥的氧气,可选用装置组合为 _____ (选填序号);实验室制取二氧化碳和氧气可选用发生装置 C 或 B , C 装置的优点是 ,用此装置制取 O 2的化学方程式是 _ ;( 3)实验室常用甲酸( HCOO )溶液滴加到浓硫酸中制 HCO 气体,可选用的制取装置是 _____ (选填序号)。
该反应中浓硫酸既是催化剂又是脱水剂,试写出该反应的化学方程式 ____________ 。
Ⅱ . 某同学将氢氧化钠溶液滴入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。
该同学对生成蓝绿色而不是蓝色固体的现象产生疑惑。
(查阅资料)(1) . CuCl 2溶液与 NaOH 溶液反应可生成蓝色固体( Cu(OH )2),在氢氧化钠较少的情况下 会生成蓝绿色碱式氯化铜( Cu x (OH )y Cl z ),其不溶于水,能与酸反应。
(2) . Cu (OH ) 2在 60℃开始分解生成两种氧化物,100℃分解完全。
碱式氯化铜在 300℃开始分解生成氧化铜、水和氯化氢,在 400℃分解完全。
(猜想)蓝绿色固体可能是:① Cu (OH ) 2;② Cu x (OH )y Cl z 晶体;③。
猜想①的理由 是: _____ (用化学方程式表示)。
(验证)该同学取 31.25g 蓝绿色固体,加热至 100℃出现黑色固体。
则猜想 不 正确。
继续加热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图 ____ (选填“甲”或“乙”)装置(装置中药品足量)。
九年级化学化学综合题试题经典及解析(实验数据)①最终得到剩余固体24.00g ;②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g ;③浓硫酸装置中数据如表。
加热前100℃400℃250. 00g 251. 80g253. 60gX ∶ Y : Z = ______ 。
初三化学化学综合题试题(有答案和解析)及解析一、中考化学综合题1. 阅读下面材料, 回答问题。
人类赖以生存的环境由自然环境和社会环境组成。
自然环境由生物圈、岩石圈、大气圈、水圈组成(如图所示), 四个圈层经过漫长演化, 既相对稳定、动态平衡, 又相互作用、不断变化, 各圈层之间的物质和能量不停循环, 这些循环既跟物质的组成、结构和性质有关, 也受人类活动的影响, 并通过复杂的物理变化和化学变化实现。
(一)内涵决定身份﹣﹣物质的组成与分类(l)用化学符号填空:岩石圈中含量最高的金属元素是_____。
大气圈中含量最高的物质是_____。
水圈中含量最高的元素是_____。
土壤中能促进农作物根系发达的元素是_____。
(2)按要求填表: 物质名称物质的化学式用符号表示构成物质的微粒物质类别(二)甲烷﹣﹣小分子, 大作为在如图的四大圈层中, 有下列6种物质: ①甲烷;②水;③二氯化碳;④一氧化碳;⑤氢气;⑥氧气。
构成这些物质的分子虽然简单, 但这些物质有的是人类赖以生存的基本物质, 有的是物质循环关键物质, 有的是人类社会生产活动必需的物质。
请回答:(1)在这6种物质中, 元素种类共有_____种, 人类的生命活动不可缺少的物质有_____(填化学式, 下同), 植物生长必需的物质有_____, 元素种类完全相同的物质是_____。
(2)甲烷是最重要的基础有机物之一, 不仅可做燃料, 还能发生如下反应:①在隔绝空气和1000℃条件下, 甲烷分解产生炭黑和氢气;②在隔绝空气和1500℃条件下, 甲烷分解产生乙炔和氢气;③在1400℃条件下, 适当比例的甲烷和氧气反应生成氢气和一氧化碳;④在800℃和催化剂条件下, 适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳。
试写出上述②~④三个反应的化学方程式:②_____;③_____;④_____;(3)在反应①~④中, 属于置换反应的有_____。
在反应①和②中, 反应物相同, 而生成物不同, 从微观的角度看, 是因为反应条件不同导致_____。
【化学】九年级化学化学综合题及其解题技巧及练习题(含答案)含解析一、中考化学综合题1.黄铁矿(主要成分为FeS2,杂质高温下不反应。
)是我国硫酸厂制取硫酸的主要原料。
某兴趣小组欲测定某黄铁矿中FeS2含量,设计了如下实验 (假设每步反应均完全)。
【查阅资料】①4FeS2+11O2 2Fe2O3+8SO2②Na2SO3+H2O2 =Na2SO4+H2③BaSO4为一种不溶于水、不溶于盐酸的沉淀。
【实验探究】Ⅰ.称取4.80g黄铁矿样品放入下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。
Ⅱ.反应结束后,将B瓶中的溶液按上图流程进行处理。
【问题讨论】(1)Ⅰ中B瓶内发生反应的化学反应方程式是______和______;(2)Ⅰ中通入的空气中作用是______和______;(3)Ⅱ中加入盐酸溶液的目的是______;(4)Ⅱ中检验滤渣洗涤是否干净的方法是______。
【含量测定】(5)另取 4.80g黄铁矿样品在空气中加热,测出样品的固体残留率(固体样品的剩余质量固体样品的起始质量×100%)随温度的变化如下图所示,计算该黄铁矿中FeS2的质量分数为______。
(请写出计算过程)【答案】CO2+2NaOH=Na2CO3+H2O SO2+2NaOH=Na2SO3+H2O;提供反应所需的氧气将生成的二氧化硫气体排入装置B中除去产生的BaCO3沉淀;取最后一次洗涤液1~2mL于试管中,向其中滴加硝酸银(或稀硫酸、碳酸钠)溶液,若无白色沉淀生成,则表明已洗涤干净。
75%【解析】(1)根据空气中的二氧化碳与氢氧化钠溶液反应生成碳酸钠和水及FeS2与氧气反应生成的二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水解答;(2)根据空气能提供与硫化亚铁反应所需的氧气和将生成的二氧化硫气体排入装置B中解答;(3)根据盐酸能将反应生成的碳酸钡除去解答;(4)根据过滤出来的硫酸钡沉淀是湿润的分析解答;(5)根据反应的化学方程式计算解答。
最新九年级化学化学综合题题20套(带答案)一、中考化学综合题1.如下图装置可用于气体的吸收、检验和分离等,请回答下列问题。
(1)利用装置 A (其中液体试剂足量)可以将二氧化碳和一氧化碳的混合气体进行分离。
首先打开活塞 a ,缓缓通入混合气体,广口瓶中观察到的现象是______,发生反应的化学方程式为__________;此时从导管 c 逸出的主要气体是_________,为了检验该气体,将导管按 c-d-e-f-g 顺序连接,B 处观察到的现象为_________,发生反应的化学方程式为____________。
(2)实验中 A 和 C 两处用到澄清石灰水,其中 A 处澄清石灰水的作用是___________ (3)装置 C 中还应进行的操作是_____________ ;一段时间后,断开 AB 装置,关闭活塞 a ,打开活塞 b ,滴加足量的稀盐酸,此时逸出的主要气体是______________。
(4)现有36.5 g 质量分数为20%的盐定质氢氧化钙溶液恰好完全反应,生成的氯化钙溶液中溶质的质量分数为22.2%。
请计算所得氯化钙溶液的质量是_____________。
【答案】 澄清石灰水变浑浊 Ca(OH)2 + C02 = CaCO 3↓ + 2H 20 CO 黑色固体变红色 Cu0+C0@Cu+C02 吸收二氧化碳 将尾气点燃 C02 50g【解析】(1)首先打开活塞a ,缓缓通入混合气体,广口瓶中观察到的现象是澄清石灰水变浑浊,是因为氢氧化钙和二氧化碳反应生成了碳酸钙沉淀和水,发生反应的化学方程式为:Ca(OH)2+CO 2═CaCO 3↓+H 2O ;此时从导管c 逸出的主要气体是一氧化碳,为了检验该气体,将导管按c−d−e−f−g 顺序连接,B 处观察到的现象为黑色固体变成红色固体,是因为高温条件下,氧化铜和一氧化碳反应生成铜和二氧化碳,发生反应的化学的化学方程式为:CuO+CO @Cu+CO 2;(2)实验中A 和C 两处用到澄清石灰水,其中A 处澄清石灰水的作用是吸收二氧化碳气体;(3)装置C 中还应进行的操作是处理尾气,方法是把尾气点燃或收集起来;一段时间后,断开AB 装置,关闭活塞a ,打开活塞b ,滴加足量的稀盐酸,碳酸钙和稀盐酸反应生成二氧化碳,此时逸出的主要气体是二氧化碳;(4)设生成氯化钙质量为x ,Ca(OH)2+2HCl═CaCl 2+2H 2O , 73 111 36.5g×20% x7311136.5g 20%x=⨯, x =11.1g ,所得氯化钙溶液的质量为:11.1g÷22.2%=50g , 答:所得氯化钙溶液的质量为50g 。
(化学)九年级化学化学综合题题20套(带答案)及解析一、中考化学综合题1.实验室常用下列装置制取气体,请你根据所学知识回答下列问题。
①实验室使用高锰酸钾制取氧气时,选用的发生装置与收集装置是_______(填字母序号)。
若改用下图装置收集氧气,则气体应从______进(填“a”或“b”)。
②小明与小华取一定浓度的盐酸与石灰石反应制取气体,反应的化学方程式为__________________;将生成的气体通入澄清石灰水中,未见变浑浊。
小明认为是石灰水已经完全变质,而小华则认为是气体中混有挥发出来的HCl气体。
为探究其原因,进行了如下实验:取少量澄清石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色。
于是排除了小明的猜想,你认为排除的理由是__________________________。
他们想探究所得气体中是否有挥发出来的HCl气体,设计如下实验。
请你帮他完成实验,填写以下表格:实验步骤实验现象实验结论__________________气体中有HCl③如果用上述原料制得纯净的二氧化碳气体,所选仪器的连接顺序为______(填字母)。
(2)“低钠盐”可以控制钠的摄入量从而防治高血压等疾病。
制备“低钠盐”在食盐中用NaCl中按照配方比例添加食用KCl。
国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2)。
①测得某“低钠盐”样品a中含有NaCl和KCl的质量分数均为50%。
该样品a的水溶液中,含量最多的离子是____________(填离子符号)。
②探究某“低钠盐”样品b中是否添加镁盐,以及添加的是何种镁盐(MgSO4或MgCl2中的一种)。
请设计实验方案,完成下列表格。
限选试剂:BaCl2溶液、NaOH溶液、AgNO3溶液、蒸馏水实验操作预期现象及结论步骤1:取少量样品b于烧杯中,加入足量样品溶解,形成无色溶液.蒸馏水步骤2:取少量步骤1形成的溶液于试管_______,说明样品b中添加了镁盐中,在滴加少量NaOH溶液,振荡步骤3:__________________________________【答案】AC b CaCO3+2HCl=CaCl2+CO2↑+H2O酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2将生成的气体通入....气体中有HCl B H E C Cl﹣..中,产生白色沉淀....3.溶液..AgNO有白色沉淀生成取少量步骤1 形成的溶液于试管中,再滴加少量的BaCl2溶液振荡若有白色沉淀产生,则添加的是MgSO4;若无明显现象,则添加的是MgCl2【解析】(1)①实验室使用高锰酸钾制取氧气时,选用的发生装置是固固加热型发生装置A,氧气的密度比空气的大,可以用向上排空气法收集,收集装置是C。
专题七各学科交叉综合题
一、选择题
1、(江苏苏州,10题)今年3月《江苏苏州日报》报导:“太仓奥特斯维能源等一批
大项目建成后,我市光伏电池产突破7000兆瓦。
”下列有关“光伏电池”能量形式转化的叙述正确的是
A.化学能转化为电能B.电能转化为化学能
C.太阳能转化为电能D.风能转化为电能
2、(广东揭阳,7题)下列在对海洋资源利用时的做法不.可取的是
A.在休鱼期间禁止捕捞 B.船舶垃圾直接倒入海中
C.开发利用海底“可燃冰” D.将海水引入盐田进行晒盐
3、(广东揭阳,10题)自然界中存在氧循环和碳循环,其中能将二氧化碳转化为氧气的是A.水变成水蒸气 B.动植物的呼吸
C.植物的光合作用 D.化石的燃料的燃烧
4、(江西,14题)小茜设计了一个趣味实验(见右图装置),其气密性良好。
若要使B中尖嘴导管口有“喷泉”产生,则A中加入的固体和液体物质可能是()
A.氯化钠和水B.硝酸铵和水
C.二氧化锰和过氧化氢溶液D.
C 锌粒和稀硫酸(或氧化钙和水等)
5、(江西南昌,10题)小明设计了趣味实验装置(见右图),其
气密性良好。
若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体
和液体可能是
A.氯化钠和水B.硝酸铵和水
C.二氧化锰和过氧化氢溶液D.铜和稀硫酸
6、(甘肃兰州,22题)下列图像不能正确反映所对应叙述关系的是()
A. ①煅烧一定质量的石灰石
B. ②镁在空气中燃烧
C.③等质量的锌和镁分别于等质量的等体积得稀硫酸(足量)反应
D.④氧气的溶解度随压强变化得关系
二、填空、简答题
1、(浙江衢州,22题)我国的长征系列运载火箭顺利完成了多项发射任务。
火箭在加速上升过程中,燃料燃烧时化学能转化为▲能,从而使火箭的机械能增大;火箭利用向后喷出气流而使自身受力前进,这是运用了力的作用是▲的原理。
内(或热) 相互
2、(福建福州,13题)联合国第63届大会决定将作为国际化(IYC),
其主题是“化学-人类的生活,人类的未来”。
请回答下列化学与人类生活相关的问题。
(1)下列服装主要用有机合成材料制成的是。
(填标号)
A.羊毛衫
B.涤纶连衣裙
C.腈纶运动衣
D.纯棉T恤
(2)自热米饭是一种快餐食品。
请根据图6、7及表1信息,回答下列问题:
①自热米饭的营养素中,主要负责提供能量的是,构成细胞的基础物质是。
②图7中菜肴包的包装材料是符合卫生标准的铝箔。
铝可以压制成铝箔,说明铝具有良好的的。
③该自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反应的化学方程式为,其基本反应类型是。
(3)良好的家居环境带来美好的生活。
①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的性。
②图8所示的“火立熄”是一种新型的家用灭火用品。
“火立熄”接触到火焰
3-5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃气体,使火焰
熄灭。
“火立熄”的灭火原理是。
(填标号)
A.清除可燃物
B.使燃烧物与氧气隔绝
C.降低燃烧物的着火点
(4)汽车是现代生活中常见的一种交通工具。
①喷漆可以延缓汽车钢铁外壳的锈蚀,其防锈原理是隔绝和。
②CNG双燃料环保汽车已在福州投入使用,这种汽车所用的燃料是汽车和压缩天然气。
写出天然气完全燃烧的化学方程式:。
(1)BC (2)①糖类蛋白质②延展性③CaO+H2O=Ca(OH)2化合反应(3)①吸附②
B (4)①氧气水②CH4+2O2点燃CO2+2H2O
3、(浙江温州,27题)某晶牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明。
原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒。
(1)当强光照射时,溴化银分解为银和溴,使镜片呈现暗棕色。
此过程中,光能转化成________能。
(2)当光线变暗时,银和溴(Br2)在氧化铜的催化作用下,重新化合生成溴化银(AgBr),镜片的颜色变浅。
该反应的化学方程式为____________________。
(3)光进入眼球时,瞳孔根据光线的强弱可进行调节。
完成这一反射活动的
神经结构叫做____________。
(1)化学·(2)2Ag+Br2些2AgBr (3)反射弧
4、(浙江丽水,22题)5月,上海一农贸市场里销售使用过植物激素——膨大增甜剂的西瓜,专家指出长期食用这种西瓜影响人体健康,膨大增甜剂的有效成分是:胺鲜脂、芸苔素、细胞分裂素、增甜素。
其中芸苔素的化学式为:C29H50O6,你认为芸苔素由种元素组成。
植物激素很多,早在1934年科学家就从植物体中分离出了一种植物激素,植物的
向光性与这种激素有关,它是。
三生长素。