促肾上腺皮质激素(ACTH)测定试剂盒(电化学发光免疫分析法)产品技术要求北京联众泰克
- 格式:docx
- 大小:28.55 KB
- 文档页数:2


促肾上腺皮质激素(ACTH)标准操作规程一、目的:规范促肾上腺皮质激素测定的标准操作程序,确保促肾上腺皮质激素测定的结果准确有效。
二、适用范围:在AutoLumo A2000化学发光检测仪上定量测定人血清中的促肾上腺皮质激素。
三、临床意义ACTH是脊椎动物脑垂体分泌的一种多肽类激素,含39个氨基酸,分子量为4500。
它能促进肾上腺皮质的组织增生以及皮质激素的生成和分泌。
它的生成和分泌受下丘脑促肾上腺皮质激素释放因子(CRF)的直接调控。
分泌过盛的皮质激素反过来也能影响垂体和下丘脑,减弱它们的活动[1]。
ACTH的分泌呈现日节律波动,入睡后ACTH分泌逐渐减少,午夜最低,随后又逐渐增多,至觉醒起床前进入分泌高峰,白天维持在较低水平,入睡时再减少。
由于ACTH分泌的日节律波动,糖皮质激素的分泌也出现相应的波动[4]。
ACTH 增高可见于原发性肾上腺皮质功能减退症、异位ACTH综合征、库欣病、Nelson综合征、先天性肾上腺皮质增生症、遗传性肾上腺皮质对ACTH不反应综合征、周期性ACTH、ADH分泌增多综合征、其他(如手术、创伤、休克、低血搪、使用SU4885等均可使ACTH分泌增多)[3]。
ACTH 降低可见于垂体前叶功能减退症、肾上腺皮质腺瘤或癌、单纯性ACTH缺乏综合征、医源性ACTH减少等[2]。
四、方法原理本试剂盒采用夹心法原理进行检测。
用ACTH抗体包被磁微粒,辣根过氧化物酶标记ACTH抗体制备酶结合物。
通过免疫反应形成抗体-抗原-酶标抗体复合物,该复合物催化发光底物发出光子,发光强度与ACTH的含量成正比。
五、标本的采集与处理5.1.应用正确医用技术采集患者上午7:00~10:00 EDTA血浆样本用于测定。
5.2.样本中的沉淀物和悬浮物可能会影响试验结果,应离心除去。
5.3.严重溶血、脂血或浑浊的样本不能用于测定。
5.4.样本收集后如果不能在1小时内检测,需将样本放置在2~8℃的冰箱中;若需24小时以上保存或运输,则应冻存于-20℃以下,避免反复冻融。
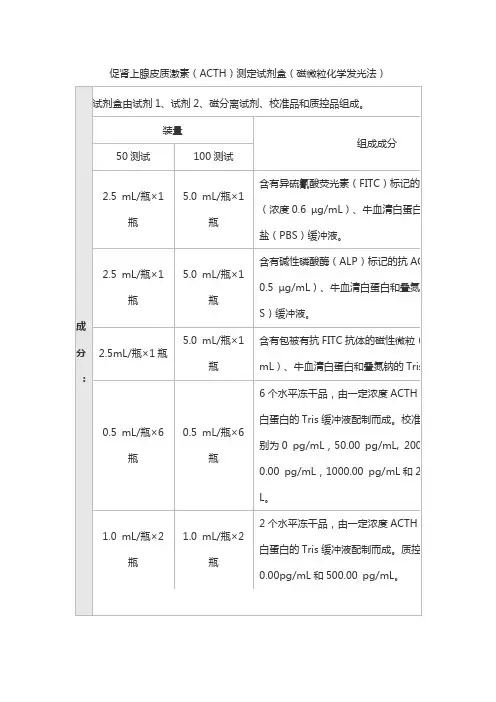
促肾上腺皮质激素(ACTH)测定试剂盒(磁微粒化学发光法)2.1外观2.1.1试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后为均匀悬浊液,无明显凝集;2.1.3液体组分应无沉淀或絮状物;2.1.4包装标签应清晰,易识别。
2.2准确度回收率应在85.0%-115.0%范围内。
2.3空白限应不大于1.00 pg/mL。
2.4线性在[1.50,2000.00]pg/mL的测量范围内,试剂盒的相关系数r应≥0.9900。
2.5重复性用(50.00±10.00)pg/mL和(500.00±100.00)pg/mL的样本各重复检测10次,变异系数(CV)应不大于10.00%。
2.6批间差用三个不同批号的试剂盒分别检测(50.00±10.00)pg/mL和(500.00±100.00)pg/mL的样本,其批间变异系数应≤15%。
2.7质控品的赋值有效性质控品的测量值应在质控范围内。
2.8 校准品和质控品的批内瓶间差2.8.1 校准品的批内瓶间差校准品B~校准品F的批内瓶间差CV≤10.0%。
2.8.2 质控品的批内瓶间差质控品的批内瓶间差CV≤10.0%。
2.9 稳定性2.9.1 效期稳定性试剂盒2℃~8℃保存有效期为12个月,在有效期满后检测试剂盒的准确度、空白限、线性、重复性、质控品的赋值有效性,应符合2.2、2.3、2.4、2.5、2.7的要求。
2.9.2 复溶稳定性2.9.2.1 校准品和质控品开瓶复溶后,室温保存,可稳定4小时,试剂盒用新开瓶复溶的校准品和质控品定标、质控,检测室温放置5小时后的校准品和质控品,校准品B~校准品F和质控品的相对偏差应在±10%范围内。
用复溶后室温放置5小时的校准品给试剂盒定标后检测试剂准确度和线性,结果应符合2.2、2.4要求。
用复溶后室温放置5小时的质控品对试剂盒进行质控后检测试剂批内精密度和质控品的赋值有效性,结果应符合2.5、2.7要求。

2性能指标
2.1外观和性状
2.1.1颜色性状
质控品复融前外观应呈现粉末块状固体,不起泡,不塌陷,复融后应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
2.1.2包装
分装瓶应为棕色玻璃瓶,应盖有塑料外盖;盒贴、瓶贴、标签标识、说明书、参考值表应完整、清晰牢固。
塑料瓶盖与玻璃瓶身配合后应无泄漏;塑料外盖应无明显划痕、崩缺。
2.2测量准确度
2.2.1质控参考值表
质控品应可提供一份参考值表,包含适用型号的迈瑞化学发光免疫分析系统
的检测项目参考值及参考范围。
2.2.2赋值准确性
经校准的迈瑞全自动化学发光免疫分析仪检测质控品所包含的检测项目,结果应在参考范围内(不同批次的质控品参考范围参见参考值表)。
2.3均一性
2.3.1瓶内均一性
质控品瓶内均一性应满足变异系数CV≤8.0%。
2.3.2瓶间均一性
质控品瓶间均一性应满足变异系数CV≤5.0%。
2.4生物安全性
使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂灵敏度的检测试剂,对质控品中乙型肝炎病毒表面抗原、人类免疫缺陷病毒抗体
(HIV-I型和HIV-II型)、丙型肝炎病毒抗体、梅毒螺旋体抗体的检测应为阴性。
1。



2性能指标
2.1外观
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;Ra 组分应为棕色含固体微粒的液体,无板结、无絮状物。
Rb 组分应为清澈透明的液体,无沉淀、无悬浮物、无絮状物。
2.2装量
应不少于试剂瓶的标示装量值。
2.3准确度
对具有溯源性的两个浓度水平的正确度控制品进行检测,检测结果与标定浓度的相对偏差在±10% 范围内。
2.4最低检测限
应不大于1 pg/mL。
2.5线性
试剂盒在1 pg/mL~2000 pg/mL 区间内,其相关系数(r)应不低于0.9900。
2.6重复性
变异系数CV 应≤ 6%。
2.7批间差
变异系数CV 应≤ 10%。
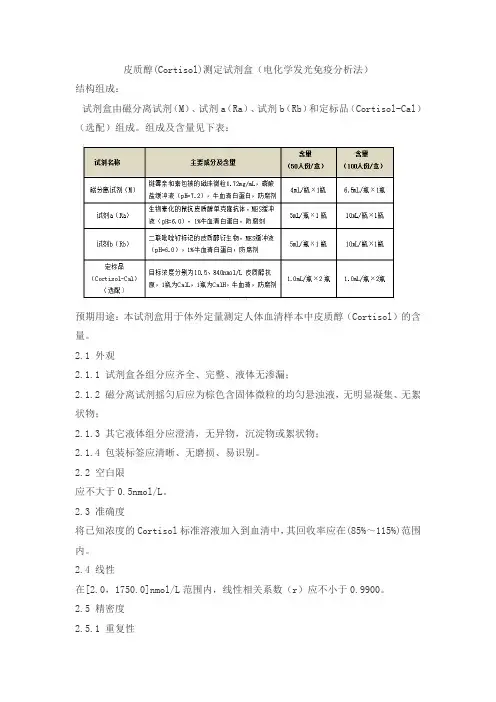
皮质醇(Cortisol)测定试剂盒(电化学发光免疫分析法)结构组成:试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(Cortisol-Cal)(选配)组成。
组成及含量见下表:预期用途:本试剂盒用于体外定量测定人体血清样本中皮质醇(Cortisol)的含量。
2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限应不大于0.5nmol/L。
2.3 准确度将已知浓度的Cortisol标准溶液加入到血清中,其回收率应在(85%~115%)范围内。
2.4 线性在[2.0,1750.0]nmol/L范围内,线性相关系数(r)应不小于0.9900。
2.5 精密度2.5.1 重复性在试剂盒的线性范围内,检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于8%。
2.5.2 批间差在试剂盒的线性范围内,用3个批号试剂盒分别检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于15%。
2.6 效期末稳定性本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.7 溯源性依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求提供皮质醇(Cortisol)定标品的来源、赋值过程以及测量不确定度等内容,定标品溯源至企业工作校准品。
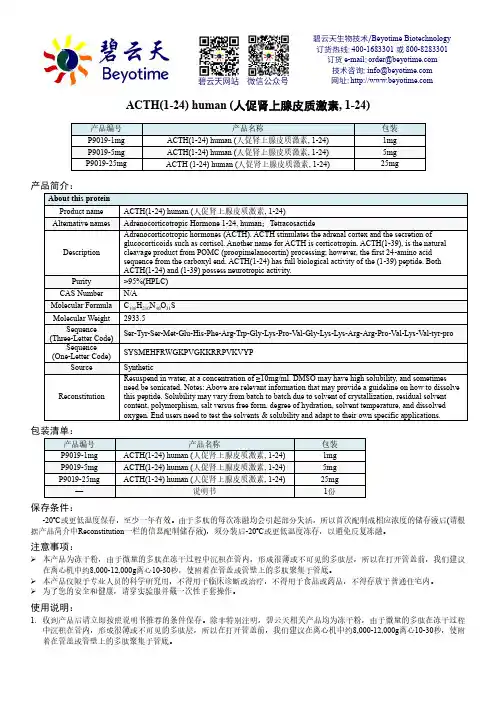
ACTH(1-24) human (人促肾上腺皮质激素, 1-24)保存条件:-20ºC 或更低温度保存,至少一年有效。
由于多肽的每次冻融均会引起部分失活,所以首次配制成相应浓度的储存液后(请根据产品简介中Reconstitution 一栏的信息配制储存液),须分装后-20ºC 或更低温度冻存,以避免反复冻融。
注意事项:本产品为冻干粉,由于微量的多肽在冻干过程中沉积在管内,形成很薄或不可见的多肽层,所以在打开管盖前,我们建议在离心机中约8,000-12,000g 离心10-30秒,使附着在管盖或管壁上的多肽聚集于管底。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明:1. 收到产品后请立即按照说明书推荐的条件保存。
除非特别注明,碧云天相关产品均为冻干粉,由于微量的多肽在冻干过程中沉积在管内,形成很薄或不可见的多肽层,所以在打开管盖前,我们建议在离心机中约8,000-12,000g 离心10-30秒,使附着在管盖或管壁上的多肽聚集于管底。
Beyotime Biotechnology 400-1683301800-8283301 e-mail *********************************** 2.请根据实验目的并按照产品简介中Reconstitution一栏中的信息配制储存液。
大多数多肽冻干粉是非常容易溶解的,一般用移液枪的枪头轻吹几下或者轻轻摇晃瓶子,即可使多肽完全溶解。
请勿用vortex剧烈振荡,以免多肽变性而失活。
3.具体的最佳工作浓度请自行参考相关文献,或者根据实验目的,以及特定细胞和动物,通过实验进行摸索和优化。
Version 2022.12.30 2 / 2 P9019ACTH(1-24) human (人促肾上腺皮质激素, 1-24) 400-1683301/800-8283301 碧云天/Beyotime。

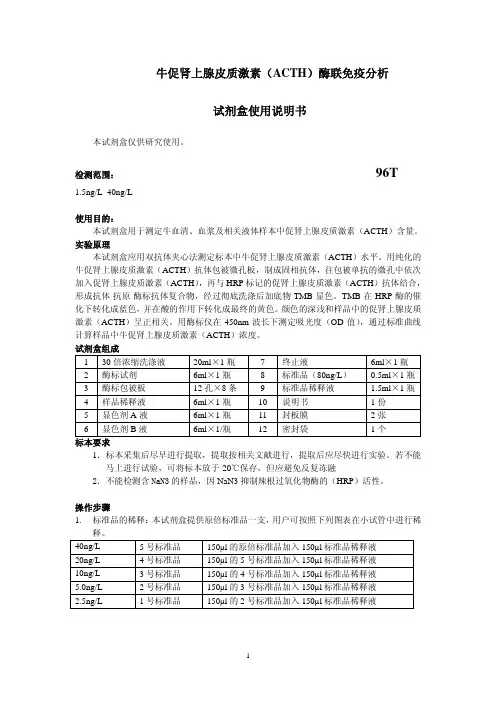
人促肾上腺皮质激素(ACTH)酶联免疫分析试剂盒使用说明书本试剂盒仅供研究使用预期应用ELISA法定量测定人血清、血浆或其它相关液体中促肾上腺皮质激素(ACTH)含量。
实验原理本试剂盒应用双抗体夹心酶标免疫分析法测定标本中ACTH水平。
用纯化的抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入ACTH抗原、生物素化的抗人ACTH抗体、HRP标记的亲和素,经过彻底洗涤后用底物TMB显色。
TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的ACTH呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),计算样品浓度。
试剂盒组成及试剂配制1.酶联板:一块(96孔)标准品(冻干品):2瓶,每瓶临用前以样品稀释液稀释至1ml,盖好后静置10分钟以上,然后反复颠倒/搓动以助溶解,其浓度为50ng/ml,做系列倍比稀释后,分别稀释25ng/ml,12.5ng/ml,6.25ng/ml,3.12ng/ml,1.56ng/ml,0.78ng/ml,0.39ng/ml,样品稀释液直接作为标准浓度0ng/ml,临用前15分钟内配制。
如配制25ng/ml标准品:取0.5ml50ng/ml的上述标准品加入含有0.5ml样品稀释液的Eppendorf管中,混匀即可,其余浓度以此类推。
2.样品稀释液:1×20ml/瓶。
3.检测稀释液A:1×10ml/瓶。
4.检测稀释液B:1×10ml/瓶。
5.检测溶液A:1×120ul/瓶(1:100)临用前以检测稀释液A1:100稀释,稀释前根据预先计算好的每次实验所需的总量配制(每孔100ul),实际配制时应多配制0.1-0.2ml。
如1ul检测溶液A加99ul检测稀释液A的比例配制,轻轻混匀,在使用前一小时内配制。
6.检测溶液B:1×120ul/瓶(1:100)临用前以检测稀释液B1:100稀释。
促甲状腺激素(TSH)测定试剂盒(磁微粒化学发光免疫分析法)适用范围:用于体外定量测定人血清或血浆中促甲状腺激素(TSH)的含量。
1.1产品规格100管份/盒。
1. 1.2主要组成成分校准品靶值批特异,详见标签。
质控品质控范围批特异,详见标签。
2.1 外观a)试剂盒中的组份应澄清,应无沉淀和絮状物,内外标签、标识清晰,易识别;b)分离试剂摇匀后,应为均匀悬浊液,无明显凝集;c)冻干组分呈白色或淡黄色疏松体,加水后应在20分钟内完全溶解,所得液体应无沉淀和不溶物质。
2.2 校准品溯源根据GB/T21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,溯源至国家标准品(编号:150530)。
2.3 净含量试剂盒各液体组份的体积不得少于标称体积。
2.4 最低检出限试剂盒的最低检出限不高于0.1µIU/ml。
2.5 线性在(0.4,50µIU/ml)范围内剂量-反应曲线相关系数(r)的绝对值应≥0.9900。
2.6 精密度2.6.1分析内精密度:用高低两个浓度水平的样本,各重复检测10次其变异系数(CV)应不大于8%(全自动操作法)或不大于15%(手工操作法)。
2.6.2分析间精密度:在多次独立分析之间,质控品测定结果的变异系数CV应不大于20%(仅限手工操作法)。
2.6.3批间精密度:用三个批号试剂盒检测同一样本,则三个批号试剂盒试剂盒之间的变异系数(CV)应不大于20%。
2.7 冻干粉瓶间差质控品按照规定复溶后,瓶间浓度变异系数CV≤15%。
2.8 准确性试剂盒内校准品与相应浓度的国家标准品(编号:150530)同时进行分析测定,用双对数或其他适当的数学模型拟合,要求两条剂量-反应曲线不显著偏离平行;以TSH国家标准品为对照品,试剂盒内校准品的实测值与标示值的效价比应在0.900~1.100 之间。
2.9 质控品测定值质控品的测定结果应在质控范围内。
2.10 特异性试剂盒与表中有关潜在交叉反应物应无显著的交叉反应。
促甲状腺激素测定试剂盒产品技术要求北京美联泰科促甲状腺激素测定试剂盒(磁微粒化学发光法)是一种用来检测人体内促甲状腺激素水平的试剂盒。
在促甲状腺激素测定的过程中,该试剂盒采用磁微粒化学发光法,通过特定的试剂盒,可以快速、准确地检测出人体内促甲状腺激素的浓度。
根据国家相关标准和技术要求,促甲状腺激素测定试剂盒(磁微粒化学发光法)的产品技术要求包括以下几个方面:
1.试剂盒的稳定性要求:试剂盒必须具有较长的保存期限,并且在保存期间,其性能稳定性应能满足测量的需要。
2.试剂盒的灵敏度和特异性要求:试剂盒使用的抗体必须具有较高的灵敏性,能够检测出较低浓度的促甲状腺激素。
此外,试剂盒还应具有较高的特异性,确保只能检测出促甲状腺激素,而不受其他物质的干扰。
3.试剂盒的精确度和准确性要求:试剂盒的使用应具有较高的精确度和准确性,确保能够得到可靠的测量结果。
同时,试剂盒的成本控制也是一个考虑因素。
4.试剂盒的操作简便性要求:试剂盒的操作应简便易行,不需要复杂的专业技能,便于广泛应用于临床实验室。
5.试剂盒的安全性要求:试剂盒必须符合相关的安全标准和规定,确保操作人员的安全。
6.试剂盒的报告范围和结果解释要求:试剂盒显示的测量结果应具有合理的报告范围,且结果能够清楚地解释,并与实际情况相符。
除了上述技术要求外,促甲状腺激素测定试剂盒(磁微粒化学发光法)还需要符合国家食品药品监督管理部门的相关注册要求,包括质量控制要
求和生产工艺要求等。
同时,还需要进行相关的临床验证和评估,以确保
其在实际应用中的可靠性和准确性。
1.目的:用于体外定量测定人EDTA-血浆样本中促肾上腺皮质激素的含量2.适用机型:LIAISON分析仪。
3.测定原理:采用免疫夹心化学发光检测方法。
在磁微粒(固相)上包被有特异性的鼠单克隆抗体(N-端),另一种单克隆抗体(针对ACTH的C-端碎片)与异鲁米诺衍生物结合(异鲁米诺抗体结合物)在孵育过程中,校准液、样本或质控品中的ACTH与固相上的单克隆抗体结合,然后异鲁米诺抗体结合物与已结合到固相的ACTH反应。
孵育完毕后,未结合的物质会被清洗移除,最后,加入启动试剂,引发瞬时化学发光反应,产生光信号。
通过光电倍增管测出的相对光单位(RLU)指示异鲁米诺-抗体结合物的数量,从而得出校准品、样本或质控品中的ACTH的浓度。
4.测定步骤:4.1仪器测试准备:按LIAISON操作手册打开系统,进行每日使用前的维护。
包括清洗、光路检测等。
4.2样本的采集、原料及保存:样本中的ACTH 分子降解速度很快,因此在处理样本时必须严格遵循以下要求。
必须使用冷冻储存的人EDTA血浆样本。
采用静脉穿刺方法采集血样并保存在含EDTA抗凝剂的硅化玻璃试管、真空采血管(紫帽)或类似的容器里。
避免溶血。
样本采集后应立即将样本管置于冰浴中低温保存。
样本采集后120分钟内,使用冷冻离心机离心,并立即分装上清液。
分装的上清液应保存在塑料或硅化玻璃试管里并于-20 ° C或以下低温冷冻。
每份分装的上清液的最小体积为300μL。
检测前,谨慎解冻混匀样本,检查是否有气泡并清除气泡。
解冻的样本应置于2-8℃并在6小时内用完。
高度溶血、高度脂血、含有颗粒物质或明显被微生物污染的样本不能用于检测。
禁止使用凝血样本。
避免反复冻融。
任何没有用完的分装液都应该丢弃。
检测样本一次需要的最小量为 300 μL (150 μL 样本+ 150 μL 保护体积)4.3试剂的准备:在揭开密封纸之前,先轻轻地水平摇晃试剂整盒(为了防止泡沫形成!)。
抗缪勒管激素(AMH)测定试剂盒(电化学发光免疫分析法)适用范围:本试剂盒用于体外定量测定人体血清样本中抗缪勒管激素(AMH)的含量。
1.1包装规格:50人份/盒、100人份/盒。
1.2主要组成成分试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(AMH-Cal)(选配)组成。
组成及含量见下表:注:1、定标品靶值批特异,详见靶值单。
2、试剂盒条码卡内含主校准曲线。
2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限应不大于0.01ng/mL。
2.3 准确度将已知浓度的AMH标准溶液加入到血清中,其回收率应在(85%~115%)范围内。
2.4 线性在[0.1,23.0]ng/mL范围内,线性相关系数(r)应不小于0.9900。
2.5 精密度2.5.1 重复性在试剂盒的线性范围内,检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于8%。
2.5.2 批间差在试剂盒的线性范围内,用3个批号试剂盒分别检测高、低两个水平的样品,检测结果的变异系数(CV)应不大于15%。
2.6 效期末稳定性本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.7 溯源性依据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求提供抗缪勒管激素(AMH)定标品的来源、赋值过程以及测量不确定度等内容,定标品溯源至企业工作校准品。
促肾上腺皮质激素(ACTH)测定试剂盒(电化学发光免疫分析法)
适用范围:本试剂盒用于体外定量测定人体血清样本中促肾上腺皮质激素(ACTH)的含量。
1.1包装规格:50人份/盒、100人份/盒。
1.2主要组成成分
试剂盒由磁分离试剂(M)、试剂a(Ra)、试剂b(Rb)和定标品(ACTH-Cal)(选配)组成。
组成及含量见下表:
注:1、定标品靶值批特异,详见靶值单。
2、试剂盒条码卡内含主校准曲线。
2.1 外观
2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;
2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;
2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;
2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限
应不大于1.0pg/mL。
2.3 准确度
将已知浓度的ACTH标准溶液加入到血清中,其回收率应在(85%~115%)范围内。
2.4 线性
在[3.00,2000.0]pg/mL范围内,线性相关系数(r)应不小于0.9900。
2.5 精密度
2.5.1 重复性
在试剂盒的线性范围内,测定高、低两个水平的样品,检测结果的变异系数(CV)应不大于8%。
2.5.2 批间差
在试剂盒的线性范围内,用3个批号试剂盒分别测定高、低两个水平的样品,检测结果的变异系数(CV)应不大于15%。
2.6 效期末稳定性
本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
2.7 溯源性
依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求提供促肾上腺皮质激素(ACTH)定标品的来源、赋值过程以及测量不确定度等内容,定标品溯源至企业工作校准品。