原子核外电子排布2
- 格式:pptx
- 大小:2.09 MB
- 文档页数:16

[1]H氢1s1[2]He氦1s2[3]Li锂1s2 2s1 [4]Be铍1s2 2s2 [5]B硼1s2 2s2 2p1 [6]C碳1s2 2s2 2p2 [7]N氮1s2 2s2 2p3[8]O氧1s2 2s2 2p4[9]F氟1s2 2s2 2p5 [10]Ne氖1s2 2s2 2p6 [11]Na钠1s2 2s2 2p6 3s1 [12]Mg镁1s2 2s2 2p6 3s2 [13]Al铝1s2 2s2 2p6 3s2 3p1 [14]Si硅1s2 2s2 2p6 3s2 3p2[15]P磷1s2 2s2 2p6 3s2 3p3 [16]S硫1s2 2s2 2p6 3s2 3p4 [17]Cl氯1s2 2s2 2p6 3s2 3p5 [18]Ar氩1s2 2s2 2p6 3s2 3p6 [19]K钾1s2 2s2 2p6 3s2 3p6 4s1 [20]Ca钙1s2 2s2 2p6 3s2 3p6 4s2 [21]Sc钪1s2 2s2 2p6 3s2 3p6 3d1 4s21s2 2s2 2p6 3s2 3p6 3d2 4s2 [23]V 钒1s2 2s2 2p6 3s2 3p6 3d3 4s2 *[24]Cr铬1s2 2s2 2p6 3s2 3p6 3d5 4s1 [25]Mn锰1s2 2s2 2p6 3s2 3p6 3d5 4s2 [26]Fe铁1s2 2s2 2p6 3s2 3p6 3d6 4s2 [27]Co钴1s2 2s2 2p6 3s2 3p6 3d7 4s2 [28]Ni镍1s2 2s2 2p6 3s2 3p6 3d8 4s21s2 2s2 2p6 3s2 3p6 3d10 4s1 [30]Zn锌1s2 2s2 2p6 3s2 3p6 3d10 4s2 [31]Ga镓1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p1 [32]Ge锗1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p2 [33]As砷1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p3 [34]Se硒1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4 [35]Br溴1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5[36]Kr氪1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6例3.不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如下图所示。

原子核外电子的排布一、选择题1.下列叙述中,正确的是()A.在多电子的原子里,能量高的电子通常在离核近的区域内运动B.核外电子总是先排在能量低的电子层上,例如只有排满了M层后才排N层C.某原子M层上电子数为L层电子数的4倍D.某离子的核电荷数与最外层电子数相等2.关于原子结构的叙述正确的是()A.所有的原子核都是由质子和中子构成的B.原子的最外层电子数不超过8C.稀有气体原子的最外层电子数均为8D.原子的次外层电子数都是83.下列各原子结构示意图中所表示的核外电子排布正确的是()4.已知W粒子的结构示意图为,下列关于它的说法不正确的是()A.y=2B.若x=18,则z=8C.若x=14,则其氢化物的化学式为H2WD.若x=17,则其最高价氧化物的化学式为W2O75.下列说法中,肯定错误的是()A.某原子K层上只有1个电子B.某原子M层上电子数为L层上电子数的4倍C.某离子M层上和L层上的电子数均为K层的4倍D.某原子的核电荷数与最外层电子数相等6.下列化学符号表示同一种元素的是()①3517X②3717X③④A.①③B.①②③C.②③D.①②③④7.已知最外层电子数相同的原子具有相似的化学性质。
氧原子的核外电子分层排布示意图为,下列原子中,与氧原子化学性质相似的是()8.下列叙述中,正确的是()A.核外电子排布完全相同的两种微粒,其化学性质一定相同B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布C.核外电子排布相同的两原子一定属于同种元素D.任一阴离子的核外电子排布一定与其上一周期稀有气体元素原子的核外电子排布相同9.某短周期元素的原子最外层电子数是次外层电子数的3倍,那么该原子()A.有3个电子层B.有2个电子层C.最外层电子数是8D.核电荷数是1010.下列说法中,正确的是()A.原子最外层电子少于3个的元素均是金属元素B.原子核外能量越低的电子离核越远,能量越高的电子离核越近C.两个简单微粒的电子层排布完全相同,则它们一定是同一种元素D.在短周期元素中,原子最外层电子数等于电子层数的元素是H、Be、Al11.已知元素X、Y的核电荷数分别是a和b,它们的离子X m+和Y n-的核外电子排布相同,则下列关系式中正确的是()A.a=b+m+nB.a=b-m+nC.a=b+m-nD.a=b-m-n12.短周期元素A和B,其中A元素的原子最外层电子数是a,次外层电子数是b;B元素的原子M层电子数是(a-b),L层电子数是(a+b),则A、B两种元素形成的化合物的化学式可能表示为()A.B3A2B.AB2C.A3B2D.BA213.短周期元素中,A元素原子最外层电子数是次外层电子数的2倍;B元素原子最外层电子数是其内层电子总数的3倍;C元素原子M层电子数等于其L层电子数的一半;D 元素原子最外层有1个电子,D的阳离子与B的阴离子电子层结构相同,则这4种元素原子序数关系中正确的是()A.C>D>B>AB.D>B>A>CC.A>D>C>BD.B>A>C>D二、非选择题14.根据下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:(1)五种粒子中,属于原子的是________,属于离子的是_________。


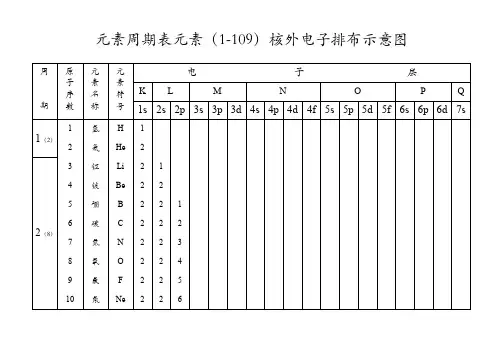


核外电子排布规律总结原子核外电子排布规律①能量最低原理:电子层划分为KvLvMvOvPv对应电子层能量增大;原子核外电子排布按照能量较低者低优先排布原则.②每个电子层最多只能容纳2n2个电子③最外层最多只能容纳8个电子(K层为最外层时不能超过2个)次外层最多只能容纳18个电子(K层为次外层时不能超过2个倒数第三层最多只能容纳32个电子注意:多条规律必须同时兼顾。
简单例子的结构特点:⑴离子的电子排布:主族元素阳离子跟上一周期稀有气体的电子层排布相同,如钠离子、镁离子、铝离子和氖的核外电子排布是相同的。
阴离子更同一周期稀有气体的电子排布相同:负氧离子,氟离子和氖的核外电子排布是相同的。
(2)等电子粒子(注意主要元素在周期表中的相对位置)①10 电子粒子:CH4、N3、NH,、NH3、NH4、O2、OH、H, O H3O、F、HF、Ne Na、Mg2、Al 3等。
②18 电子粒子:SiH4、P3、Pli、S2、HS、H2S、Cl 、HCI、Ar、K、Ca2、PH^ 等。
特殊情况:F2、H2O2、C2H6、CI^OH③核外电子总数及质子总数均相同的阳离子有:Na、NH、H3O等;阴离子有:F、OH、NH, ;HS 、CI 等。
前18号元素原子结构的特殊性:(1)原子核中无中子的原子:;H(2)最外层有1个电子的元素:H、Li、Na;最外层有2个电子的元素:Be、Mg He(3)最外层电子总数等于次外层电子数的元素:Be Ar(4)最外层电子数等于次外层电子数2倍的元素:C ;是次外层电子数3倍的元素:O ;是次外层电子数4倍的元素:Ne(5)最外层电子数是内层电子数一半的元素:Li、P(6)电子层数与最外层电子数相等的元素:H、Be Al(7)电子总数为最外层电子数2倍的元素:Be(8)次外层电子数是最外层电子数2倍的元素:Li、Si元素周期表的规律:(1)最外层电子数大于或等于3而又小于8的元素一定是主族元素,最外层电子数为1或2 的元素可能是主族、副族或0族元素,最外层电子数为8的元素是稀有气体(He例外)(2)在元素周期表中,同周期的U A、川A族元素的原子序数差别有:①第2、3周期(短周期)元素原子序数都相差1;②第4、5周期相差11;③第6 7周期相差25(3)同主族、邻周期元素的原子序数差①位于过渡元素左侧的主族元素,即I A、U A 族,同主族、邻周期元素原子序数之差为下一周期元素所在周期所含元素总数;相差的数分别为2,8,8,18,18,32②位于过渡元素左侧的主族元素,即川A〜%A族,同主族、邻周期元素原子序数之差为下一周期元素所在周期所含元素种数。


原子核外电子排布1 氢H 12 氦He 23 锂Li 2 14 铍Be 2 25 硼 B 2 36 碳 C 2 47 氮 N 2 58 氧 O 2 69 氟 F 2 7。
10 氖 Ne 2 811 钠 Na 2 8 112 镁 Mg 2 8 213 铝 Al 2 8 314 硅 Si 2 8 415 磷 P 2 8 516 硫 S 2 8 617 氯 Cl 2 8 718 氩 Ar 2 8 8%19 钾 K 2 8 8 120 钙 Ca 2 8 8 221 钪 Sc 2 8 9 222 钛 Ti 2 8 10 223 钒 V 2 8 11 224 铬 Cr 2 8 13 125 锰 Mn 2 8 13 226 铁 Fe 2 8 14 227 钴 Co 2 8 15 228 镍 Ni 2 8 16 229 铜 Cu 2 8 18 1&30 锌 Zn 2 8 18 231 镓 Ga 2 8 18 332 锗 Ge 2 8 18 433 砷 As 2 8 18 534 硒 Se 2 8 18 635 溴 Br 2 8 18 736 氪 Kr 2 8 18 837 铷 Rb 2 8 18 8 138 锶 Sr 2 8 18 8 239 钇 Y 2 8 18 9 2)40 锆 Zr 2 8 18 10 241 铌 Nb 2 8 18 12 142 钼 Mo 2 8 18 13 143 锝 Tc 2 8 18 13 244 钌 Ru 2 8 18 15 145 铑 Rh 2 8 18 16 146 钯 Pd 2 8 18 1847 银 Ag 2 8 18 18 148 镉 Cd 2 8 18 18 249 铟 In 2 8 18 18 350 锡 Sn 2 8 18 18 4)51 锑 Sb 2 8 18 18 552 碲 Te 2 8 18 18 653 碘 I 2 8 18 18 754 氙 Xe 2 8 18 18 855 铯 Cs 2 8 18 18 8 156 钡 Ba 2 8 18 18 8 257 镧 La 2 8 18 18 9 2 〖镧系〗58 铈 Ce 2 8 18 19 9 2 〖镧系〗59 镨 Pr 2 8 18 20 9 2 〖镧系〗60 钕 Nd 2 8 18 21 9 2 〖镧系〗—61 钷 Pm 2 8 18 22 9 2 〖镧系〗62 钐 Sm 2 8 18 23 9 2 〖镧系〗63 铕 Eu 2 8 18 24 9 2 〖镧系〗64 钆 Gd 2 8 18 25 9 2 〖镧系〗65 铽 Tb 2 8 18 26 9 2 〖镧系〗66 镝 Dy 2 8 18 27 9 2 〖镧系〗67 钬 Ho 2 8 18 28 9 2 〖镧系〗68 铒 Er 2 8 18 29 9 2 〖镧系〗69 铥 Tm 2 8 18 30 9 2 〖镧系〗70 镱 Yb 2 8 18 31 9 2 〖镧系〗71 镥 Lu 2 8 18 32 9 2 〖镧系〗、72 铪 Hf 2 8 18 32 10 273 钽 Ta 2 8 18 32 11 274 钨 W 2 8 18 32 12 275 铼 Re 2 8 18 32 13 276 锇 Os 2 8 18 32 14 277 铱 Ir 2 8 18 32 15 278 铂 Pt 2 8 18 32 17 179 金 Au 2 8 18 32 18 180 汞 Hg 2 8 18 32 18 281 铊 Tl 2 8 18 32 18 382 铅 Pb 2 8 18 32 18 4-83 铋 Bi 2 8 18 32 18 584 钋 Po 2 8 18 32 18 685 砹 At 2 8 18 32 18 786 氡 Rn 2 8 18 32 18 887 钫 Fr 2 8 18 32 18 8 188 镭 Ra 2 8 18 32 18 8 289 锕 Ac 2 8 18 32 18 9 2 〖锕系〗90 钍 Th 2 8 18 32 18 10 2 〖锕系〗91 镤 Pa 2 8 18 32 20 9 2 〖锕系〗92 铀 U 2 8 18 32 21 9 2 〖锕系〗》93 镎 Np 2 8 18 32 22 9 2 〖锕系〗94 钚 Pu 2 8 18 32 24 8 2 〖锕系〗95 镅 Am 2 8 18 32 25 8 2 〖锕系〗96 锔 Cm 2 8 18 32 25 9 2 〖锕系〗97 锫 Bk 2 8 18 32 26 9 2 〖锕系〗98 锎 Cf 2 8 18 32 28 8 2 〖锕系〗99 锿 Es 2 8 18 32 29 8 2 〖锕系〗100 镄 Fm 2 8 18 32 30 8 2 〖锕系〗101 钔 Md 2 8 18 32 31 8 2 〖锕系〗102 锘 No 2 8 18 32 32 8 2 〖锕系〗103 铹 Lr 2 8 18 32 32 9 2 〖锕系〗:104 卢* Rf 2 8 18 32 32 10 2105 杜* Db 2 8 18 32 32 11 2106 喜* Sg 2 8 18 32 32 12 2107 波* Bh 2 8 18 32 32 13 2108 黑* Hs 2 8 18 32 32 14 2109 麦* Mt 2 8 18 32 32 15 2110 * Uun 2 8 18 32 32 16 2111 * Uuu 2 8 18 32 32 17 2112 * Uub 2 8 18 32 32 18 2113 * Uut 2 8 18 32 32 18 3114 * Uuq 2 8 18 32 32 18 4115 * Uup 2 8 18 32 32 18 5 116 * Uuh 2 8 18 32 32 18 6 117 * Uus 2 8 18 32 32 18 7 118 * Uuo 2 8 18 32 32 18 8。
硼原子核外电子排布
硼原子核外电子排布为2s2 2p1。
2s2 2p1 格局对应的能级为:1s2 2s2 2p1,即1s、2s和2p三个能级。
每个能级
上的电子数量分别为2、2和1个,共5个电子。
按照分子轨道理论,硼原子在原子态中的核外电子分布可以表示为:1s2 2s2 2p1。
其中,1s能级上有2个电子,2s能级上有2个电子,2p能级上有1个电子,总共
5个电子。
根据项圈定律,硼原子有6个电子,1s2 2s2 2p1的排布能满足要求,
此为硼原子最稳定的配置。
由于硼原子各能级上的电子配置已经吻合项圈定律,因此它在原子态中会表现出一定的化学活性。
例如,它可以与其他元素形成化合物;也可以在某些特殊的条件下与其他离子结合发生反应;还可以吸附分子或物质表面,形成无机薄膜等。
这些表现都得益于硼原子核外电子排布的特点。