影响溶解度大小的因素和溶解度曲线解读
- 格式:ppt
- 大小:631.00 KB
- 文档页数:13


溶解度与溶解度曲线溶解度是指在一定条件下,单位溶剂中单位温度下溶质的最大溶解量。
溶解度受到多种因素的影响,如溶质和溶剂的性质、温度、压力等。
溶解度曲线则是描述溶解度随温度变化而呈现的曲线,对于理解溶解过程有重要的意义。
一、溶解度的定义和影响因素溶解度是溶质在溶剂中溶解的程度,通常用“溶质在100克溶剂中溶解的克数”或“溶质在100毫升溶剂中溶解的克数”来表示。
溶解度的单位通常为克/100克或克/100 mL。
溶解度受到多种因素的影响,主要包括以下几个方面:1. 溶剂的性质:溶剂的极性、溶剂分子的大小与溶质分子的大小之间的相互作用力是决定溶解度的关键因素之一。
溶剂与溶质之间的相互作用力越强,溶解度越大。
2. 溶质的性质:溶质的极性、溶质分子的大小与溶剂分子的大小之间的相互作用力也是影响溶解度的重要因素。
溶质分子越小、极性越大,溶解度越大。
3. 温度:温度是影响溶解度的重要因素之一。
一般情况下,溶解度随温度的升高而增大。
但某些物质的溶解度随温度的升高而降低,这是因为在溶解过程中伴随着吸热或放热反应的发生。
4. 压力:压力对溶解度的影响在一般情况下较小。
但对于气体溶解于液体的情况下,压力的增加会导致溶解度的增大。
二、溶解度曲线与溶解度变化规律溶解度曲线是随温度变化而描绘的曲线图,用于描述溶解度随温度变化的规律。
在溶解度曲线中,横坐标表示温度,纵坐标表示溶解度。
一般来说,溶解度曲线可分为以下几种类型:1. 随温度的升高而增大的曲线:这种曲线表明溶解过程是一个吸热反应,随着温度的升高,反应愈发有利,溶解度呈现上升趋势。
2. 随温度的升高而减小的曲线:这种曲线表明溶解过程是一个放热反应,温度升高会导致溶解度的降低。
3. 温度对溶解度没有显著影响的曲线:这种曲线表明溶解过程与温度无关,溶质的溶解度在一定温度范围内保持不变。
溶解度曲线对于理解溶解过程和溶解度变化规律具有重要的指导意义。
通过研究溶解度曲线,可以确定溶解过程的热力学特征和溶解度随温度变化的规律。

化学物质的溶解度曲线溶解度是指单位溶剂在一定温度和压力下溶解的物质的最大质量或体积。
溶解度与物质性质、溶剂性质、温度和压力等因素有关。
为了研究溶解度与温度的关系,科学家通常会制作溶解度曲线,以直观地表示溶解度的变化规律。
一、溶解度曲线的概念和基本形态溶解度曲线是指在一定温度下,溶质在溶剂中的溶解度与溶液中溶质的质量或体积之间的关系曲线。
通常情况下,溶解度曲线呈现出以下几种基本形态:1. 直线型溶解度曲线:当溶质的溶解满足几乎无吸热或放热的条件时,其溶解度随溶质质量或体积的增加呈线性变化。
2. 正曲线型溶解度曲线:当溶质的溶解满足吸热条件时,其溶解度随溶质质量或体积的增加呈正曲线变化。
3. 反曲线型溶解度曲线:当溶质的溶解满足放热条件时,其溶解度随溶质质量或体积的增加呈反曲线变化。
以上三种基本形态可以通过实验数据的拟合获得溶解度曲线的数学表达式,并在坐标系中进行画图,以便直观地观察溶解度的变化规律。
二、影响溶解度曲线的因素溶解度曲线的形态及其在不同温度下的变化规律受多种因素的影响。
1. 温度:温度是影响溶解度曲线的重要因素之一。
一般情况下,温度升高会导致溶解度的增加,溶解度曲线向右移动。
但对于某些物质而言,温度的升高反而会降低其溶解度。
2. 压力:在大部分情况下,压力对溶解度的影响并不明显,因此通常在溶解度曲线的研究中不考虑压力的影响。
3. 溶质和溶剂的性质:溶质和溶剂的性质对溶解度也有一定的影响。
比如极性溶质在极性溶剂中的溶解度通常较高,而非极性溶质在非极性溶剂中的溶解度较高。
4. 其他因素:除了温度、压力、溶质和溶剂的性质外,其他因素如物质的晶体结构、溶液的浓度等也可能会对溶解度曲线产生影响。
三、溶解度曲线的应用溶解度曲线的研究对于理解物质的溶解过程、寻找合适的溶剂和控制溶解度具有重要意义。
1. 制定合理的溶解工艺:对于某些工业制品的制造过程中,需要调整溶解度来控制产品的质量。
通过研究溶解度曲线,可以确定最佳溶解条件和工艺参数,提高产品的质量和产量。


二、溶解度1.固体物质的溶解度:在一定温度下,某固体物质在100 g溶剂里达到饱和状态时所溶解的质量。
2.溶解度四要素:一定温度、100 g溶剂、饱和状态、溶质质量。
3.影响因素:影响溶解性大小的因素主要是溶质、溶剂的本性,其次是温度(固体溶质)或温度和压强(气体溶质)等。
固体物质的溶解度一般随温度的升高而增大,其中变化较大的如硝酸钾、变化不大的如氯化钠,但氢氧化钙等少数物质比较特殊,溶解度随温度的升高反而减小。
4.溶解度曲线:(1)表示:物质的溶解度随温度变化的曲线。
(2)意义:①表示同一种物质在不同温度时的溶解度;②可以比较同一温度时,不同物质的溶解度的大小;③表示物质的溶解度受温度变化影响的大小等。
5.气体的溶解度(1)定义:在压强为101 kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
(2)五要素:101 kPa、一定温度、1体积水、饱和状态、气体体积。
(3)影响因素:温度、压强。
升高温度,气体溶解度减小;降低温度,气体溶解度增大。
增大压强,气体溶解度增大;减小压强,气体溶解度减小。
【例题2】对照溶解度概念分析“36 g食盐溶解在100 g水中,所以食盐的溶解度为36 g”这句话应怎样改正。
【解析】溶解度概念包括四要素:“一定的温度”“100 g溶剂”“饱和状态”“溶质的质量”。
题中错误之处在于:一没有指明在什么温度下,因为物质的溶解度随温度的改变而改变。
二没有指明是否达到饱和状态,所以不正确。
【答案】在20 ℃时,36 g NaCl溶解在100 g水中恰好达到饱和状态,所以20 ℃时NaCl的溶解度为36 g。
【例题3】甲、乙物质的溶解度均随温度的升高而增大。
在10 ℃时,在20 g水中最多能溶解3 g甲物质;在30 ℃时,将23 g乙物质的饱和溶液蒸干得到3 g乙物质。
则20 ℃时甲、乙两种物质的溶解度的关系是()A.甲=乙 B.甲<乙C.甲>乙 D.无法确定【解析】比较不同物质的溶解度大小,一定要在相同温度下进行。
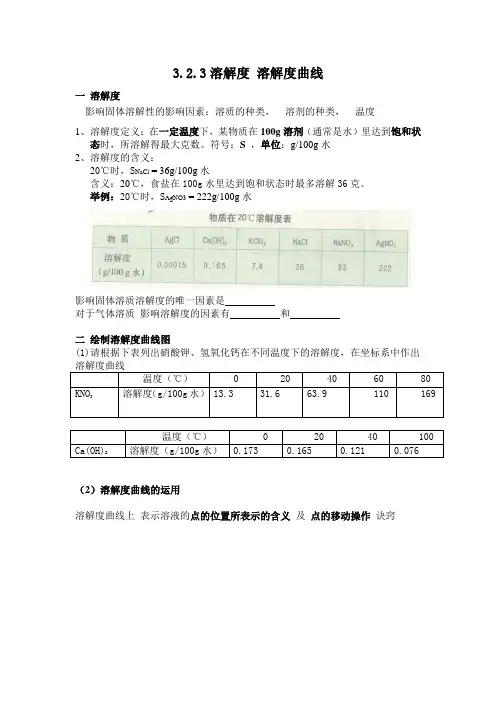
3.2.3溶解度溶解度曲线一溶解度影响固体溶解性的影响因素:溶质的种类,溶剂的种类,温度1、溶解度定义:在一定温度下,某物质在100g溶剂(通常是水)里达到饱和状态时,所溶解得最大克数。
符号:S,单位:g/100g水2、溶解度的含义:20℃时,S NaCl = 36g/100g水含义:20℃,食盐在100g水里达到饱和状态时最多溶解36克。
举例:20℃时,S AgNO3 = 222g/100g水影响固体溶质溶解度的唯一因素是对于气体溶质影响溶解度的因素有和二绘制溶解度曲线图(1)请根据下表列出硝酸钾、氢氧化钙在不同温度下的溶解度,在坐标系中作出温度(℃)0 20 40 60 80 溶解度(g/100g水)13.3 31.6 63.9 110 169 KNO3温度(℃)0 20 40 100 溶解度(g/100g水)0.173 0.165 0.121 0.076Ca(OH)2(2)溶解度曲线的运用溶解度曲线上表示溶液的点的位置所表示的含义及点的移动操作诀窍例1:右图是A、B、C三种物质的溶解度曲线,看图回答:(1)60℃时,B物质的溶解度是。
(2)10℃时,B物质的溶解度(填<、=或>)A物质的溶解度。
(3)℃时,A、B两物质的溶解度相同。
例2:.右图是X、Y、Z三种物质的溶解度曲线(1)A点所表示的意义(2)若X、Y、Z三种物质中,有一种是气态物质,该物是。
判断的依据是。
(3)20℃时,N处物质X的溶液呈(填饱和或不饱和)状态、要使该溶液从N状态变为M状态.应采取的措施有或三有关溶解度的计算公式:S 100 =m(溶质)m(溶剂)SS+100=((+(mm m溶质)溶质)溶剂)=m(m溶质)(溶液)例1、在T℃时,向80克水中加入硝酸钾固体20克,恰好达到饱和,求该温度下的溶解度例2、在20℃时,氯化钠的溶解度是36g/100g水,则在此温度下,30克水中最多能溶解氯化钠多少克?T℃,硝酸钾饱和溶液200克,蒸发20克水后析出晶体12克,则该温度时,硝酸钾的溶解度为_____________当堂训练1.下列说法正确与否,为什么?(1)20℃时,把10克食盐溶解在100克水里,所以20℃时食盐的溶解度是10 (2)20℃时,100克食盐饱和溶液里含有26.4克食盐,所以20℃时食盐的溶解度是26.4克/100克水(3)20℃时,食盐的溶解度是36克/100克水。


溶解度曲线的意义及应用一、溶解度曲线的概念在直角坐标系中,用横坐标表示温度(t),纵坐标表示溶解度(S),由t—S的坐标画出固体物质的溶解度随温度变化的曲线,称之为溶解度曲线。
二、溶解度曲线的意义1、点:曲线上的点叫饱和点。
①曲线上任一点表示对应温度下(横坐标)该物质的溶解度(纵坐标);②两曲线的交点表示两物质在交点的温度下溶解度相等。
2、线:溶解度曲线表示物质的溶解度随温度变化的趋势。
其变化趋势分为三种:①陡升型大多数固体物质的溶解度随温度升高而增大,如KNO3;②缓升型少数物质的溶解度随温度升高而增幅小,如NaCl;③下降型极小数物质的溶解度随温度升高而减小,如Ca(OH)2。
3、面(或线外的点):⑴溶解度曲线下方的面(曲线下方的点)表示不同温度下该物质的不饱和溶液。
⑵溶解度曲线上方的面(曲线上方的点)表示相应温度下的过饱和溶液(不作要求)。
三、溶解度曲线的应用例1:右图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。
据图回答:(1)P点的含义是。
(2)t2℃时30g a物质加入到50g水中不断搅拌,形成的溶液是(饱和或不饱和)溶液,溶液质量是 g。
(3)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是__________(填写物质序号)。
Q(4)在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是,所得溶液中溶质质量分数(浓度)由大到小的顺序是。
(5)把t1℃a、b、c三种物质的饱和溶液升温到t2℃时,所得a、b、c 三种物质的溶液中溶质质量分数(浓度)大小关系。
(6)若把混在a中的少量b除去,应采用___________方法;若要使b从饱和溶液中结晶出去,最好采用___________。
若要使C从饱和溶液中结晶出去,最好采用___________。
巩固练习1、图2是硝酸钾和氯化钠的溶液度曲线,下列叙述中不正确的是()A. t1℃时,120gKNO3饱和溶液中含有20gKNO320B. t2℃时,KNO3和NaCl的饱和溶液中溶质的质量分数相同C. KNO3的溶解度大于NaCl的溶解度D. 当KNO3中含有少量的NaCl时,可以用结晶方法提纯KNO32、右图为A物质的溶解度曲线。

一、饱和溶液与不饱和溶液1.饱和溶液与不饱和溶液的定义在一定温度下,向一定量溶剂里加入某液;当溶质还能继续溶解时,所得到的溶液2.对饱和溶液与不饱和溶液的理解(1)首先,要明确“一定温度”和“一定相转化的。
(2)其次,要明确“某一溶质的”饱和还能溶解KNO 3,此时的溶液是NaCl 的饱的饱和或不饱和溶液。
(3)有些物质能与水以任意比互溶3.饱和溶液与不饱和溶液的转化条件(1)一般规律:此转化条件适合大多数固体物质的溶液(2)特殊情况(如氢氧化钙):极少数物质在一定量水中溶解的最大溶液时,要升高温度;若把饱和溶液转化4.判断溶液是否饱和的方法一般地,可以向原溶液中再加入少量原继续溶解,则说明原溶液是该溶质的不饱和如果有且溶质的量不再减少,未溶解的溶质二、固体的溶解度1.定义在一定温度下,某固态物质在100 g 溶剂里度。
如果不说明溶剂,通常所说的溶解度是2.正确理解溶解度概念需要抓住的四个要(1)条件:一定温度。
因为物质的溶解度溶解度溶液加入某种溶质,当溶质不能继续溶解时,所得到的溶的溶液叫做这种溶质的不饱和溶液。
理解一定量的溶剂”。
因为改变溶剂量或温度时,饱和溶饱和溶液或不饱和溶液。
例如,在一定温度下不能再的饱和溶液,对KNO 3来说就不一定是饱和溶液了互溶,不能形成饱和溶液,如酒精没有饱和溶液。
化条件 的溶液,因为大多数固体物质在一定量水中溶解的最的最大量随温度的升高而降低(如熟石灰),此类物质转化成不饱和溶液,要降低温度。
少量原溶质,如果不能继续溶解,说明原溶液是该溶不饱和溶液。
或者在一定温度下,看该溶液中有没有不的溶质与溶液共存,那么这种溶液就是这种溶质的饱溶剂里达到饱和状态时所溶解的质量,叫做这种固态度是指物质在水里的溶解度。
四个要点溶解度随温度的变化而变化,所以不指明温度时,溶解到的溶液叫做这种溶质的饱和溶饱和溶液与不饱和溶液是可以互不能再溶解NaCl 的溶液,可能液了。
因此必须指明是哪种溶质解的最大量随温度升高而增大。

溶解度与溶解度曲线的关系溶解度是指在一定温度下,溶质在溶剂中能够溶解的最大量。
它是描述溶解过程中溶质与溶剂相互作用的重要参数。
溶解度曲线则是描述溶解度随温度变化的曲线。
溶解度与溶解度曲线之间存在着密切的关系,下面将从溶解度的影响因素、溶解度曲线的特点以及溶解度曲线的应用等方面进行探讨。
一、溶解度的影响因素溶解度受多种因素的影响,其中最主要的是温度、压力和溶质浓度。
首先,温度对溶解度的影响较为显著。
一般情况下,随着温度的升高,溶解度会增加。
这是因为温度升高会使溶质分子的动能增大,溶质分子与溶剂分子的相互作用力减弱,从而促进溶质分子进入溶剂中。
但是,对于某些溶质来说,随着温度的升高,溶解度反而会减小,这是由于溶质分子在溶剂中的溶解过程是吸热过程,温度升高会使溶解过程的熵变增大,从而导致溶解度的减小。
其次,压力对溶解度的影响相对较小,一般情况下可以忽略不计。
只有在气体溶解度较高的情况下,压力的变化才会对溶解度产生一定的影响。
当气体溶解度较高时,增大压力会使溶质分子更容易进入溶剂中,从而增加溶解度。
最后,溶质浓度对溶解度的影响也是很重要的。
溶质浓度越高,溶解度也会相应增加。
这是因为溶质浓度的增加会导致溶质分子之间的相互作用增强,从而增加溶质分子进入溶剂中的倾向。
二、溶解度曲线的特点溶解度曲线是描述溶解度随温度变化的曲线。
一般情况下,溶解度曲线呈现出以下特点。
首先,溶解度曲线的斜率代表了溶解度随温度变化的速率。
斜率越大,溶解度随温度的变化越快,反之则越慢。
其次,溶解度曲线在某些温度点上可能会出现突变。
这是因为在某些特定的温度下,溶质分子与溶剂分子的相互作用力发生了变化,导致溶解度发生突变。
最后,溶解度曲线在不同的溶剂中可能会呈现出不同的形状。
这是由于不同的溶剂有不同的分子结构和相互作用力,从而影响了溶解度随温度变化的规律。
三、溶解度曲线的应用溶解度曲线在实际应用中有着广泛的应用价值。
首先,它可以用于溶解度的预测和计算。

溶解度与溶解度曲线的解读溶解度是指单位质量的溶剂在一定温度和压力下最多能溶解的溶质质量,通常以克/100克溶剂(g/100g)或克/升溶液(g/L)表示。
溶解度是化学反应中的一个重要参数,对于溶解过程的理解以及反应速率的研究具有重要意义。
溶解度受到多个因素的影响,其中包括温度、压力和溶质与溶剂之间的相互作用力。
温度对溶解度的影响是其中最显著的因素之一。
通常情况下,随着温度的升高,溶解度会增加,呈现出正相关的趋势。
这是因为在高温下,分子的平均动能增大,导致溶质分子更容易克服吸引力和相互作用力,从而更容易融入溶剂中。
另一方面,在低温下,溶剂分子的平均动能降低,相互作用力增强,溶质的溶解度相对较低。
与温度相比,压力对溶解度的影响通常较小,尤其是对于固体溶质和液体溶剂的溶解过程。
但是,对于气体溶质和液体溶剂的情况下,压力的增大可以显著提高溶解度。
这是因为根据亨利定律,气体在液体中的溶解度与其压力成正比。
增加压力可以增加溶质分子通过液体表面进入溶液的机会,从而提高溶解度。
溶质与溶剂之间的相互作用力也是影响溶解度的重要因素。
当溶质与溶剂之间的相互作用力较大时,溶解度通常较高。
相反,当溶质与溶剂之间的相互作用力较小时,溶解度则相对较低。
这是因为相互作用力较强可以促使溶质分子在溶剂中更好地分散,并与溶剂分子形成较为稳定的溶液结构。
为了更直观地了解溶解度的变化规律,可以利用溶解度曲线进行解读。
溶解度曲线是描述在一定温度下溶质溶解度随溶剂质量或摩尔分数变化的曲线。
溶解度曲线的形态可以根据溶剂的类型和条件的不同而有所不同。
常见的溶解度曲线包括饱和溶解度曲线、过饱和溶解度曲线和不饱和溶解度曲线。
饱和溶解度曲线描述了在给定温度下溶质溶解度随溶剂质量的增加而变化的情况。
在曲线上各点的坐标表示了溶剂中存在的溶质的最大可能质量。
曲线的形状通常呈正向斜率,即溶质溶解度随溶剂质量增加而增加,直到达到饱和状态。
此时,溶液中的溶质质量无法再进一步增加。
溶解度与溶解度曲线溶解度是指在特定条件下,单位溶剂中可以溶解的最大溶质的量。
溶解度通常用溶质在单位溶剂中的摩尔或质量浓度来表示,单位常用mol/L或g/L。
溶解度受多个因素的影响,包括温度、压力和溶质与溶剂之间的相互作用力等。
其中,温度是溶解度影响最为显著的因素之一。
随着温度的升高,大部分固体溶质在溶剂中的溶解度会增加,而气体溶质的溶解度则会减小。
这是由于高温会增加溶质与溶剂之间的分子热运动,从而有利于克服溶剂与溶质之间的相互作用力,使溶质更容易溶解。
相反,低温下,热运动减弱,溶剂与溶质分子之间的相互作用力增强,导致溶质溶解度减小。
除了温度,压力也会对溶解度产生影响。
对于气体溶质,在一定温度下,随着压力的增加,气体溶质的溶解度也会增加。
这是由于增加压力会使气体溶质分子更加密集,更容易与溶剂分子发生相互作用,从而增加溶解度。
而固体或液体溶质的溶解度对压力影响较小,通常可以忽略不计。
溶剂选择也会对溶解度产生重要影响。
不同的溶剂有着不同的溶解度能力,这主要与溶剂与溶质之间的化学性质和极性相关。
相似的化学性质或极性的溶质和溶剂更容易彼此相互作用,从而溶解度较高。
此外,溶剂的溶解度也会受到温度和压力的影响,但影响程度可能与溶质的影响程度不完全相同。
溶解度曲线是描述溶解度随温度变化的曲线图。
根据溶解度与温度的关系,可以得到溶解度曲线的形状。
溶解度曲线通常可以分为两种类型:显热型和隐热型。
显热型溶解度曲线表示随着温度的升高,溶解度逐渐增加,形成一个正斜率的曲线。
这是由于溶解过程是放热的,温度升高会增加溶质与溶剂分子之间的热运动,从而有利于溶质溶解。
隐热型溶解度曲线表示随着温度的升高,溶解度逐渐减小,形成一个负斜率的曲线。
这是由于溶解过程是吸热的,温度升高会增加溶质与溶剂分子之间的热运动,导致溶质分子逃逸出溶液,从而减小溶解度。
根据溶解度曲线的形状,我们可以推断溶解过程中是否有热效应。
根据溶解度曲线的斜率,我们还可以判断溶解度对温度的敏感程度。
溶解度曲线图的含义和例题上海市清流中学朱初耀上海市浦东新区上南路 801 号 200126溶解度曲线图是初中化学的重要基础知识,有关习题涉及溶解度、溶解度计算、浓度计 算、饱和溶液与不饱和溶液相互转化、物质的结晶、物质分离等概念和知识,本文简述了溶 解度曲线的含义,并列举常见相关习题并分析,供参考。
溶解度曲线图通常有如图所示的图 A 、图 B 二类涉及的计算公式有:公式 1:S m (溶质) S m (溶质)或 100 m (溶剂) 100 S m (溶液)公式 2:C%=m (溶质) m (溶液)×100%公式3:C%(饱和溶液)=SS 100×100% 一、根据溶解度曲线图可以查出同种物质在不同温度下的溶解度数值,并 计算相应的 C%等数值。
例1:由曲线溶解度图A回答下列问题:①t2 时,B 物质的饱和溶液中溶质和溶剂的质量比为∶②t1时,将30克A物质投入60克水中,求所得溶液中溶质的质量分数为③t4时, 90克B物质溶解在150克水中,所得溶液为不饱和溶液,为了得到B物质的饱和溶液,问:a. 维持温度不变,至少要蒸发掉克水,才能使溶液饱和。
b. 维持温度不变,原溶液中至少再加入B物质克,才能使溶液饱和。
c.不改变溶液组成,只要把温度降低到℃,也能使溶液恰好达到饱和。
④要配制C%为28.6%的C物质溶液,配制时的温度应控制在℃。
解:①由图A知t2 时,S B=60 克∕100 克水,根据溶解度定义:在一定温度下,某物质在100 克溶剂里达到饱和时所溶解的克数,即当溶剂的质量为100 克时,溶质的质量为60 克,则溶质和溶剂的质量比为60∶100 或 3:5。
②由图A知t1时,S A=32克∕100克水,根据公式1计算可知,在60克水中最多溶解19.2克A物质,即30克A物质不能全部溶解,则根据公式2计算C%=19.219.260×100%=24.2%③a:已知t4时,S B=65克∕100克水,设90克B物质完全溶解并形成饱和溶液只需要溶剂水为x 克,根据公式1,65 90100 xx=138 克,由于原溶剂为150克,则150-138=12克,即蒸发12克水能使溶液达到饱和。
溶解度和溶解度曲线溶解度是指在特定条件下,溶液能够溶解的最大量溶质的性质。
溶解度可以通过溶解度曲线来表示,该曲线展示了溶质在不同温度下在溶剂中的溶解度。
1. 溶解度的定义和影响因素溶解度是指在一定温度下,单位溶剂中能溶解的最大物质的量。
溶解度受温度、溶剂性质、溶质溶剂间的相互作用等因素影响。
温度升高对于固体溶解度而言通常是有利的,但对于气体来说则相反。
2. 溶解度曲线的含义和绘制方法溶解度曲线是指在一定范围内,溶质在单位溶剂中的溶解度随着温度的变化而发生的曲线。
绘制溶解度曲线的方法是通过实验测定溶质在不同温度下的溶解度,并使用图表工具将温度和溶解度的关系表示出来。
3. 溶解度曲线的特点和解读溶解度曲线可以展示出溶质溶解度随温度变化的规律。
通常情况下,溶解度曲线呈现出以下几种特点:- 水溶液中的一些溶解度曲线是正斜率曲线,即随着温度的升高,溶解度增加;- 饱和溶液的溶解度曲线是水平的,即在饱和溶液中,溶质的溶解度不受温度的影响;- 某些溶质的溶解度曲线是倒U型曲线,即溶解度先随温度升高而增加,达到一定温度后再逐渐降低。
4. 重点溶解度曲线的实例分析以下是几个常见物质的溶解度曲线实例分析:- 饱和氯化钠水溶液的溶解度曲线是正斜率曲线;- 硝酸钙水溶液的溶解度曲线是倒U型曲线;- 汞的溶解度曲线是正斜率曲线。
5. 应用和意义溶解度曲线对于实际生产和科学研究起着重要的指导作用。
根据溶解度曲线,可以选择合适的温度和条件来调节溶解度,从而实现产品的最优化制备。
此外,溶解度曲线还能帮助科学家了解物质溶解过程中的分子间相互作用,深入研究物质的溶解动力学规律。
总结:溶解度和溶解度曲线是研究溶液中溶质溶解现象的重要概念。
溶解度曲线能够展示溶质溶解度随温度变化的规律,对于控制溶解度以及了解溶解过程的特性具有重要意义。
在实践中,我们可以根据溶解度曲线来调节溶解度以实现特定的需求。
同时,溶解度曲线也为科学家研究溶解动力学提供了重要依据,推动了科学研究的发展。
溶解度曲线及溶解度表前言在化学实验中,我们经常遇到溶解度的问题。
溶解度是指在给定条件下溶质在溶剂中的溶解量,通常以质量为单位表示。
溶解度的大小与温度、压力、溶质浓度等因素有关。
为了更好地了解溶解度的规律,我们可以通过溶解度曲线和溶解度表来进行研究和分析。
一、溶解度曲线溶解度曲线是指在不同温度下,溶质在溶剂中的溶解度随溶质浓度的变化关系所绘制的曲线。
溶解度曲线通常用来描述溶解度随温度变化的规律。
1.1 实验方法制作溶解度曲线的实验通常需要选择一个溶质和一个溶剂,并在不同温度下测定溶质在溶剂中的溶解度。
实验中,可以取一定质量的溶质加入溶剂中,充分搅拌使其溶解,然后测定溶解液的浓度。
通过多次实验,可以得到不同温度下的溶解度数据。
1.2 曲线形状溶解度曲线的形状取决于溶质在溶剂中的性质。
一般而言,溶解度随温度的升高而增大,但不同溶质的溶解度曲线可能呈现出不同的形状。
•若溶解度随温度的升高而增大,曲线呈现上升趋势;•若溶解度随温度的升高而减小,曲线呈现下降趋势;•若溶解度随温度的变化非常小,曲线呈现平直趋势。
二、溶解度表溶解度表是根据实验数据编制的,按照一定方式列出了不同溶质在不同温度下的溶解度数值。
通过溶解度表,我们可以直观地了解不同温度下溶质的溶解度。
2.1 表格结构通常,溶解度表的表格结构如下:温度(摄氏度)溶质1的溶解度(g/100mL)溶质2的溶解度(g/100mL)溶质3的溶解度(g/100mL)0 10.5 20.2 5.810 12.3 18.9 5.220 14.1 17.5 4.630 16.0 16.1 4.040 17.8 14.6 3.450 19.6 13.2 2.82.2 数据分析通过分析溶解度表中的数据,我们可以得到一些结论:1.在同一温度下,溶质1的溶解度大于溶质2和溶质3的溶解度;2.随着温度的升高,溶质的溶解度逐渐增大;3.不同溶质在相同温度下的溶解度差异很大。
三、溶解度的影响因素除了温度以外,溶解度还受其他因素的影响。
初中化学溶解度曲线图的解读与分析方法溶解度是指在一定温度下溶质在溶剂中溶解成溶液的最大量。
溶解度曲线图是描述溶解度随温度变化的图表。
通过解读和分析溶解度曲线图,我们可以了解不同物质溶解度的规律性,并对溶解过程进行深入理解。
解读溶解度曲线图的第一步是观察曲线的趋势。
溶解度曲线通常呈现出不同的形态,如正常溶解度曲线、倒U型曲线、S型曲线等。
根据曲线的形态,我们可以初步判断物质的溶解过程特点。
例如,正常溶解度曲线代表溶解度随温度的升高而增加,这表明溶解过程是吸热的;倒U型曲线则表示溶解度随温度的升高先增加后减少,这表明在一定温度范围内溶解度最大,超过该温度后溶解度降低;S型曲线则表示溶解度随温度的升高先减少后增加,这可能是由于溶质在低温下产生了某种结晶,而在高温下重新溶解所导致。
在进一步分析时,我们需要关注曲线上的特殊点或特征。
首先,峰值点通常表示溶解度达到最大值的温度。
通过观察峰值点的位置,我们可以比较不同物质的溶解度大小。
其次,曲线上的水平线段表示溶解度在该温度范围内保持不变。
这些水平线段可能与某种相变过程相关,如晶体水合物的结晶水的脱失。
最后,曲线上的斜率表示溶解度随温度变化的速率。
斜率的变化率可以反映溶解过程的速度,例如,斜率越大,表示溶解过程越快。
为进一步深入分析溶解度曲线图,我们可以考虑以下几个方面:1. 温度变化对溶解度的影响:通过比较不同物质的溶解度曲线,我们可以观察不同物质在不同温度下的溶解度变化规律。
这有助于我们理解物质的溶解特性以及温度对溶解过程的影响。
2. 物质的溶解热:根据溶解度曲线的形态,我们可以初步判断溶解过程是吸热还是放热的。
进一步分析可以计算出物质的溶解热,并比较不同物质的溶解热大小。
3. 溶液中溶质的浓度变化:通过分析溶解度曲线,我们可以了解溶质浓度随温度变化的趋势。
这可以帮助我们理解溶解过程中溶质在溶液中的分布规律。
4. 物质的晶体结构:溶解度曲线的特殊点和特征可以与物质的晶体结构相关联。