第十八章 已改杂环化合物
- 格式:doc
- 大小:120.50 KB
- 文档页数:6

第十八章杂环化合物教学要求1.了解杂环化合物的分类、命名。
2.掌握重要的五元、六元及稠环杂环化合物的结构和性质。
如:呋喃、噻吩、吡咯、喹啉(斯克奥浦合成)。
3.了解嘧啶及嘌呤的结构。
4.了解生物碱的一般概念。
杂环化合物是指组成环的原子中含有除碳以外的原子(杂原子——常见的是N、O、S等)的环状化合物。
杂环化合物不包括极易开环的含杂原子的环状化合物,例如:本章我们只讨论芳香族杂环化合物。
杂环化合物是一大类有机物,占已知有机物的三分之一。
杂环化合物在自然界分布很广、功用很多。
例如,中草药的有效成分生物碱大多是杂环化合物;动植物体内起重要生理作用的血红素、叶绿素、核酸的碱基都是含氮杂环;部分维生素,抗菌素;一些植物色素、植物染料、合成染料都含有杂环。
第一节杂环化合物的分类和命名一、分类二、命名杂环的命名常用音译法,是按外文名词音译成带“口”字旁的同音汉字。
当环上有取代基时,取代基的位次从杂原子算起依次用1,2,3,… (或α,β,γ…)编号。
如杂环上不止一个杂原子时,则从O、S、N顺序依次编号。
编号时杂原子的位次数字之和应最小。
第二节五元杂环化合物含一个杂原子的典型五元杂环化合物是呋喃、噻吩和吡咯。
含两个杂原子的有噻唑、咪唑和吡唑。
本节重点讨论呋喃、噻吩和吡咯,简单介绍一下噻唑、咪唑和吡唑。
一、呋喃、噻吩、吡咯杂环的结构呋喃、噻吩、吡咯在结构上具有共同点,即构成环的五个原子都为sp2杂化,故成环的五个原子处在同一平面,杂原子上的孤对电子参与共轭形成共轭体系,其π电子数符合休克尔规则(π电子数 = 4n+2),所以,它们都具有芳香性。
二、呋喃、噻吩、吡咯的性质1、存在与物理性质2、光谱性质3、化学性质(1)亲电取代反应从结构上分析,五元杂环为∏56共轭体系,电荷密度比苯大,如以苯环上碳原子的电荷密度为标准(作为0),则五元杂环化合物的有效电荷分布为:五元杂环有芳香性,但其芳香性不如苯环,因环上的π电子云密度比苯环大,且分布不匀,它们在亲电取代反应中的速率也比要苯快得多。
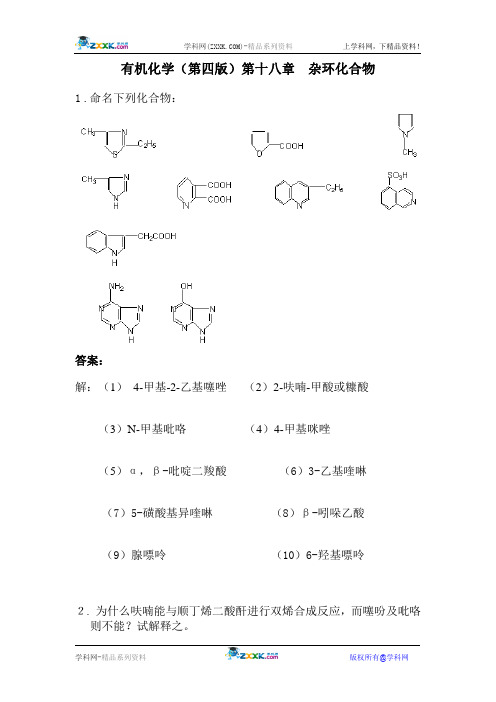
有机化学(第四版)第十八章杂环化合物1.命名下列化合物:答案:解:(1)4-甲基-2-乙基噻唑(2)2-呋喃-甲酸或糠酸(3)N-甲基吡咯(4)4-甲基咪唑(5)α,β-吡啶二羧酸(6)3-乙基喹啉(7)5-磺酸基异喹啉(8)β-吲哚乙酸(9)腺嘌呤(10)6-羟基嘌呤2.为什么呋喃能与顺丁烯二酸酐进行双烯合成反应,而噻吩及吡咯则不能?试解释之。
答案:解:五元杂环的芳香性比较是:苯>噻吩>吡咯>呋喃。
由于杂原子的电负性不同,呋喃分子中氧原子的电负性(3,5)较大,π电子共扼减弱,而显现出共扼二烯的性质,易发生双烯合成反应,而噻吩和吡咯中由于硫和氮原子的电负性较小(分别为2.5和3),芳香性较强,是闭合共扼体系,难显现共扼二烯的性质,不能发生双烯合成反应。
3. 为什么呋喃、噻吩及吡咯容易进行亲电取代反应,试解释之。
答案:解:呋喃、噻吩和吡咯的环状结构,是闭合共扼体系,同时在杂原子的P轨道上有一对电子参加共扼,属富电子芳环,使整个环的π电子密度比苯大,因此,它们比苯容易进行亲电取代反应。
4. 吡咯可发生一系列与苯酚相似的反应,例如可与重氮盐偶合,试写出反应式。
答案:解:5. 比较吡咯与吡啶两种杂环。
从酸碱性、环对氧化剂的稳定性、取代反应及受酸聚合性等角度加以讨论。
答案:解:吡咯与吡啶性质有所不同,与环上电荷密度差异有关。
它们与苯的相对密度比较如下:吡咯和吡啶的性质比较:6. 写出斯克劳普合成喹啉的反应。
如要合成6-甲氧基喹啉,需用哪些原料?答案:解:Skramp法合成喹啉的反应:7. 写出下列反应的主要产物:答案:.解:8. 解决下列问题:(1)区别吡啶和喹啉;(2)除去混在苯中的少量噻吩;(3)除去混在甲苯中的少量吡啶;(4)除去混在吡啶中的六氢吡啶。
答案:解;(1)吡啶溶于水,喹啉不溶。
(2)噻吩溶于浓H2SO4,苯不溶。
(3)水溶解吡啶,甲苯不溶。
(4)苯磺酰氯与六氢吡啶生成酰胺,蒸出吡啶。




有机化学Organic Chemistry 第18章杂环化合物(3’)教材:李景宁主编高等教育出版社原则上,环状机化合物中,构成环的原子,除了碳原子外,还有其他原子的,都称为杂环化合物。
2. 杂环化合物的英文?杂环化合物,heterocyclic compound。
[hetərə'saɪklɪk]By the end of eighteen century,experimenters had well established that each pure substance had its own characteristic set of properties such as density, specific heat,melting point,and boiling point. Organic chemistry is a sub-discipline within chemistry involving the scientific study of the structure,properties,composition,reactions,and preparation(by synthesis or by other means)of carbon-based compounds,hydrocarbons,and their derivatives.一、分类ON S五元 杂环第一节杂环化合物的分类和命名H 六 元 杂环NN N 单杂环稠 杂环NN H1. 母体名称呋喃吡咯噻吩咪唑噻唑82. 编号•从杂原子编起(母体的编号是固定的);•若有不同杂原子时,从O 、S 、N 顺序编号;•杂原子的位次遵循最低系列原则•例:3-1-酸类化合物以酸为母体,杂环为取代基。
N CH3甲基吡咯(β-甲基吡咯)甲基吡咯(N -甲基吡咯)α-呋喃甲酸(2-呋喃甲酸)α-噻吩磺酸N第二节五元杂环化合物OSHfuran pyrrole thiophene 呋喃吡咯噻吩一、呋喃、噻吩、吡咯杂环的结构π电子数满足4n +2,分子是闭合的共轭体系,NMR 谱图δ值为7左右,具有芳香性。
第十八章杂环化合物
1、命名下列化合物:
解:(1) 4-甲基-2-乙基噻唑(2) 糠酸(α-呋喃甲酸)
(3) N-甲基吡咯(4) 4-甲基咪唑(5) α,β-吡啶二甲酸(2,3-吡啶二甲酸)(6)β-乙基喹啉(3-乙基喹啉)(7) 5-异喹啉磺酸(8) β-吲哚乙(3-吲哚乙酸)(9) 6-氨基嘌呤(10) 6-羟基嘌呤
2、为什么呋喃能与顺丁烯二酸酐进行双烯合成反应,而噻吩及吡咯则不能?试解释之。
解:在呋喃、吡啶和噻吩中,杂原子分别是O、N和S。
电负性是O>N>>S ,提供电子对构成具有芳香性的芳环的能力与此电负性的关系相反。
因此芳香性:呋喃>吡啶>噻吩。
另一方面,反应出来的共轭二烯性:呋喃>吡啶>噻吩。
因此,呋喃易与顺—丁烯二酸酐发生环加成反应而吡啶、噻吩则需反应性更强的双烯体,如苯炔、丁炔二酸脂等。
3、为什么呋喃、噻吩及吡咯容易进行亲电取代反应,试解释之。
解:在呋喃、噻吩和吡咯中,具有五原子环六个π电子芳香共轭体系,符合[4n+2]休克尔规则,都具有芳香性。
因此芳香性大小是:呋喃>吡啶>噻吩。
这些芳环又是富电子的芳香共轭体系,易发生亲电取代。
4、吡咯可发生一系列与苯酚相似的反应,例如可与重氮盐偶合,试写出反应式。
N
H C6H5N2 X
N
N N C6H5
2—吡咯偶氮苯
5、比较吡咯与吡啶两种杂环。
从酸碱性、环对氧化剂的稳定性、取代反应及受酸聚合性等角度加以讨论。
解: 吡咯和吡啶分子中的氮原子都是sp2杂化的。
在吡啶中,有一对未共用电子对处在未参与共轭的sp2杂化轨道上,因此吡啶的碱性很强;另外吡啶氮上的未共用电子对能与水分子形成氢键,吡啶易溶于水,吡咯不具备与水形成氢键的结构特征,因此难溶于水。
在吡咯中,氮原子提供一对未参与杂化的p轨道上电子参与芳香体系的形成,因此其碱性很弱;氮原子上的氢电离后形成的负离子未破坏其芳香性,因此,吡啶的性质类似于硝基苯;为一缺电子芳香性分子,对氧化剂较不稳定,亲电取代反应活性也较高。
吡啶和强酸作用可生成盐,不破坏其芳香性;吡咯和酸作用时,氮原子提供一对p轨道上的电子和酸结合,破坏了其芳香性,生成聚合产物。
6、写出斯克劳普合成喹啉的反应。
如要合成6-甲氧基喹啉,需用哪些原料?
解:
HC OH CH2OH CH2OH 24CH
CH2
NO
2
CHO
N H
CH 2
CH 2CHO N H
CH 2
CH 2CHOH 烯醇化
2关环
NH
硝基苯
N
合成6-甲氧基喹啉所需的原料:
NH 2
H 3CO
;
CH
CH 2OH
2OH
OH
;
NO 2
CH 3
O
7、 写出下列反应的主要产物:
O (CH 3CO)2O
BF
3
O
C CH
3
CH 3COOH
(1)
S
H 2SO 4。
C
S
SO 3
H
(2)
(3)
O
Br 2
25。
C
O
Br
N
H
CH 3
MgI
N
H
CH 4
(4)
(5)
S
C C
O O
O AlCl 3
S
S O
HOOC
(6)
O
CHO
Cl 2
O
CHO
Cl
浓NaOH O
Cl
CH 2OH
O
Cl
COONa
8、 解决下列问题:
(1) 区别吡啶和喹啉;
(2) 除去混在苯中的少量噻吩;
(3) 除去混在甲苯中的少量吡啶;
(4) 除去混在吡啶中的六氢吡啶。
解:(1)吡啶溶于水,喹啉在水中的溶解度很小(这是由于多了一个疏水性苯基的结果。
)
(2)向混合物中加入浓硫酸,振摇,使生成的2-噻吩磺酸溶于下层的硫酸中得以分离。
(3)向混合物中加入水,振摇,吡啶溶于下层的水中得以分离。
(4)苯磺酰氯与六氢吡啶生成酰胺,蒸出吡啶。
或根据六氢吡啶的碱性比吡啶的碱性强得多,将混合物先溶于乙醚等有机溶剂,再向溶液中加入适量的酸,将六氢吡啶和酸生成的盐沉淀出来。
9、合成下列化合物:
(1) 由N CH3
合成N
O
(2) 由苯胺、吡啶为原料合成磺胺吡啶H2N S N
H
O
O N
(3) 由合成(1)
N CH3
H
4
N
AlCl3
N
O
该题不能将两边反过来设计,因为吡啶环不能发生傅-克反应。
(2)
NH 2
(CH 3CO)2O
NHCOCH 3
HOSO Cl 。
C
NHCOCH 3
S O
O N
NH 2
H 2N
S N H
O
O
N
(2)OH
O
S O
N H
N
H 3COCHN
(3)
CH
3
HNO 3N 2SO 4
CH 3
2
COOH
2Fe ,HCl
COOH
2
CH
OH
CH 2OH CH 2OH 浓H 2SO 4
N H
HOOC
N
HOOC
混酸
N
HOOC 2
10、 杂环化合物C 5H 4O 2经氧化后生成羧酸C 5H 4O 3,把此羧酸的钠盐与碱石灰作用,转变为C 4H 4O ,后者与钠不起反应,也不具有醛和酮的性质,原来的C 5H 4O 2是什么? 解:C 5H 4O 2 [O]
C 5H 4O 3
O
CHO [O]
O
COOH
O
COONa CaO,NaOH
O
11、 用浓硫酸将喹啉在220~230°C 时磺化,得喹啉磺酸(A ),把(A )与碱共熔,得喹啉的羟基衍生物(B )。
(B )与应用斯克劳普法从邻氨基苯酚制得的喹啉衍生物完全相同,(A )和(B )是什么?磺化时苯环活泼还是吡啶环活泼? 解:
喹啉磺酸(A )
N 3H
NaOH(s)
N (B)
NH 2
24
CH
CH 2OH
CH 2OH
N (B)
磺化时苯环比吡啶环更活泼。
12、 α、β-吡啶二甲酸脱羧生成β-吡啶甲酸(烟酸):
解:脱羧时涉及到碳—碳键异裂,吡啶环具有负电荷。
碳—碳键异裂时,负电荷处在α-位能被电负性大的氮原子所分散,负电荷处在β-位则不能被有效的分散。
因此脱羧在α-位。
(缺少一个图)
13、毒品有哪几类,它的危害是什么? 解:略,请参见教材229-232页。