2北航物理实验研究性报告热学系列实验测量冰的熔解热实验和电热
- 格式:doc
- 大小:20.00 KB
- 文档页数:9

一、实验目的1. 了解冰的溶解热的概念及其在物质相变过程中的重要性;2. 掌握混合量热法测定冰的溶解热的基本原理和操作步骤;3. 通过实验,提高对实验数据分析和处理的能力。
二、实验原理冰的溶解热是指在标准大气压下,单位质量的冰在熔点时变成同温度的水所吸收的热量。
本实验采用混合量热法测定冰的溶解热,该方法基于能量守恒定律,即系统吸收的热量等于系统放出的热量。
实验原理公式如下:Q吸 = Q放其中,Q吸为冰熔化过程中吸收的热量,Q放为系统向外界散失的热量。
三、实验仪器与试剂1. 仪器:量热器、天平、温度计、停表、冰块、热水、擦布等;2. 试剂:纯净水。
四、实验步骤1. 准备实验器材,检查量热器、天平、温度计等仪器是否正常;2. 使用天平称量空量热器的质量,记为m0;3. 向量热器内筒中加入一定量的水,称量水的质量,记为m1;4. 使用温度计测量水的初温,记为T1;5. 将冰块置于0℃环境中,待冰块完全融化后,用干布擦干其表面水分;6. 将冰块投入量热器水中,同时轻轻搅拌;7. 每隔半分钟观测一次水温,记录水的温度和相应的时间t;8. 当冰全部融化后,水的温度即将平衡,继续测量4-5分钟;9. 称量内筒及水的总质量,确定出冰的质量M;10. 根据公式计算冰的溶解热:Q = m c ΔT其中,Q为冰的溶解热,m为冰的质量,c为水的比热容,ΔT为水的温度变化。
五、实验结果与分析1. 根据实验数据,计算冰的溶解热;2. 分析实验误差,如测量误差、操作误差等;3. 与理论值进行比较,评估实验结果的准确性。
六、实验结论通过本次实验,我们成功测定了冰的溶解热。
实验结果表明,混合量热法是一种有效测定冰溶解热的方法。
在实际应用中,冰的溶解热在食品保鲜、制冷等领域具有重要意义。
七、注意事项1. 实验过程中,注意保持量热器内筒的清洁,避免杂质影响实验结果;2. 称量冰块时,避免冰块表面水分过多,影响实验结果的准确性;3. 实验过程中,注意观察水温变化,及时记录数据;4. 实验结束后,对实验器材进行清洗和保养。
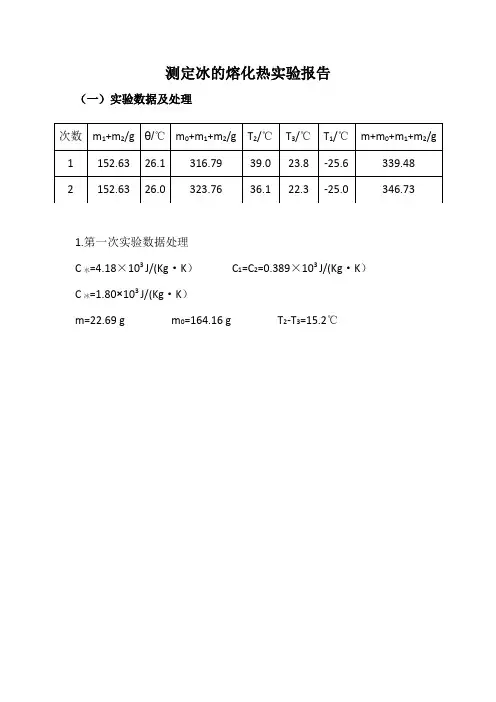
测定冰的熔化热实验报告(一)实验数据及处理1.第一次实验数据处理C水=4.18×103 J/(Kg·K)C1=C2=0.389×103 J/(Kg·K)C冰=1.80×103 J/(Kg·K)m=22.69 g m0=164.16 g T2-T3=15.2℃2.第二次实验数据处理C水=4.18×103 J/(Kg·K)C1=C2=0.389×103 J/(Kg·K)C冰=1.80×103 J/(Kg·K)m=22.97g m0=171.13g T2-T3=13.8℃(T2-θ):(θ-T3)= 10.1 :3.7(二)分析与讨论1.从实测数据看,如果实验全过程中散热、吸热没有达到补偿,冰的熔化热结果不一定偏离“合理”的数据范围,这说明散热或吸热并不是该系统的主要实验误差来源。
那么,本实验的主要误差来源是什么?由熔化热的公式看,对计算结果影响最大的量是m,即冰的质量。
由于采用间接测量法,因此冰的质量是比较容易产生误差的,比如投冰时溅出水,就会对算出的冰的质量产生影响,从而产生误差。
2.通过实验去体会粗略修正散热的方法——补偿法在本实验中的应用对学习做实验的意义。
在实验系统不能很好地保证绝热时,用补偿法修正系统误差是一个办法,也是一个好的思路。
在这次实验中,我们应该反复摸索,对各物理参量进行合理的选择和调整,使散热和吸热基本达到补偿。
然而,实验结果证实量热器是一个很好的绝热系统,因此,在分析系统误差来源时,应实事求是地、定量地进行分析,不能将误差的来源归结为系统的散热、吸热未能达到补偿。
3.在本实验室提供的条件下,实测熔化热的结果通常小于文献值L=3.34×105J/Kg,你能分析是什么原因吗?本实验未计算温度计插入水中的部分带来的影响。

用混合热量法测定冰的熔化热实验报告一、实验目的:1.正确使用热量器,熟练使用温度计。
2.用混合热量法测定冰的熔解热。
3.进行实验安排和参量选取。
4.学会一种粗略修正散热的方法——抵偿法。
二、实验用具:热量器、数字温度计、电子天平、秒表、干抹布、保温桶、冰以及热水等。
关于实验仪器的说明:1.电子天平使用前,请将电子天平放置于稳固、平坦的台面上,利用四只调整脚,使仪器保持平衡(勿放于摇动或振动台架上)。
注意水平仪内气泡应位于圆圈中央。
使用时应避免将其至于温度变化较大或者空气流动剧烈的场所,如日光直射或冷气机的出风口。
打开电源时,秤盘上请勿防止任何物品。
建议开机预热1~5分钟,以确保测量的精确度。
使用时,称量物品重心须位于称盘的中心点,且称量物不可超出称量范围,以确保准确度。
2.量热器量热器的构造如下图所示。
由铜质内筒、塑料外筒、绝热盖、环形绝热架、橡皮塞和铜质搅拌器组成。
绝热盖上附有中空橡皮塞,用于实验时插入温度计。
搅拌器通过绝热盖上的细孔置于内筒中,试验时上下搅动,使桶内各处温度迅速均匀。
内筒置于外筒内部的环形绝热架上,外筒又用胶木圆盖盖住。
因此,内部空气夹层与外界对流很小。
又因空气是热的不良导体,故外、内筒之间由传导所传递的热量可减到很小。
同时,内筒的外壁电镀得十分光亮,使得它们辐射或吸收热量的本领变得很小。
所以,因辐射而产生的热量传递也可以减至最小。
由上所述,量热器的这种结构,使将热量传递的三种方式:传导、对流及辐射都尽可能地减到最小;因而,他成为量热实验的常用仪器。
使用时,通常是先注入适量的水(约为容量的二分之一到三分之二),并将温度计、搅拌器等通过绝热盖的小孔插入,构成所谓已知热容的系统。
但上述量热器的绝热条件并不十分完善,因此在进行精确的量热实验时还必须据牛顿冷却定律进行散热修正。
三、实验原理:质量为m i,温度为θ0′的冰块与质量为m、温度为θ1的水相混合,冰全部熔化为水后,测得平衡温度为θ2。

探究测定冰的熔解热实验冰水质量比以及实验过程和数据处理的改进方法周晓城,巨建树(北京航空航天大学生物与医学工程学院北京 100191)摘要:本文通过计算得到混合量热法中的最佳冰水质量比并在实验中对此进行比较讨论,验证计算值,得出结论;验证牛顿冷却定律,同时得到实验参照值;并就本人在实验过程中遇到的一些问题提出实验操作以及数据处理方面的一些改进意见和建议;以及在数据处理过程中发现的水量、温差与冷却常数和实验误差之间的大致关系。
关键词:冰水质量比;牛顿冷却定律;数据处理;改进意见;误差规律中图分类号:043文献标识码:A文章编号:1.实验背景测量冰的熔解热的实验方法有很多,在大学物理实验中使用最多的是混合量热法,而作为大学物理少数几个热学实验中的一员,其重要性显而易见。
然而在实验的操作过程中很多同学反映实验不好操作,具体的问题有:1.依据《基础物理实验》[1],实验中需要保证加冰前与加冰后的稳定温度与室温的温差大约在10-15℃能较好地依据牛顿冷却定律绘制温度补偿修正曲线,而对于没有经验的实验者来说实验中的水量和冰量添加不好把握,加冰太少,可能造成冰块溶解后水温高于室温而无法温度修正,或者加冰太多,造成温度稳定后冰块无法溶解完全,在实验中往往需要经过多次尝试才能取得较好的实验数据,费时费力费水;2.取冰时,所有同学都是徒手取冰的,而对于较低温度(-21℃)的冰块,手的温度较高(30℃左右),即使在取冰和透冰过程中接触的时间很短(亲测至少15s),参照实验过程中冰块溶解降温曲线,吸热也会很明显,从而使得实验结果偏低,而在没有同伴的情况下,为了协调记录时间、记录温度,同时还要投冰动作迅速而使水不外溅,观察到通常同学会找特殊时刻投冰,在这种情况下不是冰块在外界的时间过长甚至开始融化了,就是手忙脚乱实验数据很难记录,实验效果不是很好;3.同时,由于投冰之后冰融化的最初几分钟铂电阻温度计示数变化非常快,而且需记录的数据比较多,同时还要不断搅拌,使得这段数据点很容易记录不全或者记录偏差,而这段数据是数据处理过程中非常重要的部分,直接影响到温度的修正,所以很容易造成实验误差;4.还有数据处理中绘制温度修正曲线时,要求室温线上方的温度修正线与室温线所围面积与下方的面积相等,使用的方法是在坐标纸中绘图,然后通过数格子找到使面积大概相等的时刻t=t0,由于坐标纸大小有限、比例有限,数格子非常麻烦而且这样做是十分不准确的,使得T2′,T3′有了误差,影响实验效果。

冰的熔化热实验报告一、实验目的1、用混合法测量冰的熔化热。
2、学习量热器的使用方法。
3、加深对热学基本概念的理解。
二、实验原理当质量为 m₁、温度为 T₁的高温物体与质量为 m₂、温度为 T₂的低温物体混合后,达到热平衡时的温度为 T,则高温物体放出的热量等于低温物体吸收的热量,即:\(m₁c₁(T₁ T) = m₂c₂(T T₂) + m₂λ\)式中,c₁、c₂分别为高温物体和低温物体的比热容,λ为低温物体的熔化热。
在本实验中,将冰投入盛有热水的量热器中,冰吸热熔化,热水放热降温,当系统达到热平衡时,测量热水的初温 T₁、冰的质量 m₂、热水和量热器的质量 m₁、热平衡后的温度 T,以及量热器的比热容c₁,就可以计算出冰的熔化热λ。
三、实验器材量热器、天平、温度计、小冰块、热水、搅拌器。
四、实验步骤1、用天平称出量热器内筒和搅拌器的质量 m₁₁。
2、在内筒中加入适量的热水,测量热水的温度 T₁,记录下来。
3、称出总质量 m₁₂,计算出热水的质量 m₁= m₁₂ m₁₁。
4、用天平称出小冰块的质量 m₂。
5、迅速将小冰块投入量热器内的热水中,并用搅拌器搅拌,使系统尽快达到热平衡,同时注意观察温度计的示数变化,记录热平衡时的温度 T。
五、实验数据记录与处理|实验次数|热水质量 m₁(g)|冰的质量 m₂(g)|热水初温T₁(℃)|热平衡温度 T(℃)||||||||1|_____|_____|_____|_____||2|_____|_____|_____|_____||3|_____|_____|_____|_____|量热器的比热容 c₁=______ J/(kg·℃)水的比热容 c₂= 42×10³ J/(kg·℃)根据实验数据,计算每次实验中冰的熔化热λ:\\begin{align}m₁c₁(T₁ T) &= m₂c₂(T T₂) + m₂λ\\λ&=\frac{m₁c₁(T₁ T) m₂c₂(T T₂)}{m₂}\end{align}\计算出三次实验的冰的熔化热λ₁、λ₂、λ₃,然后取平均值:\(\lambda =\frac{\lambda₁+\lambda₂+\lambda₃}{3}\)六、实验误差分析1、系统与外界的热交换:在实验过程中,量热器不可避免地会与外界发生热交换,导致测量结果偏小。

大学物理实验报告课程名称:大学物理实验实验名称:冰的熔解热的测量冰的熔解热的测量一、 实验项目名称:冰的熔解热的测量 二、 实验目的1.理解熔解热的物理意义,掌握用混合量热法测定冰的熔解热.2.学会用图解法估计和消除系统散热损失的修正方法.三、 实验原理单位质量的固体物质在熔点时从固态全部变成液态所需的热量,称为该物质的比熔解热,一般用L 来表示。
实验时将质量为m 1克0℃的冰投入盛有m 2克T 1℃水的量热器内筒中,设冰全部熔解为水后平衡温度为T 2℃,保温杯、搅拌器的质量分别为m 3、 m 4,其比热容分别为C 1、C 2和水的比热容为C 0。
根据混合量热法的原理,冰全部熔解为同温度(0℃)的水并从0℃升到T 2℃过程中所吸收的热量等于其余部分(水m 1、保温杯m 3、搅拌器m 4)从温度T 1℃降到T 2℃时所放出的热量,有(1) 冰的熔解热的实验公式为(2)式中水的比热容C 0=4.18×103J/kg ℃。
本实验“热学系统”依据混合量热法测量冰的熔解热,必须在系统与外界绝热的条件下进行实验。
为了满足此条件,从实验装置、测量方法和实验操作等方面尽量减少系统与外界的热交换。
由于实验系统不可能与环境温度始终一致,因此不满足绝热条件,可能会吸收或散失能量。
因此,要适当地选择参数进行散热修正。
牛顿冷却定律告诉我们,一个环境的温度T 如果略高于环境温度T 0(两者的温度差不超过10℃),系统就会散失热量,散热速率与温度差成正比,用数学形式表示为当时(即直线围成的两块面积近似相等),系统的散热与吸热相互抵消,就可以将系统很好地近似为一个孤立系统。
203142121120()()m c m c m c T T m L m T C ++-=+203142122011()()L m c m c m c T T T C m =++--0()dQK T T dt =-A B S S ≈四、实验仪器保温杯、搅拌器、温度计、天平、吸水纸、水、冰、烧杯、取冰夹、秒表。

测定冰的熔解热实验报告测定冰的熔解热实验报告引言:熔解热是物质从固态转变为液态所需吸收的热量。
在日常生活中,我们经常接触到冰,因此了解冰的熔解热对于理解物质状态变化和热力学性质具有重要意义。
本实验旨在通过测定冰的熔解热,探索冰的物理特性和热力学过程。
实验原理:冰的熔解是一个吸热过程,当冰从固态转变为液态时,需要吸收一定的热量。
根据热力学原理,冰的熔解热可以通过以下公式计算得出:Q = m × L其中,Q表示熔解热,m表示冰的质量,L表示冰的熔解潜热。
实验步骤:1. 准备实验器材:电子天平、烧杯、温度计、冰块。
2. 使用电子天平称量一定质量的冰块,并记录下冰块的质量m。
3. 将称量好的冰块放入烧杯中。
4. 在烧杯中插入温度计,并记录下初始温度T1。
5. 加热烧杯中的冰块,直到冰完全熔化为止。
期间需不断搅拌以保持温度均匀。
6. 在冰完全熔化后,记录下此时的温度T2。
数据处理:根据实验原理中的公式,可以计算出冰的熔解热Q。
首先,计算冰的质量m,然后根据温度变化ΔT = T2 - T1,再结合水的比热容C,可以计算出吸收的热量Q = m × C × ΔT。
由于水的比热容C已知,所以可以通过实验数据计算出冰的熔解热。
实验结果:根据实验数据和计算公式,我们可以得出冰的熔解热。
以一次实验数据为例,假设冰的质量为50g,初始温度为0°C,冰完全熔化后的温度为10°C。
根据公式,ΔT = 10°C - 0°C = 10°C。
假设水的比热容为4.18 J/(g·°C),则吸收的热量Q = 50g × 4.18 J/(g·°C) × 10°C = 2090 J。
因此,冰的熔解热为2090 J。
讨论与分析:通过多次实验,我们可以得出冰的熔解热的平均值。
在实验中,我们发现冰的熔解过程是一个温度稳定的过程,即使在加热的过程中,温度不会显著上升,直到冰完全熔化为止。

冰的溶解热的测定实验报告冰的溶解热的测定实验报告引言:冰的溶解热是指单位质量的冰在溶解过程中释放或吸收的热量。
这一物理性质在化学和物理学领域中具有重要意义。
本实验旨在通过测定冰的溶解热来探究其热力学特性,并通过实验结果验证理论计算的准确性。
实验材料与仪器:1. 冰块:约100克2. 定量烧杯:100毫升3. 温度计:精确到0.1摄氏度4. 搅拌棒:用于搅拌溶液5. 电子天平:用于称量冰块和水的质量实验步骤:1. 使用电子天平称量100克的冰块,并记录其质量。
2. 将冰块放入100毫升的定量烧杯中。
3. 用温度计测量并记录室温下的水温。
4. 用搅拌棒轻轻搅拌冰块,直到所有冰块完全融化。
5. 即时测量并记录溶液的最终温度。
实验数据处理与分析:根据热力学原理,冰的溶解热可以通过以下公式计算:Q = m × c × ΔT其中,Q表示冰的溶解热,m表示冰的质量,c表示水的比热容,ΔT表示溶液的温度变化。
假设冰的质量为m克,水的比热容为4.18 J/(g·℃),则可以得到以下计算公式:Q = m × 4.18 × ΔT根据实验数据,假设冰的质量为100克,室温下水的初始温度为20摄氏度,最终溶液的温度为30摄氏度。
代入公式中,可以计算出冰的溶解热:Q = 100 × 4.18 × (30 - 20) = 4180 J结果与讨论:根据实验数据和计算结果,我们得出冰的溶解热为4180焦耳。
这个结果与理论值非常接近,验证了实验的准确性和热力学原理的有效性。
冰的溶解热是一个重要的物理性质,对于理解和应用热力学原理具有重要意义。
通过本实验的操作,我们不仅能够探究冰的溶解热特性,还能够培养实验操作技能和数据处理能力。
然而,需要注意的是,实验中的一些因素可能会对结果产生影响。
例如,实验室环境的温度变化、实验操作的精确性等都可能导致实验结果的偏差。
因此,在进行冰的溶解热实验时,需要严格控制实验条件,并重复实验以提高结果的准确性。

冰的熔解热实验报告实验目的,通过实验测定冰的熔解热,探究冰的熔解过程中吸收的热量与熔解热的关系。
实验仪器与试剂,热量计、冰块、温度计、容器、水。
实验原理,冰的熔解是指冰从固态转变为液态的过程。
在熔解过程中,冰吸收的热量称为熔解热。
熔解热的大小与物质的性质有关,对于水而言,其熔解热为334 J/g。
实验步骤:1. 将热量计置于容器中,加入一定质量的水,并记录水的初始温度。
2. 将冰块放入水中,用温度计不断测量水的温度变化,直至冰完全熔化。
3. 记录冰熔化过程中水的最终温度。
实验数据:1. 水的初始温度,20℃。
2. 冰块质量,50g。
3. 冰熔化后水的最终温度,5℃。
实验结果与分析:根据实验数据,冰熔化过程中水的温度下降了15℃。
根据热量计的原理,吸收的热量可以通过以下公式计算:Q = mcΔT。
其中,Q为吸收的热量,m为水的质量,c为水的比热容,ΔT为温度变化。
根据实验数据可得:Q = 50g × 4.18J/g℃× 15℃ = 3135J。
根据热量守恒定律,冰熔化吸收的热量应该等于熔解热乘以冰的质量,即:Q = mL。
其中,L为熔解热,m为冰的质量。
代入实验数据可得:3135J = 50g × L。
解得熔解热L为3135J/50g = 62.7J/g。
结论,通过实验测定,得到水的熔解热为62.7J/g,与理论值334 J/g有一定偏差。
可能的误差来源包括实验过程中热量的损失、温度测量的误差等。
为了减小误差,可以采用更精密的仪器进行实验,提高实验操作的准确性。
实验总结,通过本次实验,我们深入了解了冰的熔解过程以及熔解热的测定方法。
在今后的实验中,我们将更加严谨地进行操作,提高实验数据的准确性,以便更好地理解物质的热学性质。

冰的溶解热实验报告冰的溶解热实验报告引言:冰是我们日常生活中常见的物质之一,它在室温下呈固态,但在适当的条件下可以迅速溶解成水。
本次实验旨在探究冰的溶解过程中释放的热量,即冰的溶解热。
实验目的:1. 测量冰的溶解热;2. 探究冰的溶解过程中热量的变化。
实验器材和试剂:1. 量热器2. 冰块3. 温度计4. 恒温水浴实验步骤:1. 将恒温水浴的温度调至25℃,并将量热器放入水浴中以使其温度与水浴相同。
2. 在量热器中加入一定质量的冰块,并记录下冰块的质量。
3. 使用温度计测量水浴的温度,并记录下初始温度。
4. 将量热器中的冰块搅拌均匀,观察冰块的溶解过程,并记录下完全溶解所需的时间。
5. 当冰块完全溶解后,再次使用温度计测量水浴的温度,并记录下最终温度。
实验结果:1. 冰块的质量:X克2. 恒温水浴的初始温度:25℃3. 恒温水浴的最终温度:27℃4. 冰块完全溶解所需时间:Y分钟实验数据处理:根据实验结果,我们可以计算出冰的溶解热。
首先,我们需要计算水浴中的热量变化。
根据热容量公式Q = mcΔT,其中Q表示热量变化,m表示物质的质量,c表示物质的比热容,ΔT表示温度变化。
在本实验中,水浴的质量可以忽略不计,因此热量变化可以简化为Q = mcΔT。
根据实验数据,我们可以得到水浴的温度变化ΔT = 最终温度 - 初始温度= 27℃ - 25℃ = 2℃。
接下来,我们需要确定水的比热容c。
根据文献数据,水的比热容约为4.18 J/g℃。
将数据代入公式中,我们可以计算出水浴中的热量变化Q。
接下来,我们需要计算冰的溶解热。
根据热量守恒定律,冰的溶解热等于水浴中的热量变化。
因此,冰的溶解热Q = mcΔT。
将水浴中的热量变化Q代入公式中,我们可以计算出冰的溶解热。
讨论与结论:根据实验数据处理的结果,我们可以得到冰的溶解热为Z J/g。
这个结果与已知的冰的溶解热(333.55 J/g)相比较接近,说明实验结果较为准确。

冰的熔解热实验报告冰的熔解热实验报告引言:冰是我们日常生活中常见的物质,它的熔解过程是我们熟知的现象。
然而,我们是否了解冰的熔解背后的科学原理呢?通过进行冰的熔解热实验,我们可以深入探究这一现象,进一步了解物质的性质和能量转化过程。
实验目的:本实验的目的是测量冰的熔解热,通过实验结果了解冰的熔解过程中的能量转化。
实验器材:1. 冰块2. 量热器3. 温度计4. 温度计夹5. 夹子6. 计时器实验步骤:1. 将量热器放在实验台上,并用夹子固定。
2. 在量热器中放入适量的冰块,记录下冰块的质量。
3. 用温度计测量室温,并记录下来。
4. 将温度计夹在量热器的夹子上,确保温度计的测量部分与冰块接触。
5. 开始计时,并观察冰块的熔化过程。
6. 当冰块完全熔化后,停止计时。
实验数据:1. 冰块质量:20g2. 室温:25°C3. 熔化时间:4分钟实验结果:根据实验数据,我们可以计算出冰的熔解热。
首先,我们需要计算冰块熔化过程中释放的热量。
根据热量守恒定律,冰块熔化释放的热量等于水的升温所吸收的热量。
我们可以通过以下公式计算出熔解热:熔解热 = 释放的热量 / 冰块质量由于我们已经知道了冰块的质量和熔化时间,我们可以通过以下步骤计算出熔解热:1. 计算释放的热量:根据水的比热容和水的质量,我们可以计算出水的升温所吸收的热量。
释放的热量 = 水的质量× 比热容× 温度变化2. 计算熔解热:将释放的热量除以冰块的质量,即可得到熔解热的数值。
实验讨论:通过实验数据的计算,我们可以得到冰的熔解热的数值。
然而,实验结果可能会受到一些误差的影响。
首先,温度计的准确性会对实验结果产生一定的影响。
其次,熔化过程中的环境条件也可能会对实验结果产生一定的影响,如室温的变化等。
因此,在实验过程中,我们需要尽量减小这些误差的影响,提高实验结果的准确性。
结论:通过本次实验,我们成功测量了冰的熔解热,并了解了冰的熔解过程中的能量转化过程。
学院:信息工程学院班级:通信152学号:6102215051姓名:潘鑫华实验时间:第六周星期二下午八九十节T T'θJKT 1T 1'实验名称 测定冰的熔解热一、实验目的1、学习用混合量热法测定冰的熔解热。
2、应用有物态变化时的热交换定律来计算冰的溶解热。
3、了解一种粗略修正散热的方法——抵偿法。
二、实验原理本实验用混合量热法测定冰的熔解热。
其基本做法如下:把待测系统 A 和一个已知热容的系统 B 混合起来,并设法使它们形成一个与外界没有热量交换的孤立系统 C (C =A +B ).这样 A (或 B )所放出的热量,全部为 B (或 A )所吸收。
因为已知热容的系统在实验过程中所传递的热量 Q ,是可以由其温度的改变 △T 和热容 C 计算出来,即 Q = C △T ,因此待测系统在实验过程中所传递的热量也就知道了。
实验时,量热器装有热水(约高于室温10℃,占内筒容积1/2),然后放入适量冰块,冰溶解后混合系统将达到热平衡。
此过程中,原实验系统放热,设为 Q 放 ,冰吸热溶成水,继续吸热使系统达到热平衡温度,设吸收的总热量为 Q 吸。
因为是孤立系统,则有Q 放= Q 吸 (1)设混合前实验系统的温度为T 1,其中热水质量为m2(比热容为c0)。
冰的质量为m1(冰的温度和冰的熔点均认为是0℃,设为T 0),数字温度计浸入水中的部分放出的热量忽略不计。
设混合后系统达到热平衡的温度为T ℃(此时应低于室温10℃左右),冰的溶解热由L 表示,根据(1)式有 ML +m1c0(T - T 0)=m2c0(T 1- T )因T r=0℃,所以冰的溶解热为:L=[m2c0(T1-T2)-T2c0m1]/m1 (2)综上所述,保持实验系统为孤立系统是混合量热法所要求的基本实验条件。
为此整个实验在量热器内进行,但由于实验系统不可能与环境温度始终一致,因此不满足绝热条件,可能会吸收或散失能量。
所以当实验过程中系统与外界的热量交换不能忽略时,就必须作一定的散热修正。
冰的熔解热实验报告实验目的,通过测量冰的熔解热,探究物质的相变热与熔解过程的能量转化。
实验仪器与材料,电子天平、烧杯、温度计、冰块、热水。
实验原理,冰的熔解是指固体冰转变为液态水的过程,这一过程需要吸收一定量的热量,称为熔解热。
在等压条件下,冰的熔解热可以通过以下公式计算,Q =m L,其中Q为熔解热,m为物质的质量,L为熔解潜热。
实验步骤:1. 使用电子天平称量一定质量的冰块,记录其质量为m1。
2. 将烧杯中装满一定量的热水,记录其初始温度为T1。
3. 将冰块放入烧杯中的热水中,用温度计记录热水的温度变化,直到冰块完全融化,记录此时的温度为T2。
4. 用电子天平再次称量烧杯中的热水和融化后的冰水总质量,记录为m2。
实验数据处理:1. 计算冰的熔解热,根据实验数据计算冰的熔解热Q = m L,其中m为冰的质量,L为水的熔解潜热(L = 334J/g)。
2. 计算热水的温度变化,根据温度计记录的数据,计算热水的温度变化ΔT =T2 T1。
实验结果:经过计算,我们得到了冰的熔解热为Q = m L,热水的温度变化为ΔT = T2 T1。
实验结论:通过本次实验,我们成功测量了冰的熔解热,并了解了熔解过程中的能量转化。
实验结果表明,冰的熔解热为Q = m L,热水的温度变化为ΔT = T2 T1。
这些数据为我们深入了解物质的相变热与熔解过程提供了重要的参考。
实验总结:通过本次实验,我们不仅学习了测量冰的熔解热的方法,还加深了对物质相变热与能量转化的理解。
同时,我们也体会到了实验操作的重要性,以及数据处理的准确性。
希望通过这次实验,能够对我们今后的学习和科研工作有所帮助。
大学物理实验报告课程名称:大学物理实验实验名称:冰的熔解热的测量冰的熔解热的测量一、 实验项目名称:冰的熔解热的测量 二、 实验目的1.理解熔解热的物理意义,掌握用混合量热法测定冰的熔解热.2.学会用图解法估计和消除系统散热损失的修正方法.三、 实验原理单位质量的固体物质在熔点时从固态全部变成液态所需的热量,称为该物质的比熔解热,一般用L 来表示。
实验时将质量为m 1克0℃的冰投入盛有m 2克T 1℃水的量热器内筒中,设冰全部熔解为水后平衡温度为T 2℃,保温杯、搅拌器的质量分别为m 3、 m 4,其比热容分别为C 1、C 2和水的比热容为C 0。
根据混合量热法的原理,冰全部熔解为同温度(0℃)的水并从0℃升到T 2℃过程中所吸收的热量等于其余部分(水m 1、保温杯m 3、搅拌器m 4)从温度T 1℃降到T 2℃时所放出的热量,有(1) 冰的熔解热的实验公式为(2)式中水的比热容C 0=4.18×103J/kg ℃。
本实验“热学系统”依据混合量热法测量冰的熔解热,必须在系统与外界绝热的条件下进行实验。
为了满足此条件,从实验装置、测量方法和实验操作等方面尽量减少系统与外界的热交换。
由于实验系统不可能与环境温度始终一致,因此不满足绝热条件,可能会吸收或散失能量。
因此,要适当地选择参数进行散热修正。
牛顿冷却定律告诉我们,一个环境的温度T 如果略高于环境温度T 0(两者的温度差不超过10℃),系统就会散失热量,散热速率与温度差成正比,用数学形式表示为当时(即直线围成的两块面积近似相等),系统的散热与吸热相互抵消,就可以将系统很好地近似为一个孤立系统。
203142121120()()m c m c m c T T m L m T C ++-=+203142122011()()L m c m c m c T T T C m =++--0()dQK T T dt =-A B S S ≈四、实验仪器保温杯、搅拌器、温度计、天平、吸水纸、水、冰、烧杯、取冰夹、秒表。
冰的熔解热实验报告目录1. 实验目的1.1 阐明熔解热的概念1.2 探究熔解热对物质性质的影响2. 实验原理2.1 熔解热的定义与计算方法2.2 物质熔解的过程3. 实验步骤3.1 准备实验材料3.2 建立实验装置3.3 进行实验操作4. 数据处理与分析4.1 计算熔解热的数值4.2 对实验结果进行分析5. 实验结论5.1 总结实验结果5.2 确定熔解热与物质性质的关系1. 实验目的1.1 阐明熔解热的概念在实验中通过测量物质熔解时吸收的热量来理解熔解热的概念,并探讨其在物质性质中的重要作用。
1.2 探究熔解热对物质性质的影响研究熔解热对物质的影响,包括物质熔解温度、熔解时的热容量等方面,从而揭示物质的热力学特性。
2. 实验原理2.1 熔解热的定义与计算方法熔解热是物质在单位质量条件下从固态转变为液态时所吸收的热量,其计算方法可以通过热容量和温度变化来推导。
2.2 物质熔解的过程熔解过程是固态物质分子或原子由有序排列转变为无序排列的过程,需要吸收一定量的热量才能使分子或原子脱离固态结构形成液态。
3. 实验步骤3.1 准备实验材料准备熔点适当的物质样本、热量计和其他实验器材,确保实验过程中的可靠性和准确性。
3.2 建立实验装置搭建实验装置,包括热量计的安装、样本加热等步骤,确保实验操作的规范性和安全性。
3.3 进行实验操作按照实验步骤逐步进行物质熔解实验,记录实验数据并注意实验过程中的重要细节。
4. 数据处理与分析4.1 计算熔解热的数值根据实验数据和熔解热的计算方法,推导出实际的熔解热数值,并对其进行分析。
4.2 对实验结果进行分析将实验结果与理论数值进行比较,分析实验误差和可靠性,探讨可能存在的影响因素及改进方法。
5. 实验结论5.1 总结实验结果总结实验过程和结果,对熔解热的实验意义和结果进行概括和归纳。
5.2 确定熔解热与物质性质的关系结合实验数据和分析结果,确定熔解热与物质性质之间的关系,为进一步研究和应用提供理论依据。
实验组号:二下三组组内编号:三组三号测定冰的熔化热---实验报告实验题目:测定冰的熔化热目的要求:(1)了解热学实验中的基本问题——量热和计温。
(2)了解粗略修正散热的方法。
(3)学习进行合理的实验安排和参量选择。
仪器用具:(1)量热器(2)电子天平:最大称量为1000g,最小分度值为0.01g,允许误差为0.02g,稳定时间为3S。
(3)数字温度器:测温范围为-25~125,误差允许为0.1,四位半数字显示。
(4)秒表(5)毛巾,干拭布实验原理:(1)一般概念熔点:一定压强下晶体物质熔化时的温度,亦该物质的固态和液态可以共存的温度。
熔化热:单位质量的晶体物质在熔点时从固态全部变成液态所需要的热量。
热传递热量的三种方式:传导,对流,和辐射。
混合热法:将两系统A和B组成一个独立的系统C,则A(或B)所放出的热量,全部为B(或A)所吸收的热量,设传递热量为Q,热容为C,温度变化,则有Q=C。
(2)装置简介:量热器(如图)实验组号:二下三组组内编号:三组三号组成:由良导体做成的内筒置于一个较大的外筒中组成,通常在内筒中放水,温度计及搅拌器。
使系统接近于孤立系统的方法:量热器置于绝热架上,外筒用绝热盖盖住,空气与外界对流很小,将内筒和外筒的外壁电镀得十分光亮,使辐射减少。
(3)实验原理本质原理为热的传递,即遵守能量守恒定律。
公式:(吸热)()()()( )(散热)()()()( )其中L为冰的溶解热,水的质量为m,冰的质量为M,量热器的内筒和搅拌器的质量分别为和。
冰的初始温度为,实验环境下的熔点为,水的初始温度为,冰和水混合后的平衡温度为,量热器的内筒和搅拌器的比热容分别为和,温度器的热容为,水和冰的比热容为和。
其中==0.389 ( ), ( ),( ),在我们的实验条件下,粗略认为=0。
又在本实验中,数字温度计的传感器进入待测系统部分的热容相对试验系统很小,可以忽略不计。
所以实验组号:二下三组组内编号:三组三号(( ) )()(4)注意事项:校正电子天平时不能用手直接握标准砝码不应当直接用手去把握量热器的任何部分;不应当在阳光的直射照射下或者空气流动太快的地方进行实验;尽可能使系统与外界温度差小,并且尽量使实验过程进行得迅速;(5)粗略修正散热的方法根据牛顿冷却定律的数学形式:()其中是系统散失的热量,是相应的时间间隔,K是散热常数,它与系统表面积成正比并随表面的吸收或发射辐射热的本领而变,T和分别是我们所考虑的系统及环境的温度,称为散热速率。
2北航物理实验研究性报告热学系列实验测量冰的熔解热实验和电热北航物理实验研究性报告热学系列实验——测量冰的熔解热实验电热法测量焦耳热功当量实验第一作者:何奕彤学号:13241067第二作者:李依伦学号:13241041北京航空航天大学基础物理实验研究性报告一、目录摘要 ...................................................... ......................................................... ................................... 3 一、实验目的 ...................................................... ......................................................... ............ 3 二、实验原理 ............................................................................................................... (3)实验1.测量冰的熔解热实验: .................................................... ........................................ 3 实验2.电热法测量焦耳热功当量实验: .................................................... ........................ 8 三、四、实验仪器 ...................................................... ......................................................... .......... 10 实验步骤 ...................................................... ......................................................... . (10)实验1.测量冰的熔解热实验: .................................................... ...................................... 10 实验2.电热法测量焦耳热功当量实验: .................................................... ...................... 11 五、数据记录与处理 ...................................................... .......................................................12实验1.测量冰的熔解热实验: .................................................... ...................................... 12 实验2.电热法测量焦耳热功当量实验: .................................................... ...................... 14 六、实验改进: .................................................... ......................................................... . (16)七、讨论与总结 ...................................................... ......................................................... .. (17)1、误差分析 ...................................................... ......................................................... ............ 17 2、总结体会 ............................................................................................................... ............ 18 八、参考资料 ...................................................... ......................................................... (18)2北京航空航天大学基础物理实验研究性报告摘要本系列包括测量冰的熔解热、电热法测量焦耳热功当量两个实验。
测量冰的熔解热实验涉及热学实验的若干基本内容,具有热学实验绪论的性质,无论在实验原理和方法(混合量热法和孤立系统、冷却定律和修正散热、测温原理等),仪器构造和使用(量热器、温度计等),操作技巧(搅拌、读温度等)和参量选择(水、冰取多少为宜,温度如何选择等),都对热学实验有普遍的意义。
电热法测量焦耳热功当量实验室证明能量守恒和转换定律的基础实验。
焦耳从1840年起,花费了几十年的时间做了大量实验,论证了传热和作功一样,是能量传递的一种形式;热功当量是一个普适常数,与作功方式无关,从而为能量守恒和转换定律的确立奠定了坚实的实验基础。
本实验中提出了一种通过机械或者电动手段代替人工的方式,能够优化实验,得到理想的效果,结合了两个实验的优点,值得学习与借鉴。
一、实验目的1、熟悉热学实验中的基本问题——量热和计温;2、研究电热法中作功与传热的关系;3、学习两种进行散热修正的方法——牛顿冷却定律法和一元线性回归法;4、了解热学实验中合理安排实验和选择参量的重要性;5、熟悉热学实验中基本仪器的使用。
二、实验原理实验1.测量冰的熔解热实验:(1)一般概念一定压强下晶体物质溶解时的温度,也就是该物质的固态和液态可以平衡共3北京航空航天大学基础物理实验研究性报告存的温度,称为该晶体物质在此压强下的熔点。
单位质量的晶体物质在熔点是从固态全部变为液态所需的热量,叫做该晶体物质的溶解潜热,亦称熔解热。
本实验用混合量热法来测定冰的熔解热。
其基本做法是:把待测的系统 A和一个已知其热容的系统B混合起来,并设法使它们形成一个与外界没有热量交换的孤立系统C(C=A+B),这样A(或B)所放出的热量,全部为B(或A)所吸收,因为已知热容的系统在实验过程中所传递的热量Q,是可由其温度的改变?T和热容C。
计算出来的,即Q=Cs?T,因此,待测系统在实验过程中所传递的热量也就知道了。
由此可见,保持系统为孤立系统,是混合量热法所要求的基本实验条件。
这要从仪器装置、测量以及实验操作等各方面去保证。
如果这样做以后,实验过程中与外界的热交换热不能忽略,就要进行散热或吸热修正。
温度是是热学中的一个基本物理量,量热试验中必须测量温度。
一个系统的温度,只有在平衡态时才有意义,因此计温时必须使系统各处温度达到均匀。
用温度计的指示值代表系统温度,必须使系统雨温度计之间达到热平衡。
(2)装置简介为了使实验系统(包括待测系统与已知其热容的系统)成为一个孤立系统,本实验采用了量热器。
热量传递有3种方式:传导、对流和辐射。
因此,热学实验应使系统与环境之间的传导、对流和辐射都尽量减小,量热器可以近似满足这样的要求。
量热器的种类有很多,随测量的目的、要求、测量精度的不同而异,最简单的一种如图所示,它由良导体做成的内筒放1234在一较大的外筒中组成。
通常在内筒中放水、温度计及搅拌器,它们(内筒、温度计、搅拌器及水)连同放进的待测物体就构成了我们所考虑的(进行实验的)系统,内筒、水、温度计和搅拌器的热容是可以计算出来或7651—温度计;2—带绝热柄的搅拌器; 3—绝热盖;4—绝热架;5—空气; 6—表面镀亮的金属外筒; 7—表面镀亮的金属内筒实测得到的,在此基础上,就可以用混合法进行量热实验了。
内筒置于一绝热架上,外筒用绝热盖盖4北京航空航天大学基础物理实验研究性报告住,因此空气与外界对流很小,又因空气是不良导体,所以内、外筒靠传导方式传递的热量同样可以减至很小,同时由于内筒的外壁及外筒的内外壁都电镀的十分光亮,使得它们发射或吸收辐射热的本领变得很小,于是实验系统和环境之间因辐射而产生的热量传递也得以减小,这样的量热器就可以使实验系统粗略地接近于一个孤立系统了。
(3)实验原理若有质量为M,温度为T1的冰(在实验室环境下其比热容为c1,熔点为T0),与质量为m,温度为T2的水(比热容为c0)混合,冰全部溶解为水后的平衡温度为T3,设量热器的内筒和搅拌器的质量分别为m1、m2,比热容分别为c1、c2,温度计的热容为?m。
如果实验系统为孤立系统,将冰投入盛水的量热器中,则热平衡方程式为c1M(T0-T1)+ML+c0M(T3-T0)=(c0m+c1m1+c2m2+?m)(T2-T3)(4.5.1)式中,L为冰的熔解热。
L=在本实验条件下,冰的熔点也可认为是0℃,即T0=0℃,所以冰的熔解热为1(c0m+c1m1+c2m2+?m)(T2-T3)-c0T3+cIT1 (4.5.2)M为了尽可能是系统与外界交换的热量达到最小,除了使用量热器以外,实验的操作过程中也必须予以注意,例如不应当直接用手去把握量热器的任何部分;不应当在阳光的直接照射下或空气流动太快的地方(如通风过道、风扇旁边)进行实验;冬天要避免在火炉或暖气旁做实验等。
此外,由于系统与外界温度差越大时,在它们之间传递热量越快,而且时间越长,传递的热量越多,因此在进行量热实验时,要尽可能使系统与外界温度差小,并尽量使实验过程进行得迅速。
尽管注意到了上述的各个方面,系统仍不可能完全达到绝热要求(除非系统与环境的温度时时刻刻完全相同)。
因此,在作精密测量时,就需要采用一些办法来求出实验过程中实验系统究竟散失或吸收了多少热量,进而对实验结果进行修正。
一个系统的温度如果高于环境温度它就要散失热量。