2016年初三化学溶解度曲线知识点与习题
- 格式:doc
- 大小:763.00 KB
- 文档页数:6

初三化学中考专题(5)溶解度曲线练习及答案1.a、b两种物质的溶解度曲线如图所示。
下列说法不正确的是A.将t1℃时b的饱和溶液加水可变为不饱和溶液B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变C.t2℃时,两种物质的饱和溶液中溶质质量分数a>bD.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等2.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.t2℃时,甲、乙两种物质的溶解度相等B.甲的溶解度随温度的升高而增大C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t1℃时,丙的饱和溶液中溶质的质量分数为40%3.下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t2℃时的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系正确的是A.甲>乙>丙B.甲=乙=丙C.甲=乙>丙D.丙>甲=乙4.(多选)甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是A.t1℃时,甲物质的溶解度为20gB.t1℃时,30g甲加入到50g水中最多可得70g溶液C.t2℃时,乙物质的饱和溶液升温变成不饱和溶液D.t2℃时,甲乙两物质的饱和溶液分别降温到t1℃时,所得溶液溶质质量分数的大小关系是:甲<乙5.(多选)甲、乙两种固体物质的溶解度曲线如图所示。
20℃时,进行了如下图所示的实验,下列叙述正确的是A.甲的溶解度大于乙的溶解度B.实验过程中,属于不饱和溶液的是A溶液和C溶液C.实验过程中,只有B溶液和D溶液属于饱和溶液D.实验过程中,B溶液与E溶液中溶质的质量分数相同6.(多选)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少C.分别将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关系是乙>甲>丙D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多丙溶液中无晶体析出7.甲、乙、丙三种物质的溶解度曲线如下图所示。

初三化学溶解度曲线习题(含答案)和溶液,将它们混合并搅拌均匀,会发生下列哪种情况()A.溶液变成淡黄色B.溶液变成白色浑浊C.溶液变成淡红色D.没有任何变化10.下列说法正确的是()A.溶液的浓度与溶剂的质量无关B.溶解固体的溶解度随温度升高而升高C.溶解气体的溶解度随温度升高而降低D.溶解气体的溶解度随压力升高而升高11.下列说法正确的是()A.溶液的沸点与溶质的种类有关,与溶液浓度无关B.溶液的沸点与溶液浓度有关,与溶质的种类无关C.溶液的沸点与溶液浓度和溶质的种类都有关D.溶液的沸点与溶液浓度和溶质的种类都无关12.下列说法正确的是()A.溶解固体时,固体的溶解度随温度升高而升高B.溶解气体时,气体的溶解度随温度升高而升高C.固体的溶解度随溶剂温度升高而降低D.气体的溶解度随溶剂温度升高而降低13.下列说法正确的是()A.溶解固体时,固体的溶解度随压力升高而升高B.溶解气体时,气体的溶解度随压力升高而升高C.固体的溶解度随溶剂压力升高而降低D.气体的溶解度随溶剂压力升高而降低14.下列说法正确的是()A.在相同条件下,饱和溶液的溶质质量分数与溶液浓度相等B.在相同条件下,饱和溶液的溶质质量分数与溶液浓度无关C.在相同条件下,饱和溶液的溶质质量分数随溶液浓度升高而升高D.在相同条件下,饱和溶液的溶质质量分数随溶液浓度升高而降低15.下列说法正确的是()A.溶质在溶液中的质量分数越大,溶液的浓度越低B.溶质在溶液中的质量分数越小,溶液的浓度越低C.溶质在溶液中的质量分数越大,溶液的浓度越高D.溶质在溶液中的质量分数越小,溶液的浓度越高16.下列说法正确的是()A.溶解固体时,固体的溶解度随溶剂温度升高而升高B.溶解气体时,气体的溶解度随溶剂温度升高而升高C.固体的溶解度随溶剂压力升高而升高D.气体的溶解度随溶剂压力升高而升高1.下列选项中,对于“10%的食盐溶液”的解释错误的是()。
A。
在100g食盐溶液中溶解了10g食盐B。

化学溶解度曲线专题例题:A 、B 、C 三种物质的溶解度曲线如图所示:判断下列说法是正确的打“√”错误的打“×”。
1、B 的溶解度小于A 的溶解度。
( )2、t 3℃时,将A 、B 的饱和溶液都蒸发掉10克水,A 析出的晶体质量大。
( )3、通过降低温度可使C 的不饱和溶液变为饱和溶液。
( )4、A 物质的饱和溶液从t 2℃降温到t 1℃时变为不饱和溶液。
( )5、t 2℃时A 、B 两溶液的溶质质量分数相等。
( )6、t 2℃时A 、B 两饱和溶液的溶质质量分数相等。
( )7、t 2℃时A 、B 两饱和溶液分别含A 、B 两物质的质量相等。
(即溶质质量相等)。
( )8、降低温度可使接近饱和的B 溶液变成饱和溶液。
( )9、t 3℃时,A 的饱和溶液的溶质质量分数为a% ( )10、采用降低温度、增加溶质、蒸发溶剂都可使C 的不饱和溶液变为饱和溶液。
( )11、对A 物质的M 点溶液降温至t 2℃时,其溶质质量分数增大。
( )12、t 3℃时,N 点表示A 、B 两物质的不饱和溶液,表示C 物质的饱和溶液。
( )13、t 2℃时B ,C 两物质的饱和溶液降温到t 1℃时都会析出晶体。
( )14、A 物质的溶液分别处于M 、Q 、P 、N 四点时,溶液中A 的质量分数大小关系是M>Q>P=N 。
( )M NP15、把t 1℃时A 、C 两饱和溶液升温到t 2℃时,两溶液仍都为饱和溶液。
( )16、t 2℃时A 的饱和溶液降温到t 1℃时,溶液变稀了。
( )17、把t 1℃时C 的饱和溶液升温到t 2℃时,溶质质量分数不变。
( )18、把t 1℃时A 的饱和溶液升温到t 2℃时,溶质质量分数不变。
( )19、把t 2℃时C 的饱和溶液降温到t 1℃时,溶质质量分数不变。
( )20、把t 2℃时A 的饱和溶液降温到t 1℃时,溶质质量分数不变。
( )21、用降温结晶的方法可除去混在A 中的C 物质。


A B C0 t 1 20 t 2 温度/℃ g 40溶解度全国中考化学汇编之溶解度曲线1.右图是a 、b 两种固体物质(不含结晶水)的溶解度曲线。
下列说法正确的是 A.b 的溶解度大于a 的溶解度B.t 1℃时,将a 、b 两种物质的饱和溶液分别恒温蒸发 等质量的水,析出晶体的质量一定相等C.将t 2℃时的b 的不饱和溶液降温至t 1℃, 一定能得到b 的饱和溶液D.t 2℃时,a 溶液的溶质质量分数一定小于 b 溶液的溶质质量分数2.右图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题: (1)t 1℃时,甲物质的溶解度 乙物质的溶解 度(填“>”、“=”或“<”)。
(2)甲、乙两种物质的溶解度受温度影响较小的是 物质。
(3)t 2℃时,把100g 乙物质放入100g 水中,充分搅拌, 所得溶液是 溶液(填“饱和”或“不饱和”)。
(4)t 2℃时,有一接近饱和的甲溶液,可采用 的方法(任写一种)使它变为饱和溶液。
3.右图是甲、乙两种物质的溶解度曲线,下列说法正确的是 A .甲的溶解度受温度影响比乙小 B .15℃时甲、乙的溶解度相等C .30℃时乙的溶解度为30gD .升高温度可使接近饱和....的甲溶液变为饱和.. 4.请根据图7中A 、B 两种固体物质的溶解度曲线,回答下列问题。
(l)在____℃时,A 、B 两种物质溶解度相同。
(2) t 2℃时,100g 水中溶解_ gA 物质恰好达到饱和,该饱和溶液中溶质的质量分数为_ ___,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水 g 。
(3)将t 2℃时A 、B 两种物质的饱和溶液降温至t 1℃(其它条件不变),溶质的质量分数保持不变的是___ _。
5.(5分) 右图为A 、B 、C 三种物质的溶解度曲线,据图回答: ⑴ t 20C 时,A 、B 、C 三种物质的溶解度由大到小顺序是 ______。
⑵ 将t 20C 时三种物质等质量的饱和溶液分别降温到00C 时,析出溶质最多的是 ___ ,无溶质析出的是 __ 。


初三化学溶解度曲线知识点天高鸟飞,海阔鱼跃;考试这舞台,秀出你特殊的杰出;一宿好的睡眠,精神能百倍;一颗淡定的平常心,冷静应对,努力备考,考入理想院校!下面是作者给大家带来的初三化学溶解度曲线知识点,欢迎大家浏览参考,我们一起来看看吧!初三化学溶解度曲线知识点一、溶解度曲线图上的点1、溶解度曲线上的点:表示在该点所示温度下某物质的溶解度。
如A点表示当温度为t2时,物质R的溶解度为ag。
2、两条曲线的交点:表示在该点所示温度下,两种物质的溶解度相同。
如B点表示当温度为t1时,物质R和N的溶解度相等,都为bg。
二、溶解度曲线图上的线每一条曲线都表示这种物质的溶解度随温度变化而变化的总趋势,主要有:1、陡升型:绝大多数固体物质的溶解度随温度的升高而增大,曲线峻峭。
如曲线R,代表物质有KNO3、NH4NO3等。
2、缓升型:少数固体物质的溶解度受温度的影响较小。
如曲线M,代表物质有NaCl。
3、降落型:极少数固体物质的溶解度随温度的升高而减小。
如曲线N,代表物质有Ca(OH)2。
三、溶解度曲线图上的面1、在溶解度曲线上方平面上的任何点:表示在该点所示温度下形成了含有部分固体溶质的饱和溶液,即依照该点所示温度和溶质质量,在100g溶剂中配制得到的溶液是饱和溶液,且还有未溶解完的溶质存在。
如C点。
2、在溶解度曲线下方平面上的任何点:表示在该点所示温度下形成了不饱和溶液,即依照该点所示温度和溶质质量,在100g溶剂中配制得到的溶液是不饱和溶液。
如D点。
四、溶解度曲线图的综合运用1、溶解度曲线上的每一点都代表着对应温度下该物质的溶解度,所以利用溶解度曲线可以查找出某种物质在不同温度时的溶解度。
2、根据溶解度曲线的走向,可以判定或比较各物质的溶解度随温度变化的趋势。
3、可以比较在同一温度下不同物质的溶解度大小。
如在t3时,R、M、N三种物质的溶解度由小到大的顺序为N M R。
初三化学,溶解度曲线解题技能溶解度曲线题型可从点、线、面和交点四个方面进行解答:1.溶解度曲线上的点:溶解度曲线上的每一个点都是表示的是某温度下某种物质的溶解度。


小专题(一) 溶解度及溶解度曲线1.溶解度固体溶解度定义一定温度下,某固态物质在100 g溶剂里达到饱和状态时所溶解的质量影响因素内因:溶质和溶剂的性质外因:温度类型①大多数物质的溶解度随温度的升高而增大(如KNO3)②少数物质的溶解度受温度的影响不大③极少数物质的溶解度随温度的升高而减小气体溶解度,与温度、压强关系,温度升高,溶解度减小;气压增大,溶解度增大影响因素,内因:溶质和溶剂的性质外因:温度和压强 2.溶解度曲线的意义(1)溶解度曲线上的点:①表示固体物质在该温度下的溶解度,如图,P点表示t1℃时A的溶解度为a1g。
②两条曲线的交点:表示该温度下两种物质的溶解度相等或该温度下两种物质饱和溶液的质量分数相等。
如图,Q点表示t2℃时A、B的溶解度相等。
(2)溶解度曲线:①表示物质的溶解度随温度的变化趋势,如图:A、B的曲线表示A和B物质的溶解度随温度的升高而增大,C的曲线表示C物质的溶解度随温度的升高而减小。
②曲线的倾斜程度:表示物质的溶解度受温度的影响程度,如图A,倾斜程度大,表示A物质的溶解度受温度的影响大;B物质的倾斜程度小,表示B物质的溶解度受温度的影响小。
(3)溶解度曲线的上面和下面:①溶解度曲线上面区域内所有的点:表示该温度下,物质形成的溶液是饱和溶液,且有未溶解的溶质存在。
②溶解度曲线下面区域内所有的点:表示该温度下,物质形成的溶液是不饱和溶液。
考点一溶解度【例1】食盐的溶解度为36 g,这句话最主要的错误是( )A.未指明在100 g水中B.未指明达到饱和C.未指明温度D.未指明36 g为最大克数【解析】溶解度四要素:①一定温度;②100 g溶剂;③达到饱和;④溶质的质量。
溶解度是指100 g水中溶解某溶质达到饱和状态,溶质的质量随温度而变,即主要的错误是没有指明温度,故选C。
【答案】C【例2】(2015石家庄中考模拟)一木块漂浮于50 ℃时的KNO3饱和溶液中(见图A),当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积(V排)随时间(t)发生了如图B所示的变化。
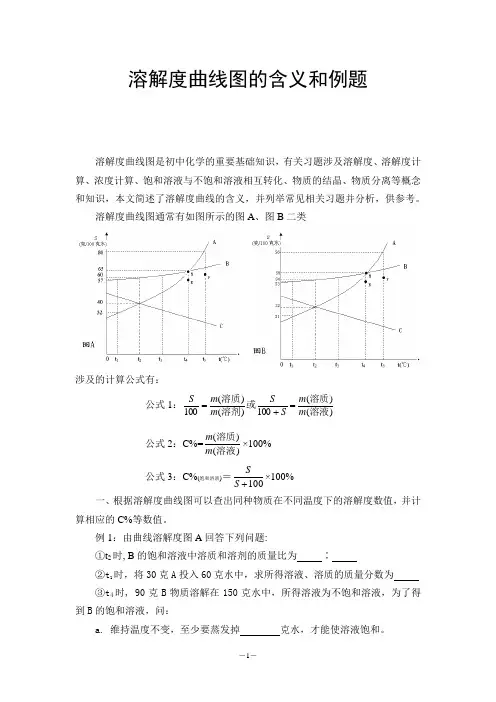
溶解度曲线图的含义和例题溶解度曲线图是初中化学的重要基础知识,有关习题涉及溶解度、溶解度计算、浓度计算、饱和溶液与不饱和溶液相互转化、物质的结晶、物质分离等概念和知识,本文简述了溶解度曲线的含义,并列举常见相关习题并分析,供参考。
溶解度曲线图通常有如图所示的图A、图B二类涉及的计算公式有:公式1:)()(100)()(100溶液溶质或溶剂溶质mmSSmmS=+=公式2:C%=)()(溶液溶质mm×100%公式3:C%(饱和溶液)=100+SS×100%一、根据溶解度曲线图可以查出同种物质在不同温度下的溶解度数值,并计算相应的C%等数值。
例1:由曲线溶解度图A回答下列问题:①t2时, B的饱和溶液中溶质和溶剂的质量比为∶②t1时,将30克A投入60克水中,求所得溶液、溶质的质量分数为③t4时, 90克B物质溶解在150克水中,所得溶液为不饱和溶液,为了得到B的饱和溶液,问:a. 维持温度不变,至少要蒸发掉克水,才能使溶液饱和。
b. 维持温度不变,原溶液中至少再加入B 克,才能使溶液饱和。
c.不改变溶液组成,只要把温度降低到 ℃,也能使溶液恰好达到 饱和。
④要配制C%为28.6%的C 物质溶液,配制时的温度应控制在 ℃。
解:①由图A 知t 2时,S B =60克∕100克水,由公式1,则溶质和溶剂的质量比为60∶100②由图A 知t 1时,S A =32克∕100克水,根据公式可知在60克水中最多溶解19.2克A 物质,则C%=602.192.19+×100%=24.2% ③a :已知t 4时,S B =65克∕100克水,根据公式1,x 9010065= x =138克, 则150-138=12克,即蒸发12克水可使溶液饱和。
b :同理15010065y = y =97.5 97.5-90=7.5,即加入7.5克B 物质可使溶液饱和。
c :同理,根据公式1,15090100=S S =60克∕100克水,即把温度降低 到t 2时,溶液恰好饱和。
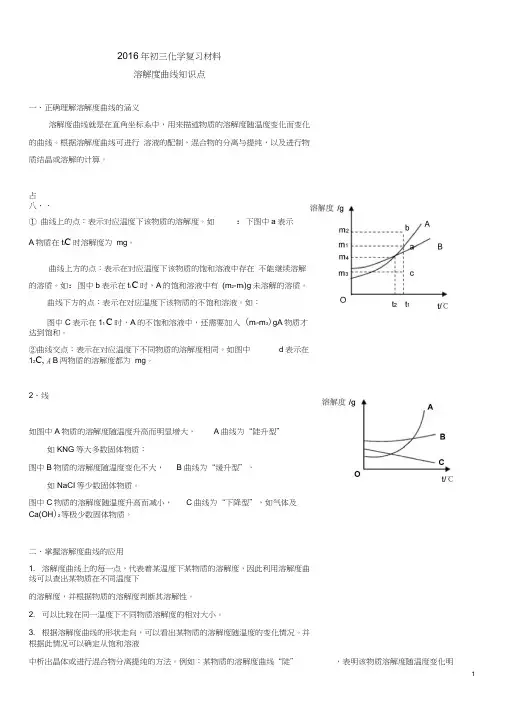
2016年初三化学复习材料溶解度曲线知识点一、正确理解溶解度曲线的涵义溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。
占八、、① 曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a表示A物质在t i C时溶解度为mg。
曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。
如:图中b表示在t i C时,A的饱和溶液中有(m2-m i)g未溶解的溶质。
曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中C表示在11 C时,A的不饱和溶液中,还需要加入(m i-m3)gA物质才达到饱和。
②曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d表示在12C, A B两物质的溶解度都为mg。
2、线如图中A物质的溶解度随温度升高而明显增大,A曲线为“陡升型”如KNG等大多数固体物质:图中B物质的溶解度随温度变化不大,B曲线为“缓升型”,如NaCI等少数固体物质。
图中C物质的溶解度随温度升高而减小,C曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
二、掌握溶解度曲线的应用1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2. 可以比较在同一温度下不同物质溶解度的相对大小。
3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。
例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。
某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。
4. 从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。
5. 利用溶解度曲线可以确定一定质量的某物质的饱和溶液降温时析出晶体的质量。
一、有关溶解度曲线的题1、溶解度曲线知识(1)、比较不同温度时溶解度的大小。
在t 1℃时,三种物质的溶解度的大小顺序是 。
(2)、图中M 点表示的意义是 。
(3)、温度因素对溶解度的影响A 。
B 。
C 。
(4)、不饱和溶液变饱和溶液的方法A , , 。
B , 。
C , , 。
(5)、饱和溶液变不饱和溶液的方法A , 。
B , 。
C , 。
(6)、A 物质中含有少量B 物质提纯的方法是 。
B 物质中含有少量A 物质提纯的方法是 。
(7)、溶解度曲线上的点表示 ,溶解度曲线以上的点表示 ,溶解度曲线以下的点表示 。
2、规律知识总结(1)溶解度曲线题解答要点:①温度②物质③溶解度 (2)两溶液中溶质质量分数和溶质质量的大小比较 ①同种溶质A 同温→饱和比不饱和的 大B 同温、等量溶液→饱和比不饱和含的 多。
②不同溶质A 同温、饱和→溶解度大的物质 大B 同温、饱和、等量溶液→溶解度大的物质含的 多。
(3)溶解度曲线X 穿越溶解度曲线Y 的条件:①低温t 1℃,S x <S y (比小的小)②高温t 3℃,S x >S y (比大的大) (4)曲线中溶质质量分数大小比较(平移法)①t 3℃甲、乙、丙三种物质饱和溶液降温到t 1℃时,三种物质溶质质量分数的大小顺序是 。
②t 3℃等质量的甲、乙、丙三种物质饱和溶液降温到t 1℃时,三种溶液所含溶质质量的大小顺序是 。
二、河北中考试题1、(2006河北中考)如图是a 、b 、c 三种固体物质的溶解度曲线,下列说法不正确的是( )A.t 2℃时a 的溶解度等于b 的溶解度B. t 1℃时a 、c 饱和溶液的溶质质量分数相同C.c 的饱和溶液由t 1℃升温至t 2℃时,变成不饱和溶液D.当a 中含有少量b 时,可以采用降温的方法提纯a2、(2007河北中考)图1是a 、b 两种物质的溶解度曲线。
室温时,将盛有a 、b 饱和溶液的试管分别放入烧杯内的水中,均无晶体析出。
初三化学中考专题 (5) 溶解度曲线练习及答案1.a 、b 两种物质的溶解度曲线以下图。
以下说法不正确的选项是A. 将 t 1℃时 b 的饱和溶液加水可变为不饱和溶液B. 将 t 2℃时 a 的饱和溶液降温至t 1℃,溶液质量不变C.t 2℃时,两种物质的饱和溶液中溶质质量分数a>bD.将 t 2℃时 a、 b 的饱和溶液分别降温至t 1℃,两溶液的溶质质量分数相等2.以下图是甲、乙、丙三种固体物质的溶解度曲线,以下说法错误的选项是A.t 2℃时,甲、乙两种物质的溶解度相等B.甲的溶解度随温度的高升而增大C. 分别将 t 3℃时甲、乙、丙的饱和溶液降温至 t 1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t 1℃时,丙的饱和溶液中溶质的质量分数为40%3. 以下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t 2℃时的饱和溶液降温至t 1℃,所得溶液的溶质质量分数关系正确的选项是A. 甲>乙>丙B.甲=乙=丙C.甲 =乙>丙D.丙>甲=乙4.(多项选择)甲、乙两固体物质的溶解度曲线以下图,以下说法正确的选项是A.t 1℃时,甲物质的溶解度为20gB.t 1℃时, 30g 甲加入到50g 水中最多可得70g 溶液C.t 2℃时,乙物质的饱和溶液升温变为不饱和溶液D.t 2℃时,甲乙两物质的饱和溶液分别降温到t 1℃时,所得溶液溶质质量分数的大小关系是:甲<乙5. (多项选择)甲、乙两种固体物质的溶解度曲线以下图。
20℃时,进行了以以下图所示的实验,以下表达正确的选项是A.甲的溶解度大于乙的溶解度B.实验过程中,属于不饱和溶液的是A 溶液和 C 溶液C.实验过程中,只有 B 溶液和 D溶液属于饱和溶液D.实验过程中, B 溶液与 E 溶液中溶质的质量分数同样6.(多项选择)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线以下图,以下说法中正确的选项是A.t 2℃时将 50g 甲物质放入 50g 水中,充足搅拌后获得 100g 甲溶液B.t 2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少C. 分别将t 2℃时三种物质的饱和溶液降温到t 1℃,所得溶液中溶质的质量分数的大小关系是乙>甲>丙D. 分别将 t 2℃时三种物质的饱和溶液降温到t 1℃,甲溶液中析出的晶体最多丙溶液中无晶体析出7.甲、乙、丙三种物质的溶解度曲线以以下图所示。
一题了解溶解度曲线如下图是甲、乙、丙三种固体在水中的溶解度曲线,回答下列问题。
1.曲线类型:甲:;乙:;丙:(填“陡升型”、“平缓型”或“下降型”)2.甲t2时溶解度是;含义是或3.n点含义是或4.t2时,甲乙丙溶解度大小关系是;t1时,甲乙丙溶解度大小关系是5.t2时,甲的饱和溶液溶质的质量分数是6.t2时,60g甲加入50g水中,溶质质量: g;溶液质量:g;溶质的质量分数:7.t2时,60g甲加入50g水中,降温到t1,析出晶体: g;溶质质量:;溶质质量分数:8.t2时,在各含100gH2O的烧杯中溶解甲乙丙恰好达到饱和状态:★★①溶质的质量大小关系:②溶液的质量大小关系:③溶质的质量分数大小关系:④结论是:9.t2时,等质量的甲乙丙完全溶解在H2O中恰好达到饱和状态:★★①需要的溶剂质量大小关系:②得到的溶液质量大小关系:③溶质的质量分数大小关系:10.t2时,等质量的甲乙丙饱和溶液,降温到t1:★★★①溶液状态:甲,乙,丙(填“饱和状态”或“不饱和状态”)②析出晶体质量大小关系:③溶质的质量大小关系:④溶液的质量大小关系:⑤溶质的质量分数大小关系:11.根据曲线进行物质分离实验:①甲中混有少量乙Ⅰ.分离类型:(填“陡中有缓”或“缓中有陡”)Ⅱ.分离方法:(填“过滤”、“降温结晶”或“蒸发结晶”)Ⅲ.分离步骤:、、、②乙中混有少量甲Ⅰ.分离类型:(填“陡中有缓”或“缓中有陡”)Ⅱ.分离方法:(填“过滤”、“降温结晶”或“蒸发结晶”)Ⅲ.分离步骤:、、、一题了解溶解度曲线(答案)如下图是甲、乙、丙三种固体在水中的溶解度曲线,回答下列问题1.曲线类型:甲:陡升型;乙:平缓型;丙:下降型(填“陡升型”、“平缓型”或“下降型”)2.甲t2时溶解度是80g ;含义是t2时,100g水中最多溶解80g甲或t2时,100g水中溶解甲达到饱和状态的质量是80g3.n点含义是t1时,S(甲)=S(丙)或t1时,甲丙溶解度相同4.t2时,甲乙丙溶解度大小关系是甲>乙>丙;t1时,甲乙丙溶解度大小关系是乙>甲=丙5.t2时,甲的饱和溶液溶质的质量分数是44.4% ω=80/180×100%=44.4%6.t2时,60g甲加入50g水中,溶质质量:40 g;溶液质量 90:g;溶质的质量分数:44.4%解析:80:100=x:50,解得x=40g;m(溶液)=40+50=90g;ω同上7.t2时,60g甲加入50g水中,降温到t1,析出晶体:27.5 g;溶质质量: 12.5g;溶质质量分数:20% 解析:(80-25):100=y:50,解得y=27.5g;m(溶质)=40-27.5=12.5g;ω=25/125×100%=20%8.t2时,在各含100gH2O的烧杯中溶解甲乙丙恰好达到饱和状态:★★①溶质的质量大小关系:甲>乙>丙解析:溶解度:甲>乙>丙②溶液的质量大小关系:甲>乙>丙③溶质的质量分数大小关系:甲>乙>丙解析:ω=S/(S+100)=1/(1+100/S);S越大,ω越大④结论是:同温度下,溶解度越大,溶质的质量分数越大或同温度下,S越大,ω越大9.t2时,等质量的甲乙丙完全溶解在H2O中恰好达到饱和状态:★★①需要的溶剂质量大小关系:丙>乙>甲;解析:同温度下,溶解度越大,溶解等质量固体需要的水越少②得到的溶液质量大小关系:丙>乙>甲③溶质的质量分数大小关系:甲>乙>丙;解析:同温度下,S越大,ω越大10.t2时,等质量的甲乙丙饱和溶液,降温到t1:★★★①溶液状态:甲饱和,乙饱和,丙不饱和(填“饱和状态”或“不饱和状态”)②析出晶体质量大小关系:甲>乙>丙解析:t2时,溶解度:甲>乙>丙;溶质的质量分数:甲>乙>丙;③溶质的质量大小关系:乙>甲>丙等质量溶液中:溶质质量:甲>乙>丙;溶剂质量:丙>乙>甲④溶液的质量大小关系:丙>乙>甲降温到t1,析出晶体质量:甲>乙,丙不析出晶体,即:甲>乙>丙⑤溶质的质量分数大小关系:乙>甲>丙溶液质量:丙>乙>甲;溶质质量:乙>甲>丙;质量分数:乙>甲>丙11.根据曲线进行物质分离实验:①甲中混有少量乙Ⅰ.分离类型:陡中有缓(填“陡中有缓”或“缓中有陡”)Ⅱ.分离方法:降温结晶(填“过滤”、“降温结晶”或“蒸发结晶”)Ⅲ.分离步骤:热水溶解、降温、结晶、过滤②乙中混有少量甲Ⅰ.分离类型:缓中有陡(填“陡中有缓”或“缓中有陡”)Ⅱ.分离方法:蒸发结晶(填“过滤”、“降温结晶”或“蒸发结晶”)Ⅲ.分离步骤:溶解、蒸发、结晶、趁热过滤。
溶解度曲线习题汇总1、图1分别为A、B、C三种物质的溶解度曲线图,按下列各小题要求,把适当的答案填入各空格内。
图1(1)A、B、C三种物质中,属于可溶性物质的是__,属于微溶性物质的是____,属于难溶性物质的是________;(2)在上述三种物质中,随着温度升高,溶解度增大的物质有_______;随着温度升高,溶解度降低的物质有________;(3)A物质在35℃时的溶解度为________,B物质在0℃时的溶解度为_______。
2、右图是X、Y、Z三种固体物质的溶解度曲线,当它们的溶液接近饱和时,分别采用增加溶质、蒸发溶剂、升高温度三种方法,均可以变成饱和溶液的是()A.X溶液B.Y溶液C.Z溶液 D.X、Y溶液3、右图是某物质的溶解度曲线,图中表示不饱和溶液的点是()A.a点 B.b点C.c点 D.无4、现有a、b两种物质在t1℃的饱和溶液,将它们的温度分别升高到t2℃,a溶液有晶体析出而b溶液还可以继续溶解一些b晶体。
则能表示a、b两种物质的溶解度曲线是()5、图5是A、B两种物质的溶解度曲线,根据图示回答下列问题:(1)在____t1____℃时,A和B物质的溶解度相等。
在t℃时,A物质的溶解度比B物质的溶解度____2大____(填“大”或“小”);(2)当A物质的溶液接近饱和时,采用__降温 __、__蒸发溶剂___、__加溶质__三种方法均可使其变为饱和溶液。
6、根据溶解度曲线回答问题.(1)溶解度随温度升高而增大的物质是________.(2)t2℃时,溶解度相等的是_______.(3)t2℃时,100 g水中加入20 g a物质,溶液不饱和,为使其饱和,可再加入a物质________g,或使其温度降到________℃.7、右图是 a、b、c三种物质的溶解度曲线,据图回答:(1)当温度是℃,a、b两种物质的溶解度相等;(2)t3 ℃时三种物质的溶解度由大到小的顺序是_________8、甲乙两种固体的溶解度曲线如右图所示。
溶解度和溶解度曲线1.将200g溶有物质M的溶液从95℃降低到10℃,不同温度时析出溶质M的质量如下表所示。
下列说法正确的是()温度/℃9590803010析出M的质量/g0015100116A.95℃时该溶液为饱和溶液B.M的溶解度随温度的升高而减小C.30℃时析出M后所得溶液中含100g水D.从M的不饱和溶液中析出M可采用先蒸发溶剂、再冷却结晶的方法2.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是()A.M的溶解度曲线为a曲线B.升温可以使N的饱和溶液变浑浊C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N3.盐湖地区人们常采用“夏天晒盐,冬天捞碱”的方法来获取NaCl和Na2CO3.结合溶解度曲线判断,下列说法错误的是()A.NaCl的溶解度随温度变化不大B.44℃时Na2CO3饱和溶液的质量分数为50%C.“夏天晒盐”的原理是让湖水蒸发结晶得到NaClD.“冬天捞碱”的原理是让湖水降温结晶得到Na2CO34.小明自制了一杯蔗糖水(无固体剩余),用于缓解运动后出现的低血糖症状,之后他结合下表蔗糖的溶解度数据,归纳出以下问题,其中正确的是()温度/℃01020406080100182191204238287362487溶解度/gA.配制的蔗糖溶液下层比上层甜B.降温,糖水中一定有晶体析出C.20℃时,蔗糖饱和溶液质量一定为304gD.升温,糖水中蔗糖的质量分数不变5.向2个盛有100g 60℃水的烧杯中,分别加入40g的NaCl和KCl固体,充分溶解。
根据实验和溶解度曲线判断,下列说法正确的是()A.①得到的溶液质量为140gB.KCl的溶解度比NaCl的溶解度大C.②得到的溶液为饱和溶液D.②中溶液溶质的质量分数约为28.6%6.A、B、C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是()A.t2℃时,A、B两种溶液中溶质的质量分数相同B.t1℃时,三种物质的溶解度从大到小关系:B>C>AC.t1℃时,30g固体A放入50g水中充分溶解,形成饱和溶液65gD.要从B溶液中得到B固体,通常采用蒸发溶剂的方法7.在20℃时,将40g氯化钠固体加入100g水中,充分搅拌后,有4g固体未溶解。
小专题(一) 溶解度及溶解度曲线1。
溶解度固体溶解度定义一定温度下,某固态物质在100 g溶剂里达到饱和状态时所溶解的质量影响因素内因:溶质和溶剂的性质外因:温度类型①大多数物质的溶解度随温度的升高而增大(如KNO3)②少数物质的溶解度受温度的影响不大③极少数物质的溶解度随温度的升高而减小气体溶解度,与温度、压强关系,温度升高,溶解度减小;气压增大,溶解度增大影响因素,内因:溶质和溶剂的性质外因:温度和压强2。
溶解度曲线的意义(1)溶解度曲线上的点:①表示固体物质在该温度下的溶解度,如图,P点表示t1℃时A的溶解度为a1g.②两条曲线的交点:表示该温度下两种物质的溶解度相等或该温度下两种物质饱和溶液的质量分数相等。
如图,Q点表示t2℃时A、B的溶解度相等。
(2)溶解度曲线:①表示物质的溶解度随温度的变化趋势,如图:A、B的曲线表示A和B物质的溶解度随温度的升高而增大,C 的曲线表示C物质的溶解度随温度的升高而减小。
②曲线的倾斜程度:表示物质的溶解度受温度的影响程度,如图A,倾斜程度大,表示A物质的溶解度受温度的影响大;B物质的倾斜程度小,表示B物质的溶解度受温度的影响小。
(3)溶解度曲线的上面和下面:①溶解度曲线上面区域内所有的点:表示该温度下,物质形成的溶液是饱和溶液,且有未溶解的溶质存在。
②溶解度曲线下面区域内所有的点:表示该温度下,物质形成的溶液是不饱和溶液。
考点一溶解度【例1】食盐的溶解度为36 g,这句话最主要的错误是( )A.未指明在100 g水中B.未指明达到饱和C.未指明温度D.未指明36 g为最大克数【解析】溶解度四要素:①一定温度;②100 g溶剂;③达到饱和;④溶质的质量.溶解度是指100 g水中溶解某溶质达到饱和状态,溶质的质量随温度而变,即主要的错误是没有指明温度,故选C。
【答案】C【例2】(2015石家庄中考模拟)一木块漂浮于50 ℃时的KNO3饱和溶液中(见图A),当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积(V排)随时间(t)发生了如图B所示的变化。
溶解度/gt/℃21m m m m 溶解度曲线知识点一、正确理解溶解度曲线的涵义溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。
点① 曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a 表示 A 物质在t 1℃时溶解度为m 1g 。
曲线上方的点:表示在对应温度下该物质的饱和溶液中存在 不能继续溶解的溶质。
如:图中b 表示在t 1℃时,A 的饱和溶液中有 (m 2-m 1)g 未溶解的溶质。
曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中C 表示在t 1℃时,A 的不饱和溶液中,还需要加入(m 1-m 3)gA 物质才达到饱和。
②曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d 表示在t 2℃,A 、B 两物质的溶解度都为m 4g 。
2、线如图中A 物质的溶解度随温度升高而明显增大,A 曲线为“陡升型”。
如KNO 3等大多数固体物质:图中B 物质的溶解度随温度变化不大,B 曲线为“缓升型”,如NaCl 等少数固体物质。
图中C 物质的溶解度随温度升高而减小,C 曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
二、掌握溶解度曲线的应用1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2. 可以比较在同一温度下不同物质溶解度的相对大小。
3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。
例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。
某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。
4. 从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。
5. 利用溶解度曲线可以确定一定质量的某物质的饱和溶液降温时析出晶体的质量。
溶解度/gt/℃溶解度曲线专题练习1. 甲、乙两物质的溶解度曲线如图所示,下列说确的是 A .甲和乙的饱和溶液,从t 1℃升温到t 2℃,仍是饱和溶液 B .t 1℃时,甲和乙的溶解度相等C .t 1℃时,甲和乙各30g 分别加入80g 水中,均能恰好完全溶解D .t 2℃时,在100g 水中放入60g 甲,形成不饱和溶液2. 右图是a 、b 两种固体物质的溶解度曲线。
从图中可获得的信息是 A. 固体物质的溶解度均随温度升高而增大 B .t ℃,相同质量的a 、b 溶解时放出热量相同 C .升高温度,可使a 或b 的饱和溶液变为不饱和溶液D .将相同质量的a 、b 分别加入100g 水中,所得溶液质量分数相同3.右图是甲、乙两种固体物质的溶解度曲线,下列说确的是 A .甲的溶解度大于乙的溶解度 B .乙的不饱和溶液降温可变成饱和溶液 C .20oC 时,甲、乙两种物质的溶解度相等D .50o C 时,甲的饱和溶液中溶质的质量分数为40%4. 右图是a 、b 两种固体物质(不含结晶水)的溶解度曲线。
下列说确的是 A.b 的溶解度大于a 的溶解度B.t 1℃时,将a 、b 两种物质的饱和溶液分别恒温蒸发等质量的水, 析出晶体的质量一定相等C.将t 2℃时的b 的不饱和溶液降温至t 1℃,一定能得到b 的饱 和溶 液D.t 2℃时,a 溶液的溶质质量分数一定小于b 溶液的溶质质量分数5.右图是a 、b 两种固体物质的溶解度曲线,下列说法中正确的是A .a 的溶解度大于b 的溶解度B .在20℃时,a 、b 的溶液中溶质的质量分数相同C .a 、b 的溶解度都随温度升高而增大D .a 、b 都属于易溶物质6.t 2℃时往盛有100g 水的烧杯中先后加入a g M 和a g N (两种物质溶解时互不50-40- 30- 20- 10-甲乙温度/t 1t 2 溶解度/g影响,且溶质仍是M、N),充分搅拌。
将混合物的温度降低到t1℃,下列说确的是A.t2℃时,得到M的饱和溶液B.t2℃时,得到N的不饱和溶液C.温度降低到t1℃时,M、N的溶质质量分数相等,得到M、N的不饱和溶液D.温度降低到t1℃时,M、N的溶解度相等,得到M、N的饱和溶液7.右图是a、b、c三种固体物质的溶解度曲线,下列叙述正确的是A.将a、b、c三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数大小关系是a>b>cB.t2℃时30g物质a加入到50g水中不断搅拌,形成80g溶液C.t1℃时a、b、c三种物质的饱和溶液中含有溶质质量按由小到大的顺序排列是b>a=c D. 若a中混有少量c,可以采用冷却热饱和溶液的方法提纯a8.两种不含结晶水的固体物质a、b的溶解度曲线如右图,下列说确的是A.b的溶解度小于a的溶解度B.分别将t2℃时a、b两种物质的溶液降温至t1℃,肯定都有晶体析出C.要从含有少量a的b溶液中得到较多的b晶体,通常可采用降温结晶的方法D.在t2℃时,用a、b两种固体和水分别配制等质量的两种物质的饱和溶液,需要量取相同体积的水9.右图所示曲线a、b、c分别代表A、B、C三种物质的溶解度曲线。
下列说确的是A.t1 ℃时,三种物质溶解度大小的顺序是B>C>AB.t2℃时,A和B两种物质的饱和溶液中溶质质量相同C.t3℃时,在100g水里分别加入三种物质各mg,只有b能形成饱和溶液D.从混有少量C的A物质中提取较纯净的A,最适宜用蒸发溶剂的方法10.右图是a、b、c三种固体的溶解度曲线,下列说确的是A.b的溶解度一定小于a的溶解度B.当a中含有少量b时,可以用降温结晶的方法提纯aC.通过降低温度可将c的不饱和溶液变为饱和溶液D.a的饱和溶液从t2℃降温至t1℃时变为不饱和溶液11.有关a、b两种物质的溶解度曲线如图所示,下列叙述不正确的是A.a物质的溶解度随着温度的升高而增大B.在t2℃时,a、b两种物质的溶液中溶质的质量分数一定相等C.将a、b两种物质的饱和溶液从t3℃降温至t1℃,a有晶体析出,b无晶体析出D.t3℃时,a物质的溶解度大于b物质的溶解度温度/℃12ba溶解度 \ g甲乙溶解度 g0 t 1 t 2 温度/℃30 50 20 401012.a 、b 、c 三种物质的溶解度曲线如右图所示。
现有t 1℃时的a 、b 、c 三种物质的饱和溶液,将其都升温至t 2℃时,下列说法中,正确的是 A .b 溶液为饱和溶液 B .a 溶液中有晶体析出 C .c 溶液为不饱和溶液 D .b 溶液中的溶质质量分数最大13.右图所示为甲、乙两物质(均不含结晶水)的溶解度曲线。
50℃时,取甲、乙两种物质各50g ,分别加人100g 水中,使之充分溶解。
下列有关说法不正确的是………( )A .上述混合物在20℃时,甲和乙形成溶液的质量相等B .在0℃时,溶液中溶质的质量分数甲小于乙C .温度高于50℃时,甲和乙形成的溶液都变为不饱和溶液D .50℃时,将甲、乙两种物质的混合物分别降温至20℃,溶液中未溶解晶体的质量相等14、右图是a 、b 两种固体物质的溶解度曲线图,下列说法中不正确的是A .任何温度下,a 的溶解度大于b 的溶解度B .a 的溶解度受温度变化的影响比b 的大C .t 1 ℃至t 2 ℃之间b 曲线以下区域为a 、b 两物质的不饱和溶液D .对于a 与b 混合溶液,可利用冷却结晶的方法来分离15.甲、乙两物质的溶解度曲线如右图所示。
下列叙述中,正确的是 A .t 1℃时,甲和乙的溶解度均为30B .t 2℃时,甲和乙的饱和溶液中溶质质量分数相等C .t 2℃时,在100 g 水中放入60 g 甲,其溶质的质量分数为37.5%D .t 2℃时, 分别在100 g 水中各溶解20 g 甲、乙,同时降低温度,甲先达到饱和16.根据右图A 、B 、C 三种物质的溶解度曲线,判断下列说法是否正确 A. 温度从t 2℃降到t 1℃时三种物质析出晶体由多到少的顺序为 A>B>C B.t 2℃时A 溶液溶质的质量分数最大,C 溶液溶质的质量分数最小 C.A 物质中混有C 物质,可以用蒸发溶剂的方法提纯A D.t 1℃时,A 、B 、C 三种物质的饱和溶液溶质的质量分数相等17、几种物质的溶解度曲线如右图。
则下列说确的是 A .氯化铵的溶解度最大B .随着温度升高,硫酸钠的溶解度不断增大C .40℃时硫酸钠饱和溶液溶质的质量分数为50%D .把40℃时等质量的三种物质的饱和溶液降温到20℃, 硫酸钠析出晶体最多溶 解 度 g0 t 1 t 2 温度/℃ab c氯化铵溶解度/g 2030405060硫酸钠氯化钠18.右图表示A 、B 两种物质的溶解度(s)随温度(t)的变化情况, 下列说确的是A .A 的溶解度大于B 的溶解度B .升高温度可使A 的不饱和溶液变为饱和C .t 3℃时,在100g 水中溶解60gA 能形成饱和溶液D .t 2℃时,A 和B 的饱和溶液的溶质质量分数相等19、右图中M 、N 分别表示二种固体物质(不含结晶水)的溶解度曲线,试根据图中曲线判断下列说确的是A .图中A 点表示M 、N 二种物质在t 1℃时均达到饱和B .M 、N 二种饱和溶液,当温度从t 1降至t 2时,一定析出相同质量的晶体C .同处A 点的相同质量的M 、N 二种溶液,当温度从t 1降至t 2后,剩余溶液 的质量分数相等D .0℃时,M 、N 具有相同的溶解度20、右图是a 、b 、c 三种固体物质的溶解度曲线。
由图示判断下列说法中正确的是 A .b 物质的溶解度大于c 物质的溶解度 B .a 物质的溶解度大于c 物质的溶解度C .a 物质的饱和溶液从t 2℃降温至t 1℃时变为不饱和溶液D .c 物质的不饱和溶液从t 2℃降温至t 1℃时变为饱和溶液21.右图是A 、B 两种固体物质的溶解度曲线。
下列说法中错误的是A .A 物质的溶解度受温度变化的影响较大,B 物质的溶解度受温度变化的影响较小 B .t ℃时,等质量的A 、B 饱和溶液中含有相同质量的溶质C .当温度大于t ℃时,A 溶液一定比B 溶液浓D .B 中含有少量A 时,用溶解、蒸发、结晶的方法除去B 中的A22.右图是A 、B 、C 三种物质的溶解度曲线,据图回答:(1) t 1℃时A 、B 、C 三种物质的溶解度由大到小的顺序是 (填写序号,下同)。
(2) t 1℃时30gA 物质加入到50g 水中不断搅拌,形成的溶液质 量是 g 。
(3) 将t 1℃时A 、B 、C 三种物质饱和溶液的温度升高到t 2℃时, 三种溶液的溶质质量分数由大小关系是(3)右图是a 、b 两种物质的溶解度曲线。