中考总复习名校化学一轮思维方法:第五讲物质的微粒观
- 格式:doc
- 大小:548.00 KB
- 文档页数:21

专题二分子运动现象探究及构成物质的微粒重点突破分子运动现象的探究1.实验目的:认识分子的运动。
2.实验装置3.实验步骤( 1 )向盛有约20 mL蒸馏水的小烧杯A中加入5~6滴酚酞溶液,搅拌均匀,观察溶液的颜色。
( 2 )从烧杯A中取少量溶液于试管中,向其中慢慢滴加浓氨水,观察溶液颜色的变化。
( 3 )另取一个小烧杯B,加入约5 mL浓氨水。
用一个大烧杯或水槽罩住A、B两个小烧杯(如图所示),观察现象。
4.实验现象5.实验结论:酚酞遇氨水变红;分子是在不断运动的。
6.实验改进基础练1.建立宏观与微观的联系是一种科学的思维方法。
下列叙述正确的是()A.品红在水中扩散,是因为分子在不断的运动B.冰与干冰的化学性质不同,是因为分子的运动速率不同C.化学反应都遵循质量守恒定律,是因为化学反应中分子的种类与数目不变D.金刚石与石墨的化学性质相似,是因为碳原子的排列方式相同【答案】A【解析】A、品红在水中扩散,是因为品红分子是在不断的运动的,运动到水分子中间去了,故选项解释正确。
B、冰与干冰的化学性质不同,是因为它们分子的构成不同,不同种的分子化学性质不同,故选项解释错误。
C、化学反应都遵循质量守恒定律,是因为化学反应中原子的种类与数目不变,故选项解释错误。
D、金刚石与石墨的化学性质相似,是因为碳原子的排列方式不同,故选项解释错误。
2.建立宏观和微观之间的联系是化学学科特有的思维方式,下列对宏观事实的微观解释错误的是()宏观现象微观解释A 水沸腾时能掀开壶盖分子的大小随温度的升高而增大B 湿衣服在太阳晒着的地方干得快说明分子的运动速率与温度有关C 6000mL氮气可以压缩在40mL钢瓶中增大压强可以减小分子间间隔D 电解水生成氢气和氧气分子在化学变化中可以再分【答案】A【解析】A、水沸腾时能掀起壶盖,是因为分子间的间隔(而不是大小)随温度变化而改变,故选项解释错误。
B、湿衣服晾在太阳底下干得快,是因为温度升高,分子运动的速率加快,说明分子运动速率与温度有关,故选项解释正确。

专题05 构成物质的微粒一、新课标的要求:1.认识物质的微粒性,知道分子、原子、离子等都是构成物质的微粒。
2.能用微粒的观点解释某些常见的现象。
3.知道原子是由原子核和核外电子构成的。
4.知道原子可以结合成分子、同一元素的原子和离子可以互相转化,初步认识核外电子在化学反应中的作用。
二、考情分析:1、考查情况:化学是在分子、原子的基础上研究物质的组成、结构、性质及其变化规律的一门基础的自然学科。
从此可以看出构成物质的微粒在化学学科中的重要地位。
构成物质的微粒是各地中考必考的一个知识点,也是中考化学的热点内容。
2、考查形式:纵观近几年的各地中考试题,不难发现该知识点考查形式有:物质的微粒性、微粒基本性质、原子的构成、三种微粒的联系与区别等。
从题型上来说,可主要有选择和填空题。
从题目形式上说,有识记形、理解形、判断正误形和推断推理形。
3、命题方向:该考点的命题方向主要是通过创设相关问题情景或图表信息等,既可以考查学生对相关知识点的理解和掌握情况;还可以去考查学生分析、解答相关的实际问题的能力等。
4、试题难度:由于该知识点涉及微观知识,比较抽象且琐碎,是学生在理解上有一定难度的知识,使得分的难度增加。
试题难度一般为中等或难等的题目。
☆知识梳理☆一、:构成物质的微粒构成物质的基本微粒有三种:分子、原子和离子。
1、由原子构成的物质有:2、由分子构成的物质有:3、由离子构成的物质:注意:1、上述规律对初中的大多数物质起作用。
2、混合物的构成微粒要按其中所含物质的成分来分析。
二、微粒的基本性质:构成物质的微粒有以下性质:1、微粒很小(质量小、体积小)2、微粒时刻不停地做规则运动(运动速率与温度成正比)3、微粒间有间隔(间隔与温度成正比,与压强成反比)4、同种微粒,化学性质相同注意:1、微粒时刻不停地做规则运动,温度高时运动速率快;温度低时运动速率慢,但不是不运动。
此观点可解释扩散现象。
2、微粒间的间隔与温度成正比,温度高时微粒间的间隔变大,温度低时微粒间的间隔变小。



2020备战中考化学专题复习专题五:构成物质的微粒一、选择题1.【2018年四川省成都市】咏梅诗句“二十里中香不断,青羊宫到浣花溪”。
诗人间到香味的原因是()A.分子很轻B.分子不断运动C.分子体积小D.分子间有间隙【答案】B【解析】在远处可以闻到花香是因为花香分子在做无规则的运动,故答案选B。
2.【2018年四川省成都市】下列化学用语正确的是()A.2个氢原子:H2B.2个氮分子:2NC.氧化铁:FeOD.氯酸钾:KClO3【答案】D【解析】A.2个氢原子表示为2H,故该选项错误;B.氮分子是双原子分子,故2个氮分子表示为2N2,故该选项错误;C.氧化铁的化学式为Fe2O3,故该选项错误;D.氯酸钾的化学式正确;故答案选D。
3.【2018年四川省乐山市】类推是学习化学的重要方法之一,但盲目类推又可能得出错误结论。
下列类推正确的是()A.原子和分子均是微观粒子,原子在化学变化中不能再分,则分子在化学变化中也不能再分B.锌和铜均是金属,锌能与稀硫酸反应放出氢气,则铜也能与稀硫酸反应放出氢气C.金刚石和石墨均是碳的单质,金刚石十分坚硬,则石墨也十分坚硬D.H2SO4与HCl均是酸,H2SO4在水溶液中能电离出H+,则HCl在水溶液中也能电离出H+【答案】D【解析】A.分子在化学变化中是可以再分的,故该选项说法错误;B.锌和铜均是金属,但铜的活动性位于H后,不能与稀硫酸反应放出氢气,故该选项说法错误;C.金刚石十分坚硬,而石墨却十分软,故该选项说法错误;D.硫酸与盐酸均是酸,H2SO4在水溶液中能电离出H+,HCl在水溶液中也能电离出H+,故该选项说正确;故答案选D。
4.【2018年江西省】氧气在降温加压变成液态氧的过程中,下列说法正确的是()A.分子之间的间隔变小B.分子质量变小C.分子体积变大D.分子运动速率变大【答案】A【解析】氧气由气态变为液态,只是状态发生了变化,变化的是分子之间的间隔,分子之间的间隔变小,分子的质量不变,分子的体积不变,分子运动速率减慢。
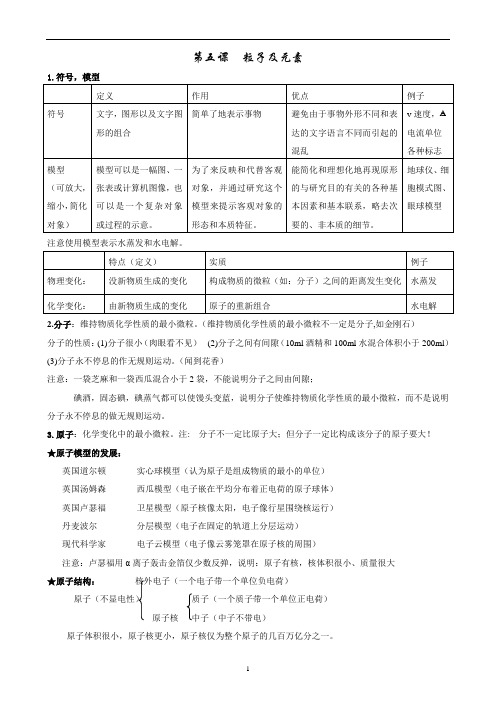
第五课粒子及元素1.符号,模型定义作用优点例子符号文字,图形以及文字图形的组合简单了地表示事物避免由于事物外形不同和表达的文字语言不同而引起的混乱v速度,○A电流单位各种标志模型(可放大,缩小,简化对象)模型可以是一幅图、一张表或计算机图像,也可以是一个复杂对象或过程的示意。
为了来反映和代替客观对象,并通过研究这个模型来提示客观对象的形态和本质特征。
能简化和理想化地再现原形的与研究目的有关的各种基本因素和基本联系,略去次要的、非本质的细节。
地球仪、细胞模式图、眼球模型注意使用模型表示水蒸发和水电解。
特点(定义)实质例子物理变化:没新物质生成的变化构成物质的微粒(如:分子)之间的距离发生变化水蒸发化学变化:由新物质生成的变化原子的重新组合水电解2.分子:维持物质化学性质的最小微粒。
(维持物质化学性质的最小微粒不一定是分子,如金刚石)分子的性质:(1)分子很小(肉眼看不见)(2)分子之间有间隙(10ml酒精和100ml水混合体积小于200ml)(3)分子永不停息的作无规则运动。
(闻到花香)注意:一袋芝麻和一袋西瓜混合小于2袋,不能说明分子之间由间隙;碘酒,固态碘,碘蒸气都可以使馒头变蓝,说明分子使维持物质化学性质的最小微粒,而不是说明分子永不停息的做无规则运动。
3.原子:化学变化中的最小微粒。
注: 分子不一定比原子大;但分子一定比构成该分子的原子要大!★原子模型的发展:英国道尔顿实心球模型(认为原子是组成物质的最小的单位)英国汤姆森西瓜模型(电子嵌在平均分布着正电荷的原子球体)英国卢瑟福卫星模型(原子核像太阳,电子像行星围绕核运行)丹麦波尔分层模型(电子在固定的轨道上分层运动)现代科学家电子云模型(电子像云雾笼罩在原子核的周围)注意:卢瑟福用α离子轰击金箔仅少数反弹,说明:原子有核,核体积很小、质量很大★原子结构:核外电子(一个电子带一个单位负电荷)原子(不显电性)质子(一个质子带一个单位正电荷)原子核中子(中子不带电)原子体积很小,原子核更小,原子核仅为整个原子的几百万亿分之一。
中考总复习:构成物质的几种粒子——分子、原子、离子【考纲要求】1.理解分子、原子、离子的概念,知道分子、原子、离子等都是构成物质的微粒;了解微粒的基本性质,能用微粒观点解释某些常见的现象。
2.知道原子的构成,理解原子结构示意图和离子结构示意图的关系和含义;知道同一元素的原子和离子可以互相转化。
【知识网络】概念:保持物质化学性质的最小微粒分子体积和质量都很小特征分子间有一定的间隔构构分子在不停的运动成成概念:化学变化中的最小微粒特征:同分子的特征相似物质原子质子(带正电)构成原子核(带正电)结构中子(不带电)构核外电子(带负电)成概念:带电的原子或原子团阳离子离子分类阴离子【考点梳理】考点一、分子(高清课堂《物质构成的奥秘》一、2)1.概念:分子是保持物质化学性质的最小粒子(由分子构成的物质)。
“性质”是指化学性质。
分子有什么化学性质,由这种分子聚集成的物质就有什么化学性质。
如一氧化碳分子能与氧分子反应生成二氧化碳分子,所以一氧化碳有可燃性。
分子不能保持物质的物理性质,因为物质的物理性质是由分子的聚集状态决定的,单个分子不能表现物质的物理性质。
如水分子间距离很小时水呈液态,水分子间的距离较大时水呈气态,水分子规则排列,不能自由移动时水呈固态(冰)。
分子是构成物质的一种粒子,有些物质直接由原子或原子团构成。
2.分子基本性质:(1)分子在不停地运动。
(2)质量和体积都很小。
1个水分子的质量大约是3×10-26kg,一滴水(约0.05 g)中约有1.7×1021个水分子。
(3)分子间有间隙,且不断运动,运动速率与温度有关。
用此性质可解释一些物理现象,如热胀冷缩、分子扩散、蒸发等。
(4)同种物质的分子化学性质相同,不同种物质的分子化学性质不同。
如氢分子能与氧分子反应,而水分子不能与氧分子反应。
【要点诠释】用分子理论解释物理、化学现象:1.物理变化和化学变化:由分子构成的物质在发生物理变化时,分子本身没有变化,如水加热变成水蒸气,水分子本身没变;通电氢气+氧气,在此反在发生化学变化时,分子本身发生了变化,变成了其他物质的分子,如水−−−→应中,水分子变成了氢气分子和氧气分子。
中考总复习系列丛书化学思想方法的应用第五讲物质的微粒观【题型特点】从微观的视角认识化学物质及其变化,是化学学科的重要特征。
“物质微粒观”作为一种重要的化学基本观念,它的形成对于学生理解和解释宏观的事实和现象, 理解化学反应的实质, 了解化学符号的意义等方面具有重要的意义。
特别是对于初中学生来说, 物质微粒观的建立, 是他们开启化学之门的基础。
“物质微粒观”其核心是微粒作用观,即不同层次的微粒本身是有结构的,微粒结构就是内部微粒间作用的结果;物质变化是微粒间的“强”相互作用代替“弱”相互作用。
物质微粒观的内容是丰富多彩的,它贯穿于整个中学化学学习过程中。
在初中阶段, 对物质微粒观的认识是以分子、原子概念的建立为标志的。
【主要考查内容】1.物质是由肉眼看不见的微粒构成的;2.微粒总是在不断运动的;3.微粒间有一定的间隔;4.微粒间存在着相互作用。
【必备知识梳理】1.微粒的基本性质:构成物质的微粒有以下性质:①微粒很小(质量小、体积小)②微粒时刻不停地做规则运动(运动速率与温度成正比)③微粒间有间隔(间隔与温度成正比,与压强成反比)④同种微粒,化学性质相同注意:①微粒时刻不停地做规则运动,温度高时运动速率快;温度低时运动速率慢,但不是不运动。
此观点可解释扩散现象。
②微粒间的间隔与温度成正比,温度高时微粒间的间隔变大,温度低时微粒间的间隔变小。
此观点可解释热胀冷缩现象。
③微粒本身的大小不受温度影响。
2.物质、元素、微粒之间的关系【典型例题】例1:1.(2018•成都)【解析】水由水分子构成,水分子由氧原子和氢原子构成,水中只有氢元素和氧元素,A错误。
【答案】A例2:(2018∙长沙)2018 年 12 月 16 日第一批“共享单车”进入长沙,方便了长沙市民的绿色出行;随着夏季气温的升高,“共享单车”的充气轮胎容易发生爆炸的主要原因是( )A.分子停止运动 B.分子质量变大C.分子本身的体积变大,分子运动速率减慢 D.分子间隔变大,分子运动速率加快【解析】宏观物质由微观粒子构成,微粒间是有间隔的,温度升高间隔变大,气体的体积和压强增大,当气体膨胀发生在有限的空间里,易产生爆炸。
【答案】D例3:(2018•威海)干冰和二氧化碳气体都是由二氧化碳分子直接构成的。
对于两者中的二氧化碳分子的比对结果,正确的是()A.分子运动速率相同 B分子之间相互作用的强弱相同C.化学性质相同 D.分子之间的间隔相同【解析】干冰是固态的二氧化碳,干冰和二氧化碳气体都是由二氧化碳分子直接构成,二者分子种类相同,因此化学性质也相同,C正确;分别对比两种状态下的二氧化碳分子可知,干冰和二氧化碳气体的分子运动速度、分子之间相互作用、分子之间间隔都不相同,A、B、D错误。
【答案】C例4:(2018∙成都)图是 X、Y 两种微粒的结构示意图。
下列说法正确的是()X YA.X 为原子,Y 为离子 B.X、Y 均属于非金属元素C.X 在反应中可失去 6 个电子 D.X 与 Y 形成化合物的化学式为 YX【解析】X、Y都为原子,A错误;X最外层电子数为6>4,属于非金属元素,Y最外层电子数为2<4,属于金属元素,B错误;X在反应当中易得到2个电子,C错误;X易得到2个电子,Y易失去2个电子,所以X与Y形成的化合物的化学式为YX,D正确。
【答案】D例5:(2018∙自贡)铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为( )A.24 B.58 C.82 D.140【解析】在原子中,质子数=核外电子数,故该原子的核外电子数为58 。
【答案】B【分类突破】1. (2018•桂林)宏观/微观之间存在必然的联系,建立正确的微粒观有助于化学的学习.请用微粒的知识回答下列问题.(1)阿伏加德罗指出分子和原子的区别,完善了道尔顿的原子学说。
分子和原子的本质区别是在化学变化中分子可以再分而原子不可以再分。
(2)“醋酸糖甜”是因为_分子构成不同_。
(3)空气和氧气的主要区别是_空气中含有多种分子,氧气中含有一种分_ 。
(4)原子内部含有带电荷的质子和电子,而整个原子不显电性的原因是原子核内的质子和电子所带的电量相等,电性相反,正负抵消,所以整个原子不显电性.(5)稀盐酸和稀硫酸具有相似的化学性质,原因是_溶液中都含有氢离子_。
【解析】(1)分子和原子的本质区别是在化学变化中分子可以再分而原子不可以再分;(2)“醋酸糖甜”是因为分子构成不同;(3)空气和氧气的主要区别是空气中含有多种分子,氧气中含有一种分子;(4)原子核内的质子和电子所带的电量相等,电性相反,正负抵消,所以整个原子不显电性;(5)稀盐酸和稀硫酸具有相似化学性质的原因是溶液中都含有氢离子。
2. (2018∙通辽)表中所列事实与相应的解释不相符的是()A.A B.B C.C D.D【解析】A.50 mL水和50 mL酒精混合后的溶液体积小于100 mL,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,故选项解释正确.B.变瘪的乒乓球放入热水中能鼓起来,是因为是分子间有间隙,温度增大,分子间间隔变大,故选项解释错误.C.稀有气体的化学性质稳定,是因为稀有气体的原子的最外层电子均达到相对稳定结构,故选项解释正确.D.氧气和臭氧(O3)化学性质不相同,是因为它们分子的构成不同,不同种的分子性质不同,故选项解释正确.【答案】B.3. (2018•南充)下列对一些事实的微观解释不正确的是【解析】金刚石和石墨物理性质差异很大,是因为它们碳原子的排列方式不同,A正确;加压时,6000L 氧气可装入容积为40L的钢瓶中,是因为分子间有间隔,气体受压后,分子间隔变小,B正确;搅拌能加快蔗糖在水中的溶解,是因为搅拌使蔗糖分子在水中溶解的速率更快,C不正确;稀盐酸、稀硫酸均显酸性,化学性质相似,是因为溶液中都含有氢离子,D正确。
【答案】D4.( 2018∙苏州)下列有关分子的说法中,不正确的是A.分子的质量和体积都很小 B.温度升高,分子的体积变大C.分子在不停她运动 D.温度越高,分子运动速率越快【解析】A.分子很小,正确;B.温度升高,分子的体积不变,但分子间的间隔变大,错误;C.分子在不断的运动,正确;D.温度越高,分子运动越剧烈,正确。
【答案】B5.(2018∙枣庄) 下列关于“酒精温度计遇热读数上升”的微观解释正确的是A.分子质量增大 B.分子体积扩大 C.分子间隔变大 D.分子个数增多【解析】温度升高,分子间隔变大,体积变大,故选C。
【答案】C6. (2018∙天津)根据下列粒子结构示意图,回答问题。
(1) A、B、C、D所示粒子共表示______种元素(填数字)。
(2) D所示粒子在化学反应中容易_____电子(填“得到”或“失去”) 。
(3)若E中x=10 时,则该粒子属于____(填“原子”或“离子”)。
【解析】(1)质子数决定元素的类别,A、B、C、D所示粒子共表示三种元素;(2)D所示粒子,最外层电子数大于4,在化学反应中容易得到电子;(3)若E中x=10 时,则该粒子呈电中性,属于原子。
【答案】(1)3;(2)得到;(3)原子。
7. (2018∙苏州)下列物质由离子构成的是A.二氧化碳 B.氯化钠 C.铁 D.水【解析】A、二氧化碳是由二氧化碳分子构成的;B、氯化钠是由钠离子和氯离子构成的;C、铁是由铁原子构成的;D、水是由水分子构成的。
故选B。
【答案】B8. (2018∙广州)下列有关分子与原子的说法不正确...的是A.分子不同性质不同 B.化学反应前后原子的种类和数目不变C.分子在不断运动 D.干冰升华时分子间的间距不变【解析】由分子构成的物质,分子是保持物质化学性质的最小粒子,分子不同,则性质不同,A正确;化学反应前后原子的种类和数目不变,B正确;分子都在不停地运动,C正确;干冰升华,二氧化碳由固态变为气态,分子间的间隔变大,D不正确。
【答案】D9. (2018∙威海)在化学变化中,下列说法正确的是()①原子不能被创造也不能被消灭②原子核不能被创造但能被消灭③分子既可以被创造也可以被消灭④电子不能被创造但能被消灭.A.②④ B.①④ C.①③ D.②③【解析】原子是化学变化中最小的微粒,在化学反应中不能再分,原子核位于原子的中心,因而在化学变化中原子和原子核都是既不可以被创造也不可能被消灭,①的说法正确、②的说法错误;在化学变化中分子的种类一定发生变化,因而分子既可以被创造也可以被消灭,③的说法正确;原子得失电子可以形成离子,离子得失电子也可以变成原子,因而电子在化学变化中既能被创造又能被消灭,④的说法错误;【答案】C10. (2018∙广州)右图是元素X的一种粒子结构示意图,下列说法正确的是A.X是非金属元素 B.X的最外层电子数为8C.该粒子最外层电子层已达到相对稳定结构D.该粒子可表示为X-【解析】A.X是金属元素,错误;B.X的最外层电子数为1,错误;C.最外层电子数是8个的结构是相对稳定结构,正确;D.该粒子可表示为X+,错误。
故选C。
【答案】C11. (2018∙达州)根据下图提供的信息,请回答下列问题:(1)A图表示原子其中X的值是。
(2)化学性质相似的原子是(填字母序号,下同)。
(3)具有稳定结构的原子。
(4)属于同种元素的粒子是。
【解析】(1)原子中核内质子数=核外电子数,可知X=2+7=9。
(2)元素的化学性质与原子核外最外层电子数关系密切,图中最外层电子数相等的粒子为A、C及B、D,其中D图所示微粒核外电子数>核内质子数,属于离子,因此化学性质相似的原子是AC。
(3)最外层电子数是8(氦是2)的结构被称为稳定结构,图中具有稳定结构的原子是B。
(4)核内质子数决定元素种类,图中C、D所示粒子核内质子数相同,属于同种元素。
【答案】(1)9 (2)AC (3)B (4)CD12. (2018∙温州)5月9日,2机构发布等四种元素的中文名称。
元素的核电荷数为118,相对原子质量为294,则原子核外电子数为A.118 B.176 C.294 D.412【解析】在原子中,质子数=核电荷数=核外电子数。
元素的核电荷数为118,故它的核外电子数也为118 。
【答案】A2020年中考化学模拟试卷一、选择题1.“分类”可以使人们有序的研究物质,下列分类正确的是()A.复合材料:玻璃钢、钢筋混凝土B.碱:烧碱、纯碱C.盐:氯化钾、氯化氢D.合金:金、青铜2.逻辑推理是化学学习中常用的思维方法,下列推理正确的是()A.CO(NH2)2、NH4NO3都是氮肥,NH4NO3属于铵态氮肥,所以CO(NH2)2也属于铵态氮肥B.氮气可做保护气,所以稀有气体也可做保护气C.在化合物中,金属元素显正价,所以非金属元素一定显负价D.硝酸钾饱和溶液中不能溶解硝酸钾固体,所以也不能溶解氯化钾固体3.铼高温合金材料用于制造航空发动机。