难溶电解质的溶解平衡(全面)
- 格式:doc
- 大小:584.31 KB
- 文档页数:11



难溶电解质的溶解平衡【知识要点】一、溶解平衡1. 不同电解质在中的溶解度差别很大。
在20℃时电解质的溶解性与溶解度的关系如下:2. 生成沉淀的离子反应之所以能发生,是因为_____________________ 。
3. 溶解平衡的建立:从固体溶解的角度来看,AgCl在水中存在两个过程:①在水分子的作用下,少量Ag+与Cl—脱离AgCl表面溶入水中,②溶液中的Ag+与Cl—受AgCl表面正、负离子的吸引,回到AgCl 表面析出沉淀。
在一定温度下,当沉淀溶液和生成的速率相等时,得到AgCl的饱和溶液,即建立下列平衡:AgCl(s)Ag+(aq)+ Cl—(aq)正是这种平衡的存在,决定了Ag+与Cl—的反应不能进行到底。
(1)定义:在一定条件下,难溶强电解质溶于水,当沉淀溶解的速率和沉淀生成的速率相等时,形成溶质的饱和溶液,达到平衡状态,这种平衡称为沉淀溶解平衡。
思考1. 将一块形状不规则的NaCl固体放入NaCl饱和溶液中,一昼夜后观察发现,固体变为规则的立方体,而质量却未发生变化,为什么?(2)特征:(与化学平衡相比较)①:可逆过程②:v(溶解)=v(沉淀)③:动态平衡,v(溶解)=v(沉淀)≠ 0④:达到平衡时,溶液中各离子浓度保持不变⑤:当外界条件改变时,溶解平衡将发生移动,达到新的平衡。
(3)生成难溶电解质的离子反应的限度化学上通常认为残留在溶液中的离子浓度小于,沉淀就达完全。
(4)影响沉淀溶解平衡的因素①内因:②外因:遵循原理浓度:加水,平衡向方向移动。
温度:绝大数难溶盐的溶解是吸热过程,升高温度,多数平衡向方向移动。
少数平衡向生成沉淀的方向移动,如Ca(OH)2的溶解平衡。
同离子效应:向平衡体系中加入相同的离子,使平衡向的方向移动。
例1. 将足量BaCO3分别加入:① 30mL 水②10mL 0.2mol/LNa2CO3溶液③50mL 0.01mol/L 氯化钡溶液④100mL 0.01mol/L盐酸中溶解至溶液饱和。

《难溶电解质的溶解平衡》[学习目标] 1.了解难溶电解质的溶解平衡。
2.了解溶度积的意义。
3.知道沉淀生成、沉淀溶解、沉淀转化的本质是沉淀溶解平衡的移动。
[重点·难点] 重点:溶度积的意义,沉淀生成、溶解与转化的本质。
难点:溶度积的应用。
一、对“Ag +与Cl —的反应不能进行到底”的理解1、不同电解质在中的溶解度差别很大,有的很大,有的很小。
在20℃时电解质的溶解性与溶解度的关系如下: 物质在水中“溶”与“不溶”是相对的,“不溶”是指“难溶”,绝对不溶的物质是没有的。
2、生成沉淀的离子反应之所以能发生,是因为。
3、溶解平衡的建立固态物质溶于水中时,一方面,在水分子的作用下,分子或离子脱离固体表面进入水中,这一过程叫溶解过程;另一方面,溶液中的分子或离子又在未溶解的固体表面聚集成晶体,这一过程叫结晶过程。
当这两个相反过程速率相等时,物质的溶解达到最大限度,形成饱和溶液,达到溶解平衡状态。
4、沉淀溶解平衡(1)定义: 绝对不溶解的物质是不存在的,任何难溶物质的溶解度都不为零。
以AgCl 为例:在一定温度下,当沉淀溶解和生成的速率相等时,便得到饱和溶液,即建立以下动态平衡:AgCl(s)Ag +(aq)+Cl -(aq)难溶电解质在水中建立起来的沉淀溶解平衡和化学平衡、电离平衡等一样,符合平衡的基本特征,满足平衡的变化基本规律.(2)特征:(与化学平衡相比较)等:达到沉淀溶解平衡时,沉淀_________速率的与沉淀__________速率相等 逆:沉淀生成过程与溶解过程时_________的动:动态平衡,达沉淀溶解平衡时,沉淀的生成和溶解仍在进行,只是速率相等。
溶解 沉淀定:达沉淀溶解平衡,溶质各离子浓度保持不变。
变:当条件改变,平衡会破坏,后建立新的平衡。
(3)表达式:如: AgCl (s) Cl-(aq)+Ag+(aq)AgCl===Ag++Cl-与AgCl (s) Cl-(aq)+Ag+(aq)区别[练习]书写碘化银、氢氧化镁溶解平衡的表达式碘化银:氢氧化镁(4)生成难溶电解质的离子反应的限度不同电解质在水中的溶解度差别很大,例如AgCl和AgNO3。



难溶电解质的溶解平衡知识点【篇一:难溶电解质的溶解平衡知识点】⑴难溶电解质的溶解平衡在一定重要条件下,当沉淀与溶解的速度相等时,便达到固体难溶电解质与溶液中离子间的平衡状态。
例如:baso4(s) ba2+(aq) + so42-(aq)⑵溶度积:在一定温度下,在难溶电解质的饱和溶液中,各离子浓度幂之乘积为一常数,称为溶度积常数,简称溶度积。
用符号ksp表示。
对于ambn型电解质来说,溶度积的公式是:ksp=[an+]m[bm+]n①溶度积与溶解度的关系溶度积和溶解度都可以表示物质的溶解能力,溶度积的大小与溶解度有关,它反映了物质的溶解能力。
②溶度积规则,可以判断溶液中沉淀的生成和溶解。
③离子积qc与溶度积ksp的区别与联系某难溶电解质的溶液中任一情况下有关离子浓度的乘积qc当qc<ksp时,为不饱和溶液;当qc=ksp时,为饱和溶液;当qc>ksp时,为过饱和溶液。
2. 了解沉淀转化的原理⑴沉淀的生成:可通过调节溶液ph或加入某些沉淀剂。
⑵沉淀的溶解:①生成弱电解质。
如生成弱酸、弱碱、水或微溶气体使沉淀溶解。
难溶物的ksp越大、生成的弱电解质越弱,沉淀越易溶解。
如cus、hgs、as2s3等ksp太小即使加入浓盐酸也不能有效降低s2-的浓度使其溶解。
②发生氧化还原反应,即利用发生氧化还原反应降低电解质离子浓度的方法使沉淀溶解。
③生成难电离的配离子,指利用络合反应降低电解质离子浓度的方法使沉淀溶解。
⑶沉淀的转化:把一种难溶电解质转化为另一种难溶电解质的过程叫沉淀的转化。
在含有沉淀的溶液中加入另一种沉淀剂,使其与溶液中某一离子结合成更难溶的物质,引起一种沉淀转变成另一种沉淀。
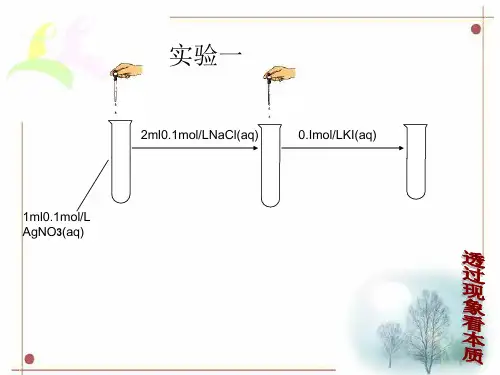
例如:caso4(s)+na2co3 = caco3(s)+na2so4在氯化银饱和溶液中,尚有氯化银固体存在,当分别向溶液中加入下列物质时,将有何种变化?在氯化银饱和溶液中,尚有氯化银固体存在,当分别向溶液中加入下列物质时,将有何种变化?。



难溶电解质的溶解平衡1.沉淀溶解平衡(1)概念在一定温度下,当难溶电解质溶于水形成饱和溶液时,沉淀溶解速率和沉淀生成速率相等的状态。
(2)溶解平衡的建立固体溶质溶解沉淀溶液中的溶质⎩⎪⎨⎪⎧v溶解大于v沉淀,固体溶解v溶解等于v沉淀,溶解平衡v溶解小于v沉淀,析出晶体(3)特点(4)表示AgCl在水溶液中的电离方程式为AgCl===Ag++Cl-。
AgCl的溶解平衡方程式为AgCl(s)Ag+(aq)+Cl-(aq)。
2.沉淀溶解平衡的影响因素(1)内因难溶电解质本身的性质。
溶度积(K sp)反映难溶电解质在水中的溶解能力。
对同类型的电解质而言,K sp数值越大,电解质在水中溶解度越大;K sp数值越小,难溶电解质的溶解度也越小。
(2)外因①浓度(K sp不变)a.加水稀释,平衡向溶解的方向移动;b.向平衡体系中加入难溶物相应的离子,平衡逆向移动;c.向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向溶解的方向移动。
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解的方向移动,K sp 增大。
(3)实例 以AgCl (s )Ag +(aq )+Cl -(aq ) ΔH >0为例20 ℃时电解质在水中的溶解度与溶解性存在如下关系: (1)沉淀的生成 ①调节pH 法如除去CuCl 2溶液中的杂质FeCl 3,可以向溶液中加入CuO ,调节溶液的pH ,使Fe 3+形成Fe(OH)3沉淀而除去。
离子方程式为Fe 3++3H 2OFe(OH)3+3H +,CuO +2H+===Cu 2++H 2O 。
②沉淀剂法如用H 2S 沉淀Hg 2+的离子方程式为Hg 2++H 2S===HgS ↓+2H +。
(2)沉淀的溶解①酸溶解法:如CaCO 3溶于盐酸,离子方程式为CaCO 3+2H +===Ca 2++CO 2↑+H 2O 。
②盐溶解法:如Mg(OH)2溶于NH 4Cl 溶液,离子方程式为Mg(OH)2+2NH +4===Mg 2++2NH 3·H 2O 。
难溶电解质的溶解平衡1.难溶、可溶、易溶界定20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:2.沉淀溶解平衡(1)溶解平衡的建立溶质溶解的过程是一个可逆过程:固体溶质溶解结晶溶液中的溶质⎩⎪⎨⎪⎧v溶解>v结晶固体溶解v溶解=v结晶溶解平衡v溶解<v结晶析出晶体(2)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)3.影响沉淀溶解平衡的因素(1)内因难溶电解质本身的性质,这是决定因素。
(2)外因①浓度:加水稀释,平衡向沉淀溶解的方向移动;②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向沉淀溶解的方向移动;③同离子效应:向平衡体系中加入难溶物溶解产生的离子,平衡向生成沉淀的方向移动;④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向沉淀溶解的方向移动。
深度思考(1)以AgCl(s)Ag+(aq)+Cl-(aq)ΔH>0为例,填写外因对溶解平衡的影响外界条件移动方向平衡后c(Ag+)平衡后c(Cl-)K sp升高温度正向增大增大增大加水稀释正向不变不变不变加入少量逆向增大减小不变AgNO3通入HCl 逆向减小增大不变通入H2S 正向减小增大不变(2)试用平衡移动原理解释下列事实:①已知Ba2+有毒,为什么医疗上能用BaSO4做钡餐透视,而不能用BaCO3做钡餐?②分别用等体积的蒸馏水和0.01 mol·L-1的盐酸洗涤AgCl沉淀,用水洗涤造成的AgCl的损失大于用稀盐酸洗涤的损失量。
答案①由于胃液的酸性很强(pH为0.9~1.5),H+与BaCO3电离产生的CO2-3结合生成CO2和H2O,使BaCO3的溶解平衡:BaCO3(s)Ba2+(aq)+CO2-3(aq)向右移动,c(Ba2+)增大,会引起人体中毒。
而SO2-4是强酸根离子,不能与胃液中的H+结合,因而胃液中H+浓度对BaSO4的溶解平衡基本没影响,Ba2+浓度可以保持安全的浓度标准以下。
《难溶电解质的溶解平衡》[学习目标] 1.了解难溶电解质的溶解平衡。
2.了解溶度积的意义。
3.知道沉淀生成、沉淀溶解、沉淀转化的本质是沉淀溶解平衡的移动。
[重点·难点] 重点:溶度积的意义,沉淀生成、溶解及转化的本质。
难点:溶度积的应用。
一、对“Ag +与Cl —的反应不能进行到底”的理解1、不同电解质在中的溶解度差别很大,有的很大,有的很小。
在20℃时电解质的溶解性与溶解度的关系如下: 物质在水中“溶”与“不溶”是相对的,“不溶”是指“难溶”,绝对不溶的物质是没有的。
2、生成沉淀的离子反应之所以能发生,是因为 。
3、溶解平衡的建立固态物质溶于水中时,一方面,在水分子的作用下,分子或离子脱离固体表面进入水中,这一过程叫溶解过程;另一方面,溶液中的分子或离子又在未溶解的固体表面聚集成晶体,这一过程叫结晶过程。
当这两个相反过程速率相等时,物质的溶解达到最大限度,形成饱和溶液,达到溶解平衡状态。
4、沉淀溶解平衡(1)定义: 绝对不溶解的物质是不存在的,任何难溶物质的溶解度都不为零。
以AgCl 为例:在一定温度下,当沉淀溶解和生成的速率相等时,便得到饱和溶液,即建立下列动态平衡:AgCl(s)Ag +(aq)+Cl -(aq)难溶电解质在水中建立起来的沉淀溶解平衡和化学平衡、电离平衡等一样,符合平衡的基本特征,满足平衡的变化基本规律.(2)特征:(与化学平衡相比较)等:达到沉淀溶解平衡时,沉淀_________速率的与沉淀__________速率相等 逆:沉淀生成过程与溶解过程时_________的动:动态平衡,达沉淀溶解平衡时,沉淀的生成和溶解仍在进行,只是速率相等。
溶解 沉淀定:达沉淀溶解平衡,溶质各离子浓度保持不变。
变:当条件改变,平衡会破坏,后建立新的平衡。
(3)表达式:如: AgCl (s) Cl-(aq)+Ag+(aq)AgCl===Ag++Cl-与AgCl (s) Cl-(aq)+Ag+(aq)区别[练习]书写碘化银、氢氧化镁溶解平衡的表达式碘化银:氢氧化镁(4)生成难溶电解质的离子反应的限度不同电解质在水中的溶解度差别很大,例如AgCl和AgNO3。
习惯上将溶解度小于0.01g的称为难溶电解质。
对于常量的化学反应来说,0.01g是很小的,所以一般情况下,相当量的离子互相反应生成难溶电解质,就可以认为反应完全了。
化学上通常认为残留在溶液中的离子浓度小于,沉淀就达完全。
4.影响溶解平衡的因素:(1)内因:电解质本身的性质不同的电解质在水溶液中溶解的程度不一样,而且差别很.注意:①绝对不溶的电解质是没有的,同是难溶电解质,溶解度差别也很大。
②易溶电解质做溶质时只要是饱和溶液也可存在溶解平衡。
(2)外因:(难溶电解质的溶解平衡作为一种平衡体系,遵从平衡移动原理)①浓度:加水,平衡向溶解方向移动。
改变平衡体系中某离子的浓度,平衡向削弱这种改变的方向移动。
②温度:升温,多数平衡向溶解方向移动。
但也有少数电解质,溶解度随温度升高而减小(如Ca(OH)2)。
升高温度,平衡向沉淀方向移动。
③其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向溶解方向移动,但K sp不变。
同离子效应:在难溶电解质溶液中加入与其含有相同离子的易溶强电解质,而使难溶电解质的溶解度降低的作用。
思考:对于平衡:AgClAg + + Cl -改变条件,平衡有何影响?条 件 平衡移动方向C(Ag +)C(Cl —)Ksp 溶解度(S )升高温度 加 水 加NaCl(s) 加AgNO 3(s) 加AgCl 固体[练习] 石灰乳中存在下列平衡:Ca(OH)2(s) Ca 2+(aq)+2 OH ―(aq),加入下列溶液,可使Ca(OH)2减少的是( )A. Na 2CO 3溶液B. AlCl 3溶液C. NaOH 溶液D. CaCl 2溶液[练习]:将足量BaCO 3分别加入:① 30mL 水 ②10mL 0.2mol/LNa 2CO 3溶液 ③50mL 0.01mol/L 氯化钡溶液④100mL 0.01mol/L 盐酸中溶解至溶液饱和。
请确定各溶液中Ba 2+的浓度由大到小的顺序为: 。
二、溶度积1.溶度积常数Ksp(或溶度积)难溶固体在溶液中达到沉淀溶解平衡状态时,离子浓度保持不变(或一定)。
各离子浓度幂的乘积是一个常数,这个常数称之为溶度积常数简称为溶度积,用符号Ksp 表示。
即:AmBn(s)mA n+(aq)+nB m -(aq) Ksp =[A n+]m·[B m -]n例如:常温下沉淀溶解平衡:AgCl(s)Ag +(aq)+Cl -(aq),Ksp(AgCl)=[Ag +][Cl -] =1.8×10-10常温下沉淀溶解平衡:Ag 2CrO 4(s)2Ag +(aq)+CrO 42-(aq),Ksp(Ag 2CrO 4)=[Ag +]2[CrO 2- 4] =1.1×10-12平衡2.溶度积K SP的性质(1)溶度积K SP的大小和平衡常数一样,它与难溶电解质的性质和温度有关,与浓度无关,离子浓度的改变可使溶解平衡发生移动,而不能改变溶度积K SP的大小。
(2)溶度积K SP反映了难溶电解质在水中的溶解能力的大小。
相同类型的难溶电解质的Ksp越小,溶解度越小,越难溶于水;反之Ksp越大,溶解度越大。
如:Ksp(AgCl)= 1.8×10-10 ;Ksp(AgBr) = 5.0×10-13;Ksp(AgI) = 8.3×10-17.因为:Ksp (AgCl) > Ksp (AgBr) > Ksp (AgI),所以溶解度:AgCl) > Ksp (AgBr) > Ksp (AgI)。
不同类型的难溶电解质,不能简单地根据Ksp大小,判断难溶电解质溶解度的大小。
4、影响Ksp的因素:温度:绝大数难溶盐的溶解是吸热过程,升高温度,向移动。
Ksp 。
少数盐的溶解是放热过程,升高温度,向生成移动,Ksp 。
如Ca(OH)2。
5、判断规则通过比较溶度积与溶液中有关离子浓度幂的乘积(离子积)Qc的相对大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解。
Qc Ksp时:溶液过饱和,平衡向生成沉淀的方向移动——有沉淀生成Qc Ksp时:溶液饱和,处于平衡状态Qc Ksp时:溶液不饱和,平衡向沉淀溶解的方向移动——沉淀溶解例1:下列情况下,有无CaCO3沉淀生成?已知Ksp,CaCO3=4.96 10-9(1)往盛有1.0 L纯水中加入0.1 mL浓度为0.01 mol /L 的CaCl2和Na2CO3;(2)改变CaCl2和Na2CO3的浓度为1.0 mol /L 呢?例2: 在1L 含1.0×10-3mol •L -1 的SO 42-溶液中,注入0.01mol BaCl 2溶液(假设溶液体积不变)能否有效除去SO 42-?已知:K sp (BaSO 4)= 1.1×10-10 mol 2•L -2例3:若某溶液中Fe 3+和Mg 2+的浓度均为0.10 mol /L, 使Fe 3+完全沉淀而使Mg 2+不沉淀的pH 条件是什么?( Ksp (Fe(OH)3)= 4×10-39Ksp (Mg(OH)2)= 1.8×10-11)例4:已知:某温度时,Ksp(AgCl)=[Ag +][Cl -] =1.8×10-10,Ksp(Ag 2CrO 4)=[Ag +]2[CrO 2- 4] =1.1×10-12,试求此温度下AgCl 饱和溶液和Ag 2CrO 4饱和溶液中Ag +的物质的量浓度,并比较两者的大小。
溶度积与溶解度之间的换算例1:已知25℃时,AgCl 的溶解度是1.92×10-3g/L ,求它的溶度积。
已知AgCl 的摩尔质量为143.5g/mol 。
例2:已知25℃时KSP(AgCl)=1.8×10-10,把足量的AgCl放入1L 1 .0 mol /L的盐酸溶液中溶解度是多少?(g/L)练习:已知Cu(OH)2(s) Cu2++2OH-,K sp=c(Cu2+)c2(OH-)=2×10-20 mol3·L-3。
(1)在CuSO4溶液中c(Cu2+)=0.020 mol·L-1,如果生成Cu(OH)2沉淀,应调整溶液pH在___ ____范围。
(2)要使0.2 mol·L-1 CuSO4溶液中Cu2+沉淀较为完全(使c(Cu2+)降为原来的千分之一),则应调整pH=________。
三、沉淀溶解平衡的应用1.沉淀的生成(1)调节pH法如除去NH4Cl溶液中的FeCl3杂质,可加入氨水调节pH至7~8,离子方程式为:________________________________________________________________________。
(2)沉淀剂法如用H2S沉淀Cu2+,离子方程式为:_____________________________________原则:(1)沉淀剂的选择,要求除去溶液中的某种离子,又不能影响其他离子的存在,并且由沉淀剂引入溶液的杂质离子还要便于除去。
(2)生成沉淀的反应能发生,且进行得越完全越好如:被沉淀离子为Ca2+离子,可用生成CaCO3,CaSO4或CaC2O4形成沉淀出来,但这三种沉淀物的溶解度CaC2O4<CaCO3<CaSO4,因此,沉淀成CaC2C4的形式,Ca2+离子去除的最完全[练习]为除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入的一种试剂是A、NaOHB、Na2CO3C、氨水D、MgO2.沉淀的溶解(1)酸溶解法如CaCO3溶于盐酸,离子方程式为_________________________________________。
(2)盐溶液溶解法如Mg(OH)2溶于NH4Cl溶液,离子方程式为________________________________。
(3)氧化还原溶解法如不溶于盐酸的硫化物Ag2S溶于稀HNO3。
3.沉淀的转化(1)实质:____________的移动(沉淀的溶解度差别________,越容易转化)。
(2)应用:锅炉除垢、矿物转化等。
问题思考为什么不能用BaCO3作钡餐?注意(1) 沉淀的转化的方法:加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子。
使平衡向溶解的方向移动。
(2) 沉淀的转化的实质:是沉淀溶解平衡的移动。
一般来说,溶解度小的沉淀转化成溶解度更小的沉淀容易实现[练习]现向含AgBr的饱和溶液中:(1)加入固体AgNO3,则c(Ag+)________(填“变大”、“变小”或“不变”,下同);(2)加入更多的AgBr固体,则c(Ag+)________;(3)加入AgCl固体,则c(Br-)________,c(Ag+)________;(4)加入Na2S固体,则c(Br-)________,c(Ag+)________。