药店药房-中药饮片装斗复核记录(药房)
- 格式:doc
- 大小:44.00 KB
- 文档页数:3



中药饮片装斗清斗复核记录日期:xxxx年xx月xx日目的:对中药饮片装斗清斗进行复核,确保质量和安全性。
参与人员:装填人员、清洗人员、质检人员装填记录:1.按照工艺要求,装填人员将待装填的中药饮片放入清洗后的斗中,然后将斗推入装填斗清斗运输车。
2.确保每个斗中装填的饮片数量均匀,避免出现明显过多或过少的情况。
3.注意区分不同饮片的装填位置,保证不同药材之间的交叉污染。
清洗记录:1.清洗人员使用清洗液和清洗器具对装斗进行彻底清洗。
2.清洗液应使用无污染的水源和无污染的清洗剂,确保对装斗进行彻底清洗。
3.清洗人员应认真检查装斗,确保无残留的药渣和异物。
质检记录:1.质检人员对装斗进行外观检查,确保无破损、变形等问题。
2.质检人员对清洗后的装斗进行气味检查,确保无异味。
3.质检人员随机抽取一定数量的装斗进行重量检查,确保装填的饮片数量准确。
4.质检人员还可以根据需要对装斗进行抽查,检验装斗内饮片的质量。
总结:本次复核记录对中药饮片装斗清斗的装填、清洗和质检过程进行了详细记录。
装填人员和清洗人员严格按照工艺要求进行操作,保证了装填的饮片质量和安全。
质检人员对装斗进行了全面的检查,确保装斗无破损、异味和装填饮片的数量准确。
通过本次复核记录,可以确保中药饮片装斗清斗的质量和安全性符合要求。
附:装填工艺要求1.装填人员必须穿戴洁净的工作服、工作帽和口罩。
2.装填斗清斗运输车必须保持清洁,避免交叉污染。
3.清洗液必须符合相应的质量标准,不能使用有污染的水源。
4.装填斗清斗运输车必须定期进行清洗和消毒,避免卫生问题。
5.质检人员必须经过专业培训,熟悉相关质检标准和要求。
以上记录仅为示范,实际复核记录根据具体情况进行调整和补充。

药品经营企业在质量管理中的每一个环节,都应有相应的文字记录,质量管理工作是否完善,实际操作是否到位,从原始记录就能查看出来。
因此GSP记录是否完整、规范最能体现门店对质量管理是否重视,门店的各项管理工作是否到位,认真做好每一项记录,是门店全体员工的必修课。
记录填写指导一、基本要求1、统一用黑色水性笔填写。
2、记录不得涂改、粘贴、不得留有空行。
3、记录时逐行填写,不得打省略号。
4、记录有误时,用直尺划一横线(红色)并在旁边注明更正日期和更正人姓名,另取一行重新填写正确的内容。
5、每项记录都要有专用封面,装订固定后放入资料盒中备查。
6、记录封面应填写记录名称及起始日期。
二、温湿度记录1、记录前先填好店名、月份。
2、手工填写适宜温度范围。
3、营业场所:0~30 ℃;冷藏柜:2~10 ℃;阴凉柜:20℃以下4、适宜相对湿度范围35﹪~75﹪5、每天上午9:00~10:00、下午3:00~4:00各填写一次,每次记录完毕应及时签名。
6、调控措施后应将调控到适宜范围内温湿度数据重新填写。
三、养护设备使用及维护记录1、夏季室温达到30℃以上是开空调降温,时间从上午8时开始,至晚上21时左右为止。
作好记录。
(设施设备使用记录,应与温湿度记录相对应)2、相对湿度达到或超过75﹪时,采用通风或开空调的方法除湿。
3、生物制品等需2℃~10 ℃以内保存的药品应放入冷藏柜密封保存(如:人血白蛋白注射液、人免疫球蛋白、诺和灵30R笔芯、胰岛素制剂、重组人干扰素α-2b凝胶等)。
4、室温达到或超过20℃时,需20 ℃以下保存的药品应放入阴凉柜密封保存,如:乌体林斯注射液;卡介菌多糖核酸注射液/斯奇康注射液;阿托伐他汀片/阿乐;非洛地平缓释片/波依定;双氯芬酸钠双释放肠溶胶囊/戴芬胶囊;去氧孕烯炔雌醇片/妈富隆;阿卡波糖片/拜糖平片;糠酸莫米松软膏/艾洛松氟伐他汀胶囊/来适可胶囊;阿司匹林维生素C泡腾片/拜阿司匹灵等。
5、填写时应标明以下内容:门店名称、设备名称、规格型号、设备编号、年份等。

中药饮片处方的审核、调配、核对的管理制度1、目的:为加强中药饮片的经营管理,确保科学、合理、安全地经营中药饮片。
2、依据:《药品管理法》、《药品经营质量管理规范》3、适用范围:门店中药饮片经营的全过程4、责任人:中药饮片调配、复核、销售人员5、内容:5.1门店所经营的中药饮片必须从配送公司购进。
5.2门店所购进的中药饮片应有包装,并附有质量合格的标志,每件包装上应标明品名、规格、产地、生产企业、产品批号、生产日期、实施批准文号管理的中药饮片还必须注明批准文号。
5.3购进进口中药饮片的应有加本公司质管科原印章的《进口药材批件》及《进口药材检验报告书》复印件或电子扫描件。
5.4该炮制而未炮制的中药饮片不得购入。
5.5中药饮片装斗前应做质量复核、净选、过筛后装斗,做好装斗复核记录,不得错斗、串斗,及时清理格斗,防止混药,斗前应标明中药饮片名称。
5.6调配中药饮片的处方必须经执业中药师审核后方可调配、销售。
审核、调配和销售人员应在处方上签字或盖章。
处方留存五年备查。
5.7对有配伍禁忌或超剂量的处方应当拒绝调配销售,必要时经处方医师更正或重新签字,方可调配、销售。
5.8严格按配方、发药操作规程操作,坚持一审方、二核价、三开票、四配方、五核对、六发药的程序。
5.9按方配制,称准分匀,总贴误差不大于±2%,分贴误差不大于±5%,处方配完后应先自行核对,无误后签字交处方复核员复核,严格审查无误后签字方可发给顾客。
5.10应对先煎、后下、包煎、烊化、兑服等特殊用法单包注明,并向顾客交待清楚,并主动耐心介绍服用方法。
5.11经营中药饮片应配置所需调配处方和临方炮制的设备。
5.12中药饮片的储存有防尘、防潮、防污染、防鼠、防霉变的设备,并按其不同特性进行养护。

药店GSP记录全套填写指南记录填写指导一、基本要求1、统一用黑色水性笔填写。
2、记录不得涂改、粘贴、不得留有空行。
3、记录时逐行填写,不得打省略号。
4、记录有误时,用直尺划一横线(红色)并在旁边注明更正日期和更正人姓名,另取一行重新填写正确的内容。
5、每项记录都要加上公司统一印制的专用封面,用塑料杆夹固定放入资料盒中备查。
6、记录封面应填写记录名称及起始日期。
二、温湿度记录1、记录前先填好店名、月份。
2、手工填写适宜温度范围。
3、营业间:0~30 ℃;冷藏柜:2~8 ℃4、适宜相对湿度范围35﹪~75﹪5、每天上午9:00~10:00、下午3:00~4:00各填写一次,每次记录完毕应及时签名。
6、调控措施后应将调控到适宜范围内温湿度数据重新填写。
三、养护设备使用及维护记录1、夏季开机时间从上午9时开始,至晚上21时左右为止,中间时间可视情况(室温降至26℃以下时)停机。
2、相对湿度达到或超过75﹪时,采用通风或开空调的方法除湿。
3、室温达到或超过8 ℃时,生物制品等需2℃~8 ℃以内保存的药品应放入冷藏柜密封保存(如:人血白蛋白注射液、人免疫球蛋白、诺和灵30R笔芯、胰岛素制剂、重组人干扰素α-2b凝胶等)。
4、室温达到或超过25℃时,需25 ℃以下保存的药品应放入冷藏柜密封保存,如:乌体林斯注射液;卡介菌多糖核酸注射液/斯奇康注射液;阿托伐他汀片/阿乐;非洛地平缓释片/波依定;双氯芬酸钠双释放肠溶胶囊/戴芬胶囊;去氧孕烯炔雌醇片/妈富隆;阿卡波糖片/拜糖平片;糠酸莫米松软膏/艾洛松氟伐他汀胶囊/来适可胶囊;阿司匹林维生素C泡腾片/拜阿司匹灵等。
5、填写时应标明以下内容:门店名称、设备名称、规格型号、设备编号、年份等。
6、空调、冷藏柜(无药品)未使用时,保持清洁卫生,保持随时启用状态,按月试机,作好记录。
四、药品养护记录、中药饮片养护记录1、对陈列的药品每月进行检查。
2、近效期的药品、易霉变、易潮解的药品、拆零药品、冷藏药品作为重点养护品种,每月定期做好养护记录(可集中在每月的26日左右填写)。

零售药店中药饮片质量管理制度一、目的为规范中药饮片的经营活动,特制定本制度。
二、范围适用于门店中药饮片的验收、陈列、检查及销售的全过程。
三、管理要求1.中药饮片验收1.1中药饮片应有包装,并附有质量合格证。
验收员凭配送单对照实物进行品名、规格、批号、产地、生产日期、生产厂商、供货单位、到货数量、验收合格数量、验收结果等。
实施批准文号管理的中药饮片还应记录批准文号。
1.2所验收的中药饮片按批号在计算机系统中查验同批号的加盖本公司质量管理部专用原印章的电子版检验报告书;进口中药饮片,应查验《进口药材批件》及《进口药材检验报告书》。
1.3有虫蛀、发霉、泛油、变色、气味散失严重、风化、潮解、产生异味等变异现象及掺杂、伪品等不合格中药饮片应放置不合格品区,验收结果备注不合格,并报告质量管理部。
1.4 验收完毕后,验收员在配送单上签字,此配送单即为验收记录。
验收员按要求在验收记录上做验收结论,并签署姓名和验收日期,每月按时间顺序将验收记录装订成册,验收记录内容必须真实、准确、完整、便于追朔。
2.中药饮片陈列2.1职责2.1.1药店配置有中药饮片陈列、存放的斗柜和处方调配使用的调剂台、铜盅、戥称、台秤等设备。
2.1.2中药质量管理员负责指导、检查、督促营业员将中药饮片装斗、陈列。
2.1.3营业员负责中药饮片的装斗、陈列检查、清斗等具体运作。
2.2工作要求2.2.1每月对陈列、存放的中药饮片进行检查,同时清理抽斗内碎末、杂物,防止饮片生虫、发霉、变质。
2.2.2不同批号的中药饮片装斗前应清斗,并记录。
2.2.3应对装入斗内的饮片进行质量复核,并做装斗复核记录,发现有虫蛀、发霉、泛油、变色、气味散失严重、风化、潮解等变异现象时,不得装斗,报请中药质量管理员处理。
2.2.4装斗饮片碎末太多,应清理碎末后再装斗。
2.2.5对易虫蛀、发霉、泛油、变色、气味散失、风化、潮解等的中药饮片,应控制装斗量。
2.2.6装斗应仔细,不得错斗、串斗,防止混药。

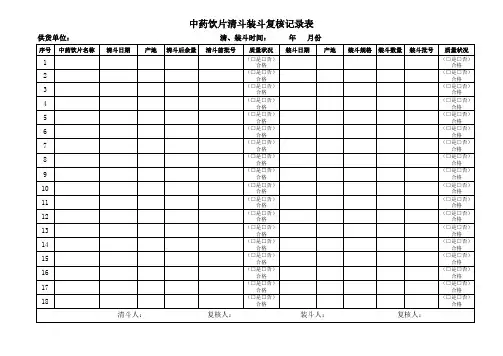
中药饮片装斗复核记录1.复核目的:本次复核旨在确保中药饮片装斗的质量符合相关标准要求,以确保产品的安全性和有效性。
2.复核范围:本次复核将对生产过程中的关键环节进行检查复核,包括原料选择、加工工艺、贮存条件、包装要求等环节。
3.复核时间及地点:复核时间:2024年10月1日至10月10日复核地点:生产车间4.复核人员:复核人员包括质量监控人员、生产人员、采购人员等相关人员。
5.复核内容:5.1原料选择复核:5.1.1检查原料供应商合格证和相关资质证书。
5.1.2检查原料是否符合国家药材标准要求。
5.1.3对常用原料进行随机抽样,送往实验室进行质量检测。
5.2加工工艺复核:5.2.1检查加工工艺流程是否符合国家药典要求。
5.2.2检查加工设备是否正常运行。
5.2.3观察加工人员操作是否规范,是否符合卫生要求。
5.3贮存条件复核:5.3.1检查贮存库房温湿度是否符合要求。
5.3.2检查贮存环境是否整洁,是否存在异味污染。
5.3.3检查贮存记录是否完整,包括温湿度记录、入库记录等。
5.4包装要求复核:5.4.1检查包装材料是否符合国家药品包装材料标准。
5.4.2检查包装过程是否符合要求,是否存在异物污染。
6.复核结果:6.1原料选择复核结果:6.1.1原料供应商合格证和相关资质证书全部齐全。
6.1.2原料符合国家药材标准要求。
6.1.3随机抽样的原料通过实验室检测,质量合格。
6.2加工工艺复核结果:6.2.1加工工艺流程符合国家药典要求。
6.2.2加工设备运行正常。
6.2.3加工人员操作规范,符合卫生要求。
6.3贮存条件复核结果:6.3.1贮存库房温湿度符合要求。
6.3.2贮存环境整洁,无异味污染。
6.3.3贮存记录完整,包括温湿度记录、入库记录等。
6.4包装要求复核结果:6.4.1包装材料符合国家药品包装材料标准。
6.4.2包装过程符合要求,无异物污染。
7.复核结论:根据上述复核结果,中药饮片装斗的质量符合相关标准要求,复核合格。

药店GSP中药饮片处方审核、调配、核对管理制度1、目的:为加强中药(包括中药材和中药饮片)管理,保证中药质量和保障人们使用中药有效。
2、依据:《药品经营质量管理规范》。
3、适用范围:企业中药饮片销售。
4、责任:质量管理人员、中药师对本制度的实施负责。
5、内容:5.1 中药配方营业员在配方时应思想集中,严格按处方要求核对品名配药、售药。
5.2 配方使用的中药饮片,必须是经过加工炮制的中药品种。
5.3 不合格药品的处理按《不合格药品管理制度》执行。
严禁不合格药品上柜销售。
5.4 对处方所列药品不得擅自更改,对有配伍禁忌或超剂量的处方应当拒绝调配、销售,必要时,经处方医师更正或重新签字,方可调配、销售。
5.5严格按配方、发药操作规程操作。
坚持一审方、二核价、三开票、四配方、五核对、六发药的程序。
5.6 严格执行物价政策,严禁串规、串级,按规定价格算方计价,发票项目填写全面,字迹清晰。
5.7 按方配制,称准分匀,总贴误差不大于2%,分贴误差不大于5%。
处方配完后应先自行核对,无误后签字交复核员复核,严格复核无误后签字,才可发给顾客。
5.8 应对先煎、后下、包煎、分煎、烊化、兑服等特殊用法单包注明,并向顾客交待清楚,并主动耐心介绍服用方法。
5.9 配方营业员不得调配自带配方,对鉴别不清,有疑问的处方不调配,并向顾客讲清楚情况。
5.10 配方用毒性中药饮片按《特殊管理药品管理制度》执行。
5.11 每天配方前必须校对衡器,配方完毕整理营业场所,保持柜厨内外清洁。
5.12 中药饮片来料加工的场所、工具应保持清洁,人员符合有关规定。
5.13中药上柜必须执行先进先出,易变先出的原则,不合格饮片一律不得上柜。
5.14 严把中药饮片销售质量关,过筛后装斗,装斗前应复核,防止混装、错装。
饮片斗前应写正名正字(以中国药典的为准,若药典没有规定的,以通用名为准);及时清理格斗,并做好记录。
相关文件:1、《中药饮片销售记录》3、《中药饮片装斗复核记录》。