吸收习题课的题
- 格式:doc
- 大小:344.00 KB
- 文档页数:10

吸收练习题一、填空题:(31)1、压力__ _,温度____,将有利于解吸的进行。
2、由双膜理论可知,____ ___为吸收过程主要的传质阻力;吸收中,吸收质以_____的方式通过气膜,并在界面处溶解,再以_ __ ____的方式通过液膜。
3、吸收操作的依据是____ ____,以达到分离气体混合物的目的。
4、亨利定律的表达式Exp*,若某气体在水中的亨利系数E值很大,说明该气体为___气体。
5、对极稀溶液,吸收平衡线在坐标图上是一条通过点的线。
6、由于吸收过程中,气相中的溶质组分分压总是___ _____溶质的平衡分压,因此吸收操作线总是在平衡线的____ ____。
7、吸收过程中,XK是以___ _为推动力的总吸收系数,它的单位是____。
8、吸收操作中增加吸收剂用量,操作线的斜率___ ___,吸收推动力___ ___。
9、当吸收剂用量为最小用量时,完成一定的吸收任务所需填料层高度将为__ _。
10、用吸收操作分离气体混合物应解决下列三方面问题:_ 、与。
11、填料塔操作中,气液两相在塔内互成__ _ 流接触,两相的传质通常在____的液体和气体间的界面上进行。
12. 气体吸收计算中,表示设备(填料)效能高低的一个量是,而表示传质任务难易程度的一个量是。
13.分子扩散中菲克定律的表达式为,气相中的分子扩散系数D随温度升高而(增大、减小),随压力增加而(增大、减小)。
14.易溶气体溶液上方的分压,难溶气体溶液上方的分压,只要组份在气相中的分压液相中该组分的平衡分压,吸收就会继续进行。
15.某低浓度气体吸收过程,已知相平衡常数m=1 ,气膜和液膜体积吸收系数分别为kya =2×10-4kmol/m3.s, kxa=0.4kmol/m3.s, 则该吸收过程及气膜阻力占总阻力的百分数分别为;该气体为溶气体。
二、选择题(40)1、吸收操作的目的是分离。
A.液体均相混合物B.气液混合物C.气体混合物D.部分互溶的液体混合物2、难溶气体的吸收是受______。

第七章 吸 收7-1 总压101.3 kPa ,温度25℃时,1000克水中含二氧化硫50克,在此浓度范围内亨利定律适用,通过实验测定其亨利系数E 为4.13 MPa , 试求该溶液上方二氧化硫的平衡分压和相平衡常数m 。
(溶液密度近似取为1000kg/m 3)解:溶质在液相中的摩尔分数:50640.01391000501864x ==+ 二氧化硫的平衡分压:*34.13100.0139kPa=57.41kPa p Ex ==⨯⨯相平衡常数:634.1310Pa40.77101.310PaE m P ⨯===⨯7-2 在逆流喷淋填料塔中用水进行硫化氢气体的吸收,含硫化氢的混合气进口浓度为5%(质量分数),求填料塔出口水溶液中硫化氢的最大浓度。
已知塔内温度为20℃,压强为1.52×105 Pa ,亨利系数E 为48.9MPa 。
解:相平衡常数为:6548.910321.711.5210E m P ⨯===⨯ 硫化氢的混合气进口摩尔浓度:15340.04305953429y ==+若填料塔出口水溶液中硫化氢达最大浓度,在出口处气液相达平衡,即:41max 0.0430 1.3410321.71y x m -===⨯7-3 分析下列过程是吸收过程还是解吸过程,计算其推动力的大小,并在x - y 图上表示。
(1)含NO 2 0.003(摩尔分率)的水溶液和含NO 2 0.06 (摩尔分率) 的混合气接触,总压为101.3kPa ,T=15℃,已知15℃时,NO 2水溶液的亨利系数E =1.68×102 kPa ;(2)气液组成及温度同(1),总压达200kPa (绝对压强)。
解:(1)相平衡常数为:51311.6810Pa 1.658101.310Pa E m P ⨯===⨯ *1 1.6580.0030.00498y m x ==⨯=由于 *y y >,所以该过程是吸收过程。

第五章 吸收相组成的换算【5-1】 空气和CO 2的混合气体中,CO 2的体积分数为20%,求其摩尔分数y 和摩尔比Y 各为多少?解 因摩尔分数=体积分数,.02y =摩尔分数 摩尔比 ..020251102y Y y ===--. 【5-2】 20℃的l00g 水中溶解lgNH 3, NH 3在溶液中的组成用摩尔分数x 、浓度c 及摩尔比X 表示时,各为多少?解 摩尔分数//117=0.010*******/18x =+浓度c 的计算20℃,溶液的密度用水的密度./39982s kg m ρ=代替。
溶液中NH 3的量为 /311017n kmol -=⨯ 溶液的体积 /.33101109982 V m -=⨯溶液中NH 3的浓度//.33311017==0.581/101109982n c kmol m V --⨯=⨯ 或 . 3998200105058218s sc x kmol m M ρ==⨯=../ NH 3与水的摩尔比的计算 //1170010610018X ==.或 ..00105001061100105x X x ===--. 【5-3】进入吸收器的混合气体中,NH 3的体积分数为10%,吸收率为90%,求离开吸收器时NH 3的组成,以摩尔比Y 和摩尔分数y 表示。
吸收率的定义为122111Y Y Y Y Y η-===-被吸收的溶质量原料气中溶质量解 原料气中NH 3的摩尔分数0.1y = 摩尔比 (11101)01111101y Y y ===-- 吸收器出口混合气中NH 3的摩尔比为 ()...211109011100111Y Y η=-=-⨯=()摩尔分数 (22200111)=0010981100111Y y Y ==++ 气液相平衡【5-4】 l00g 水中溶解lg 3 NH ,查得20℃时溶液上方3NH 的平衡分压为798Pa 。
此稀溶液的气液相平衡关系服从亨利定律,试求亨利系数E(单位为kPa )、溶解度系数H[单位为/()3kmol m kPa ⋅]和相平衡常数m 。

吸收习题课1、在填料吸收塔中,用清水吸收含有溶质A的气体混合物,两相逆流流动。
进塔气体初始浓度为5%(体积%),在操作条件下相平衡关系为y e=3x,试分别计算液气比为4、2和3时的出塔气体的极限浓度和液体出口浓度。
2、在填料高度为4m的常压填料塔中,用清水吸收尾气中的可溶组分。
已测得如下数据:尾气入塔组成为0.02,吸收液排出的浓度为0.008(以上均为摩尔分率),吸收率为0.8,并已知此吸收过程为气膜控制,气液平衡关系为y e=1.5x。
(1)计算该塔的H OG和N OG;(2)操作液气比为最小液气比的倍数;(3)若法定的气体排放浓度必须≤0.002,可采取哪些可行的措施?并任选其中之一进行计算,求出需改变参数的具体数值。
3、常压逆流连续操作的吸收塔,用清水吸收空气-氨混合气中的氨,混合气的流率为0.02kmol/m2s,入塔时氨的浓度为0.05(摩尔分率,下同),要求吸收率不低于95%,出塔氨水的浓度为0.05。
已知在操作条件下气液平衡关系为y e=0.95x,,气相体积传质总系数K y a=0.04kmol/m3s,且K y a∝G0.8。
(1)所需填料层高度为多少?(2)采用部分吸收剂再循环流程,新鲜吸收剂与循环量之比L/L R=20,气体流率及新鲜吸收剂用量不变,为达到分离要求,所需填料层的高度为多少?4、空气和CCl4混合气中含0.05(摩尔分率,下同)的CCl4,用煤油吸收其中90%的CCl4。
混合气流率为150kmol惰气/m2.h,吸收剂分两股入塔,由塔顶加入的一股CCl4组成为0.004,另一股在塔中一最佳位置(溶剂组成与塔内此截面上液相组成相等)加入,其组成为0.014,两股吸收剂摩尔流率比为1:1。
在第二股吸收剂入口以上塔内的液气比为0.5,气相总传质单元高度为1m,在操作条件下相平衡关系为y e=0.5x,吸收过程可视为气膜控制。
试求:(1)第二股煤油的最佳入塔位置及填料层总高度;(2)若将两股煤油混合后从塔顶加入,为保持回收率不变,所需填料层高度为多少?5、逆流吸收-解吸系统,两塔的填料层高度相同。

化⼯原理第五章吸收题说课讲解化⼯原理第五章吸收题六吸收浓度换算2.1甲醇15%(质量)的⽔溶液, 其密度为970Kg/m3, 试计算该溶液中甲醇的:(1)摩尔分率; (2)摩尔⽐; (3)质量⽐; (4)质量浓度; (5)摩尔浓度。
分⼦扩散2.2 估算1atm及293K下氯化氢⽓体(HCl)在(1)空⽓,(2)⽔(极稀盐酸)中的扩散系数。
2.3⼀⼩管充以丙酮,液⾯距管⼝1.1cm,20℃空⽓以⼀定速度吹过管⼝,经5 ⼩时后液⾯下降到离管⼝2.05cm,⼤⽓压为750[mmHg],丙酮的蒸汽压为180[mmHg] , 丙酮液密度为7900[kg/m3],计算丙酮蒸汽在空⽓中的扩散系数。
2.4 浅盘内盛⽔。
⽔深5mm,在1atm⼜298K下靠分⼦扩散逐渐蒸发到⼤⽓中。
假定传质阻⼒相当于3mm厚的静⽌⽓层,⽓层外的⽔蒸压可忽略,求蒸发完所需的时间。
2.5 ⼀填料塔在常压和295K下操作,⽤⽔除去含氨混合⽓体中的氨。
在塔内某处,氨在⽓相中的组成y a=5%(摩尔百分率)。
液相氨的平衡分压P=660Pa,物质通量N A= 10 - 4[kmol/m2·S],⽓相扩散系数D G=0.24[cm2/s],求⽓膜的当量厚度。
相平衡与亨利定律2.6 温度为10℃的常压空⽓与⽔接触,氧在空⽓中的体积百分率为21%,求达到平衡时氧在⽔中的最⼤浓度, (以[g/m3]、摩尔分率表⽰)及溶解度系数。
以[g/m3·atm]及[kmol/m3·Pa]表⽰。
2.7 当系统服从亨利定律时,对同⼀温度和液相浓度,如果总压增⼤⼀倍则与之平衡的⽓相浓度(或分压) (A)Y增⼤⼀倍; (B)P增⼤⼀倍;(C)Y减⼩⼀倍; (D)P减⼩⼀倍。
2.8 25℃及1atm下,含CO220%,空⽓80%(体积%)的⽓体1m3,与1m3的清⽔在容积2m3的密闭容器中接触进⾏传质,试问⽓液达到平衡后,(1)CO2在⽔中的最终浓度及剩余⽓体的总压为多少?(2)刚开始接触时的总传质推动⼒ΔP,Δx各为多少?⽓液达到平衡时的总传质推动⼒⼜为多少?仅供学习与交流,如有侵权请联系⽹站删除谢谢1362.9 在填料塔中⽤清⽔吸收⽓体中所含的丙酮蒸⽓,操作温度20℃,压⼒1atm。

习题第五章1. 酸度是指 H +的活度 ,常用 pH 表示;酸的浓度是指 酸的分析浓度 ,等于 c ,其单位用 mol/L 表示。
2. 根据酸碱质子理论,OH ‾ 的共轭酸是 H 2O ,HAc 的共轭酸是 H 2Ac + 。
3. 某弱酸H 2A 的pK a1 = 2.0,pK a2 = 5.0,当[H 2A] = [A 2-] 时,溶液的pH 值是 3.5 。
4. 浓度为C HAc (mol/L)的HAc 溶液中加入C HCl (mol/L)HCl 和C NaOH (mol/L)NaOH 后的质子 条件式是( D )A. [H +] + C HCl = [Ac -] + C NaOH + [OH -]B. [H +] = [Ac -] + C NaOH + C HCl + [OH -]C. [H +] + C NaOH + C HCl = [Ac -] + [OH -]D. [H +] + C NaOH = [Ac -] + [OH -] + C HCl5. 用0.1000 mol/L 的NaOH 滴定0.1000 mol/L 的HAc K a =1.7×10-5,化学计量点的pH 值是( A )。
A. 8.73B. 5.27C. 7.00D. 9.006.用0.1mol/L HCl 滴定0.1mol/L NaOH 时的pH 突跃范围是9.7~4.3,用0.01mol/L HCl 滴定0.01mol/L NaOH 的突跃范围是( C )A. 9.7~4.3B. 8.7~4.3C. 8.7~5.3D. 10.7~3.37. 用0.100 mol/L HCl 滴定同浓度NH 3溶液(pK b = 4.74)时,pH 突跃范围为6.3~4.3。
若用0.100 mol/L HCl 滴定同浓度的某碱液B (pK b = 3.74)时,pH 突跃范围为 7.3~4.3 。
8. 通常以_cK a ≥10-8 _作为判断一元弱酸能否直接进行准确滴定的条件。



第五章 吸收相组成的换算【5-1】 空气和CO 2的混合气体中,CO 2的体积分数为20%,求其摩尔分数y 和摩尔比Y 各为多少?解 因摩尔分数=体积分数,.02y =摩尔分数 摩尔比 ..020251102y Y y ===--. 【5-2】 20℃的l00g 水中溶解lgNH 3, NH 3在溶液中的组成用摩尔分数x 、浓度c 及摩尔比X 表示时,各为多少?解 摩尔分数//117=0.010*******/18x =+浓度c 的计算20℃,溶液的密度用水的密度./39982s kg m ρ=代替。
溶液中NH 3的量为 /311017n k m ol -=⨯ 溶液的体积 /.33101109982 V m -=⨯溶液中NH 3的浓度//.33311017==0.581/101109982n c kmol m V --⨯=⨯ 或 . 3998200105058218s sc x kmol m M ρ==⨯=../ NH 3与水的摩尔比的计算 或 ..00105001061100105x X x ===--. 【5-3】进入吸收器的混合气体中,NH 3的体积分数为10%,吸收率为90%,求离开吸收器时NH 3的组成,以摩尔比Y 和摩尔分数y 表示。
吸收率的定义为解 原料气中NH 3的摩尔分数0.1y = 摩尔比 (11101)01111101y Y y ===-- 吸收器出口混合气中NH 3的摩尔比为 摩尔分数 (22200111)=0010981100111Y y Y ==++ 气液相平衡【5-4】 l00g 水中溶解lg 3 NH ,查得20℃时溶液上方3NH 的平衡分压为798Pa 。
此稀溶液的气液相平衡关系服从亨利定律,试求亨利系数E(单位为kPa )、溶解度系数H[单位为/()3kmol m kPa ⋅]和相平衡常数m 。
总压为100kPa 。
解 液相中3NH 的摩尔分数/.//1170010511710018x ==+气相中3NH 的平衡分压 *.0798 P k P a = 亨利系数 *./.0798*******E p x ===/ 液相中3NH 的浓度 /./.333110170581 101109982n c kmol m V --⨯===⨯/ 溶解度系数 /*./../(3058107980728H c p k m o l m kP a ===⋅液相中3NH 的摩尔分数 //1170010511710018x ==+./气相的平衡摩尔分数 **.0798100y p p ==// 相平衡常数 * (079807610000105)y m x ===⨯ 或 //.76100076m E p === 【5-5】空气中氧的体积分数为21%,试求总压为.101325kPa ,温度为10℃时,31m 水中最大可能溶解多少克氧?已知10℃时氧在水中的溶解度表达式为*.6331310p x =⨯,式中*p 为氧在气相中的平衡分压,单位为kPa x ;为溶液中氧的摩尔分数。

1.常压下,用煤油从苯蒸汽与空气混合物吸收苯,吸收率为99%,混合气量为53kmol/h ,入塔气含苯2%(体积),入塔煤油中含苯0.02%(摩尔分率),溶剂用量为最小用量的1.5倍,在操作温度50℃下,相平衡关系为y *=0.36x ,总传质系数K Y a=0.015kmol/m 2·s ,塔径为1.1米,试求所需填料层高度(m )。
解:由题意,可得:y 1=0.02 Y 1=y 1/(1-y 1)=0.0204≈0.02 Y 2=Y 1(1—φ)=0.0204×(1—0.99)=0.0002 X ’1= Y 1/m=0.02/0.36=0.0556 X 2=0.0002 ∴(L/V)min =(Y 1—Y 2) /(x’1—x 2)=(0.02—0.0002)/[(0.0556—0.0002)=0.3577 (L/V)=1.5(L/V)min =1.5×0.3577=0.5366∴X 1=X 2+( V / L)(Y 1—Y 2)=0.0002+(1/0.5366)(0.02—0.0002)=0.0371 △Y 1=Y —Y*=0.02—0.36×0.0002=0.00664 △Y 2=Y 2—Y 2*=0.0002—0.36×0.0002=0.000128 ∴△Y m =(△Y 1—△Y 2)/ln(△Y 1/△Y 2) =(0.00664—0.000128) /ln(0.00664/0.000128)=0.00165H OG=V/(K Y a Ω)= (53/3600)/ [ (π/4×1.12) *0.015]=1.033m N OG =(Y 1—Y 2)/ △Y m=(0.02—0.0002)/0.00165=12 ∴H=H OG ×N OG=1.033×12=12.4m 2. 在一逆流操作的填料塔中,用纯矿物油吸收混合气体中的溶质,进口混合气体中溶质含量为1.5%(体积%),吸收率为85%,操作条件下的平衡关系y*=0.5x 。
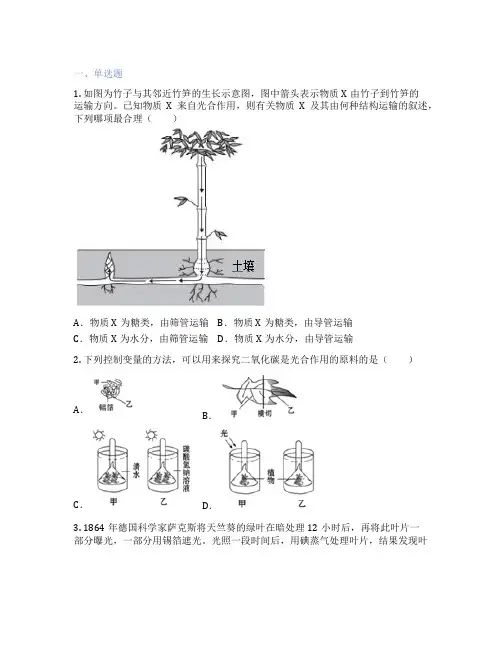
一、单选题1. 如图为竹子与其邻近竹笋的生长示意图,图中箭头表示物质X由竹子到竹笋的运输方向。
已知物质X来自光合作用,则有关物质X及其由何种结构运输的叙述,下列哪项最合理()A.物质X为糖类,由筛管运输B.物质X为糖类,由导管运输C.物质X为水分,由筛管运输D.物质X为水分,由导管运输2. 下列控制变量的方法,可以用来探究二氧化碳是光合作用的原料的是()A.B.C.D.3. 1864年德国科学家萨克斯将天竺葵的绿叶在暗处理12小时后,再将此叶片一部分曝光,一部分用锡箔遮光。
光照一段时间后,用碘蒸气处理叶片,结果发现叶片的曝光部分显蓝色,遮光部分显棕色(如图)。
该实验可以证明()A.光合作用需要叶绿素和产生了淀粉B.光合作用需要光和产生了淀粉C.光合作用需要光和叶绿素D.光合作用需要水和光4. “春雨满囤粮”。
这句俗语强调庄稼进行光合作用过程中离不开的一种重要原料是()A.水B.二氧化碳C.氧气D.淀粉5. 土豆的可食用部分是它的块茎,其中含有大量的淀粉,这些淀粉的来源是()A.由土豆果实制造的B.由叶肉细胞制造后运输到块茎细胞的C.块茎细胞利用无机物自身合成的D.块茎细胞从土壤中吸收并积累而成的6. 林地空气凉爽而湿润。
这主要是由于A.植物的光合作用和呼吸作用B.植物的分泌物有杀菌作用C.植物的光合作用和蒸腾作用D.林木遮的阳作用和植物的蒸腾作用7. 在冬季种植蔬菜的大棚中,保持一定的温度很关键,可有时温度并不高,白天还需要通风,其主要原因是()A.获得更多氧气B.获得更多二氧化碳C.获得更多新鲜空气D.通风降温8. 如图为某同学总结的光合作用公式.据图分析可知光合作用()二氧化碳+水+氧气A.有光和无光时都能进行B.把简单的有机物转变成复杂的有机物C.原料是二氧化碳、水、光D.把光能转变成化学能储存在有机物里9. 河南每年的小麦产量占全国小麦总产量的四分之一。
小麦生长过程中,种子中的有机物来自于()A.根部吸收的无机盐B.土壤中的有机物分解C.叶片进行的光合作用D.从空气中吸收的氧气10. 下列关于光合作用意义的叙述中,不正确的是()A.为植物自身提供营养物质和能量B.为动物和人提供食物和能量C.吸收氧气,放出二氧化碳,使大气中碳—氧平衡D.吸收二氧化碳,放出氧气,为动物和人类的呼吸提供氧气二、填空题11. 光合作用的主要场所是________,绿色植物制造有机物的主要器官是________。
第10章 红外吸收光谱法10-1 试说明影响红外吸收峰强度的主要因素。
答:影响红外吸收峰强度的主要因素有两方面:振动能级跃迁几率及分子振动时偶极矩变化的大小。
(1)跃迁几率越大,吸收越强。
从基态向第一激发态跃迁,即从=0跃迁至υ=1,跃迁的几率大,因此,基频吸收带一般较强。
υ(2)振动时偶极矩变化越大,吸收越强。
偶极矩变化的大小与分子结构和对称性有关。
化学键两端所连接的原子电负性差别越大,分子的对称性越差,振动时偶极矩的变化就越大,吸收就越强。
一般说来,伸缩振动的吸收强于变形振动,非对称振动的吸收强于对称振动。
10-2 HF 中键的力常数约为9N/cm 。
(1)计算HF的振动吸收峰频率;(2)计算DF 的振动吸收峰频率。
解:根据胡克定律:,。
其中σ为波数(cm -1),c 为真空中光速(3×1010cm s -1),k为化学键力常数⋅(N cm -1),因此⋅(1)HF 的振动吸收峰频率为(2)DF的振动吸收峰频率为10-3 分别在950g/L乙醇和正己烷中测定2-戊酮的红外吸收光谱,试预计νC=O吸收带在哪一溶剂中出现的频率较高?为什么?υ答:(1)C=O吸收带在正己烷中出现的频率较高。
(2)因为吸收带出现的频率和溶剂与待测物的分子间的作用有关。
2-戊酮的最强吸υ收带是羰基的伸缩振动(C=O),在乙醇中,醇羟基可与C=O形成分子间氢键,使羰基的伸缩振动频率向低波数方向移动,而正己烷不能与戊酮形成分子间氢键,因此在此溶液中的频率较高。
10-4 分子在振动过程中,有偶极矩的改变才有红外吸收。
有红外吸收的称为红外活性;相反,称为非红外活件。
指出下列振动是否有红外活性。
答:乙烯的正常振动模式如下:由红外活性的定义可知,有偶极矩的改变才有红外吸收,因此有红外活性的为②③⑤。
10-5 CS2是线性分子,试画出它的基本振动类型,并指出哪些振动是红外活性的?答:对于CS2分子,3n-5=4,即有4种振动类型。
第五章 吸收课后习题答案一、 填空1.减小;靠近。
2.不变;增加。
3.对数平均推动力法;脱吸因数法。
4.气;液;吸收;液;气;解吸5. 散装填料 二、选择1. B ;2.A ;3.C ;4.D ;5.A . 三、计算题相组成的换算【5-1】在吸收塔中用水吸收混于空气中的氨。
已知入塔混合气中氨含量为5.5%(质量分数,下同),吸收后出塔气体中氨含量为0.17%,试计算进、出塔气体中氨的摩尔比Y 1、Y 2。
解:先计算进、出塔气体中氨的摩尔分数1y 和2y 。
0903.029/945.017/055.017/055.01=+=y0029.029/9983.017/0017.017/0017.02=+=y进、出塔气体中氨的摩尔比1Y 、2Y 为10.09030.099310.0903Y ==-0029.00029.010029.02=-=Y气液相平衡【5-2】 某系统温度为10℃,总压101.3kPa ,试求此条件下在与空气充分接触后的水中,每立方米水溶解了多少克氧气?(已知10℃时,氧气在水中的亨利系数E 为3.31×106kPa 。
)解:由于ssEM Hρ≈,所以34-6A A m /kmol 1057.3181031.327.211000⨯=⨯⨯⨯===*sAs EM p Hp c ρ故 m A =3.57×10-4×32×1000=11.42 g/m 3【5-3】 在温度为40 ℃、压力为101.3 kPa 的条件下,测得溶液上方氨的平衡分压为15.0 kPa 时,氨在水中的溶解度为76.6 g (NH 3)/1 000 g(H 2O)。
试求在此温度和压力下的亨利系数E 、相平衡常数m 及溶解度系数H 。
解:水溶液中氨的摩尔分数为76.6170.07576.610001718x ==+ 由*p Ex =亨利系数为*15.0kPa 200.00.075p E x ===kPa相平衡常数为t 200.0 1.974101.3E m p === 由于氨水的浓度较低,溶液的密度可按纯水的密度计算。
1,解:(1) y =0.008 x = + y= 7.17 ⨯104 kmol 3 (3) y = = 9.875⨯10-5 kmol 3 2,解: y = 0.09 x = 0.05 y = 0.97x= 1.71⨯10-5 m 故 D G = s 1⨯ 21.52+ 20.12 粘度 (293K )μ = 1.005CP , 分子体积 V A = 3.7 + 24.6 = 28.3cm molD L = 7.4 ⨯10-8 (2.6 ⨯13)2 ⨯ 293 ()= 1.99 ⨯10-5 cm 2 s 或1.99 ⨯10-9 m 2s(96.2 +100.6)= 98.4 kN m 2 代入式P BM = ( )10 = - 0.24 ⨯10-48.314 ⨯ 295x (101.3 )(0.66 - 5.07) 5,解:查 25 C 水汽在空气中扩散系数为D = 0.256 cm s ⎛ T ⎫ 80 C 下 , D 2 = D 1 2 ⎪⎪ ⎛ 353 ⎫第七章 吸收* 10 10 17 10001718= 0.1047 m = * x = 0.008 0.01047= 0.764E = mp = 0.764 ⨯1.013⨯105 = 7.74 ⨯104PaH = C E = 55.5 7.74 ⨯104 m ⋅ Pa (2) P = 301.9KPa H,E 不变,则 m = E P = 7.74 ⨯104301.9 ⨯1030.2563 *5.9 ⨯103 301.9 ⨯103= 0.0195 x = 0.01047 m = y * x = 0.0195 0.01047= 1.862E = mp = 1.862 ⨯ 301.9 ⨯103 = 5.62 ⨯105PaH = C E = 55.5 5.62 ⨯105 m ⋅ Pa * y * = 0.97 ⨯ 0.05 = 0.0485 < y = 0.09 ∴吸收同理也可用液相浓度进行判断3,解:HCl 在空气中的扩散系数需估算。
二年级语文上册第7课《妈妈睡了》知识点总结、同步练习题【知识点】01、我会写:哄hǒng(哄人、哄我、哄逗)先xiān(首先、先生、先后)闭bì(关闭、闭门、闭合)脸liǎn(脸色、笑脸、前脸)事shì(事情、故事、事故)沉chén(沉没、沉浮、沉思)发fà(理发、头发、白发)窗chuāng(窗户、窗外、窗前)02、我会认:紧jǐn(紧张、紧闭、松紧)滋rùn(湿润、滋润、红润)等děng(等待、相等、等会儿)吸xī(呼吸、吸气、吸收)粘zhān(粘贴、粘住、粘土)汗hàn(出汗、汗水、汗珠)额é(额头、额角、前额)沙shā(沙子、沙哑、沙发)乏fá(困乏、乏了、缺乏)03、多音字:发fà(头发) fā(发现)觉jué(觉得)jiào(睡觉)04、近义词:美丽——漂亮明亮——透亮温柔——温和乌黑——漆黑05、反义词:美丽——丑陋明亮——昏暗温柔——粗暴乌黑——雪白06、理解词语:午睡:午饭后短时间的睡眠。
美丽:使人看了产生快感的;好看。
沙滩:水边或水中由沙子淤积成的陆地。
稻田:生长水稻的水田;种稻的田。
队旗:本课指中国少年先锋队的旗帜。
乌黑:深黑。
散步:随便走走。
07、句子解析:明亮的眼睛闭上了,紧紧地闭着;弯弯的眉毛,也在睡觉,睡在妈妈红润的脸上。
运用拟人化的手法,写出了睡梦中妈妈的安静,妈妈的美。
妈妈微微地笑着。
是的,她在微微地笑着,嘴巴、眼角都笑弯了,好像在睡梦中,妈妈又想好了一个故事,等一会儿讲给我听……这句话运用拟人的修辞手法,一个“笑”字,把妈妈的嘴巴、眉毛写的生动、形象。
08、问题归纳:1.眉毛会睡觉吗?为什么这样写?你能写一个这样的句子吗?眉毛不会睡觉。
作者把眉毛当作人来写,写出了睡觉中妈妈的安静与美丽。
仿写:小雨点在雨伞上跳着欢乐的舞蹈。
从本课中,你感受到母子间的什么关系?我觉得孩子爱妈妈,妈妈更爱孩子。
第15章 吸光光度法5 将1.0000 g 钢样用HNO 3溶解,钢中的锰用KIO 4氧化成KMnO 4,并稀释至100 mL 。
用1 cm 比色皿在波长525 nm 测得此溶液的吸光度为0.700。
浓度为-4-11.5210 mol L ⨯⋅的KMnO 4标准溶液在同样的条件下测得吸光度A 为0.350。
计算钢样中含Mn 的质量分数。
(0.17%)解 根据公式A c c A =⋅测测标标 -4-4-10.700=1.5210=3.0410 m o l L 0.350⨯⨯⨯⋅ -4Mn%100%1003.041054.941000 100%1.0000.17%c M ⨯⨯=⨯⨯⨯⨯=⨯=测式量冲稀因数试样重6 某溶液用5 cm 比色皿测定时,测得T 为27.9%,如改用1 cm 、3 cm 厚的比色皿时,其T 和A 各是多少?(77.5%、0.111、46.5%、0.333)解 根据公式2log A T =-,先求出5 cm 比色器时的A 值2log 2log 27.92 1.4450.555A T =-=-=-=已知b = 5 cm ,计算ac = A abc0.555 =0.1115A ac b == 计算:(1) = = = 10.111 = 0.111A abc b ac ⨯⨯log 220.111 1.899 = 77.5%T A T =-=-= (2) = = = 30.111 = 0.333A abc b ac ⨯⨯log 20.333 1.677 = 46.5% T T =-=7 用双硫腙光度法测Pb 2+,Pb 2+的浓度为0.08 mg·(50mL)-1,用2.00 cm 厚的比色皿于波长520 nm 测得T = 50%,求吸光系数a 和摩尔吸光系数ε。
(-1-14-1-193.8 L g cm 1.910 L mol cm ⋅⋅⨯⋅⋅,)解(1) 将Pb 2+换算成g·L -1和mol·L -1表示23-1[Pb ]0.08 mg /50 mL 1.610 g L c +-===⨯⋅查得Pb 的原子量 = 207.2(2) 求出此反应的A ,已知T = 50%2log 2 1.700.30A T ∴=-=-=根据:A = abc 和A = εbc ,分别求出a 和ε1130.3093.8 L g cm 2.0 1.610A a bc ---===⋅⋅⨯⨯41160.31.910 L g cm2.07.710ε---==⨯⋅⋅⨯⨯8 测定钢中的铬和锰,称取钢样0.5000 g ,溶解后移入100 mL 容量瓶中,用水稀释至刻度,摇匀,用移液管吸取25.00 mL 于锥形瓶中,加氧化剂加热,将锰氧化成MnO 4-,铬氧化成Cr 2O 72-,放冷,移入100 mL 容量瓶中,加水至刻度。
1.最小液气比(L/V)min只对()(设计型,操作型)有意义,实际操作时,若(L/V)﹤(L/V)min ,产生结果是()。
答:设计型吸收率下降,达不到分离要求2.相平衡常数m=1,气膜吸收系数k y=1×10-4Kmol/(m2.s),液膜吸收系数 k x 的值为k y 的100倍,这一吸收过程为()控制,该气体为()溶气体,气相总吸收系数K Y=() Kmol/(m2.s)。
(天大97)答:气膜易溶 9.9×10-43.某一吸收系统,若1/k y 》1/k x,则为气膜控制,若 1/k y《1/k x,则为液膜控制。
(正,误)。
答:错误,与平衡常数也有关。
4.气体吸收计算中,表示设备(填料)效能高低的一个量是传质单元高度,而表示传质任务难易程度的一个量是传质单元数。
5在吸收塔某处,气相主体浓度y=0.025,液相主体浓度x=0.01,气相传质分系数k y=2kmol/m2·h,气相传质总K y=1.5kmol/m2·h,则该处气液界面上气相浓度y i应为⎽⎽0.01⎽⎽⎽。
平衡关系y=0.5x。
6 根据双膜理论,当被吸收组分在液相中溶解度很小时,以液相浓度表示的总传质系数 B 。
A大于液相传质分系数 B 近似等于液相传质分系数C小于气相传质分系数 D 近似等于气相传质分系数7 对一定操作条件下的填料吸收塔,如将填料层增高一些,则塔的H OG将⎽⎽⎽C⎽⎽⎽,N OG将⎽⎽A⎽⎽⎽⎽。
A 增大B 减小C 不变D 不能判断8 吸收塔的设计中,若填料性质及处理量(气体)一定,液气比增加,则传质推动力 A ,传质单元数 B ,传质单元高度 C ,所需填料层高度 B 。
A 增大B 减小C 不变D 不能判断9.含SO2为10%(体积)的气体混合物与浓度C= 0.02 Kmol/m3的SO2水溶液在一个大气压下接触,操作条件下两相的平衡关系为 p*=1.62 C (大气压),则 SO2将从()相向()转移,以气相组成表示的传质总推动力为()大气压,以液相组成表示的传质总推动力为()Kmol/m3 。
1、吸收剂部分再循环对塔高的影响 常压逆流连续操作的吸收塔,用清水吸收空气-氨混合气中的氨,混合气的流率为0.02kmol/(m 2.s ),入塔时氨的浓度为0.05(摩尔分率,下同),要求吸收率不低于95%,出塔氨水的浓度为0.05。
已知在操作条件下气液平衡关系为y *=0.95x ,,气相体积传质总系数K y a=0.04kmol/(m 3.s ),且K y a ∝G 0.8 。
(1)所需填料层高度为多少?(2)采用部分吸收剂再循环流程,新鲜吸收剂与循环量之比L/L R =20,气体流率及新鲜吸收剂用量不变,为达到分离要求,所需填料层的高度为多少?(3)示意绘出带部分循环与不带循环两种情况下的操作线与平衡线。
(4)求最大循环量L R(max) 。
解:(1) 低浓气体吸收,y Y x X ≈≈,()()y y a b =-=-⨯=1109500500025η...液气比:L G y y x x =--=-=b a b a 00500025005095....而 m LG ==095.,所以S =1∆∆y y y m a a ===00025.N y yy OG b a m =-=-=∆00500025002519...又 H GK a y OG m ===00200405...∴==⨯=h H N 0051995OG OG m ..(2) 吸收剂再循环此时吸收剂入口浓度:00238.012005.0R bR a a =+=++='L L xL Lx x塔'=+=+=L L L L L L R 120105.95.005.11'==='L mGS因为为易溶气体,且K a G y ∝08.所以L 再循环后,K a y 不变,即H G K ay OG m ==05.不变 ()()'=-'-'-'-'+'⎡⎣⎢⎤⎦⎥=---⨯-⨯+⎡⎣⎢⎤⎦⎥=N S S y mx y mx S OG b a a a 111110951095005095000238000250950002380954784ln .ln ......... ∴'='=⨯=h H N 00547842392OG OG m ... (3)见上图。
(4)当循环量加大,↑'a x ,当my x x a a =='*a 时,气液两相在塔顶平衡,0=∆a y ,达到分离要求,塔高无限,此时,循环量为最大循环量。
'(max)(max))(a R b R a x L L x L Lx +=+,00263.095.00025.0*a===='m y x x a a s)kmol/(m 10055.100263.005.000263.095.002.023''(max)⋅⨯=-⨯⨯=-=-a b aR x x Lx L 从计算结果可以看出,吸收剂部分再循环,吸收塔进口液体溶质浓度增加,平均传质推动力减小,若过程为气膜控制,循环吸收剂流量增加,传质系数a K y 不变,所以导致吸收塔塔高增加。
问题:从上述结果看吸收剂部分循环对吸收是不利的,但工业上为什么有时还采用这种操作呢?在下列情况下采用循环总的看来是有利的:(1)若吸收过程的热效应很大,以至吸收剂进吸收塔前需要塔外冷却来降低吸收温度,这样相平衡常数m 降低,全塔平均推动力提高,祢补了因部分再循环吸收塔进口液体溶质浓度增加导致的平均传质推动力减小。
(2)若吸收工艺要求较小的新鲜吸收剂用量,以至不能保证填料被很好的润湿,致使单位体积填料有效传质面积降低,此时采用吸收剂部分再循环,提高单位体积填料有效传质面积,即提高体积传质系数,补偿了因循环而降低吸收推动力,如果总体上仍使塔高降低,使用再循环是有意义的。
2、提高吸收率的具体措施在填料高度为4m 的常压填料塔中,用清水吸收尾气中的可溶组分。
已测得如下数据:尾气入塔组成为0.02,吸收液排出的浓度为0.008(以上均为摩尔分率),吸收率为0.8,并已知此吸收过程为气膜控制,气液平衡关系为y *=1.5x 。
(1)计算该塔的H OG 和N OG ; (2)操作液气比为最小液气比的倍数; (3)若法定的气体排放浓度必须 ≤0.002,可采取哪些可行的措施?并任选其中之一进行计算,求出需改变参数的具体数值;(4)定性画出改动前后的平衡线和操作线。
解:(1) y b =<0025%10%.~可当作低浓气体吸收,y Y x X ≈≈,()()y y a b =-=-⨯=11080020004η...L G y y x x =--=-=b a b a 002000400082... S mG L ===152075.. ()()N S S y mx y mx S OG b a a a =----+⎡⎣⎢⎤⎦⎥=--+⎡⎣⎢⎤⎦⎥=11111075107500200040752773ln .ln .....∴===H h N OG OG m 0427731443..(2) L G y y x x y y y m x ⎛⎝ ⎫⎭⎪=--=--=⨯=*min ...ba b a b a b a150812 ∴⎛⎝ ⎫⎭⎪⎛⎝ ⎫⎭⎪==L G L G min ..2121667(3) 可采取的措施:a.增加填料层高度H G K a y OG =不变(G 不变,气膜控制K a y 不变) S mG L==075.不变 ()()'=---'-+⎡⎣⎢⎤⎦⎥=--+⎡⎣⎢⎤⎦⎥=N S S y mx y mx S OG b a a a 11111075107500200020754715ln .ln .....∴'='=⨯=h H N 014434715680OG OG m ...∴'==∆h h 0028470%. b.增大用水量因为G 不变,气膜控制,所以K a y 不变,H OG 不变又h 0不变,所以N OG 也不变 即 ()'=-'-'-'-+'⎡⎣⎢⎤⎦⎥N S S y mx y mx S OG b a a a 111ln()27731110020002.ln ..=-'-'+'⎡⎣⎢⎤⎦⎥S S S试差'=S 027.或由N S y mx y mx OG b a a a ~~--图,查得'=S 027. '='==L L S S 075027278... c.其它操作条件不变,降低操作温度,m 变小,↓=L mG S ,而塔高、气相总传质单元高度、气相总传质单元数不变,根据()⎥⎦⎤⎢⎣⎡+----=S mx y mx y S S N a a a b OG 1ln 11的关系图可知,↑⎥⎦⎤⎢⎣⎡a b y y ,y b 不变,故气体出口浓度y a 降低。
d.其它操作条件不变,增大操作压力,由p E m =,m 变小,↓=LmG S ,而塔高、气相总传质单元高度、气相总传质单元数不变,根据()⎥⎦⎤⎢⎣⎡+----=S mx y mx y S S N a a a b OG 1ln 11的关系图可知,↑⎥⎦⎤⎢⎣⎡a b y y ,y b 不变,故气体出口浓度y a 降低。
e.其它条件不变,选用对溶质溶解度大的吸收剂,即m 小。
与c 、d 分析相同,得到y a 降低。
f. 其它条件不变,改用另一种吸收性能较好的填料,提高吸收总传质系数及单位体积填料的有效传质面积增大,即↑a K Y ,气相总传质单元高度变小,塔高不变,气相总传质单元数变大,又因S 也不变,故根据()⎥⎦⎤⎢⎣⎡+----=S mx y mx y S S N a a a b OG 1ln 11的关系图可知,↑⎥⎦⎤⎢⎣⎡a b y y ,y b 不变,故气体出口浓度y a 降低。
从本题的结果看:工业上提高吸收率,降低出口气体浓度的具体措施可以从吸收过程的设计方面入手,如增加塔高、改换吸收剂及改用性能良好的填料。
另外一方面从吸收操作方面入手降低气体出口浓度更为方便,如降低吸收温度、提高吸收压力、适度增大吸收剂用量,若非清水为吸收剂,还可降低吸收剂入口浓度。
3、气液流动方式对吸收过程的影响 用吸收操作除去某气体混合物中的可溶有害组分,在操作条件下的相平衡关系为Y *=1.5X ,混合气体的初始浓度为0.1(摩尔比,下同),吸收剂的入塔浓度为0.001,液气比为2.0。
已知在逆流操作时,气体出口浓度为0.005,试计算在操作条件不变的情况下改为并流操作,气体的出口浓度为多少?逆流操作时所吸收的可溶组分是并流操作的多少倍?计算时近似认为K Y a 与流动方式无关。
解:原工况:逆流操作时()()X G L Y Y X b B S b a a =-+=-+=12010005000100485....∆Y Y mX a a a =-=-⨯=000515000100035....∆Y Y mX b b b =-=-⨯=010048515002725.... ()∆∆∆∆∆Y Y Y Y Y m b a b a ln =-⎛⎝ ⎫⎭⎪=-=0027250003500272500035001157..ln ...∴=-=-=N Y Y Y OG b a m ∆010005001157821....新工况:并流操作时h H N H N 0==OG OG OG OG 逆逆并并H G K a y OG =不变,所以N OG 不变即并流后'=N OG 821.物料衡算:()()L X X G Y Y S b a B a b '-=-' ()()∴'=-'+=-'+=-'X G L Y Y X Y Y b B S a b a b b 12010001005105....(1)∆'=-Y Y mX a a a∆'='-'Y Y mX b b b ()()()()∆∆∆∆∆'='-'''⎛⎝ ⎫⎭⎪=--'-'-'-'⎛⎝ ⎫⎭⎪=-'+'--'-'⎛⎝ ⎫⎭⎪Y Y Y Y Y Y mX Y mX Y mX Y mX Y Y m X X Y mX Y mX m a b a b a a b b a a b b a b b a a a b bln ln ln()()()()∴=-''=-'-'+'--'-'=-'-'+-'-'-'=+-'-'N Y Y Y Y Y Y Y m X X Y mX Y mX Y Y Y Y mG LY Y Y mX Y mX mG L Y mX Y mX OG a b m a b a b b a a a b b a b a b a b a a b b a a b b ∆ln ln ln 11∴=+-⨯'-'821111520115000115..ln ....Y X b b'-'=⨯-Y X b b 1556717108.. (2)式(1)和(2)联立:'=Y b 00437.,'=X b 00292.逆流与并流所吸收溶质量之比: ()()m m G Y Y G Y Y 逆并=--'=--=B b aB a b 01000501004371687..... 从本题的结果可以看出,在同一吸收塔,若操作条件完全相同,逆流操作的吸收效果好于并流操作,吸收液从塔底流出之前与入塔气接触,可得到浓度较高的吸收液。