分子晶体有哪些物理特性,为什么?
2、物理特性:
(1)较低的熔点和沸点,易升华; (2)较小的硬度; (3)一般都是绝缘体,熔融状态也不导电。
原因:分子间作用力较弱
3、典型的分子晶体:
–非金属氢化物:H2O,H2S,NH3,CH4,HX –酸:H2SO4,HNO3,H3PO4 –部分非金属单质:X2,O2,H2, S8,P4, C60 –部分非金属氧化物: CO2, SO2, NO2, P4O6, P4O10 –大多数有机物:乙醇,冰醋酸,蔗糖
思考与交流
石墨和金刚石同属于碳的单质,为什么在硬度上会相 差如此之大?
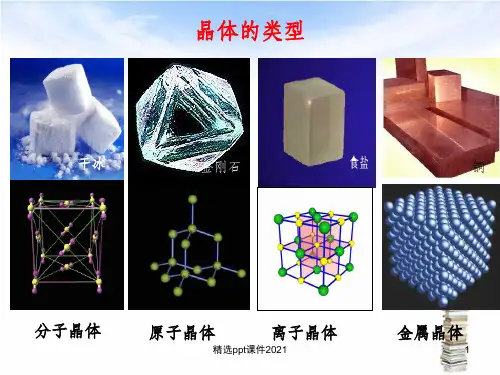
观察与思考: 下列两种晶体有什么共同点?
干冰晶体结构
碘晶体结构
一、分子晶体
1、概念
分子间以分子间作用力(范德华力,氢键)相 结合的晶体叫分子晶体
(1)构成分子晶体的粒子是分子。 (2)粒子间的相互作用是分子间作用力。 (3)范德华力远小于化学键的作用; (4)分子晶体熔化破坏的是分子间作用力。
〖思考3〗为何干冰的熔沸点比冰低,密 度却比冰大? 由于冰中除了范德华力外还有氢键作用, 破坏分子间作用力较难,所以熔沸点比干冰高。 由于分子间作用力特别是氢键的方向性, 导致晶体中有相当大的空隙,所以相同状况下 体积较大 由于CO2分子的相对分子质量>H2O,所 以干冰的密度大。
科学视野:笼装化合物
• 〖思考1〗是不是在分子晶体中分子间只存在 范德华力?
不对,分子间氢键也是一种分子间作用力, 如冰中就同时存在着范德华力和氢键。
• 〖思考2〗为什么冰融化为水时,密度增大? 在冰晶体中,每个分子周围只有4个紧邻的水分子, 由于水分子之间的主要作用力是氢键,氢键跟共价 键一样具有方向性,即氢键的存在迫使在四面体中 心的每个水分子与四面体顶角方向的4个相邻水分 子相互吸引,这一排列使冰晶体中的水分子的空间 利用率不变,留有相当大的空隙。当冰刚刚融化为 液态水时,热运动使冰的结构部分解体,水分子间的 空隙减小,密度反而增大。