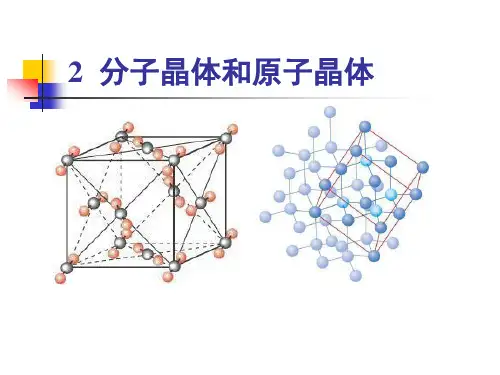
Na+
Cl-
晶胞中的氯离子数=12× 1 +1=4
钠离子数 = 8× 1
8
+ 6×4 12
= 4。
即钠离子与氯离子个数比为4:4=1:1,
故氯化钠的化学式为NaCl
CsCl晶体的结构:
(2)CsCl:体心立方结构(基本结构单元是体心 立方体)
5、每个Cs+离子周围有__8__个Cl-离子,每 个Cl- 离子周围有___8_个Cs+ 离子
状结构的晶体。
如金刚石是以碳碳单键结合而成的正四面
体的空间网状结构。
键长 :1.55×10-10m 键角:109°28′
熔点: 3550℃
沸点:4827℃
性质:熔沸点高,硬度大,难溶于一般溶剂。
课堂练习题
下列不存在化学键的晶体是:
A.硝酸钾 B.干冰 C.石墨 D.固体氩
常温常压下的分子晶体是:
阴、阳 离子
离子键
较高
较 硬
易溶于 极性溶
剂
导电性
溶于水 或熔融 时导电
思考题: 离子晶体的熔、沸点,硬度与离子键强 弱有何关系?为什么?
思考2 比较NaCl、CsCl熔点和沸点的高低
NaCl CsCl
熔点
8010C 6450C
沸点
14130C 12900C
为什么NaCl 的熔点和沸点比CsCl的高?
•
5、心情就像衣服,脏了就拿去洗洗,晒晒,阳光自然就会蔓延开来。阳光那么好,何必自寻烦恼,过好每一个当下,一万个美丽的未来抵不过一个温暖的现在。
•
6、无论你正遭遇着什么,你都要从落魄中站起来重振旗鼓,要继续保持热忱,要继续保持微笑,就像从未受伤过一样。