硫酸硫酸盐和硫酸的工业制法
- 格式:doc
- 大小:280.00 KB
- 文档页数:3



硫酸的工业制法三个方程式
硫酸是一种重要的化工原料,在工业上有几种制备方法。
其中最常见的三种制法分别为铁硫矿氧化法、硫三氧化二硫催化剂法和硫酸盐矿石法。
首先是铁硫矿氧化法,其化学方程式为,2FeS2 + 7O2 + 2H2O → 2FeSO4 + 2H2SO4。
这个过程中,铁硫矿(黄铁矿)被氧化成硫酸铁和硫酸。
其次是硫三氧化二硫催化剂法,其化学方程式为,2SO2 + O2 → 2SO3。
这个过程中,二氧化硫被氧化成三氧化硫,而后者溶于水形成硫酸。
最后是硫酸盐矿石法,其化学方程式为,CaSO4 + 2C + O2 → 2CO2 + 2CO + 2SO2 + CaS。
这个过程中,硫酸盐矿石(石膏)经过还原反应生成二氧化硫,再经过催化氧化反应生成硫三氧化二硫,最终形成硫酸。
这三种工业制法分别从硫化物、二氧化硫和硫酸盐矿石出发,通过不同的化学反应途径最终制得硫酸。
这些方程式展示了硫酸的
工业制备过程,每个方程式都代表着不同的反应路径和条件。
希望这些信息能够满足你的需求。


工业制硫酸反应方程式引言硫酸是一种广泛应用于工业生产和实验室的重要化学品。
它是一种无色、无臭的液体,具有强酸性。
硫酸的制备方法有很多种,其中工业制硫酸反应方程式是最常用的一种方法之一。
本文将详细介绍工业制硫酸反应方程式的原理、条件和具体步骤。
工业制硫酸反应方程式的原理工业制硫酸的反应方程式是一种氧化还原反应。
具体来说,硫酸的制备是通过将硫磺或硫化物氧化为二氧化硫,然后再将二氧化硫进一步氧化为三氧化硫,最后与水反应生成硫酸的过程。
反应方程式如下所示:2 SO2 + O2 → 2 SO3SO3 + H2O → H2SO4在这个反应过程中,二氧化硫和氧气首先反应生成三氧化硫。
然后,三氧化硫与水反应生成硫酸。
整个过程是一个连续的反应链,需要适当的温度、压力和催化剂的存在。
工业制硫酸反应方程式的条件工业制硫酸的反应条件如下: - 温度:反应温度通常在400-500°C之间,这是为了保证反应速率和产率的最优化。
- 压力:反应压力通常在1-2 atm之间,这是为了保持反应体系的稳定性和安全性。
- 催化剂:反应需要催化剂的存在,常用的催化剂有铁、钒等金属催化剂。
工业制硫酸反应方程式的步骤工业制硫酸的反应步骤如下: 1. 原料准备:将硫磺或硫化物作为反应的原料,将其加入反应釜中。
2. 氧化反应:加热反应釜,使硫磺或硫化物与氧气反应生成二氧化硫。
这个过程需要控制温度和压力。
3. 催化反应:将二氧化硫和氧气进一步反应,生成三氧化硫。
催化剂的存在可以加速这个反应。
4. 吸收反应:将三氧化硫与水反应,生成硫酸。
这个过程需要控制温度和压力,并且需要适当的吸收剂来吸收生成的硫酸。
5. 分离与纯化:将反应产物进行分离和纯化,得到高纯度的硫酸。
工业制硫酸反应方程式的应用工业制硫酸的反应方程式是制备硫酸的重要方法,硫酸在工业生产中有广泛的应用,包括但不限于以下几个方面: - 化肥生产:硫酸是制造化肥的重要原料,可以用于制造磷酸二氢铵、硫酸铵等化肥。
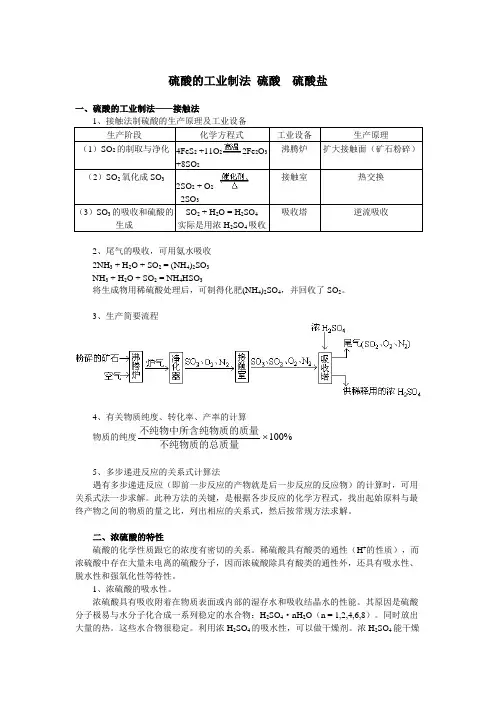
硫酸的工业制法硫酸硫酸盐一、硫酸的工业制法——接触法1、接触法制硫酸的生产原理及工业设备生产阶段化学方程式工业设备生产原理(1)SO2的制取与净化4FeS2+11O22Fe2O3+8SO2沸腾炉扩大接触面(矿石粉碎)(2)SO2氧化成SO32SO2 + O22SO3接触室热交换(3)SO3的吸收和硫酸的生成SO2 + H2O = H2SO4实际是用浓H2SO4吸收吸收塔逆流吸收2、尾气的吸收,可用氨水吸收2NH3 + H2O + SO2 = (NH4)2SO3NH3 + H2O + SO2 = NH4HSO3将生成物用稀硫酸处理后,可制得化肥(NH4)2SO4,并回收了SO2。
3、生产简要流程4、有关物质纯度、转化率、产率的计算物质的纯度不纯物中所含纯物质的质量不纯物质的总质量100%5、多步递进反应的关系式计算法遇有多步递进反应(即前一步反应的产物就是后一步反应的反应物)的计算时,可用关系式法一步求解。
此种方法的关键,是根据各步反应的化学方程式,找出起始原料与最终产物之间的物质的量之比,列出相应的关系式,然后按常规方法求解。
二、浓硫酸的特性硫酸的化学性质跟它的浓度有密切的关系。
稀硫酸具有酸类的通性(H+的性质),而浓硫酸中存在大量未电离的硫酸分子,因而浓硫酸除具有酸类的通性外,还具有吸水性、脱水性和强氧化性等特性。
1、浓硫酸的吸水性。
浓硫酸具有吸收附着在物质表面或内部的湿存水和吸收结晶水的性能。
其原因是硫酸分子极易与水分子化合成一系列稳定的水合物:H2SO4·nH2O(n = 1,2,4,6,8)。
同时放出大量的热。
这些水合物很稳定。
利用浓H2SO4的吸水性,可以做干燥剂。
浓H2SO4能干燥H 2、O 2、CO 等中性气体,也能干燥SO 2、Cl 2、CO 2、HCl 、HF 等酸性气体;但不能干燥NH 3等碱性气体,也不能干燥HBr 、HI 、H 2S 等有强还原性的气体。
2、浓硫酸的脱水性。
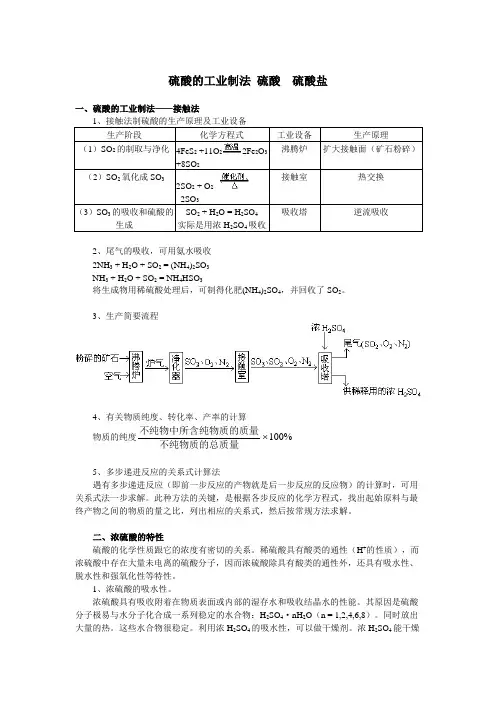
硫酸的工业制法硫酸硫酸盐一、硫酸的工业制法——接触法1、接触法制硫酸的生产原理及工业设备生产阶段化学方程式工业设备生产原理(1)SO2的制取与净化4FeS2+11O22Fe2O3+8SO2沸腾炉扩大接触面(矿石粉碎)(2)SO2氧化成SO32SO2 + O22SO3接触室热交换(3)SO3的吸收和硫酸的生成SO2 + H2O = H2SO4实际是用浓H2SO4吸收吸收塔逆流吸收2、尾气的吸收,可用氨水吸收2NH3 + H2O + SO2 = (NH4)2SO3NH3 + H2O + SO2 = NH4HSO3将生成物用稀硫酸处理后,可制得化肥(NH4)2SO4,并回收了SO2。
3、生产简要流程4、有关物质纯度、转化率、产率的计算物质的纯度不纯物中所含纯物质的质量不纯物质的总质量100%5、多步递进反应的关系式计算法遇有多步递进反应(即前一步反应的产物就是后一步反应的反应物)的计算时,可用关系式法一步求解。
此种方法的关键,是根据各步反应的化学方程式,找出起始原料与最终产物之间的物质的量之比,列出相应的关系式,然后按常规方法求解。
二、浓硫酸的特性硫酸的化学性质跟它的浓度有密切的关系。
稀硫酸具有酸类的通性(H+的性质),而浓硫酸中存在大量未电离的硫酸分子,因而浓硫酸除具有酸类的通性外,还具有吸水性、脱水性和强氧化性等特性。
1、浓硫酸的吸水性。
浓硫酸具有吸收附着在物质表面或内部的湿存水和吸收结晶水的性能。
其原因是硫酸分子极易与水分子化合成一系列稳定的水合物:H2SO4·nH2O(n = 1,2,4,6,8)。
同时放出大量的热。
这些水合物很稳定。
利用浓H2SO4的吸水性,可以做干燥剂。
浓H2SO4能干燥H 2、O 2、CO 等中性气体,也能干燥SO 2、Cl 2、CO 2、HCl 、HF 等酸性气体;但不能干燥NH 3等碱性气体,也不能干燥HBr 、HI 、H 2S 等有强还原性的气体。
2、浓硫酸的脱水性。


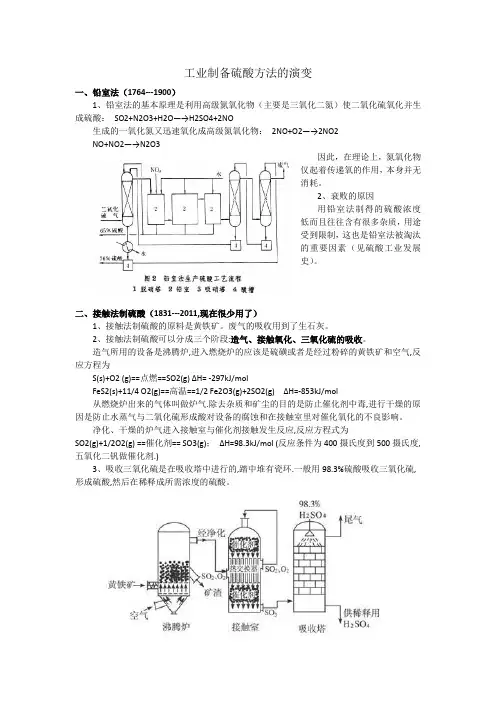
工业制备硫酸方法的演变一、铅室法(1764---1900)1、铅室法的基本原理是利用高级氮氧化物(主要是三氧化二氮)使二氧化硫氧化并生成硫酸:SO2+N2O3+H2O—→H2SO4+2NO生成的一氧化氮又迅速氧化成高级氮氧化物:2NO+O2—→2NO2NO+NO2—→N2O3因此,在理论上,氮氧化物仅起着传递氧的作用,本身并无消耗。
2、衰败的原因用铅室法制得的硫酸浓度低而且往往含有很多杂质,用途受到限制,这也是铅室法被淘汰的重要因素(见硫酸工业发展史)。
二、接触法制硫酸(1831---2011,现在很少用了)1、接触法制硫酸的原料是黄铁矿。
废气的吸收用到了生石灰。
2、接触法制硫酸可以分成三个阶段:造气、接触氧化、三氧化硫的吸收。
造气所用的设备是沸腾炉,进入燃烧炉的应该是硫磺或者是经过粉碎的黄铁矿和空气,反应方程为S(s)+O2 (g)==点燃==SO2(g) ΔH= -297kJ/molFeS2(s)+11/4 O2(g)==高温==1/2 Fe2O3(g)+2SO2(g) ΔH=-853kJ/mol从燃烧炉出来的气体叫做炉气.除去杂质和矿尘的目的是防止催化剂中毒,进行干燥的原因是防止水蒸气与二氧化硫形成酸对设备的腐蚀和在接触室里对催化氧化的不良影响。
净化、干燥的炉气进入接触室与催化剂接触发生反应,反应方程式为SO2(g)+1/2O2(g) ==催化剂== SO3(g);ΔH=98.3kJ/mol (反应条件为400摄氏度到500摄氏度,五氧化二钒做催化剂.)3、吸收三氧化硫是在吸收塔中进行的,踏中堆有瓷环.一般用98.3%硫酸吸收三氧化硫,形成硫酸,然后在稀释成所需浓度的硫酸。

总结硫酸生产工艺硫酸是一种广泛应用于化工、冶金、环保等行业的重要化工原料。
目前,硫酸的生产主要在工业规模上存在两种工艺:硫磺制酸法和硫氧化制酸法。
以下是对这两种工艺的简要总结。
一、硫磺制酸法:硫磺制酸法是一种传统的硫酸生产工艺,其主要步骤包括硫磺的燃烧、氧化产生二氧化硫、氧化反应生成三氧化硫、与水反应生成硫酸的吸收过程。
硫磺燃烧:硫磺通过燃烧产生二氧化硫。
传统的硫磺制酸法采用炉窑燃烧硫磺,炉温控制在1200-1300℃,燃烧后产生硫磺氧化物。
氧化反应:氧化反应是硫磺制酸的关键步骤,其中的氧化反应主要有两步:硫磺氧化生成二氧化硫,二氧化硫进一步氧化生成三氧化硫。
这两个反应是通过催化剂的存在来加速进行的。
硫酸吸收:三氧化硫与吸收剂(通常为浓硫酸)进行反应,生成硫酸。
反应发生在吸收塔中,通过吸收器的设置,将吸收剂花洒在塔上,与上方从塔底部喷出的三氧化硫气体进行接触,吸收生成硫酸的气体。
二、硫氧化制酸法:硫氧化制酸法是一种比较新的硫酸生产工艺,主要步骤包括硫的含氧化物的形成、催化剂催化转化、尾气净化和吸收生成硫酸的过程。
硫化物氧化:硫化物氧化是硫氧化制酸的关键步骤,其中的硫化物可以来自于石油加工过程产生的硫化氢和石膏、矿石中的硫酸盐等。
硫化物在反应器中通过氧化剂(如空气或氧气)氧化生成硫的含氧化物。
催化剂催化转化:在氧化反应中,硫的含氧化物通过催化剂的作用进行催化转化,生成二氧化硫。
尾气净化:硫氧化制酸法中产生的尾气中含有二氧化硫和少量的氧化副产物,需要通过脱硫、脱氮等净化工艺进行处理,以达到环保要求。
吸收生成硫酸:净化后的气体进入吸收器,与硫酸或硫酸溶液进行接触,吸收生成硫酸的气体。
总结:目前,硫磺制酸法和硫氧化制酸法是较为常用的硫酸生产工艺。
硫磺制酸法是传统的工艺,流程较为简单,但存在炉温高、能源消耗大等缺点。
而硫氧化制酸法相对较新,流程中采用催化剂催化转化,在尾气净化方面更加环保,但在硫化物氧化和脱硫等方面存在一定的技术难度。
第1篇一、概述硫酸是一种重要的无机化工原料,广泛应用于化肥、农药、冶金、石油、医药、造纸、玻璃、染料等工业部门。
硫酸的生产方法主要有接触法、接触法-转化法、转化法、转化法-转化法等。
本文以接触法为例,详细介绍硫酸的生产工艺流程。
二、原料及设备1. 原料:硫磺、空气、水。
2. 设备:沸腾炉、转化炉、吸收塔、接触室、鼓风机、压缩机、泵、冷却器、加热器、冷凝器、过滤器、分离器、真空泵等。
三、生产工艺流程1. 硫磺燃烧将硫磺送入沸腾炉,在沸腾炉中与空气混合,在高温(800℃-1000℃)下进行燃烧,生成二氧化硫(SO2)。
反应方程式:S + O2 → SO22. 二氧化硫转化将燃烧生成的SO2气体送入转化炉,与水蒸气在催化剂的作用下进行转化反应,生成三氧化硫(SO3)。
反应方程式:2SO2 + O2 → 2SO33. 三氧化硫吸收将转化炉生成的SO3气体送入吸收塔,与水进行反应,生成硫酸。
反应方程式:SO3 + H2O → H2SO44. 硫酸浓缩将吸收塔中生成的硫酸溶液送入接触室,进行浓缩。
浓缩过程中,硫酸溶液与空气混合,加热至沸点,使部分水分蒸发,提高硫酸浓度。
5. 硫酸冷却将浓缩后的硫酸溶液送入冷却器,进行冷却,使其温度降至常温。
6. 硫酸分离将冷却后的硫酸溶液送入分离器,分离出硫酸和未反应的水蒸气。
7. 硫酸储存与输送将分离出的硫酸溶液储存于硫酸储罐中,待使用时通过泵送至用户。
四、生产工艺参数1. 硫磺燃烧温度:800℃-1000℃2. 转化炉温度:450℃-500℃3. 吸收塔温度:50℃-60℃4. 硫酸浓度:98%5. 催化剂活性:95%五、生产工艺特点1. 生产效率高:接触法生产工艺具有生产效率高、设备简单、操作方便等优点。
2. 原料来源广泛:硫磺资源丰富,且价格相对较低。
3. 环保:接触法生产工艺在燃烧过程中,SO2排放量较小,对环境污染相对较小。
4. 产品质量稳定:采用接触法生产工艺生产的硫酸,质量稳定,产品纯度高。
硫酸生产工艺流程知识分享硫酸生产是化学工业中最重要的基础化学品之一,广泛用于肥料、农药、石油炼制、纺织、橡胶、塑料等行业。
下面将详细介绍硫酸的生产工艺流程。
硫酸的生产工艺主要包括硫磺燃烧、烟气净化、氧化和吸收四个步骤。
第一步,硫磺燃烧:硫磺燃烧是硫酸生产的第一步,可以利用燃烧炉或燃烧器将硫磺与空气中的氧气反应生成二氧化硫:S+O2→SO2实际生产中,通常使用硫磺过炉进行燃烧,将硫磺粉末连续送入过炉,与高炉煤气混合并点燃,产生高温燃烧气体。
硫磺燃烧产生的燃烧废气中含有大量的SO2第二步,烟气净化:烟气净化主要是对燃烧产生的烟气进行净化处理,以去除其中的不纯物质,保护环境。
常见的净化方法有洗涤法和干法。
洗涤法:将燃烧废气通过吸收塔,并喷洒反应液,通过反应将废气中的SO2转化为硫酸。
常用的反应液有硫酸,氢氧化钠等。
干法:利用催化剂吸附或催化氧化烟气中的SO2,将其转化为SO3或硫酸。
如在烟气中加入V2O5催化剂进行吸附和氧化反应,生成SO3第三步,氧化:氧化是将烟气中的二氧化硫(SO2)进一步氧化为三氧化硫(SO3)的反应。
SO2+O2→2SO3常用的氧化剂有空气、氧气、过氧化氢等。
氧化反应通常在催化剂存在下进行,如使用V2O5催化剂,常温下即可完成反应。
第四步,吸收:吸收是将氧化后的SO3溶解到水中生成硫酸的反应。
SO3+H2O→H2SO4吸收通常使用带液气拖曳剂的吸收塔进行,塔内内径方向分布有多层放气板。
气体从底部进入,底层放气板将液体拖动到上层放气板,使两相进行充分接触反应,将SO3转化为硫酸。
整个硫酸生产过程中,需要注意以下几个问题:1.硫酸生产需要大量的能量供应,所以需要考虑能源的合理利用,减少能源的消耗。
2.硫酸生产中,烟尘和废气中含有大量的SO2,对环境造成严重污染。
因此,需要采取合适的净化措施,确保产生的硫酸符合环保要求。
3.在硫酸生产过程中,需要严格控制反应条件和操作参数,以确保反应的高效进行,提高硫酸的产量和质量。
第2课时硫酸硫酸根离子的检验[核心素养发展目标] 1.了解硫酸的工业制法及常见的硫酸盐。
2.掌握浓H2SO4的性质及重要实验现象。
3.掌握SO2-4的检验方法。
一、硫酸的性质及工业制法1.硫酸的工业制法硫酸是重要的化工原料,可用于生产____、________、________、染料和盐类等,工业上一般以________或其他____________(如黄铁矿)为原料来制备硫酸。
制备过程中反应的化学方程式如下:①制气:燃烧硫黄:____________________,煅烧黄铁矿:_________________________;②氧化:2SO2+O2催化剂2SO3;△③吸收:__________________________________________。
特别提醒工业制备硫酸工艺中常用98.3%浓硫酸而不用水吸收SO3,因为SO3与H2O剧烈反应放热,易产生酸雾,影响SO3的吸收。
2.硫酸的性质(1)稀硫酸硫酸在水里很容易电离出________,具有________,能使石蕊溶液变红,写出稀硫酸与下列物质反应的离子方程式。
①活泼金属Fe:_______________________________________________;②金属氧化物CuO:___________________________________________;③碱Mg(OH)2:_______________________________________________;④盐BaCO3:_________________________________________________。
(2)浓硫酸浓硫酸有三大特性:________、________和________。
①吸水性浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作________。
思考1浓硫酸做干燥剂,可以干燥哪些气体,不能干燥哪些气体?________________________________________________________________________②脱水性浓硫酸能将蔗糖、纸张、棉布和木材等________中的氢和氧按________________脱去。
有关硫酸知识点总结图硫酸的制备方法硫酸的制备方法主要有两种:硫磺氧化法和硫酸盐氧化法。
1. 硫磺氧化法硫磺氧化法是制备硫酸的主要方法之一。
它的化学反应式为:S + O2 + 2H2O -> H2SO4硫磺在空气中加热后,会与氧气反应生成二氧化硫(SO2),再与空气中的氧气进一步反应生成硫酸。
硫磺氧化法是比较常用的工业生产方法,但也存在环境污染和能源消耗较大的问题。
2. 硫酸盐氧化法另一种制备硫酸的方法是硫酸盐氧化法,即利用硫酸盐来制备硫酸。
其中,二氧化硫(SO2)是通过熔融硫酸盐(如石膏)加热而得到溶液。
制备过程如下:CaSO4 + C -> CaO + SO2 + CO2CaO + H2SO4 -> CaSO4 + H2O通过以上反应,可得到硫酸。
硫酸的物理性质硫酸是一种无色、无臭的油状液体,有极强的腐蚀性。
在常温下,硫酸呈浓缩的状况,但随着温度的升高,它可以逐渐变成无水的状况。
此外,在纯硫酸中,会有一些杂质和不溶性物质。
硫酸的化学性质硫酸具有极强的腐蚀性,可以和许多物质发生化学反应。
主要的化学性质包括:1. 与金属的反应硫酸可以和金属发生置换反应,生成相应的金属硫酸盐和氢气。
这种反应对金属有腐蚀作用。
2. 与碱性物质的反应硫酸是一种强酸,所以它能够和碱反应生成盐和水的中和反应。
3. 与有机物的反应硫酸在有机合成中有重要的应用,可以用来进行酯化和硫酸酯化反应,生成有机硫酸酯。
硫酸的应用硫酸有许多重要的应用,主要包括以下几个方面:1. 用于生产肥料硫酸是化肥生产的重要原料,可以和氢氧化钙反应生成硫酸钙,用于土壤的改良和植物的生长。
2. 用于工业生产硫酸可以用于制造清洁剂、肥皂和其他化学品,也可以用于金属加工和腐蚀清除。
3. 用于储能硫酸铅蓄电池是电动汽车和太阳能储能系统中常见的一种电池,其中使用的是硫酸电解质。
硫酸的危害硫酸是一种具有强酸性和腐蚀性的化合物,对人体和环境都有一定的危害。
硫酸 硫酸盐和硫酸的工业制法
一、硫酸的工业制法——接触法
22、尾气的吸收,可用氨水吸收
2NH 3 + H 2O + SO 2 = (NH 4)2SO 3 NH 3 + H 2O + SO 2 = NH 4HSO 3
将生成物用稀硫酸处理后,可制得化肥(NH 4)2SO 4,并回收了SO 2。
3、生产简要流程
4、有关物质纯度、转化率、产率的计算
物质的纯度
不纯物中所含纯物质的质量
不纯物质的总质量
⨯100%
5、多步递进反应的关系式计算法
遇有多步递进反应(即前一步反应的产物就是后一步反应的反应物)的计算时,可用关系式法一步求解。
此种方法的关键,是根据各步反应的化学方程式,找出起始原料与最终产物之间的物质的量之比,列出相应的关系式,然后按常规方法求解。
二、浓硫酸的特性
硫酸的化学性质跟它的浓度有密切的关系。
稀硫酸具有酸类的通性(H +的性质),而浓硫酸中存在大量未电离的硫酸分子,因而浓硫酸除具有酸类的通性外,还具有吸水性、脱水性和强氧化性等特性。
1、浓硫酸的吸水性
浓硫酸具有吸收附着在物质表面或内部的湿存水和吸收结晶水的性能。
其原因是硫酸分子极易与水分子化合成一系列稳定的水合物:H 2SO 4·nH 2O (n = 1,2,4,6,8)。
同时放出大量的热。
这些水合物很稳定。
利用浓H 2SO 4的吸水性,可以做干燥剂。
浓H 2SO 4能干燥H 2、O 2、CO 等中性气体,也能干燥SO 2、Cl 2、CO 2、HCl 、HF 等酸性气体;但不能干燥NH 3等碱性气体,也不能干燥HBr 、HI 、H 2S 等有强还原性的气体。
2、浓硫酸的脱水性
浓硫酸能把纸张、木材、蔗糖等有机物中的氢、氧元素,按水分子里的氢、氧原子个数比(2∶ 1)脱出,使其碳化。
如: C 12H 22O 11 浓
H SO 24−→−−− 12C + 11H 2O (蔗糖)
3、浓硫酸的氧化性
硫酸分子中S 6
+有较强的得电子能力,故浓硫酸有较强的氧化性,加热时其氧化性增强。
(1)与金属的反应:在加热的条件下,绝大部分金属(除Pt 、Au 外)能被浓H 2SO 4氧化到高价态,同时H 2SO 4被还原成SO 2(一般情况下),反应中没有氢气生成。
Cu + 2H2SO4 (浓) CuSO4 + SO2↑ + 2H2O Hg + 2H2SO4 (浓) HgSO4 + SO2↑ + 2H2O
Zn + 2H2SO4 (浓) ZnSO4 + SO2↑ + 2H2O
(2)常温时浓H2SO4使铁、铝钝化。
加热时铁、铝可与浓硫酸剧烈反应。
2Fe + 6H2SO4 (浓) Fe2 (SO4)3 + 3SO2↑ + 6H2O 2Al + 6H2SO4 (浓) Al2(SO4)3 + 3SO2↑ + 6H2O (3)与非金属的反应
C + 2H2SO4 ( 浓) 2SO2↑ + CO2↑+ 2H2O S + 2H2SO4 (浓) 3SO2↑ + 2H2O
2P + 5H2SO4(浓) 2H3PO4 + 5SO2↑ + 2H2O
(4)与具有还原性的化合物反应
H2S + H2SO4 (浓) = S + SO2↑ + 2H2O 2HBr + H2SO4 (浓) = Br2↑ + SO2 ↑ + 2H2O
8HI + H2SO4(浓) = 4I2 + H2S ↑ + 4H2O
5、硫酸的性质与作用的联系
(1)硫酸的酸性实际上就是硫酸中H+的性质
Zn + H2SO4 (稀) = ZnSO4 + H2↑CuO + H2SO4 = CuSO4 + H2O 2NaOH + H2SO4 = Na2SO4 + H2O (2)硫酸可与弱酸盐反应,表现出硫酸的强酸性
FeS + H2SO4 (稀) = FeSO4 +H2S ↑Ca3(PO4)2 + 3H2SO4(浓) 3CaSO4↓ + 2H3PO4
2CH3COONa + H2SO4(浓) = Na2SO4 + 2CH3COOH
(3)硫酸的难挥发性(或称高沸点性)可以用硫酸与易挥发酸的盐反应来制取易挥发的酸,或者说可以用硫酸与低沸点酸的盐反应来制取低沸点的酸。
NaCl (固) + H2SO4 (浓) NaHSO4 + HCl ↑2NaCl(固) + H2SO4 (浓) Na2SO4 + 2HCl↑
NaNO3(固) + H2SO4 (浓) NaHSO4 + HNO3↑
在这些反应中是硫酸的难挥发性(即高沸点性)与酸性的共同表现。
(4)硫酸的稳定性:硫酸对热的稳定性强,可以用硫酸与不稳定酸的盐反应来制取不稳定酸。
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2↑
不稳定酸分解后可得到相应的气体。
(5)浓H2SO4的吸水性:在实验室用浓H2SO4做干燥剂;或把少量研细的胆矾放入浓H2SO4中,胆矾会逐渐变为白色。
这些都是浓H2SO4吸水性的表现。
(6)浓H2SO4的脱水性:浓H2SO4使蔗糖、纤维素等碳化,是浓H2SO4脱水性的表现。
(7)浓H2SO4与C、S、H2S、HBr、HI等反应时,只表现出氧化性。
(8)浓H2SO4与Cu、Ag等金属反应,或与NaBr、FeS等还原性化合物反应时,是浓H2SO4的氧化性与酸性的共同体现。
2NaBr + 3H2SO4 (浓) = 2NaHSO4 + Br2↑ + SO2↑ + 2H2O
2FeS + 6H2SO4(浓) = Fe2(SO4)3 + 2S ↓ + 3SO2↑ + 6H2O
三、硫酸根离子的检验
1、所用试剂:BaCl2溶液(或Ba(NO3)2溶液)和稀盐酸。
2、原理:Ba2+与SO42-结合生成的BaSO4,即不溶于水也不溶于稀HCl或稀HNO3。
3、操作方法:取样→加试剂→观察与描述现象→根据现象得出结论。
4、加入试剂的顺序,为了防止溶液中可能存在的Ag+、SO32-、CO32-等离子的干扰,应在待检液中先加入足量稀HCl,若无沉淀和气泡时,再加入BaCl2溶液,此时若出现白色沉淀,则可肯定原试液中必
定含有SO42-。