环烷烃的结构环戊烷的构象
- 格式:ppt
- 大小:2.80 MB
- 文档页数:87


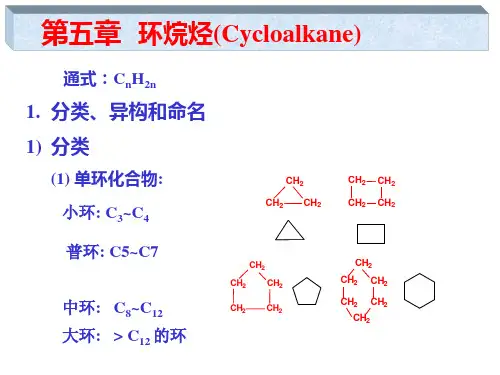

环烷烃的构象链状化合物的构象是由基团绕C—Cσ键旋转产生的;而环状化合物的构象至少涉及到两个C—Cσ键和其键角的转动和变化,有时还涉及到键长和键角的变化,比较复杂,常称环的翻转。
一、环丙烷的构象环丙烷是三个碳的环,只能是平面构象,即它的构型。
尽管只有一种构象,但这个环极不稳定,主要因为:1、所有C-H键都是重叠构象,扭转张力大。
2、C原子是不等性杂化或弯曲键,有“角张力”存在。
二、环丁烷的构象环丁烷有两种极限构象:动画演示:平面式构象:象环丙烷一样,不稳定,存在扭转张力和“角张力”。
蝶式构象:能缓解扭转张力和角张力,呈蝶式构象。
通过平面式构象,由一种蝶式翻转成为另一种蝶式构象,处于动态平衡。
蝶式是优势构象。
也有扭转能力和角张力存在。
三、环戊烷的构象环戊烷的构象主要是信封式和半椅式构象。
两者处于平衡。
因为平面构象能量较大,一般认为环戊烷采取这种构象可能性很少。
E相对=19kJ/mol 信封式半椅式四、环己烷的构象环己烷的构象经过近百年的努力才建立起来。
Baeyer 1885年提出张力学说,认为环状化合物是平面构型Sachse 1889年质疑张力学说只适合小环,提出环已烷有船式、椅式两种构象。
Hassel 1930年利用偶极矩测定法和电子衍射法研究环已烷构象,∠CCC=109.5°,气相、液相中环已烷几乎全是椅式构象。
Barton 1950年发展了构象理论,以甾族化合物为对象提出构象分析,把构象分析明确地引入有机化学中。
Hassel 和Barton获1969年Nobel化学奖1、椅式和船式构象环已烷保持碳原子的109.5°键角,提出了椅式和船式构象.1)椅式构象:C1、C2、C4、C5在一个平面上,C6和C3分别在平面的下面和平面的上面,很象椅脚和椅背,故称“椅式”。
2)船式构象:C1、C2、C4、C5在一个平面上,C3和C6在平面上面。
形状象只船,C3和C6相当船头和船尾,故称“船式”。

脂环烃的定义和命名本章所要讨论的是结构上具有环状碳骨架,而性质上与脂肪烃相似的烃类,它们总称为脂环烃。
饱和的脂环烃叫做环烷烃。
因碳骨架成环,故比烷烃少两个氢原子,其通式与烯烃一样,也是Cn H2n。
最简单的环烷烃含有三个碳原子,是一个三碳环化合物。
它是丙烯的同分异构体。
含有三个以上碳原子的环烷烃,除与碳原子数相同的烯烃互为同分异构体外,还有环状的同分异构体。
例如,含有四个碳原子的环烷烃就有两种。
由于碳原子连成环,环上C—C单键不能自由旋转。
因此,在环烷烃的分子中,只要环上有两个碳原子各连有不同的原子或基因,就有构型不同的顺反异构体存在。
例如,1,4-二甲基环己烷就有顺反异构体。
两个甲基在环平面同一边的是顺式异构体,两个甲基分布在环平面两边的是反式异构体。
在书写环状化合物的结构式时,为了表示出环上碳原子的构型,可以把碳环表示为垂直于纸面〔见上式(I)、(III)〕,将朝向前面(即向着读者)的三个键用粗线或楔形线表示。
把碳上的基团排布在环的上边和下边(若碳上没有取代基只有氢原子。
也可省略不写)。
或者把碳环表示为在纸面上[见下式(II)、(IV)],把碳上的基团排布在环的前方和后方,用实线表示伸向环平面前方的键,虚线表示伸向后方的键。
脂环烃的环上有双键的叫做环烯烃。
有两个双键和有一个叁键的则分别叫做环二烯烃和环炔烃。
它们的命名也与相应的开链烃相似。
以不饱和碳环作为母体,侧链作为取代基。
环上碳原子编号顺序应是不饱和键所在位置号码最小。
对于只有一个不饱和键的环烯(或炔)烃,因不饱和键总是在C(1)一C(2)之间,故双键(或叁键)的位置也可以不标出来。
例如:带有侧链的环烯烃命名时,若只有一个不饱和碳上有侧链,该不饱和碳编号为1;若两个不饱和碳都有侧链,或都没有侧链,则碳原子编号顺序除双键所在位置号码最小外,还要同时以侧链位置号码的加和数较小为原则。
例如:分子中含有两个碳环的是双环化合物。
其中两个环共用一个碳原子的叫做螺环化合物;共用两个或更多个碳原子的叫做桥环化合物。


环烷烃的构象和拜尔张力学说环烷烃的构象1.环己烷的构象早在1890年,沙赫斯(Sachse,H.)通过研究以为,依照正四面体的模型,六个碳原子的环能够不在同一平面上,同时还维持着正四面体的正常角度,但由于表达得不清楚,图又画得不行,因此没有引发那时化学家们的注意。
莫尔(Mohr,E.,1918)从头研究了那个问题,正式提出了非平面无张力环的学说,并画出模型。
他以为碳原子能够维持正常的键角,环己烷的六个碳原子不在同一平面上,能够形成两种折叠着的环系,如图2-19所示。
图2-19(i)的两个叫作椅型,它是一个超级对称的分子,借助于模型能够看得很清楚。
第一,在那个模型中的碳原子是处在一上一下的位置。
第二,那个模型是僵硬的,只要一个键角改变,其它键角也同时改变。
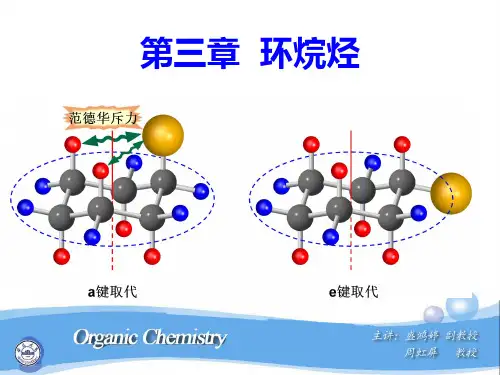
第三,还能够看到,环中相邻两个碳原子的构象都是邻交叉型的,如用纽曼式表示,成为以下的形式:最后,还能够看出,椅型的环己烷的氢原子能够分为两组:一组是六个C——H键与分子的对称轴大致是垂直的,都伸出环外,这叫作平键(或称平伏键)或e键(e是equatorial的字首,赤道的意思),三个e键略往上伸,三个e键略向下伸;另六个氢的键都是与轴平行的,这叫作直键(或称直立键)或a键(a是axial的字首,轴的意思),三个伸在环的下面,三个伸在环的上面。
图2-19(i)中带点的白球都在环的上面,不带点的白球都在环的下面。
这种关系在斯陶特模型图2-20中能够表示得更清楚一些:在图2-20中,a键的氢原子都用带黑点的球表示,e键的氢原子用白球表示。
由于成环的碳链是封锁的,因此沿着碳碳键不管如何旋转,在环上面的不可能转到环的下面来,老是维持着原先各个氢原子的空间关系。
这种构象,既无角张力,也无扭转张力,代表一个最稳固的形式,是优势构象。
另一种维持正常键角的环己烷模型如图2-19(ii)的两个,叫作船型,可用纽曼式表示如下:第一可看到,2、3和5、6两对碳原子的构象是重叠型的,这种构象虽无角张力,但有扭转张力,相当于能量高的构象。