电化学方法简介资料
- 格式:ppt
- 大小:79.50 KB
- 文档页数:16
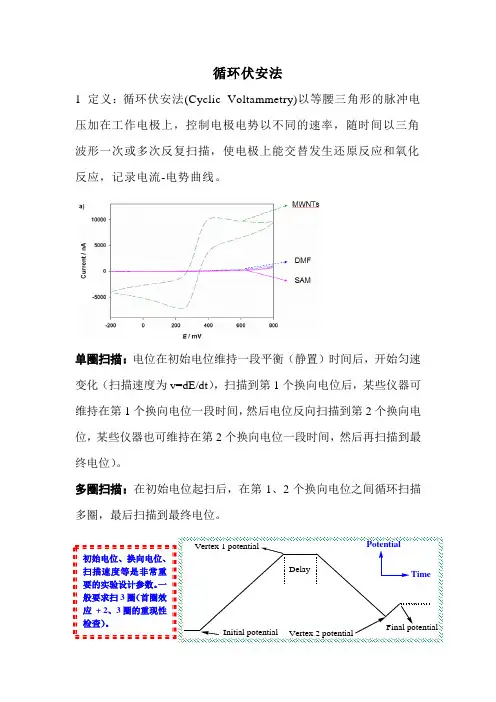
循环伏安法1 定义:循环伏安法(Cyclic Voltammetry)以等腰三角形的脉冲电压加在工作电极上,控制电极电势以不同的速率,随时间以三角波形一次或多次反复扫描,使电极上能交替发生还原反应和氧化反应,记录电流-电势曲线。
单圈扫描:电位在初始电位维持一段平衡(静置)时间后,开始匀速变化(扫描速度为v=dE/dt ),扫描到第1个换向电位后,某些仪器可维持在第1个换向电位一段时间,然后电位反向扫描到第2个换向电位,某些仪器也可维持在第2个换向电位一段时间,然后再扫描到最终电位)。
多圈扫描:在初始电位起扫后,在第1、2个换向电位之间循环扫描多圈,最后扫描到最终电位。
Initial potential Vertex 1 potential Vertex 2 potential Final potentialDelay PotentialTime 初始电位、换向电位、扫描速度等是非常重要的实验设计参数。
一般要求扫3圈(首圈效应 + 2、3圈的重现性检查)。
2 特点:Ⅰ:激励信号:施加的电压为三角波电压,双向扫描,分为氧化过程和还原过程,氧化态电势高,还原态电势低。
Ⅱ:参数设置:两个可调参数为电位范围和扫描速度。
设置电位范围时需根据溶液的初始条件设置起始电位,起始电位不应破坏溶液的初始条件;若起始电位与溶液初始条件不一致,则在静置几秒内所发生的氧化还原反应未被记录。
Ⅲ:实验条件:进行循环伏安扫描时体系应处于静止状态,若搅拌则记录的图中不会出现峰,相反呈S型。
3 所得信息:Ⅰ:判断电极反应的可逆程度,依据为峰电流比及峰电势差,对于可逆体系:i pa/i pc1;E pa/E pc nF。
Ⅱ:判断电极表面的修饰情况,峰电流大说明电极传递电子能力较强。
但这只能定性判断,实际循环伏安图中,存在充电电流的影响,因此CV峰电流测量不太容易精确。
Ⅲ:判断其控制步骤和反应机理,若i p∝v,则此过程为表面控制,发生在电极表面;若i p∝v1/2,则此过程为扩散控制,发生在溶液中。


电化学知识点总结一、电化学基础1. 电化学的基本概念电化学是研究电化学反应的科学,它涉及到电流和电势的关系,以及在电化学反应中的能量转换和催化作用。
电化学反应通常发生在电极上,电化学反应的方向与电流的流动方向相反。
2. 电化学的基本原理电化学的基本原理包括电极反应、电解、电荷传递和能量转换等。
在电池中,通过氧化还原反应产生的电能被转化为化学能,进而转化为电能,从而产生电流。
3. 电化学的基本参数电化学的基本参数包括电压、电流、电解、电极电势、电导率、离子迁移速率等。
这些参数是电化学研究的基础,也是电化学应用的基本原理。
二、电化学反应1. 电化学反应的基本类型电化学反应包括氧化还原反应、电解反应、电化学合成反应等。
氧化还原反应是电化学反应中最常见的一种,它涉及到电子的转移,产生电压和电流。
电解反应是电化学反应中电流通过电解质溶液时发生的反应,通常涉及到离子的迁移和溶液中的化学反应。
电化学合成反应是指利用电能进行化学合成反应,通常包括电极合成和电解合成两种方式。
2. 电化学反应的热力学和动力学电化学反应的热力学和动力学是电化学研究的重要内容。
热力学研究电化学反应的热能转化和热能产生的条件,动力学研究电化学反应的速率和电化学动力学理论。
三、电化学动力学1. 电化学反应速率电化学反应速率是指单位时间内电化学反应所产生的物质的变化量。
电化学反应速率与电流和电压密切相关,它是电化学反应动力学研究的关键之一。
2. 催化作用催化作用是指通过催化剂来提高电化学反应速率的现象。
催化剂可以降低反应的活化能,提高反应速率,通常在电化学反应中有着重要的应用。
3. 双电层理论双电层是电极表面和电解质溶液之间的一个电荷层,它对电化学反应速率有着重要的影响。
双电层理论是电化学研究的重要理论之一,它涉及到电极和电解质溶液中的电位差和电荷分布。
4. 交换电流交换电流是指在电化学反应中与电流方向相反的电流,它是电化学反应速率的一个重要参数,也是电化学动力学研究的重要内容。

电化学分析法[日期:2011-06-24] 来源:作者:[字体:大中小] 电化学分析法(electroanalytical chemistry)是根据电化学原理和物质在溶液中的电化学性质及其变化而建立起来的一类分析方法。
这类方法都是将试样溶液以适当的形式作为化学电池的一部分,根据被测组分的电化学性质,通过测量某种电参量来求得分析结果的。
电化学分析法可分为三种类型。
第一种类型是最为主要的一种类型,是利用试样溶液的浓度在某一特定的实验条件下与化学电池中某种电参量的关系来进行定量分析的,这些电参量包括电极电势、电流、电阻、电导、电容以及电量等;第二种类型是通过测定化学电池中某种电参量的突变作为滴定分析的终点指示,所以又称为电容量分析法,如电位滴定法、电导滴定法等;第三种类型是将试样溶液中某个待测组分转入第二相,然后用重量法测定其质量,称为电重量分析法,实际上也就是电解分析法。
电化学分析法与其他分析方法相比,所需仪器简单,有很高的灵敏度和准确度,分析速度快,特别是测定过程的电信号,易与计算机联用,可实现自动化或连续分析。
目前,电化学分析方法已成为生产和科研中广泛应用的一种分析手段。
第一节电势分析法电势分析法是一种电化学分析方法,它是利用测定原电池的电动势(即用电势计测定两电极间的电势差),以求得物质含量的分析方法。
电势分析法又可分为直接电势法(potentiometric analysis)和电势滴定法(potentiometric titration)。
直接电势法是根据测量原电池的电动势,直接求出被测物质的浓度。
应用最多的是测定溶液的pH。
近些年来,由于离子选择性电极的迅速发展,各种类型的离子选择性电极相继出现,应用它作为指示电极进行电势分析,具有简便、快速和灵敏的特点,特别是它能适用于其它方法难以测定的离子。
因此,直接电势法在土壤、食品、水质、环保等方面均得到广泛的应用。
电势滴定法是利用电极电势的变化来指示滴定终点的分析方法。


化学分析中的电化学分析方法化学分析是在现代化学中非常重要的领域。
在许多领域,比如生化、医学、化工等领域中,化学分析都在不断地作出贡献。
电化学分析作为化学分析中的一种方法,有着独特的优点。
它广泛应用于环境分析、药物检测、矿产资源开发等领域。
下面,我们就来具体了解一下电化学分析的各个方面。
电化学分析方法的基本概念电化学分析在20世纪初期就已经有人开始研究,而且具有相当长的历史。
在电化学分析中,一般利用电流强度与电压变化量的关系进行物质分析。
这里面有3个核心概念:电极、电势、电化学电池。
电势是指一个物理量,可以用来描述两个电荷体系之间的势能差。
而电极就是充当物质分析时的接口,使液体中的化学反应与极谱仪等电学装置之间得以转化。
而对电极进行压力梯度的加速也就是在进行强制电解。
电化学电池是指在含有电解质的溶液中,通过对氧化还原反应进行产生电能的装置。
电化学电池就是电池的原型,是通过化学反应来实现能量转化的设备,而其发展与研究,具有非常重要的历史地位。
电化学分析方法的基本种类电化学分析方法可以分为两类:电位法与电流法。
电位法是通过电极电势变化来测定被测物质的浓度,其中又包括最常用的恒电流电位法和线性扫描伏安法(LSV)。
恒电流电位法就是在电解质溶液中控制特定电位下的电解质浓度,通过记录电解质浓度的变化,来测定被测物质的浓度。
LSV法则是在电势愈来愈大的过程中,慢慢地增加电流,来测定缓慢进行的化学反应。
电流法是通过测定电化学过程中电流强度的变化来测定被测物质的浓度。
它包括电位阶跃法、电位扫描法和多脉冲极谱法等。
它们都是在控制特定电位下,通过电流的变化,来测定被测物质的浓度。
相比较电位法,电流法的数据处理较为方便,信噪比也比较高。
电化学分析方法的应用电化学分析是一种非常有应用价值的分析方法,被广泛应用于多种领域,比如工业生产、环境监测、矿产资源开发等。
下面,我们就从这三个方面来谈谈它的具体应用。
工业生产方面,电化学分析可用于制备专用合金、超纯金属等,还可用于检测金属表面处理质量。

化学实验中的电化学实验电化学是研究电与化学之间相互作用的学科,它在化学实验中扮演着重要的角色。
电化学实验是一种通过电流作用于化学体系进行实验研究的方法,可以用于分析物质的性质、反应机制以及合成新物质等。
本文将介绍电化学实验的基本原理、常见实验方法以及它们在化学研究中的应用。
一、电化学实验的基本原理电化学实验的基本原理是基于电解和电池的原理。
电解是指通过外加电压使电解液中发生化学反应,将化学能转化为电能的过程。
而电池则是通过化学反应产生电能的装置。
在电化学实验中,通过连接电解池和电池,我们可以通过观察电流的变化来了解电化学反应的特性和机理。
二、常见的电化学实验方法1. 电解实验电解实验是最常见的电化学实验之一。
它通过在电解池中通电,引发电解液中的化学反应。
常见的电解实验有电解水制氢气和氧气的实验,电解氯化钠制取氯气和氢氧化钠等实验。
这些实验可以通过观察电解液的气体产生、电极的气味变化等来揭示反应机制和产物性质。
2. 电化学分析实验电化学分析实验是应用电化学方法进行定量和定性分析的重要手段。
例如,电化学滴定法可以通过测定反应物的氧化还原电位来确定物质的浓度。
电化学分析实验也广泛应用于环境监测、食品安全检测等领域。
3. 电极制备实验电极是电化学实验的重要组成部分。
制备合适的电极材料对于实验结果的准确性和稳定性至关重要。
电极制备实验包括金属电极的沉积、碳纳米管电极的合成等。
这些实验可以通过改变电极材料和制备条件来探索电极性能的影响因素。
三、电化学实验在化学研究中的应用1. 电化学合成反应电化学合成反应是一种通过电流驱动化学反应进行合成的方法。
通过控制电流密度、反应时间等条件,可以实现对产物形态、结构和纯度的精确控制。
电化学合成反应在有机合成、材料合成等领域具有广泛应用。
2. 电化学催化电化学催化是指通过电流作用下改变化学反应速率和选择性的现象。
电化学催化在燃料电池、电解水制氢等领域发挥着重要作用。
通过电化学实验可以研究催化剂的性能、反应机制以及提高催化性能的方法。

什么是电化学分析法
电化学分析法是应用电化学原理和技术,利用化学电池内被分析溶液的组成及含量与其电化学性质的关系而建立起来的一类分析方法。
其操作方便,应用广泛,既可定性,又可定量;既能分析有机物,又能分析无机物,并且许多方法便于自动化,可用于生产、生活等各个领域。
电化学分析法通常将试液作为化学电池的一个组成部分,根据该电池的某种电参数(如电阻、电导、电位、电流、电量或电流-电压曲线等)与被测物质的浓度之间存在一定的关系而进行测定的方法。
其中,电位分析法是基于溶液中某种离子活度和其指示电极组成的原电池的电极电位之间关系的分析方法。
直接电位法是通过测量溶液中某种离子与其指示电极组成的原电池的电极电动势直接求算离子活度的方法。
电位滴定法是通过测量滴定过程中原电池电动势的变化来确定滴定终点的滴定分析方法。
电解分析法则是根据基于溶液中某种离子和其指示电极组成的电解池的电解原理建立的分析方法。
电化学分析法的优点包括灵敏度高、选择性好、设备简单等。
许多电化学分析法既可定性,又可定量,既能分析有机物,又能分析无机物,并且许多方法便于自动化,可用于生产、生活等各个领域。
以上信息仅供参考,如有需要,建议查阅相关书籍或咨询专业人士。

电化学方法与应用
电化学是研究电与化学的相互作用的科学。
它涉及到物质在电极表面上的电活性、电解过程、离子传输、电化学反应等内容。
电化学方法指的是利用电化学原理和技术手段进行实验研究和应用的方法。
电化学方法在许多领域都有广泛的应用。
以下是其中一些常见的应用示例:
1. 腐蚀研究:通过电化学方法可以研究金属材料在不同环境条件下的腐蚀行为,如浸泡试验、电化学阻抗谱等。
2. 电池与燃料电池:电化学方法可用于研究和开发各种类型的电池和燃料电池,如锂离子电池、燃料电池等。
3. 阳极保护与阴极保护:电化学方法可以用于研究和设计金属结构的阳极保护和阴极保护方法,以延长其使用寿命。
4. 脱氧与除氧:电化学方法可以用于水处理、金属冶炼等过程中的脱氧和除氧。
5. 电解制备与电沉积:电化学方法可以用于制备金属、合金和薄膜,并用于精密电镀等领域。
6. 生物传感器:电化学方法可用于设计和制造生物传感器,用于检测和诊断生
物样品中的特定物质和分子。
7. 环境监测:电化学方法可以用于监测和测量水体、大气和土壤中的污染物,如重金属离子、有机污染物等。
总之,电化学方法广泛应用于材料科学、环境科学、能源领域、生命科学等多个领域,在科研和工业生产中发挥着重要作用。


电化学原理和方法电化学原理和方法是研究化学反应中电荷转移过程的学科。
它通过控制电子和离子的流动来实现化学反应的调控。
电化学原理涉及电极反应、电解质与溶液的电导性、电化学平衡等基本概念。
而电化学方法则是应用电化学原理来研究和解决实际问题的具体手段。
电化学原理的核心是电化学电位,它是表征电化学反应进行方向和强度的物理量。
电化学电位可以通过标准电极电势和电极反应的物质浓度来计算。
标准电极电势是指在标准状态下,电极与其相应离子的物质浓度均为1mol/L时,电极反应达到平衡时的电位差。
电化学电势越高,表示反应越容易进行。
电解质和溶液的电导性是电化学研究中的另一个重要概念。
电解质是能在溶液中电离产生离子的物质。
离子是携带电荷的粒子,在外电场作用下可以移动。
溶液的电导性与其中的电解质浓度有关,通常用电导率来表示。
电导率是单位体积内的电导量,越高表示电导性越强。
电化学平衡是指在电化学反应过程中,正反应和逆反应达到动态平衡。
在平衡状态下,正反应和逆反应发生的速率相等,但是电位存在差异。
电化学平衡的研究可以通过测量电化学过程的电动势来实现。
电动势是电极反应导致的电势差,是判断电化学反应进行方向和速率的重要参量。
除了电化学原理,电化学研究中的方法也具有重要意义。
例如,电化学分析法可以通过测量溶液中的电位变化来确定样品中的化学成分。
电化学合成法可以利用电流在电极反应中产生化学物质。
电化学腐蚀和电镀等工艺也是基于电化学原理和方法进行的。
总之,电化学原理和方法是研究电荷转移过程的学科,涉及电化学电位、电导性、电化学平衡等基本概念。
它们在实际应用中具有重要的意义,可以用来解决实际问题和开展电化学研究工作。
电化学方法
电化学方法是一种通过控制电流和电压来实现化学反应的方法。
它广泛应用于
电化学能源转换、电化学分析、电镀、腐蚀控制和环境保护等领域。
电化学方法的原理是利用电子传递和离子传递来实现化学反应,因此在很多领域都有着重要的应用价值。
在电化学能源转换方面,电化学方法被广泛应用于电池和燃料电池的研究和生
产中。
通过控制电流和电压,可以实现正极和负极的化学反应,从而将化学能转化为电能。
同时,电化学方法也可以用于电解水制氢和氧气,实现能源的储存和转换。
在电化学分析方面,电化学方法可以用于测定物质的含量和性质。
常见的电化
学分析方法包括电位滴定、循环伏安法和交流阻抗法等。
这些方法通过测定电极的电位和电流响应,可以快速、准确地分析样品中的物质成分和浓度。
在电镀和腐蚀控制方面,电化学方法可以用于表面处理和防护。
通过控制电流
密度和电解液成分,可以实现金属表面的镀层和防腐蚀处理,提高材料的耐蚀性和耐磨性。
在环境保护方面,电化学方法可以用于废水处理和废气处理。
通过电化学方法
可以实现废水中有害物质的降解和去除,同时还可以利用电化学方法来净化废气中的有害气体,保护环境和人类健康。
总的来说,电化学方法是一种非常重要的化学方法,它在能源转换、分析检测、材料表面处理和环境保护等方面都有着广泛的应用。
通过不断的研究和创新,电化学方法将会在更多的领域发挥重要作用,为人类社会的可持续发展做出贡献。
电化学分析法[日期:2011—06—24]来源:作者:[字体:大中小]电化学分析法(electroanalytical chemistry)是根据电化学原理和物质在溶液中的电化学性质及其变化而建立起来的一类分析方法。
这类方法都是将试样溶液以适当的形式作为化学电池的一部分,根据被测组分的电化学性质,通过测量某种电参量来求得分析结果的。
电化学分析法可分为三种类型.第一种类型是最为主要的一种类型,是利用试样溶液的浓度在某一特定的实验条件下与化学电池中某种电参量的关系来进行定量分析的,这些电参量包括电极电势、电流、电阻、电导、电容以及电量等;第二种类型是通过测定化学电池中某种电参量的突变作为滴定分析的终点指示,所以又称为电容量分析法,如电位滴定法、电导滴定法等;第三种类型是将试样溶液中某个待测组分转入第二相,然后用重量法测定其质量,称为电重量分析法,实际上也就是电解分析法。
电化学分析法与其他分析方法相比,所需仪器简单,有很高的灵敏度和准确度,分析速度快,特别是测定过程的电信号,易与计算机联用,可实现自动化或连续分析。
目前,电化学分析方法已成为生产和科研中广泛应用的一种分析手段。
第一节电势分析法电势分析法是一种电化学分析方法,它是利用测定原电池的电动势(即用电势计测定两电极间的电势差),以求得物质含量的分析方法。
电势分析法又可分为直接电势法(potentiometric analysis)和电势滴定法(potentiometric titration)。
直接电势法是根据测量原电池的电动势,直接求出被测物质的浓度。
应用最多的是测定溶液的pH。
近些年来,由于离子选择性电极的迅速发展,各种类型的离子选择性电极相继出现,应用它作为指示电极进行电势分析,具有简便、快速和灵敏的特点,特别是它能适用于其它方法难以测定的离子.因此,直接电势法在土壤、食品、水质、环保等方面均得到广泛的应用.电势滴定法是利用电极电势的变化来指示滴定终点的分析方法。
循环伏安法1 定义:循环伏安法(Cyclic Voltammetry)以等腰三角形的脉冲电压加在工作电极上,控制电极电势以不同的速率,随时间以三角波形一次或多次反复扫描,使电极上能交替发生还原反应和氧化反应,记录电流-电势曲线。
单圈扫描:电位在初始电位维持一段平衡(静置)时间后,开始匀速变化(扫描速度为v=dE/dt ),扫描到第1个换向电位后,某些仪器可维持在第1个换向电位一段时间,然后电位反向扫描到第2个换向电位,某些仪器也可维持在第2个换向电位一段时间,然后再扫描到最终电位)。
多圈扫描:在初始电位起扫后,在第1、2个换向电位之间循环扫描多圈,最后扫描到最终电位。
2 特点:Ⅰ:激励信号:施加的电压为三角波电压,双向扫描,分为氧化过程和还原过程,氧化态电势高,还原态电势低。
Ⅱ:参数设置:两个可调参数为电位范围和扫描速度。
设置电位范围时需根据溶液的初始条件设置起始电位,起始电位不应破坏溶液的初始条件;若起始电位与溶液初始条件不一致,则在静置几秒内所发生的氧化还原反应未被记录。
Ⅲ:实验条件:进行循环伏安扫描时体系应处于静止状态,若搅拌则记录的图中不会出现峰,相反呈S型。
3 所得信息:Ⅰ:判断电极反应的可逆程度,依据为峰电流比及峰电势差,对于可逆体系:i pa/i pc≈1;E pa/E pc≈2.3RT/nF。
Ⅱ:判断电极表面的修饰情况,峰电流大说明电极传递电子能力较强。
但这只能定性判断,实际循环伏安图中,存在充电电流的影响,因此CV峰电流测量不太容易精确。
Ⅲ:判断其控制步骤和反应机理,若i p∝v,则此过程为表面控制,发生在电极表面;若i p∝v1/2,则此过程为扩散控制,发生在溶液中。
循环伏安法可作用于可逆的电极过程,也可作用于不可逆或准可逆的电极过程以及各种伴随航行反应的过程,不同的电极过程分别阳极峰电势Epa 和阴极峰电势Epc,并给出峰电位差△Ep和峰电流之比。
对于可逆波,Epc =E1/2-1.109RT/nFE pa =E1/2+1.109RT/nF△Ep=2.219RT/nF=58/n mV(25℃)4.应用:循环伏安法最为重要的应用是定性表征伴随氧化还原反应的前行或后行化学反应。