初中常见化学式大全
- 格式:doc
- 大小:135.00 KB
- 文档页数:4
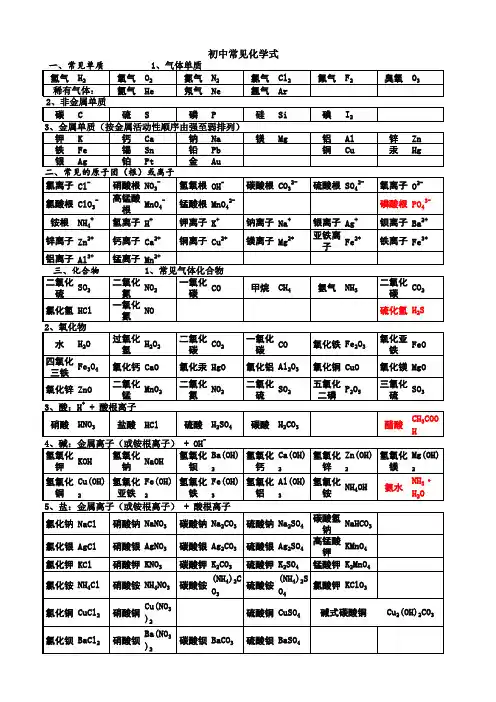
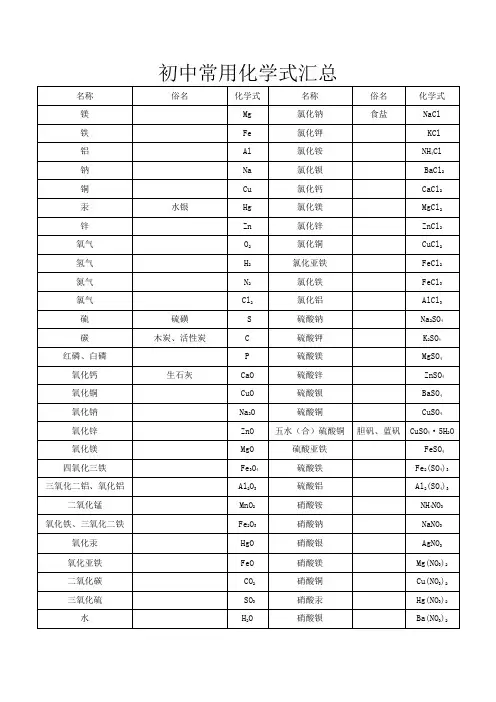
初中常用化学式汇总初中化学式大全编名称化学式式量描述号1 水H2O 182 铁锈Fe2O3·nH2O3 铜绿Cu2(OH)2CO3221 也叫孔雀石;化学名:碱式碳酸铜;绿色固体4 酒精C2H5OH 465 甲醇CH3OH 32 木精(工业酒精)6 乙酸CH3COOH 60 CH3COO-:醋酸根离子。
乙酸也叫醋酸。
7 碳酸钠晶体 Na2CO3·10H2O 2868 硫酸铜晶体CuSO4·5H2O 249.5 俗称:胆矾、蓝矾FeSO4·7H2O 278 俗称:绿矾,皂矾,青矾9 硫酸亚铁晶体10 氯化钙晶体CaCl2·6H2O 21911 硫酸钙晶体CaSO4·2H2O 172 俗称:生石膏12 硫化钠Na2S 7813 氧气O232 无色无味的气体14 氢气H2 2 爆鸣气的主要成分:H2和O2;无色无味的气体15 氮气N228 无色无味的气体16 氯气Cl27117 氨气NH317 NH3是碱性气体;无色,但有刺激性气味18 一氧化碳CO 28 无色无味的气体19 二氧化碳CO244 无色无味的气体20 二氧化硫SO264 无色,但有刺激性气味21 三氧化硫SO38022 二氧化氮NO24623 甲烷CH416 天然气(沼气)的主要成分24 乙炔C2H226 电石气:C2H2(通常含H2S、PH3等)25 氧化钙CaO 56 白色固体26 氧化镁MgO 40 白色固体27 氧化锌ZnO 8128 氧化铜CuO 79.5 黑色固体29 氧化汞HgO 217 红色固体30 二氧化锰MnO287 黑色固体31 三氧化二铝Al2O310232 三氧化二铁Fe2O3160 俗称:赤铁矿石;红色固体33 四氧化三铁Fe3O4232 俗称:磁铁矿石;黑色固体34 五氧化二磷P2O5142 白色固体35 三氧化钨WO34836 过氧化氢H2O23437 盐酸HCl 36.5 无色,但有刺激性气味;38 硝酸HNO363 具有刺激性气味的液体39 硫酸H2SO498 纯净的硫酸是没有颜色、粘稠、油状的液体,不容易挥发。


初中常见化学式 常见的化学式二、化合物一、 氧气的性质:1. 镁在空气中燃烧: 2Mg + O 2 点燃 2MgO ★2. 铁在氧气中燃烧: 3Fe + 2O 点燃 Fe 3O 43. 铜在空气中受热: 2Cu + O △ 2CuO4. 铝在空气中燃烧: 4Al + 3O 点燃 2Al 2O 3 ★5. 氢气中空气中燃烧: 2H 2 + O 2 点燃 2H 2O ★6. 红磷在空气中燃烧(测定空气中氧气含量):4P + 5O 2 点燃 2P 2O 57. 硫粉在空气中燃烧: S + O 2 点燃 SO 28. 碳在氧气中充分燃烧: C + O 2 点燃 CO 29. 碳在氧气中不充分燃烧: 2C + O 2 点燃 2CO 10. 一氧化碳在氧气中燃烧: 2CO + O 2 点燃 2CO 2 11.玻义耳研究空气的成分实验 2HgO △ 2Hg+ O 2 ↑★12.加热高锰酸钾: 2KMnO 4 △ K 2MnO 4 + MnO 2 + O 2↑ ★13.氯酸钾和二氧化锰共热制取氧气 2KClO 3 2KCl+3O 2↑★14.过氧化氢在二氧化锰作催化剂条件下分解反应: 2H 2O 2 MnO 2 2H 2O+ O 2 ↑二、自然界中的水:★15.电解水(探究水的组成实验): 2H 2O 通电 2H 2↑+ O 2 ↑ 16.生石灰溶于水: CaO + H 2O = Ca(OH)2 17.二氧化碳可溶于水: H 2O + CO 2=H 2CO 3MnO 2 △三、质量守恒定律:18.镁在空气中燃烧:2Mg + O点燃2MgO★19.铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu★20.氢气还原氧化铜:H2 + CuO △Cu + H2O四、碳和碳的氧化物:21. 碳在氧气中充分燃烧: C + O2点燃CO2★22.木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑23.焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑24.煤炉的底层: C + O2点燃CO225.煤炉的中层:CO2 + C 高温2CO26.煤炉的上部蓝色火焰的产生:2CO + O2点燃2CO2★27.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑28.碳酸不稳定而分解:H2CO3 = H2O + CO2↑29.二氧化碳可溶于水:H2O + CO2=H2CO3★30.高温煅烧石灰石(工业制CO2):CaCO3高温CaO + CO2↑★31.石灰水与二氧化碳反应(检验二氧化碳):Ca(OH)2 + CO2 = CaCO3↓+ H2O★32.一氧化碳还原氧化铜:CO+ CuO △Cu + CO2★33.一氧化碳的可燃性:2CO + O2点燃2CO2★34.碳酸钠与稀盐酸(灭火器的原理):Na2CO3 + 2HCl =2NaCl +H2O +CO2↑五、燃料及其利用:★35.甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O ★36.酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O★37.氢气中空气中燃烧:2H2 + O2点燃2H2O六、金属38.镁在空气中燃烧:2Mg + O2点燃2MgO 39.铁在氧气中燃烧:3Fe + 2O2点燃Fe3O440. 铜在空气中受热:2Cu + O△2CuO41. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3★42. 锌和稀硫酸(实验室制取氢气)Zn + H2SO4 = ZnSO4 + H2↑★43. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑44. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑45. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑46. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑47. 铁和稀盐酸Fe + 2HCl =FeCl2 + H2↑48. 镁和稀盐酸Mg+ 2HCl = MgCl2 + H2↑49.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑★50. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu51. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu52. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2 + Hg ★53.金属铁的治炼原理:3CO+ 2Fe2O3高温4Fe + 3CO2↑七、酸、碱、盐★54. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2FeCl3 + 3H2O ★55. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O56. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O57. 氧化铜和稀硫酸反应:CuO + H2SO4 =CuSO4 + H2O ★58.盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O ★59. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O60. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O61. 硫酸和烧碱反应:H2SO4 + 2NaOH =Na2SO4 + 2H2O ★62.大理石与稀盐酸反(实验室制取CO2 ):CaCO3 +2HCl =CaCl2+H2O+CO2↑★63.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑64.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑★65. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl ★66.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 67.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 68.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O ★69.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3↓+ H2O 70. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O ★71. 铁和硫酸铜溶液(波尔多液不能用铁桶装)Fe + CuSO4 = FeSO4 + Cu ★72.碳酸钠与稀盐酸(检验NaOH变质):Na2CO3+2HCl=2NaCl+H2O+CO2↑★73. 碳酸氢钠与稀盐酸(小苏打治疗胃酸过多)NaHCO3+HCl=NaCl+H2O+CO2↑★74. 氢氧化钙与碳酸钠(检验NaOH变质):Ca(OH)2+Na2CO3=CaCO3↓+ 2NaOH★75.氯化钠和硝酸银(区别食盐和蒸馏水):NaCl + AgNO3 =AgCl↓+ NaNO3★76.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓+ 2NaCl。
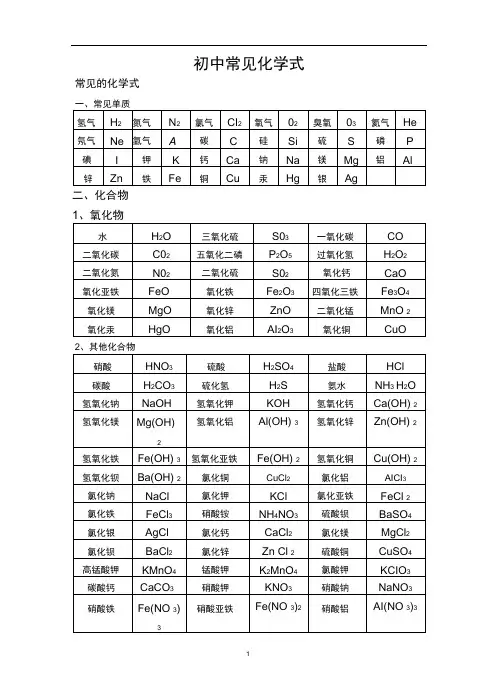
初中常见化学式常见的化学式二、化合物常见的盐硝酸镁 Mg(NO3)2、硝酸铜Cu(NO3)2、 硝酸钙Ca(NO3)2、 亚硝酸钠 NaN03、碳酸钠Na2CO3、碳酸钙 CaCO3、碳酸镁MgC03、碳酸钾K2CO3 氢氧化钠NaOH 、氢氧化钙Ca(OH)2、 氢氧化钡Ba(OH)2、氢氧化镁Mg(OH)2、氢氧化铜Cu(OH)2、 氢氧化钾KOH 、氢氧化铝Al(OH)3 (常见的碱) 氢氧化铁氢氧化亚铁Fe(OH)3、Fe(OH)2 (常见有机物) 甲烷 乙炔 甲醇乙醇碱式碳酸铜 石膏熟石膏Cu2(OH)2CO3 、 CaSO4・2H2O 、 CaSO4・H2O 明矶、KAl(SO4)2.12H2O 、绿矶 FeSO4・7H2O(常见结晶水合物)蓝矶 CuSO4.5H2O 、碳酸钠晶体 Na2CO3.10H2O(常见化肥)尿素 CO(NH2)2、硝酸铵 NH4NO3、硫酸铵(NH4)2SO4、 碳酸氢铵NH4HCO3、磷酸二氢钾KH2PO4、 硝酸钾KNO3 沉淀: 红褐色沉淀 ---- Fe(OH)3 浅绿色沉淀 ----- F e(OH)2蓝色沉淀 ----- Cu(0H)2乙酸甲醛CH4 、C2H2 、 CH3OH 、C2H5OH 、CH3COOH 、CH2O白色沉淀 -------- C aC03 、BaC03、Mg(0H)2、AI(0H)3、Zn(0H)2、AgCI、BaS04(其中仅BaS04、AgCI 是不溶于HN03的白色沉淀).淡黄色沉淀(水溶液中)----S微溶于水 ------- C a(0H)2 、CaS04、Ag2S04物质的学名、俗名及化学式⑴金刚石、石墨:C ⑵水银、汞:Hg (3)生石灰、氧化钙:Ca0(4)干冰(固体二氧化碳):C02 (5)盐酸、氢氯酸:HCI⑹亚硫酸:H2S03 (7)氢硫酸:H2S(8) 熟石灰、消石灰:Ca(0H)2(9) 苛性钠、火碱、烧碱:Na0H(10) 纯碱、苏打:Na2C03碳酸钠晶体、纯碱晶体:Na2CO3.10H2O(11) 碳酸氢钠、酸式碳酸钠:NaHC03 (也叫小苏打)(12) 胆矶、蓝矶、硫酸铜晶体:CuS04.5H2O(13) 铜绿、孔雀石:Cu2(OH)2CO3 (分解生成三种氧化物的物质)(14) 甲醇:CH30H 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16・6C冰醋酸)CH3C00H (CH3C00-醋酸根离子)具有酸的通性(17) 氨气:NH3 (碱性气体)(18) 氨水、一水合氨:NH3・H20 (为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19) 亚硝酸钠:NaN02 (工业用盐、有毒)常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4A KMnO4 为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷硫:淡黄色Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色; 凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
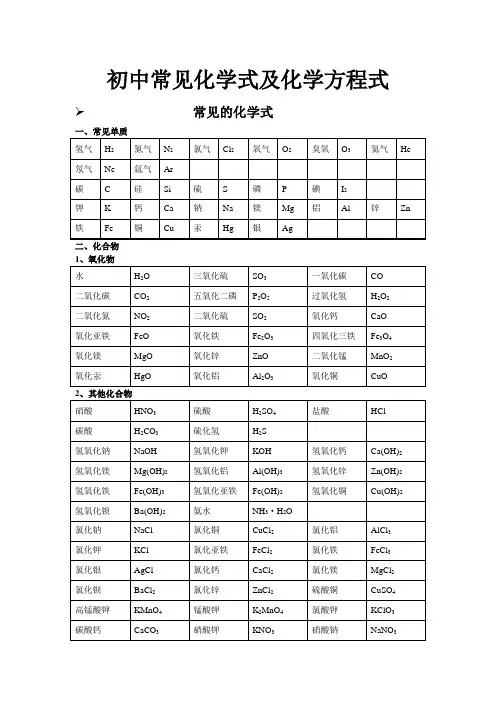
初中常见化学式及化学方程式➢常见的化学式一、常见单质二、化合物初中化学方程式全(已配平).一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO9、二氧化碳通过灼热碳层: C +CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 +O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2 点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O30、酒精在空气中燃烧:C2H5OH+ 3O2点燃 2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe+ 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C+ O2点燃 CO29. 碳在氧气中不充分燃烧:2C+ O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热 2CuO +H2O +CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe3O4高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:4CO +Fe3O4高温 3Fe+ 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸 -------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+盐(溶液) ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg (3)碱性氧化物+酸 -------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O (4)酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O 45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 ==== CaSO3↓+H2O(5)酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ Cu(OH)2==== CuCl2 +2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3 +3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 +2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2 H2O +CO2↑ 60.碳酸钠与稀盐酸反应: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2 +H2O+CO2↑ 62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4 +BaCl2 ==== BaSO4↓+ 2HCl(7)碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl 67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH(8)盐+盐 ----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3 ==== AgCl↓+ NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO4 5H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H2O ==== CuSO4·5H2化学方程式反应现象应用2Mg+ O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+ O点燃或Δ2CuO 红色金属变为黑色固体4Al+ 3O点燃或Δ2Al2O3银白金属变为白色固体3Fe+ 2O点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe +3O2高温2Fe2O3C+ O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S +O2点燃SO2剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P +5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+ 5O2点燃2H2O +4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4 MnO2 +O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧论文气2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+ O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO +H2O+ CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+ H2SO4=ZnSO4 +H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe +H2SO4=FeSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg +H2SO4 =MgSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2Δ 2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4 +4H2 Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、利用氢气的还原性WO3 +3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3 +3H2ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO +O点燃2CO2蓝色火焰煤气燃烧C+ CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4 +2C高温3Fe+ 2CO2↑ 冶炼金属C+ CO2 高温2COCO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文H2CO3 ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 +H2O+ CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰CaCO3 +2HCl=CaCl2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 +O2 点燃 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P +5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C +O2点燃 CO29. 碳在氧气中不充分燃烧:2C +O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2 +3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2 ↑14.加热高锰酸钾:2KMnO4加热 K2MnO4+ MnO2 +O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2通电2H2↑+O2 ↑17.生石灰溶于水英语六级作文:CaO +H2O == Ca(OH)218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3C + 2Fe2O3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO +O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3 == H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO+ CO2↑ 33.石灰水与中学历史教学园地二氧化碳反应(鉴别二氧化碳):Ca(OH)2 +CO2 === CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO2 35.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 2HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O 38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2 +3H2O 39.氢气中空气中燃烧:2H2+ O2点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:4Al+ 3O2 = 2Al2O3(2)金属单质酸 -------- 盐氢气(置换反应)44. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑45. 铁和稀硫酸Fe +H2SO4 = FeSO4 +H2↑46. 镁和稀硫酸Mg +H2SO4 = MgSO4+ H2↑47. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49. 铁和稀盐酸Fe +2HCl == FeCl2 +H2↑50. 镁和稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(3)金属单质盐怎样学好高中物理(溶液) ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe +CuSO4 == FeSO4 +Cu53. 锌和硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4 +Cu54. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 == Cu(NO3)2 +Hg(3)金属铁的治炼原理:55.3CO +2Fe2O3 高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸金属 -------- 盐氢气(见上)(2)酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3 +6HCl ==2FeCl3 +3H2O57. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 == Fe2(SO4)3 +3H2O58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl2 +H2O59. 氧化铜和稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O(3)酸碱 -------- 盐水(中和反应)60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl3 +3H2O63. 硫酸和烧碱反应:H2SO4+ 2NaOH == Na2SO4 +2H2O(4)酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2 +H2O+ CO2↑ 65.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl+ H2O+ CO2↑ 66.碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+H2O+ CO2↑ 67. 硫酸和氯化钡溶液反应:H2SO4 +BaCl2 == BaSO4↓+2HCl 2、碱的幼儿园小班音乐教案化学性质(1)碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O 69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3 +H2O 70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4 +H2O 71.消石灰放在空气中变质:Ca(OH)2+ CO2 == CaCO3↓+H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 == CaSO3↓+ H2O (2)碱酸-------- 盐水(中和反应,方程式见上)(3)碱盐 -------- 另一种碱另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3 == CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液)金属单质------- 另一种金属另一种盐74. 铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu(2)盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl +H2O+ CO2↑ 碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+ H2O +CO2↑(3)盐 碱 -------- 另一种碱 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 +Na 2CO 3 == CaCO 3↓+ 2NaOH (4)盐 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO 3 == AgCl↓+NaNO 3 78.硫酸钠和氯化钡:Na 2SO 4 +BaCl 2 == BaSO4↓+2NaCl一、其他反应类型1、二氧化碳通入澄清石灰水中:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O2、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O3、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH ==Na 2SO 3+ H 2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO 25、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O6、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△点燃 点燃。
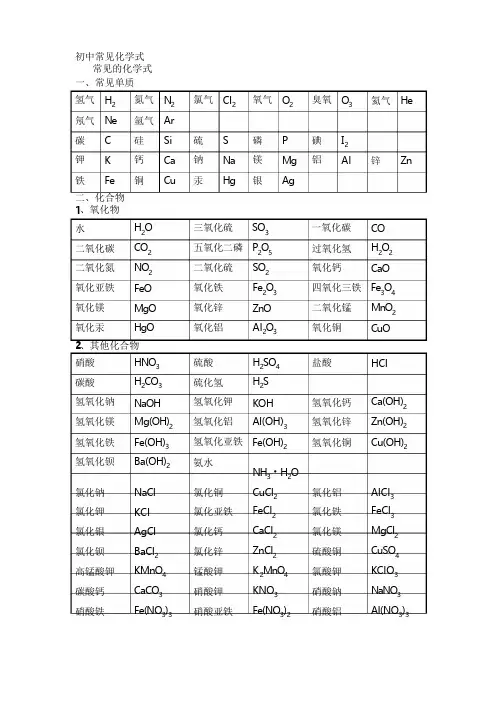
初中常见化学式常见的化学式 一、常见单质氢气 H 2 氮气 N 2 氯气 Cl 2氧气 O 2臭氧 O 3氦气 He氖气 Ne 氩气 Ar碳钾CK 硅钙 SiCa 硫钠 SNa 磷镁 PMg 碘铝I 2Al锌 Zn铁Fe铜Cu汞Hg银Ag二、化合物 1、氧化物水H 2O 三氧化硫 SO 3 一氧化碳 CO 二氧化碳 CO 2 五氧化二磷 P 2O 5 过氧化氢 H 2O 2 二氧化氮 NO 2 二氧化硫 SO 2 氧化钙CaO氧化亚铁 FeO 氧化铁 Fe 2O 3 四氧化三铁 Fe 3O 4氧化镁氧化汞MgOHgO 氧化锌氧化铝ZnOAl 2O 3 二氧化锰氧化铜MnO 2CuO2、其他化合物 硝酸碳酸氢氧化钠氢氧化镁HNO 3 H 2CO 3NaOHMg(OH)2 硫酸硫化氢氢氧化钾氢氧化铝H 2SO 4 H 2SKOHAl(OH)3盐酸氢氧化钙氢氧化锌 HClCa(OH)2 Zn(OH)2氢氧化铁氢氧化钡Fe(OH)3 Ba(OH)2 氢氧化亚铁 Fe(OH)2氨水 NH 3·H 2O 氢氧化铜Cu(OH)2氯化钠氯化钾氯化银氯化钡高锰酸钾碳酸钙硝酸铁 NaClKClAgClBaCl 2 KMnO 4 CaCO 3 Fe(NO 3)3氯化铜氯化亚铁氯化钙氯化锌锰酸钾硝酸钾硝酸亚铁 CuCl 2 FeCl 2 CaCl 2 ZnCl 2 K 2MnO 4 KNO 3 Fe(NO 3)2氯化铝氯化铁氯化镁硫酸铜氯酸钾硝酸钠硝酸铝AlCl 3 FeCl 3 MgCl 2 CuSO 4 KClO 3 NaNO 3 Al(NO 3)3碳酸钠碳酸氢钠硝酸银Na2CO3NaHCO3AgNO3碳酸钙硫酸铁硝酸钡CaCO3Fe2(SO4)3Ba(NO3)2碳酸铵硫酸亚铁硝酸铵(NH4)2CO3FeSO4NH4NO3硫酸钡BaSO43、常见有机化合物甲烷CH4乙醇C2H5OH葡萄糖C6H12O6初中化学方程式全(已配平).一、化合反应1、镁在空气中燃烧:2Mg+O点燃2MgO22、铁在氧气中燃烧:3Fe+2O点燃Fe O2343、铝在空气中燃烧:4Al+3O点燃2Al O2234、氢气在空气中燃烧:2H+O点燃2H O2225、红磷在空气中燃烧:4P+5O点燃2P O2256、硫粉在空气中燃烧:S+O点燃SO227、碳在氧气中充分燃烧:C+O点燃CO228、碳在氧气中不充分燃烧:2C+O点燃2CO29、二氧化碳通过灼热碳层:C+CO高温2CO210、一氧化碳在氧气中燃烧:2CO+O点燃2CO2211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO+H O===H CO222 12、生石灰溶于水:CaO+H O===Ca(OH)2213、无水硫酸铜作干燥剂:CuSO+5H O====CuSO·5H O424214、钠在氯气中燃烧:2Na+Cl点燃2NaCl2二、分解反应315、实验室用双氧水制氧气:2H O MnO2H O+O↑2222216、加热高锰酸钾:2KMnO加热K MnO4+MnO+O↑422217、水在直流电的作用下分解:2H O通电2H↑+O↑22218、碳酸化学物理学报不稳定而分解:H CO===H O+CO↑232219、高温煅烧石灰石(二氧化碳工业制法):CaCO高温CaO+CO↑32三、置换反应20、铁和硫酸铜溶液反应:Fe+CuSO==FeSO+Cu4421、锌和稀硫酸反应(实验室制氢气):Zn+H SO==ZnSO+H↑244222、镁和稀盐酸反应:Mg+2HCl===MgCl+H↑2223、氢气还原氧化铜:H+CuO加热Cu+H O2224、木炭还原氧化铜:C+2CuO高温2Cu+CO↑225、甲烷在空气中燃烧:CH+2O点燃CO+2H O422226、水蒸气通过灼热碳层:H O+C高温H+CO2227、焦炭还原氧化铁:3C+2Fe O高温4Fe+3CO2↑23其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO==Cu(OH)↓+Na SO4422 29、甲烷在空气中燃烧:CH+2O点燃CO+2H O4222:30、酒精在空气中燃烧:C H OH+ 3O 点燃 2CO +3H O2 5 2 2 231、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe O 高温 2Fe+ 3CO2 3 233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH) + CO ==== CaCO ↓+ H O2 23 234、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO ==== Na CO +H O2 23 235、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法) CaCO +2HCl === CaCl +H O +CO ↑3 2 2 236、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO + 2HCl === 2NaCl +HO3 2+CO ↑2一. 物质与氧气的反应: (1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O 点燃 2MgO22. 铁在氧气中燃烧:3Fe+ 2O 点燃 Fe O2 3 43. 铜在空气中受热:2Cu+ O 加热 2CuO24. 铝在空气中燃烧:4Al +3O 点燃 2Al O2 2 35. 氢气中空气中燃烧:2H +O 点燃 2H O2 2 26. 红磷在空气中燃烧:4P+ 5O 点燃 2P O2 2 57. 硫粉在空气中燃烧: S +O 点燃 SO2 28. 碳在氧气中充分燃烧:C+ O 点燃 CO2 29. 碳在氧气中不充分燃烧:2C+ O 点燃 2CO2(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O 点燃 2CO2 211. 甲烷在空气中燃烧:CH +2O 点燃 CO 2H O4 2 2 212. 酒精在空气中燃烧:C H OH +3O 点燃 2CO + 3H O2 5 2 2 2二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H O 通电 2H ↑+ O ↑2 2 214. 加热碱式碳酸铜:Cu (OH) CO 加热 2CuO +H O +CO ↑2 23 2 215. 加热氯酸钾(有少量的二氧化锰):2KClO ==== 2KCl+ 3O ↑3 216. 加热高锰酸钾:2KMnO4 加热 K MnO +MnO +O ↑2 4 2 217. 碳酸不稳定而分解:H CO === H O +CO ↑2 3 2 218. 高温煅烧石灰石:CaCO 高温 CaO +CO ↑3 2三.几个氧化还原反应:19. 氢气还原氧化铜:H + CuO 加热 Cu+ H O2 220. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO ↑22 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe O 高温 4Fe+ 3CO ↑2 3 222. 焦炭还原四氧化三铁:2C +Fe O 高温 3Fe+ 2CO ↑3 4 223. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe O 高温 2Fe +3CO2 3 225. 一氧化碳还原四氧化三铁:4CO +Fe O 高温 3Fe+ 4CO 3 4四.单质、氧化物、酸、碱、盐的相互关系2(1)金属单质+酸 -------- 盐+氢气 (置换反应) 26. 锌和稀硫酸 Zn+ H SO = ZnSO + H ↑2 4 4 227. 铁和稀硫酸 Fe +H SO = FeSO + H ↑244228.镁和稀硫酸Mg+H SO=MgSO+H↑244229.铝和稀硫酸2Al+3H SO=Al(SO)+3H↑24243230.锌和稀盐酸Zn+2HCl===ZnCl+H↑2231.铁和稀盐酸Fe+2HCl===FeCl+H↑2232.镁和语文教案格式稀盐酸Mg2HCl===MgCl+H↑2233.铝和稀盐酸2Al+6HCl==2AlCl+3H↑32(2)金属单质+盐(溶液)-------另一种金属+另一种盐34.铁和硫酸铜溶液反应:Fe+CuSO===FeSO+Cu4435.锌和硫酸铜溶液反应:Zn+CuSO===ZnSO+Cu4436.铜和硝酸汞溶液反应:Cu+Hg(NO)===Cu(NO)+Hg3232(3)碱性氧化物+酸--------盐+水37.氧化铁和稀盐酸反应:Fe O+6HCl===2FeCl+3H O233238.氧化铁和稀硫酸反应:Fe O+3H SO===Fe(SO)+3H O2324243239.氧化铜和稀盐酸反应:CuO+2HCl====CuCl+H O2240.氧化铜和稀硫酸反应:CuO+H SO====CuSO+H O244241.氧化镁和稀硫酸反应:MgO+H SO====MgSO+H O244242.氧化钙和稀盐酸反应:CaO+2HCl====CaCl+H O22(4)酸性氧化物+碱--------盐+水43.苛性钠暴露在空气中变质:2NaOH+CO====Na CO+H O223244.苛性钠吸收二氧化硫气体:2NaOH+SO====Na SO+H O223245.苛性钠吸收三氧化硫气体:2NaOH+SO====Na SO+H O324246.消石灰放在空气中变质:Ca(OH)+CO====CaCO↓+H O223247.消石灰吸收二氧化硫:Ca(OH)+SO====CaSO↓+H O2232(5)酸+碱--------盐+水48.盐酸和烧碱起反应:HCl+NaOH====NaCl+H O249.盐酸和氢氧化钾反应:HCl+KOH====KCl+H O250.盐酸和氢氧化初中家长会课件铜反应:2HCl+Cu(OH)====CuCl+2H O222 51.盐酸和氢氧化钙反应:2HCl+Ca(OH)====CaCl+2H O22252.盐酸和氢氧化铁反应:3HCl+Fe(OH)====FeCl+3H O33253.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)====AlCl+3H O33254.硫酸和烧碱反应:H SO4+2NaOH====Na SO+2H O224255.硫酸和氢氧化钾反应:H SO4+2KOH====K SO+2H O224256.硫酸和氢氧化铜反应:H SO4+Cu(OH)====CuSO+2H O224257.硫酸和氢氧化铁反应:3H SO+2Fe(OH)====Fe(SO4)+6H O24323258.硝酸和烧碱反应:HNO3+NaOH====NaNO+H O32(6)酸+盐--------另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO+2HCl===CaCl H O+CO↑322260.碳酸钠与稀盐酸反应:Na CO+2HCl===2NaCl+H O+CO↑232261.碳酸镁与稀盐酸反应:MgCO+2HCl===MgCl+H O+CO↑322262.盐酸和硝酸银溶液反应:HCl+AgNO===AgCl↓+HNO3363.硫酸和碳酸钠反应:Na CO+H SO===Na SO+H O+CO↑2324242264.硫酸和氯化钡溶液反应:H O+BaCl====BaSO↓+2HCl2S424(7)碱+盐--------另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO====Cu(OH)↓Na SO422466.氢氧化钠与氯化铁:3NaOH FeCl====Fe(OH)↓3NaCl3367.氢氧化钠与氯化镁:2NaOH MgCl====Mg(OH)↓2NaCl2268.氢氧化钠与氯化铜:2NaOH CuCl====Cu(OH)↓2NaCl2269.氢氧化钙与碳酸钠:Ca(OH)Na CO===CaCO↓2NaOH2233(8)盐+盐-----两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl+AgNO====AgCl↓+NaNO3371.硫酸钠和氯化钡:Na SO+BaCl====BaSO↓+2NaCl2424五.其它反应:72.二氧化碳溶解于水:CO+H O===H CO222373.生石灰溶于水:CaO+H O===Ca(OH)2274.氧化钠溶于水:Na O+H O====2NaOH2275.三氧化硫溶于水:SO+H O====H SO322476.硫酸铜晶体受热分解:CuSO·5H O加热CuSO5H O424277.无水硫酸铜作干燥剂:CuSO+5H O====CuSO·5H4242化学方程式反应现象应用2Mg+O点燃或Δ2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟2白色信号弹2Hg+O点燃或Δ2HgO银白液体、生成红色固体拉瓦锡实验22Cu+O点燃或Δ2CuO红色金属变为黑色固体24Al+3O点燃或Δ2Al O银白金属变为白色固体2233Fe+2O点燃Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热4Fe+3O2高温22Fe O23C+O点燃CO剧烈燃烧、白光、放热、使石灰水变浑浊22S+O点燃SO剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.22氧气中蓝紫色火焰2H O点燃2H O淡蓝火焰、放热、生成使无水CuSO变蓝的液体(水)高能燃2224料4P+5O2点燃2P O剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧25气含量CH+2O点燃2H O+CO蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4222变蓝的液体(水)甲烷和天然气的燃烧4 2C H+5O点燃2H O+4CO蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和22222使无水CuSO变蓝的液体(水)氧炔焰、焊接切割金属42KClO MnO2、Δ2KCl+3O↑生成使带火星的木条复燃的气体实验室制备氧气322KMnOΔK2MnO MnO+O↑紫色变为黑色、生成使带火星木条复燃的气体实验4422室制备氧论文气2HgOΔ2Hg+O↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验22H2O通电2H↑+O↑水通电分解为氢气和氧气电解水22Cu(OH)COΔ2CuO+H O+CO↑绿色变黑色、试管壁有液体、使石灰水变浑浊气22322体铜绿加热NH HCOΔNH↑+H O+CO↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳43322酸氢铵长期暴露空气中会消失Zn+H SO=ZnSO+H↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气2442Fe+H SO=FeSO+H↑有大量气泡产生、金属颗粒逐渐溶解2442Mg+H SO=MgSO+H↑有大量气泡产生、金属颗粒逐渐溶解24422Al+3H SO=Al(SO4)+3H↑有大量气泡产生、金属颗粒逐渐溶解24232Fe O+3HΔ2Fe+3H O红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢2322气的还原性Fe O+4HΔ3Fe+4H O黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、3422利用氢气的还原性WO+3HΔW+3H O冶炼金属钨、利用氢气的还原性322MoO+3HΔMo+3H O冶炼金属钼、利用氢气的还原性3222Na+ClΔ或点燃2NaCl剧烈燃烧、黄色火焰离子化合物的形成、2H+Cl点燃或光照2HCl点燃苍白色火焰、瓶口白雾共价化合物的形成、制备22盐酸CuSO+2NaOH=Cu(OH)↓+Na SO蓝色沉淀生成、上部为澄清溶液质量守恒定律4224实验2C+O点燃2CO煤炉中常见反应、空气污染物之一、煤气中毒原因22CO+O点燃2CO蓝色火焰煤气燃烧22C+CuO高温2Cu+CO↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶2炼金属2Fe O+3C高温4Fe+3CO↑冶炼金属232Fe O+2C高温3Fe+2CO↑冶炼金属342C+CO2高温2COCO+H O=H CO碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文2223H COΔCO↑+H O石蕊红色褪去2322Ca(OH)+CO=CaCO↓+H O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁2232CaCO+H O+CO=Ca(HCO)白色沉淀逐渐溶解溶洞的形成,石头的风化32232Ca(HCO)ΔCaCO↓+H O+CO↑白色沉淀、产生使澄清石灰水变浑浊的气体水32322垢形成.钟乳石的形成2NaHCOΔNa CO+H O+CO↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头32322CaCO高温CaO+CO↑工业制备二氧化碳和生石灰32CaCO+2HCl=CaCl+H O+CO↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实3222验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1.镁在空气中燃烧:2Mg+O点燃2MgO22.铁在氧气中燃烧:3Fe+2O点燃Fe O2343.铜在空气中受热:2Cu+O加热2CuO24.铝在空气中燃烧:4Al+3O2点燃2Al O235.氢气中空气中燃烧:2H+O点燃2H O2226.红磷在空气中燃烧(研究空气组成的实验):4P+5O点燃2P O5227.硫粉在空气中燃烧:S+O点燃SO228.碳在氧气中充分燃烧:C+O点燃CO229.碳在氧气中不充分燃烧:2C+O点燃2CO2(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O点燃2CO2211.甲烷在空气中燃烧:CH+2O点燃CO+2H O422212.酒精在空气中燃烧:C H OH+3O点燃2CO+3H O25222(3)氧气的来源:13.玻义耳研究空气的成分实验2HgO加热Hg+O↑214.加热高锰酸钾:2KMnO加热K MnO+MnO+O↑(实验室制氧气原理1)4242215.过氧化氢在二氧化锰作催化剂条件下分解反应:H O MnO2H O+O↑(实22222验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H O通电2H↑+O↑222 17.生石灰溶于水英语六级作文:CaO+H O==Ca(OH)2218.二氧化碳可溶于水:H O+CO==H CO2223三、质量守恒定律:19.镁在空气中燃烧:2Mg+O点燃2MgO220.铁和硫酸铜溶液反应:Fe+CuSO===FeSO+Cu4421.氢气还原氧化铜:H+CuO加热Cu+H O2222.镁还原氧化铜:Mg+CuO加热Cu+MgO四、碳和碳的氧化物:(1)碳的化学性质23.碳在氧气中充分燃烧:C+O点燃CO2224.木炭还原氧化铜:C+2CuO高温2Cu+CO↑225.焦炭还原氧化铁:3C+2Fe2O高温4Fe+3CO↑32(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C+O点燃CO2227.煤炉的中层:CO+C高温2CO228.煤炉的上部蓝色火焰的产生:2CO+O点燃2CO22(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO+2HCl==CaCl+H O+CO↑322230.碳酸不稳定而分解:H CO==H O+CO↑232231.二氧化碳可溶于水:H O+CO==H CO222332.高温煅烧石灰石(工业制二氧化碳):CaCO高温CaO+CO↑3233.石灰水与中学历史教学园地二氧化碳反应(鉴别二氧化碳):Ca(OH)+CO===CaCO↓+H O2232(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+CuO加热Cu+CO235.一氧化碳的可燃性:2CO+O点燃2CO22其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na CO2HCl==2NaCl+H O+CO↑2322五、燃料及其利用:37.甲烷在空气中燃烧:CH+2O点燃CO+2H O422238.酒精在空气中燃烧:C H OH+3O2点燃2CO+3H O252239.氢气中空气中燃烧:2H+O点燃2H O222六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+O点燃2MgO241.铁在氧气中燃烧:3Fe+2O点燃Fe O23442.铜在空气中受热:2Cu+O加热2CuO243.铝在空气中形成氧化膜:4Al+3O=2Al O223(2)金属单质酸--------盐氢气(置换反应)44.锌和稀硫酸Zn+H SO=ZnSO+H↑244245.铁和稀硫酸Fe+H SO=FeSO+H↑244246.镁和稀硫酸Mg+H SO=MgSO+H↑244247.铝和稀硫酸2Al+3H SO=Al(SO)+3H↑24243248.锌和稀盐酸Zn+2HCl==ZnCl+H↑2249.铁和稀盐酸Fe+2HCl==FeCl+H↑2250.镁和稀盐酸Mg+2HCl==MgCl+H↑2251.铝和稀盐酸2Al+6HCl==2AlCl+3H↑32(3)金属单质盐怎样学好高中物理(溶液)-------新金属新盐52.铁和硫酸铜溶液反应:Fe+CuSO==FeSO+Cu4453.锌和硫酸铜溶液反应:Zn+CuSO==ZnSO+Cu4454.铜和硝酸汞溶液反应:Cu+Hg(NO)==Cu(NO)+Hg3232(3)金属铁的治炼原理:55.3CO+2Fe O高温4Fe+3CO↑232七、酸、碱、盐1、酸的化学性质(1)酸金属--------盐氢气(见上)(2)酸金属氧化物--------盐水56.氧化铁和稀盐酸反应:Fe O+6HCl==2FeCl+3H O233257.氧化铁和稀硫酸反应:Fe O+3H2SO4==Fe(SO4)+3H O2323258.氧化铜和稀盐酸反应:CuO+2HCl==CuCl+H2O259.氧化铜和稀硫酸反应:CuO+H SO4==CuSO+H O242(3)酸碱--------盐水(中和反应)60.盐酸和烧碱起反应:HCl+NaOH==NaCl+H O261.盐酸和氢氧化钙反应:2HCl+Ca(OH)==CaCl+2H O22262.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)==AlCl+3H O332 63.硫酸和烧碱反应:H SO+2NaOH==Na SO+2H O24242(4)酸盐--------另一种酸另一种盐64.大理石与稀盐酸反应:CaCO+2HCl==CaCl+H O+CO↑322265.碳酸钠与稀盐酸反应:Na CO+2HCl==2NaCl+H O+CO↑232266.碳酸氢钠与稀盐酸反应:NaHCO+HCl==NaCl+H O+CO↑32267.硫酸和氯化钡溶液反应:H SO+BaCl==BaSO↓+2HCl24242、碱的幼儿园小班音乐教案化学性质(1)碱非金属氧化物--------盐水68.苛性钠暴露在空气中变质:2NaOH+CO==Na CO+H O223269.苛性钠吸收二氧化硫气体:2NaOH+SO==Na SO+H O223270.苛性钠吸收三氧化硫气体:2NaOH+SO==Na SO+H O324271.消石灰放在空气中变质:Ca(OH)+CO==CaCO↓+H O22323、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH ==Na 2SO 3+ H 2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO 26、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O72. 消石灰吸收二氧化硫:Ca(OH) +SO == CaSO ↓+ H O2 23 2(2)碱 酸-------- 盐 水(中和反应,方程式见上) (3)碱 盐 -------- 另一种碱 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH) +Na CO == CaCO ↓+ 2NaOH2 23 33、盐的化学性质(1)盐(溶液) 金属单质------- 另一种金属 另一种盐 74. 铁和硫酸铜溶液反应:Fe+ CuSO == FeSO +Cu4 4(2)盐 酸-------- 另一种酸 另一种盐75.碳酸钠与稀盐酸反应: Na CO +2HCl == 2NaCl +H O+ CO ↑2 3 2 2碳酸氢钠与稀盐酸反应:NaHCO +HCl== NaCl+ H O +CO ↑3 2 2(3)盐 碱 -------- 另一种碱 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH) +Na CO == CaCO ↓+ 2NaOH2 23 3(4)盐 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO == AgCl↓+NaNO 378.硫酸钠和氯化钡:Na SO +BaCl == BaSO4↓+2NaCl2 4 2一、其他反应类型31、二氧化碳通入澄清石灰水中:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O2、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O△5、酒精燃烧:C 2H 5OH + 3O 2点燃 2CO 2 + 3H 2O点燃。
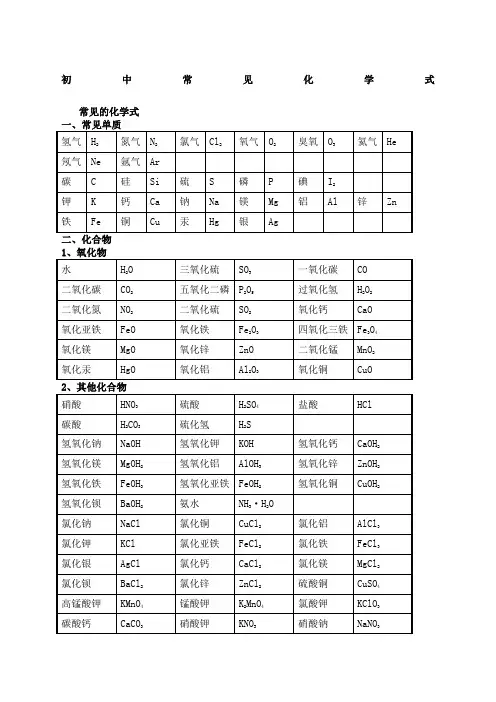
初中常见化学式常见的化学式氢气H2氮气N2氯气Cl2氧气O2臭氧O3氦气He氖气Ne 氩气Ar碳 C 硅Si 硫S 磷P 碘I2钾K 钙Ca 钠Na 镁Mg 铝Al 锌Zn 铁Fe 铜Cu 汞Hg 银Ag水H2O 三氧化硫SO3一氧化碳CO二氧化碳CO2五氧化二磷P2O5过氧化氢H2O2二氧化氮NO2二氧化硫SO2氧化钙CaO氧化亚铁FeO 氧化铁Fe2O3四氧化三铁Fe3O4氧化镁MgO 氧化锌ZnO 二氧化锰MnO2氧化汞HgO 氧化铝Al2O3氧化铜CuO硝酸HNO3硫酸H2SO4盐酸HCl碳酸H2CO3硫化氢H2S氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙CaOH2氢氧化镁MgOH2氢氧化铝AlOH3氢氧化锌ZnOH2氢氧化铁FeOH3氢氧化亚铁FeOH2氢氧化铜CuOH2氢氧化钡BaOH2氨水NH3·H2O氯化钠NaCl 氯化铜CuCl2氯化铝AlCl3氯化钾KCl 氯化亚铁FeCl2氯化铁FeCl3氯化银AgCl 氯化钙CaCl2氯化镁MgCl2氯化钡BaCl2氯化锌ZnCl2硫酸铜CuSO4高锰酸钾KMnO4锰酸钾K2MnO4氯酸钾KClO3碳酸钙CaCO3硝酸钾KNO3硝酸钠NaNO3一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2点燃 2CO9、二氧化碳通过灼热碳层:2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === CaOH213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2MnO22H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K22+O2↑172O 通电 2H2↑+O2↑1823 === H2O +CO2↑19、高温煅烧石灰石二氧化碳工业制法:CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4+Cu21、锌和稀硫酸反应实验室制氢气:Zn+ H2SO4== ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2+CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == CuOH2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O30、酒精在空气中燃烧:C2H52点燃 2CO2+3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:23高温 2Fe+ 3CO233CaOH2+ CO2==== CaCO3↓+ H2O34、氢氧化钠和二氧化碳反应除去二氧化碳:2NaOH+ CO2 ==== Na2CO3+H2O35、石灰石或小学音乐教案大理石与稀盐酸反应二氧化碳的实验室制法:CaCO3+2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应泡沫灭火器的原理: Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:1单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. 红磷在空气中燃烧:2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:2点燃 CO29. 碳在氧气中不充分燃烧:2点燃 2CO 2化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO22O12. 酒精在空气中燃烧:C2H52点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2OH2CO3加热 2CuO +H2O +CO215.3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4+MnO2+O2↑17. 碳酸不稳定而分解:H232O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑ 2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O3高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:34高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe23高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:34高温 3Fe+ 4CO21金属单质+酸 -------- 盐+氢气置换反应26. 锌和稀硫酸Zn+ H2SO4= ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4= FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4= MgSO4+H2↑29. 铝和稀硫酸2Al+ 3H2SO4= Al2SO43+3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑2金属单质+盐溶液 ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +HgNO32 === CuNO32+Hg3碱性氧化物+酸 -------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4=== Fe2SO43+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O4酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3+H2O45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:CaOH2+ CO2==== CaCO3↓+ H2O47. 消石灰吸收二氧化硫:CaOH2 +SO2==== CaSO3↓+H2O5酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ CuOH2 ==== CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+ CaOH2 ==== CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+ FeOH3 ==== FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +AlOH3 ==== AlCl3+3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4 +CuOH2==== CuSO4+2H2O57. 硫酸和氢氧化铁反应:3H2SO4+2FeOH3==== Fe2SO43+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O6酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2H2O +CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl === 2NaCl +H2O+ CO2↑61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4=== Na2SO4+H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4+BaCl2==== BaSO4↓+ 2HCl7碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== CuOH2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== FeOH3↓ 3NaCl67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== MgOH2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== CuOH2↓ 2NaCl69. 氢氧化钙与碳酸钠:CaOH2 Na2CO3=== CaCO3↓ 2NaOH8盐+ 盐 ----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO 3 ==== AgCl↓+ NaNO 3 71.硫酸钠和氯化钡:Na 2SO 4+ BaCl 2 ==== BaSO 4↓+ 2NaCl 五.其它反应:72.二氧化碳溶解于水:CO 2+ H 2O === H 2CO 3 73.生石灰溶于水:CaO+ H 2O === CaOH 2 74.氧化钠溶于水:Na 2O +H 2O ==== 2NaOH 75.三氧化硫溶于水:SO 3 +H 2O ==== H 2SO 476.硫酸铜晶体受热分解:CuSO 4·5H 2O 加热 CuSO 4 5H 2O 77.无水硫酸铜作干燥剂:CuSO 4+ 5H 24·5H 2 化学方程式 反应现象 应用 2Mg+ O 点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟 白色信号弹2Hg +O 点燃或Δ2HgO 银白液体、生成红色固体 拉瓦锡实验 2Cu+ O 点燃或Δ2CuO 红色金属变为黑色固体 点燃或Δ2Al 2O 3 银白金属变为白色固体3Fe+ 2O 点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe +3O2高温2Fe 2O 3C+ O 2 点燃CO 2 剧烈燃烧、白光、放热、使石灰水变浑浊S +O 2 点燃SO 2 剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧2H 2 O 2 点燃2H 2O 淡蓝火焰、放热、生成使无水CuSO 4变蓝的液体水 高能燃料 4P +5O2 点燃2P 2O 5 剧烈燃烧、大量白烟、放热、生成白色固体 证明空气中氧气含量CH 4+ 2O 点燃2H 2O+ CO 2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO 42C 2H 2+ 5O 点燃2H 2O +4CO 2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO 4 氧炔焰、焊接切割金属2KClO 3MnO2、Δ2KCl +3O 2↑ 生成使带火星的木条复燃的气体 实验室制备氧气 2KMnO 4Δ K2MnO 4 MnO 2 +O 2↑ 紫色变为黑色、生成使带火星木条复燃的气体 实验室2HgO Δ2Hg+ O 2↑ 红色变为银白、生成使带火星木条复燃的气体 拉瓦锡实验 通电2H 2↑+ O 2↑ 水通电分解为氢气和氧气 电解水Cu 223Δ2CuO +H 2O+ CO 2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体 铜绿加热NH 4HCO 3ΔNH 3↑+ H 2O+ CO 2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体 碳酸Zn+ H 2SO 4=ZnSO 4 +H 2↑ 有大量气泡产生、锌粒逐渐溶解 实验室制备氢气 Fe +H 2SO 4=FeSO 4 +H 2↑ 有大量气泡产生、金属颗粒逐渐溶解 Mg +H 2SO 4 =MgSO 4 +H 2↑ 有大量气泡产生、金属颗粒逐渐溶解 2Al+ 3H 2SO 4=Al 2SO43+ 3H 2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe 2O 3+3H 2 Δ 2Fe +3H 2O 红色逐渐变为银白色、试管壁有液体 冶炼金属、利用氢气的还原性Fe 3O 4 +4H 2 Δ3Fe+ 4H 2O 黑色逐渐变为银白色英语翻译、试管壁有液体 冶炼金属、利WO 3 +3H 2Δ W +3H 2O 冶炼金属钨、利用氢气的还原性 MoO 32 ΔMo +3H 2O 冶炼金属钼、利用氢气的还原性2Na+ Cl 2Δ或点燃2NaCl 剧烈燃烧、黄色火焰 离子化合物的形成、H 2 +Cl 2 点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾 共价化合物的形成、制备盐酸CuSO 4 +2NaOH=CuOH 2↓+ Na 2SO 4 蓝色沉淀生成、上部为澄清溶液 质量守恒定律实验 2C +O 点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因 2点燃2CO 2 蓝色火焰 煤气燃烧C+ CuO 高温2Cu+ CO 2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体 冶炼金属2Fe 2O 3+ 3C 高温4Fe+ 3CO 2↑ 冶炼金属 Fe 3O 4 +2C 高温3Fe+ 2CO 2↑ 冶炼金属 C+ CO2 高温2COCO 2+ H 2O = H 2CO 3 碳酸使石蕊变红 证明碳酸的酸性小学三语文教学论文 H 2CO 3 ΔCO 2↑+ H 2O 石蕊红色褪去CaOH 2 2= CaCO 3↓+ H 2O 澄清石灰水变浑浊 应用CO2检验和石灰浆粉刷墙壁 CaCO 3 +H 2O+ CO 2 = CaHCO 32 白色沉淀逐渐溶解 溶洞的形成,石头的风化CaHCO 32Δ CaCO 3↓+ H 2O +CO 2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体 水垢形成.钟乳石的形成2NaHCO 3ΔNa 2CO 3+ H 2O +CO 2↑ 产生使澄清石灰水变浑浊的气体 小苏打蒸馒头 CaCO 3 高温 CaO +CO 2↑ 工业制备二氧化碳和生石灰CaCO 3 2+ H 2O +CO 2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体 实验室制备二氧化碳、除水垢 初中化学方程式汇总 一、 氧气的性质:1单质与氧气的反应:化合反应1. 镁在空气中燃烧:2Mg+ O 2 点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O 2 点燃 Fe 3O 43. 铜在空气中受热:2Cu+ O 2 加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al 2O 35. 氢气中空气中燃烧:2H 2 +O 2 点燃 2H 2O6. 4P +5O 2 点燃 2P 2O 57. 硫粉在空气中燃烧: S +O 2 点燃 SO 28. 碳在氧气中充分燃烧:2 点燃 CO 29. 碳在氧气中不充分燃烧:2 点燃 2CO 2化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O 2 点燃 2CO 2 11. 甲烷在空气中燃烧:CH 4 +2O 2 点燃 CO 2 +2H 2O 12. 酒精在空气中燃烧:C 2H 52 点燃 2CO 2 +3H 2O 3氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O 2 ↑14.加热高锰酸钾:2KMnO 4 加热 K 242 +O 2↑实验室制氧气原理115 H 2O 2 MnO 22H 2O+ O 2 ↑实验室制氧气原理2二、自然界中的水:16.水在直流电的作用下分解研究水的组成实验:2H2O 通电 2H2↑+O2↑17.生石灰溶于水英语六级作文:CaO +H2O == CaOH218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁和硫酸铜溶液反应:44+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:1碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3高温 4Fe + 3CO2↑2煤炉中发生的三个反应:几个化合反应26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO282CO +O2点燃 2CO23二氧化碳的制法与性质:29.大理石与稀盐酸反应实验室制二氧化碳:CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3== H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石工业制二氧化碳:CaCO3高温 CaO+ CO2↑33.石灰水与中学历史教学园地二氧化碳反应鉴别二氧化碳:CaOH2 +CO2=== CaCO3↓+H2O4一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO235.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应灭火器的原理:Na2CO32HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2+2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2+3H2O39.氢气中空气中燃烧:2H2+ O2点燃 2H2六、金属1金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:2 = 2Al2O32金属单质酸 -------- 盐氢气置换反应44. 锌和稀硫酸Zn+ H2SO4= ZnSO4+ H2↑45. 铁和稀硫酸Fe +H2SO4= FeSO4+H2↑46. 镁和稀硫酸Mg +H2SO4= MgSO4+ H2↑47. 铝和稀硫酸2Al+ 3H2SO4= Al2SO43+3H2↑48. 锌和稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49. 铁和稀盐酸Fe +2HCl == FeCl2 +H2↑50. 镁和稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑3金属单质盐怎样学好高中物理溶液 ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe +CuSO4 == FeSO4+Cu53. 锌和硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4+Cu54. 铜和硝酸汞溶液反应:Cu +HgNO32 == CuNO32+Hg3金属铁的治炼原理:55.3CO +2Fe2O3高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质1酸金属 -------- 盐氢气见上2酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3+6HCl ==2FeCl3+3H2O57. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4 == Fe2SO43+3H2O58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl2+H2O59. 氧化铜和稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O3酸碱 -------- 盐水中和反应60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反应:2HCl+ CaOH2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +AlOH3 == AlCl3+3H2O63. 硫酸和烧碱反应:H2SO4+ 2NaOH == Na2SO4+2H2O4酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2+H2O+ CO2↑65.碳酸钠与稀盐酸反应: Na2CO3+2HCl == 2NaCl+ H2O+ CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+H2O+ CO2↑67. 硫酸和氯化钡溶液反应:H2SO4+BaCl2== BaSO4↓+2HCl2、碱的幼儿园小班音乐教案化学性质1 碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3+H2O70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4+H2O71.消石灰放在空气中变质:CaOH2+ CO2== CaCO3↓+H2O72. 消石灰吸收二氧化硫:CaOH2 +SO2== CaSO3↓+ H2O2碱酸-------- 盐水中和反应,方程式见上3碱盐 -------- 另一种碱另一种盐73. 氢氧化钙与碳酸钠:CaOH2 +Na2CO3== CaCO3↓+ 2NaOH3、盐的化学性质1盐溶液金属单质------- 另一种金属另一种盐74. 铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4+Cu2盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3+2HCl == 2NaCl +H2O+ CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+ H2O +CO2↑3盐碱 -------- 另一种碱另一种盐76. 氢氧化钙与碳酸钠:CaOH2 +Na2CO3== CaCO3↓+ 2NaOH4盐盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO3== AgCl↓+NaNO378.硫酸钠和氯化钡:Na2SO4+BaCl2== BaSO4↓+2NaCl一、其他反应类型1、二氧化碳通入澄清石灰水中:CO2 + CaOH2== CaCO3↓+ H2O2、氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3+ H2O3、氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH==Na2SO3+ H2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO25、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O6、甲烷燃烧:CH4 + 2O2CO2+ 2H2O△点燃点燃。
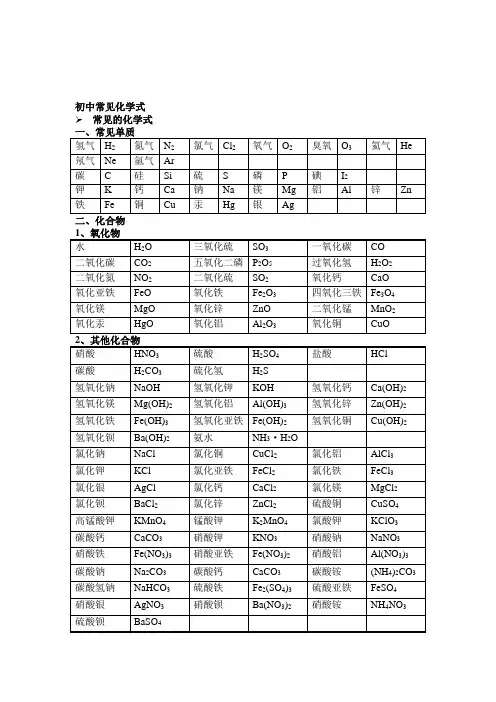
初中常见化学式 常见的化学式初中化学方程式全(已配平). 一、化合反应1、镁在空气中燃烧:2Mg+ O点燃 2MgO2、铁在氧气中燃烧:3Fe +2O点燃 Fe3O 43、铝在空气中燃烧:4Al+ 3O点燃 2Al2O 34、氢气在空气中燃烧:2H2 +O点燃 2H2O5、红磷在空气中燃烧:4P +5O点燃 2P2O 56、硫粉在空气中燃烧: S+ O点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO 9、二氧化碳通过灼热碳层: C +CO高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2MnO22H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2+O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3=== H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO高温 CaO+ CO2↑ 三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4== ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2+H2↑23、氢气还原氧化铜:H2+CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4+2O2点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2+CO27、焦炭还原氧化铁:3C +2Fe2O高温 4Fe +3CO2↑ 其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4+2O2点燃 CO2+2H2O30、酒精在空气中燃烧:C2H5OH+ 3O点燃 2CO2+3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe2O高温 2Fe+ 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2==== CaCO3↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3+H2O35、石灰石(大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl === CaCl2+H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理):Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O点燃 Fe3O 43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O点燃 2Al2O 35. 氢气中空气中燃烧:2H2+O2点燃 2H2O6. 红磷在空气中燃烧:4P+ 5O点燃 2P2O 57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C+ O点燃 CO29. 碳在氧气中不充分燃烧:2C+ O点燃 2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4+2O点燃 CO22H2O12. 酒精在空气中燃烧:C2H5OH +3O点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO加热 2CuO +H2O +CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4+MnO2+O2↑17. 碳酸不稳定而分解:H2CO3=== H2O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe3O4高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe2O高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:4CO +Fe3O4高温 3Fe+ 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸 -------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4= ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4= FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4= MgSO4+H2↑29. 铝和稀硫酸2Al+ 3H2SO4= Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3+3H2↑(2)金属单质+盐(溶液) ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2=== Cu(NO3)2+Hg(3)碱性氧化物+酸 -------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4=== Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2+H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2+H2O(4)酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3+H2O45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2==== CaCO3↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2+SO2==== CaSO3↓+H2O(5)酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化铜反应:2HCl+ Cu(OH)2 ==== CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3+3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2==== CuSO4+2H2O57. 硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3+H2O(6)酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3+2HCl === CaCl2H2O +CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl === 2NaCl +H2O+ CO2↑61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+ AgNO 3 === AgCl↓+ HNO 3 63.硫酸和碳酸钠反应:Na 2CO 3+H 2SO 4 === Na 2SO 4+H 2O +CO 2↑ 64.硫酸和氯化钡溶液反应:H 2S O 4+BaCl 2 ==== BaSO 4 ↓+ 2HCl (7)碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO 4 ==== Cu(OH)2↓ Na 2SO 4 66.氢氧化钠与氯化铁:3NaOH FeCl 3 ==== Fe(OH)3↓ 3NaCl 67.氢氧化钠与氯化镁:2NaOH MgCl 2 ==== Mg(OH)2↓ 2NaCl 68. 氢氧化钠与氯化铜:2NaOH CuCl 2 ==== Cu(OH)2↓ 2NaCl 69. 氢氧化钙与碳酸钠:Ca(OH)2 Na 2CO 3 === CaCO 3↓ 2NaOH (8)盐+ 盐 ----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl +AgNO 3 ==== AgCl↓+ NaNO 3 71.硫酸钠和氯化钡:Na 2SO 4+ BaCl 2 ==== BaSO 4↓+ 2NaCl 五.其它反应:72.二氧化碳溶解于水:CO 2+ H 2O === H 2CO 3 73.生石灰溶于水:CaO+ H 2O === Ca(OH)2 74.氧化钠溶于水:Na 2O +H 2O ==== 2NaOH 75.三氧化硫溶于水:SO 3+H 2O ==== H 2SO 476.硫酸铜晶体受热分解:CuSO 4·5H 2O 加热 CuSO 4 5H 2O77.无水硫酸铜作干燥剂:CuSO 4+ 5H 2O ==== CuSO 4·5H 2化学方程式 反应现象 应用2Mg+ O 2点燃或Δ2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟 白色信号弹 2Hg +O 点燃或Δ2HgO 银白液体、生成红色固体 拉瓦锡实验 2Cu+ O 点燃或Δ2CuO 红色金属变为黑色固体 4Al+ 3O 点燃或Δ2Al 2O 3 银白金属变为白色固体3Fe+ 2O 点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe +3O2高温2Fe 2O 3C+ O 点燃CO 2 剧烈燃烧、白光、放热、使石灰水变浑浊 S +O 点燃SO 2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2 O点燃2H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P +5O2 点燃2P2O 5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+ 5O点燃2H2O +4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+ O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO +H2O+ CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+ H2SO4=ZnSO4+H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe +H2SO4=FeSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg +H2SO4=MgSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2Δ 2Fe +3H2O红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2Δ3Fe+ 4H2O黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl点燃或光照 2HCl点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO +O2点燃2CO2蓝色火焰煤气燃烧C+ CuO 高温2Cu+ CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4+2C高温3Fe+ 2CO2↑ 冶炼金属C+ CO2 高温2COCO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性H 2CO3ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 +H2O+ CO2= Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰CaCO3 +2HCl=CaCl2+ H2O +CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg+ O点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O点燃 Fe3O 43. 铜在空气中受热:2Cu+ O加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O 35. 氢气中空气中燃烧:2H2+O2点燃 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P +5O点燃 2P2O 57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C +O点燃 CO29. 碳在氧气中不充分燃烧:2C +O点燃 2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O点燃 2CO211. 甲烷在空气中燃烧:CH4+2O2点燃 CO2+2H2O12. 酒精在空气中燃烧:C2H5OH +3O点燃 2CO2+3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2↑14.加热高锰酸钾:2KMnO加热 K2MnO4+ MnO2+O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+O2↑17.生石灰溶于水CaO +H2O == Ca(OH)218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O点燃 2MgO20.铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3C + 2Fe2O3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO +O点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3== H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO高温 CaO+ CO2↑ 33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2+CO2=== CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO235.一氧化碳的可燃性:2CO +O点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO32HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4+2O点燃 CO2+2H2O38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2+3H2O39.氢气中空气中燃烧:2H2+ O点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O点燃 Fe3O 442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:4Al+ 3O2 = 2Al2O3(2)金属单质酸 -------- 盐氢气(置换反应)44. 锌和稀硫酸Zn+ H2SO4= ZnSO4+ H2↑45. 铁和稀硫酸Fe +H2SO4= FeSO4+H2↑46. 镁和稀硫酸Mg +H2SO4= MgSO4+ H2↑47. 铝和稀硫酸2Al+ 3H2SO4= Al2(SO4)3+3H2↑48. 锌和稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49. 铁和稀盐酸Fe +2HCl == FeCl2+H2↑50. 镁和稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝和稀盐酸2Al+ 6HCl == 2AlCl3+3H2↑(3)金属单质盐(溶液) ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe +CuSO4 == FeSO4+Cu53. 锌和硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4+Cu54. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2== Cu(NO3)2+Hg(3)金属铁的治炼原理:55.3CO +2Fe2O3高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸金属 -------- 盐氢气(见上)(2)酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3+6HCl ==2FeCl3+3H2O57. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4 == Fe2(SO4)3+3H2O58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl2+H2O59. 氧化铜和稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O(3)酸碱 -------- 盐水(中和反应)60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl3+3H2O63. 硫酸和烧碱反应:H2SO4+ 2NaOH == Na2SO4+2H2O(4)酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2+H2O+ CO2↑65.碳酸钠与稀盐酸反应: Na2CO3+2HCl == 2NaCl+ H2O+ CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3+HCl== NaCl+H2O+ CO2↑67. 硫酸和氯化钡溶液反应:H2SO4+BaCl2== BaSO4↓+2HCl2、碱的化学性质(1)碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3+H2O70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4+H2O71.消石灰放在空气中变质:Ca(OH)2+ CO 2 == CaCO 3↓+H 2O 72. 消石灰吸收二氧化硫:Ca(OH)2+SO 2 == CaSO 3↓+ H 2O (2)碱 酸-------- 盐 水(中和反应,方程式见上) (3)碱 盐 -------- 另一种碱 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2+Na 2CO 3 == CaCO 3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液) 金属单质------- 另一种金属 另一种盐 74. 铁和硫酸铜溶液反应:Fe+ CuSO 4 == FeSO 4+Cu (2)盐 酸-------- 另一种酸 另一种盐75.碳酸钠与稀盐酸反应: Na 2CO 3 +2HCl == 2NaCl +H 2O+ CO 2↑ 碳酸氢钠与稀盐酸反应:NaHCO 3+HCl== NaCl+ H 2O +CO 2↑ (3)盐 碱 -------- 另一种碱 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 +Na 2CO 3 == CaCO 3↓+ 2NaOH (4)盐 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO 3 == AgCl↓+NaNO 3 78.硫酸钠和氯化钡:Na 2SO 4+BaCl 2 == BaSO4↓+2NaCl 一、其他反应类型1、二氧化碳通入澄清石灰水中:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O2、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O3、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH==Na 2SO 3+ H 2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO 25、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O6、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△ 点燃 点燃。

初三化学常见化学式一、单质1. 金属单质- 铁:Fe- 铜:Cu- 铝:Al- 镁:Mg- 锌:Zn- 银:Ag- 金:Au(初中阶段了解)- 汞(水银):Hg2. 非金属单质- 氢气:H₂- 氧气:O₂- 氮气:N₂- 氯气:Cl₂- 碳(石墨、金刚石):C- 硫:S- 磷(白磷、红磷):P二、氧化物1. 金属氧化物- 氧化镁:MgO- 氧化铝:Al₂O₃- 氧化铁(三氧化二铁):Fe₂O₃(铁锈的主要成分) - 四氧化三铁:Fe₃O₄(磁铁矿的主要成分)- 氧化铜:CuO- 氧化钙(生石灰):CaO2. 非金属氧化物- 二氧化碳:CO₂- 一氧化碳:CO- 水:H₂O- 过氧化氢(双氧水):H₂O₂- 二氧化硫:SO₂- 三氧化硫:SO₃三、酸1. 盐酸:HCl(氯化氢气体的水溶液)2. 硫酸:H₂SO₄3. 硝酸:HNO₃四、碱1. 氢氧化钠:NaOH(俗称烧碱、火碱、苛性钠)2. 氢氧化钙:Ca(OH)₂(俗称熟石灰、消石灰,其水溶液叫石灰水)3. 氢氧化钾:KOH4. 氨水:NH₃·H₂O五、盐1. 氯化钠:NaCl(食盐的主要成分)2. 碳酸钠:Na₂CO₃(俗称纯碱、苏打)3. 碳酸氢钠:NaHCO₃(俗称小苏打)4. 碳酸钙:CaCO₃(大理石、石灰石的主要成分)5. 硫酸铜:CuSO₄- 硫酸铜晶体(五水硫酸铜):CuSO₄·5H₂O(俗称胆矾、蓝矾)6. 氯化银:AgCl(不溶于水和稀硝酸的白色沉淀)7. 硫酸钡:BaSO₄(不溶于水和稀硝酸的白色沉淀)8. 硝酸钾:KNO₃(复合肥料)。

初中常见化学式大全1.水——H2O2.盐酸——HCl3.硫ic酸——H2SO44.氨水——NH3·H2O5.氯气——Cl26.氯化钠——NaCl7.亚硫酸——H2SO38.稀盐酸——HCl9.稀硝酸——HNO310.酸性氯化铁——FeCl311.氢气——H212.二氧化硫——SO213.氢氧化钾——KOH14.氧气——O215.二氧化碳——CO216.氯化铁——FeCl217.硝酸铜——Cu(NO3)218.氯化钙——CaCl219.氢氯酸——HClO420.氢氧化铝——Al(OH)321.氢氧化钠——NaOH22.硝酸铵——NH4NO323.氨——NH324.碳酸钠——Na2CO325.氢氧化镁——Mg(OH)226.氰化钾——KCN27.氢氧化铜——Cu(OH)228.氢氟酸——HF29.硫酸铜——CuSO430.硝酸铁——Fe(NO3)331.氢氧化钙——Ca(OH)232.磷酸氢二钙——CaHPO433.硝酸钠——NaNO334.氧化铁——Fe2O335.氟化钾——KF36.氯化铝——AlCl337.氯化镁——MgCl238.碳酸氢钠——NaHCO339.硫化氢——H2S40.硫酸——H2SO441.氢氧化氨——NH4OH42.硫酸钠——Na2SO443.一氧化碳——CO44.三氧化二铁——Fe2O3·3H2O45.硫化钠——Na2S46.氯化钾——KCl47.氯化镁——MgCl2·6H2O48.酒石酸氢钾——KHC4H4O649.硫酸镁——MgSO4·7H2O50.氮气——N252.碳酸钙——CaCO353.碘——I254.硝酸钾——KNO355.碘酸钾——KIO356.氢氯化铁——FeCl3·6H2O57.硒——Se58.硫酸钾——K2SO459.亚硝酸钠——NaNO260.碳——C61.乙醇——C2H5OH62.氯气水——HClO63.氯酸钾——KClO364.亚硝酸——HNO265.草酸——H2C2O466.氯酸铜——Cu(ClO3)267.氨气水——NH3·H2O68.硝酸钙——Ca(NO3)269.硝酸铜——Cu(NO3)2·3H2O70.硫酸钙——CaSO471.二氧化银——Ag2O72.氢氧化亚铁——Fe(OH)273.氢溴酸——HBr74.氯酸——HClO375.氰化物——CN-76.氟——F277.高锰酸钾——KMnO479.氧化钙——CaO80.一氧化氮——NO81.二氧化钯——PdO282.氟化氢——HF83.硫酸酯——SO484.氯酸亚铁——Fe(ClO3)285.氢氟化钾——KHF286.碳酸锂——Li2CO387.氢氧化锰——Mn(OH)288.氢氧化铬——Cr(OH)389.硫酸亚铁——FeSO490.碘酸——HIO391.氢氧化镁——Mg(OH)2·H2O92.浓硫酸——H2SO493.硝酸钴——Co(NO3)294.氯酸亚铜——Cu(ClO3)2·6H2O95.氯酸铁——Fe(ClO3)396.氢氧化钇——Y(OH)397.氯酸钠——NaClO398.硫酸亚碲——H2TeO499.氢氧化锌——Zn(OH)2100.碘化钙——CaI2101.硫酸锌——ZnSO4102.氯酸镁——Mg(ClO3)2103.氯酸铅——Pb(ClO3)2104.氢氧化铯——CsOH106.亚硫酸钙——CaSO3·0.5H2O 107.氯酸钡——Ba(ClO3)2108.氯酸钙——Ca(ClO3)2109.硫酸铜氨——CuSO4·(NH3)2 110.硫酸铁氨——FeSO4·(NH3)2 111.氯酸钇——Y(ClO3)3112.氢氧化镨——Pr(OH)3113.氮化钡——Ba3N2114.氯氧化钾——KClO4115.氯氧化钴——Co(ClO4)2116.氯氧化亚铅——Pb(ClO4)2117.氯氧化亚铜——Cu2(ClO4)2·6H2O 118.氢氧化锶——Sr(OH)2·8H2O 119.氯氧化亚铁——Fe(ClO4)2120.氢氧化铌——Nb(OH)5。
常见物质的化学式与名称:单质:C:碳S:硫P:磷Fe:铁Mg:镁Al:铝Hg:汞Zn:锌Cu:铜Ag:银O2:氧气H2:氢气N2:氮气O3:臭氧氧化物:CO:一氧化碳CO2:二氧化碳SO2:二氧化硫MnO2:二氧化锰SO3:三氧化硫H2O2:过氧化氢CuO:氧化铜CaO:氧化钙MgO:氧化镁HgO:氧化汞Fe2O3:氧化铁Al2O3:氧化铝H2O:水P2O5:五氧化二磷Fe3O4:四氧化三铁NaCl:氯化钠HCl:盐酸H2SO4:硫酸KMnO4:高锰酸钾K2MnO4:锰酸钾KClO3:氯酸钾九年级化学方程式分类:1.碳充分燃烧:C+O 2点燃CO22.碳不充分燃烧: 2C+O 2点燃2CO3.一氧化碳燃烧: 2CO+O2点燃2CO24.产生一氧化碳: C+CO2高温2CO5.硫燃烧:S+O2点燃SO26.红磷燃烧:4P+5O2点燃2P2O57.氢气燃烧:2H2+O2点燃2H2O8.铁燃烧:3Fe+2O2点燃Fe3O49.镁燃烧:2Mg+O2点燃2MgO10.铝燃烧:4Al+3O2点燃2Al2O311.甲烷燃烧:CH4+2O2点燃CO2+2H2O12.酒精燃烧:C2H5OH+3O2点燃2CO2+3H2O13.呼吸原理:C6H12O6+6O26CO2+6H2O14.高锰酸钾制氧气: 2KMnO4△K2MnO4+MnO2+O2↑15.氯酸钾制氧气:2KClO3MnO22KCl+3O2↑△16.过氧化氢制氧气: 2H2O2 MnO22H2O +O2↑17.水通电分解:2H2O2H2↑+O2↑18.氧化汞分解:2HgO△2Hg+O2↑19.实验室制氢气的原理:Zn+H2SO4=ZnSO4+H2↑20.镁或硫酸性质: Mg+H2SO4=MgSO4+H2↑21.铁或硫酸性质: Fe+H2SO4=FeSO4+H2↑22.铝或硫酸性质: 2Al+3H2SO4=Al2(SO4)3+H2↑23.镁或盐酸性质: Mg+2HCl=MgCl2+H2↑24.锌或盐酸性质: Zn+2HCl=ZnCl2+H2↑25.铁或盐酸性质: Fe+2HCl=FeCl2+H2↑26.铝或盐酸性质: 2Al+6HCl=2AlCl3+3H2↑27.酸或碱的性质: NaOH+HCl=NaCl+H2O28.酸或碱的性质: Ca(OH)2+2HCl=CaCl2+H2O29.酸或碱的性质: 2NaOH+H2SO4=Na2SO4+2H2O30.酸或碱的性质: Ca(OH)2+H2SO4=CaSO4+2H2O31.制取水煤气的原理: C+H2O高温H2+CO32.氢气还原氧化铜: H2+CuO△Cu+H2O33.碳还原氧化铜: C+2CuO高温2Cu+CO2↑34.一氧化碳还原氧化铜: CO+CuO△Cu+CO235.氢气还原氧化铁: Fe2O3+3H高温2Fe+3H2O36.碳还原氧化铁: 2Fe2O3+3C高温4Fe+3CO2↑37.工业炼铁的原理: Fe2O3+3CO高温2Fe+3CO238.铁置换硫酸铜中的铜: Fe+CuSO4=Cu+FeSO439.铜置换硝酸银中的银: Cu+2AgNO3=2Ag+Cu(NO3)240.铝置换硫酸铜中的铜: 2Al+3CuSO4=3Cu+Al2(SO4)341.生石灰制熟石灰: H2O+CaO=Ca(OH)242.碳酸不稳定: H2CO3=H2O+CO2↑43.工业制生石灰的原理: CaCO高温CaO+CO2↑44.除铁锈的原理或金属氧化物与酸的性质:Fe2O3+6HCl=2FeCl3+3H2OFe2O3+3H2SO4=Fe2(SO4)3+3H2O45.制取CO2或CaCO3 作补钙药剂:CaCO3+2HCl=CaCl2+CO2↑+H2O46.碳酸盐或酸的性质:Na2CO3+2HCl=2NaCl+CO2↑+H2O47.治疗胃酸过多症的原理:NaHCO3 +HCl=NaCl+CO2↑+H2O48.氯化钠与硝酸银反应产生白色沉淀:NaCl+AgNO3=NaNO3+AgCl↓49.制取氢氧化钠的原理:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH50.氢氧化钠与硫酸铜反应产生蓝色沉淀:2NaOH+CuSO4=Na2SO4+Cu(OH)251.检验CO2或澄清石灰水变浑浊原理:CO2+Ca(OH)2=CaCO3↓+H2O52.烧碱变质的原理:CO2+2NaOH=Na2CO3+H2O53.碱与非金属氧化物的性质:SO2+2NaOH=Na2SO3+H2O SO3+2NaOH=Na2SO4+H2O 54.非金属氧化物的性质:H2O+CO2 =H2CO3H2O+SO2 =H2SO3H2O+SO3 =H2SO4。
1.酸:HCl盐酸、H2SO4硫酸、HNO3硝酸、H3PO4磷酸、H2CO3碳酸、H2SO3亚硫酸。
2.碱:NaOH氢氧化钠、KOH氢氧化钾、Ca(OH)2氢氧化钙、Ba(OH)2氢氧化钡、Cu(OH)2氢氧化铜、Fe(OH)3氢氧化铁、Fe(OH)2氢氧化亚铁、Al(OH)3氢氧化铝、Mg(OH)2氢氧化镁。
3.盐:NaCl氯化钠、Na2CO3碳酸钠、K2CO3碳酸钾、CaCO3碳酸钙、BaCO3碳酸钡。
4.其他:CO一氧化碳、CO2二氧化碳、SO2二氧化硫、SO3三氧化硫、P2O5五氧化二磷。
5.氧化物:•CO(一氧化碳)•CO2(二氧化碳)•SO2(二氧化硫)•SO3(三氧化硫)•P2O5(五氧化二磷)•Fe2O3(氧化铁,铁红)•Fe3O4(四氧化三铁)•MnO2(二氧化锰)•H2O(水)•CuO(氧化铜,蓝黑色固体)•Ag2O(氧化银,黑色固体)6.金属单质:•K(钾)•Na(钠)•Al(铝)•Fe(铁)•Cu(铜)•Ag(银)•Zn(锌)•Mg(镁)7.非金属单质:•H2(氢气)•N2(氮气)•O2(氧气)•S(硫,黄色晶体)•P(红磷,暗红色粉末)•C(石墨,灰黑色粉末)•Cl2(氯气,黄绿色气体)8.稀有气体单质:•He(氦气)•Ne(氖气)•Ar(氩气)•Xe(氙气)•Rn(氡气)9.酸式盐:•NaHCO3(碳酸氢钠)•KH2PO4(磷酸二氢钾)•Ca(HCO3)2(碳酸氢钙)10.络合物:•CuSO4·5H2O(五水硫酸铜)•AgNO3·NH3·H2O(银氨溶液)11.其他:•NaClO4(高氯酸钠)•NaClO3(氯酸钠)•Na2SO4(硫酸钠)•Na2SO3(亚硫酸钠)•NaHSO4(硫酸氢钠)•NaHSO3(亚硫酸氢钠)•Na2S2O3(硫代硫酸钠,又名大苏打)•Na2CO3·10H2O(十水碳酸钠)•Na2CO3(碳酸钠,又名纯碱或苏打)•Na2S(硫化钠)•NaCN(氰化钠)•Na2O(氧化钠)•NaOH(氢氧化钠,又名烧碱或苛性钠)•CaO(氧化钙,生石灰)•Ca(OH)2(氢氧化钙,熟石灰)•CaCO3(碳酸钙,石灰石或大理石的主要成分)•CaCl2(氯化钙)•Ca(ClO)2(次氯酸钙,漂白粉的主要成分)12.化学式相关反应:•金属与酸反应:如铁与稀硫酸反应生成硫酸亚铁和氢气。
初中常见化学式和化学方程式➢常见的化学式
二、化合物
常见元素与原子团的化合价
常见初中化学方程式(已配平).
一、化合反应
1、镁在空气中燃烧:2Mg+ O
2
点燃 2MgO
2、铁在氧气中燃烧:3Fe +2O
2点燃 Fe
3
O
4
3、铝在空气中燃烧:4Al+ 3O
2点燃 2Al
2
O
3
4、氢气在空气中燃烧:2H
2 +O
2
点燃 2H
2
O
5、红磷在空气中燃烧:4P +5O
2点燃 2P
2
O
5
6、硫粉在空气中燃烧: S+ O
2点燃 SO
2
7、碳在氧气中充分燃烧:C +O
2 点燃 CO
2
8、碳在氧气中不充分燃烧:
2
点燃 2CO
9、二氧化碳通过灼热碳层:
2
高温 2CO
10、一氧化碳在氧气中燃烧:2CO +O
2 点燃 2CO
2
11:CO
2 +H
2
O === H
2
CO
3
12、生石灰溶于水:CaO+ H
2O === Ca(OH)
2
13、无水硫酸铜作干燥剂:CuSO
4 +5H
2
O ==== CuSO
4
·5H
2
O
14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl
二、分解反应
15、实验室用双氧水制氧气:2H
2O
2
MnO22H2O +O2↑
16、加热高锰酸钾:2KMnO
4
加热 K242 +O2↑
17:2KClO
3
MnO2 2KCl+ 3O2↑
18、水在直流电的作用下分解:2H
2O 通电 2H
2
↑+O
2
↑
19、碳酸化学性质不稳定而分解:H
232O +CO
2
↑
20、高温煅烧石灰石(二氧化碳工业制法):CaCO
3
高温 CaO+ CO2↑ 三、置换反应
21、铁和硫酸铜溶液反应:Fe+ CuSO
4 == FeSO
4
+Cu
22、锌和稀硫酸反应(实验室制氢气):Zn+ H
2SO
4
== ZnSO
4
+H
2
↑
23、氢气还原氧化铜:H
2 +CuO △ Cu +H
2
O
24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO
2
↑
25、水蒸气通过灼热碳层:H
2O +C 高温 H
2
+CO
四.单质、氧化物、酸、碱、盐的相互关系
(1)金属单质+酸 -------- 盐+氢气(置换反应)
26. 锌和稀硫酸Zn+ H
2SO
4
== ZnSO
4
+ H
2
↑
27. 铁和稀硫酸Fe +H
2SO
4
== FeSO
4
+ H
2
↑
28. 铝和稀硫酸2Al+ 3H
2SO
4
= Al
2
(SO
4
)
3
+3H
2
↑
29. 锌和稀盐酸Zn +2HCl === ZnCl
2+ H
2
↑
(2)金属单质+ 盐(溶液) ------- 另一种金属+另一种盐
30. 铁和硫酸铜溶液反应:Fe+ CuSO
4 === FeSO
4
+ Cu
31. 铜和硝酸汞溶液反应:Cu +Hg(NO
3)
2
=== Cu(NO
3
)
2
+Hg
(3)碱性氧化物+酸 -------- 盐+ 水
32. 氧化铁和稀盐酸反应:Fe
2O
3
+ 6HCl === 2FeCl
3
+ 3H
2
O
33. 氧化铁和稀硫酸反应:Fe
2O
3
+3H
2
SO
4
=== Fe
2
(SO
4
)
3
+ 3H
2
O
34. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl
2 +H
2
O
35. 氧化镁和稀硫酸反应:MgO+ H
2SO
4
==== MgSO
4
+ H
2
O
(4)酸性氧化物+碱 -------- 盐+水
36.氢氧化钠暴露在空气中变质:2NaOH +CO
2 ==== Na
2
CO
3
+H
2
O
37.氢氧化钠吸收二氧化硫气体:2NaOH +SO
2 ==== Na
2
SO
3
+H
2
O
38.氢氧化钠吸收三氧化硫气体:2NaOH+ SO
3 ==== Na
2
SO
4
+ H
2
O
39.二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)
2+ CO
2
==== CaCO
3
↓+ H
2
O
(5)酸+碱 -------- 盐+水
40.盐酸和氢氧化钠反应:HCl+ NaOH ==== NaCl+ H
2
O
41.盐酸和氢氧化铜反应:2HCl+ Cu(OH)
2 ==== CuCl
2
+2H
2
O
42. 盐酸和氢氧化铁反应:6HCl+ 2Fe(OH)
3 ==== 2FeCl
3
+3H
2
O
43.氢氧化铝药物治疗胃酸过多:6HCl +2Al(OH)
3 ==== 2AlCl
3
+3H
2
O
44.硫酸和氢氧化钾反应:H
2SO
4
+2KOH ==== K
2
SO
4
+2H
2
O
45. 硝酸和烧碱反应:HNO
3+ NaOH ==== NaNO
3
+H
2
O
(6)酸+盐 -------- 另一种酸+另一种盐
46.大理石与稀盐酸反应:CaCO
3 +2HCl === CaCl
2
+H
2
O +CO
2
↑
47.碳酸钠与稀盐酸反应: Na
2CO
3
+2HCl === 2NaCl +H
2
O+ CO
2
↑
48.盐酸和硝酸银溶液反应:HCl+ AgNO
3=== AgCl↓+ HNO
3
49. 硫酸和碳酸钠反应:Na
2CO
3
+H
2
SO
4
=== Na
2
SO
4
+H
2
O +CO
2
↑
50. 硫酸和氯化钡溶液反应:H
2SO
4
+BaCl
2
==== BaSO
4
↓+ 2HCl
(7)碱+盐 -------- 另一种碱+另一种盐
51.氢氧化钠与硫酸铜:2NaOH +CuSO
4 ==== Cu(OH)
2
↓+ Na
2
SO
4
52.氢氧化钠与氯化铁:3NaOH +FeCl
3 ==== Fe(OH)
3
↓+3NaCl
53.氢氧化钠与氯化镁:2NaOH + MgCl
2 ==== Mg(OH)
2
↓+ 2NaCl
54. 氢氧化钙与碳酸钠:Ca(OH)
2 +Na
2
CO
3
=== CaCO
3
↓+ 2NaOH
(8)盐+ 盐 ----- 两种新盐
55.氯化钠溶液和硝酸银溶液:NaCl +AgNO
3==== AgCl↓+ NaNO
3
56.硫酸钠和氯化钡:Na
2SO
4
+ BaCl
2
==== BaSO
4
↓+ 2NaCl
其他
57、甲烷在空气中燃烧:CH
4 +2O
2
点燃 CO2 +2H2O
58、一氧化碳还原氧化铜:CO +CuO △ Cu+ CO
2。