甲酸钠的生产工艺
- 格式:docx
- 大小:15.61 KB
- 文档页数:2


甲酸的简要甲酸,又称作蚁酸。
蚂蚁分泌物和蜜蜂的分泌液中含有蚁酸,当初人们蒸馏蚂蚁时制得蚁酸,故有此名。
甲酸无色而有刺激气味,且有腐蚀性,人类皮肤接触后会起泡红肿。
熔点8.4℃,沸点100.8℃。
由于甲酸的结构特殊,它的一个氢原子和羧基直接相连。
也可看做是一个羟基甲醛。
因此甲酸同时具有酸和醛和性质。
在化学工业中,甲酸被用于橡胶、医药、染料、皮革种类工业。
甲酸性质甲酸与水和大多数的极性有机溶剂混溶,在烃中也有一定的溶解性。
在烃中及气态下,甲酸以通过以氢键结合的二聚体形态出现。
在气态下,氢键导致甲酸气体与理想气体状态方程之间存在较大的偏差。
液态和固态的甲酸由连续不断的通过氢键结合的甲酸分子组成。
甲酸甲酸具有与大多数其他羧酸相同的性质,尽管在通常情况下甲酸不会生成酰氯或者酸酐。
直到不久以前,所有试图将甲酸转化成这些衍生物的尝试都以产物一氧化碳告终。
甲酸酐可由甲酰氟和甲酸钠在零下78摄氏度反应得到。
甲酰氯可由将氯化氢气体通过零下60度1-甲酰基咪唑的一氯甲烷溶液得到。
甲酸脱水分解为一氧化碳和水。
甲酸具有和醛类似的还原性。
它能起银镜反应,把银氨络离子中的银离子还原成金属银,而自己被氧化成二氧化碳和水:HCOOH+2AgOH→2Ag+2H2O+CO2甲酸是唯一能和烯烃进行加成反应的羧酸。
甲酸在酸的作用下(如硫酸,氢氟酸),和烯烃迅速反应生成甲酸酯。
但是类似于Koch反应的副反应也会发生,产物是更高级的羧酸。
大多数的甲酸盐溶于水。
物化性质主要成分:含量:一级≥90.0%; 二级≥85.0%。
外观与性状:无色透明发烟液体,有强烈刺激性酸味。
熔点(℃):8.2沸点(℃):100.8相对密度(水=1):1.23相对蒸气密度(空气=1):1.59饱和蒸气压(kPa):5.33(24℃)燃烧热(kJ/mol):254.4临界温度(℃):306.8临界压力(MPa):8.63辛醇/水分配系数的对数值:-0.54闪点(℃):68.9(O.C)引燃温度(℃):410爆炸上限%(V/V):57.0爆炸下限%(V/V):18.0溶解性:与水混溶,不溶于烃类,可混溶于醇。

甲酸钠的历史、用途和产品标准一、中国的甲酸钠、甲酸和草酸的技术源头1957年,许多科研单位和大学需要草酸试剂。
天津试剂四厂决定试制草酸,但是对草酸的生产原理和工艺设备一窍不通。
问题和愿望通过天津市化工局逐级上报,不久,化工部请来了罗马尼亚专家。
罗马尼亚专家,一个高高大大的胖子。
他到试剂四厂讲授技术原理,还带来了一套工艺流程图,没有设备图纸。
通过罗马尼亚专家的讲解,大家才明白,制造草酸首先要生产草酸的原料——甲酸钠,生产原理是煤气与苛化碱在高压卧式合成釜合成甲酸钠。
罗马尼亚的草酸工艺流程图交给天津有机合成厂工程技术人员观看讨论临摹(硫酸纸描图)后转交天津化工局设计处(现天津化工设计院),由该处进行化工设备设计。
在等待设计制造设备的期间,张树礼仔细研读翻译过来的技术文件及图纸,在序言部分,他读到“也可以使用塔式反应器合成甲酸钠……”,受到启发,张树礼和几位年青的工友决定使用钢管制造管式反应器,开始用煤气及岢化得来的烧碱试制甲酸钠。
采用小型煤气发生炉产生的煤气经过压缩机输入合成管道,当时试验的合成管道采用直径4英寸,高6米的管道制成,车间高度不够,就把管道竖在正中间,探伸到车间顶棚上面的天窗上。
由于对合成压力和管道的质量没有把握,大家担心爆炸,用装满沙土的麻袋包围着合成管道垒了一米多高的防护墙,像座碉堡。
合成管道内填充细碎的焦碳,来增加煤气与烧碱溶液的接触反应面积。
煤气从管道的底部压入,烧碱溶液从管道上端淋下,进行逆流合成反应。
合成压力4公斤,预热温度100度、102度、103度。
当时的工艺难度是确定多长的合成管道能够使合成反应温度提上来。
那时安装一个温度计都很困难,没有热电偶,只有玻璃管温度计。
最初的试验异常艰难。
二、采用罗马尼亚技术工艺试制草酸1958年,国家决定试剂四厂重新选址建设新厂,引进罗马尼亚甲酸钠、甲酸、草酸的生产工艺技术,最终能够生产甲酸钠、甲酸、草酸等。
为了组织新厂建设,天津市化工局任命了建厂委员会成员,陈健任主任,张树礼任副主任。

山 东 化 工 收稿日期:2018-08-22作者简介:陈巨喜(1966—),男,湖南衡阳人,衡阳屹顺化工有限公司总经理,化工工艺工程师,研究方向:化工工艺。
甲酸钠酸化法生产甲酸工艺改进陈巨喜(衡阳屹顺化工有限公司,湖南衡阳 421000)摘要:甲酸钠酸化法是最早工业化生产甲酸的传统工艺,但由于该工艺产能规模小、连续化程度低、生产成本高、劳动强度大、污染严重,随着国内环保力度的加大及鲁西化工和肥城阿斯德化工甲酸甲脂法年产20万t甲酸装置的建成,该法生存空间越来越窄。
本文通过对甲酸钠酸化法生产甲酸装置进行工艺改进,唤发了新的活力,市场竞争力不亚于甲酸甲脂法生产工艺。
关键词:甲酸钠酸法;甲酸;工艺改进中图分类号:TQ225.12+1 文献标识码:B 文章编号:1008-021X(2018)19-0104-03ProcessImprovementinProductionofFormicAcidbyAcidulationofSodiumFormateChenJuxi(HengyangYishunChemicalCo.,Ltd.,Hengyang 421000,China)Abstract:Acidulationofsodiumformatetoproduceformicacidisthefirsttraditionaltechnology,however,duetothesmallscaleoftheprocesscapacity,lowdegreeofcontinuity,highproductioncost,highlaborintensityandseriouspollution,withtheincreaseofdomesticenvironmentalprotectionandthebuildof200,000tonsperyearformicacidbymethylformatemethodinLuxichemicalandFeichengAsderchemical,thelivingspaceofthismethodisbecomingnarrower.Inthispaper,throughtheprocessimprovementoftheequipmentforproductionofformicacidbyacidulationofsodiumformate,reproducinganewvigor,themarketcompetitivenessisnolessthantheproductionprocessofmethylformatemethod.Keywords:acidulationofsodiumformate;formicacid;processimprovement 甲酸作为一种有机化工原料,广泛应用于有机化工产品合成、农药、皮革、染料、医药、橡胶、造纸、塑料、建材及畜牧业等行业,其衍生物的用途也十分广泛。

甲酸钠的生产工艺有哪些
一氧化碳合成法
1 、反应原理
制法:一氧化碳和氢氧化钠溶液在160~200℃和2MPa压力下反应生成甲酸钠,然后经硫酸酸解、蒸馏即得成品甲酸。
2、工艺流程简述
甲酸钠工艺流程说明
本工程使用焦炭为原料,经造气除尘、水洗、脱碳、再除尘等工艺,取得工艺所需的一氧化碳气体,再经加热加压与氢氧化钠反应生成甲酸钠溶液,后经蒸发、分离、干燥生成固体产品甲酸钠。
季戊四醇副产法
反应原理
制法:季戊四醇生产过程中利用氢氧化钠提供碱性反应条件,在反应的后续加入甲酸与氢氧化钠中和过程的同时副产甲酸钠,季戊四醇副产的甲酸钠,颜色为白色或者类白色,含量一般在90%到95%之间,一般使用于污水处理和皮革处理。
相比于合成的甲酸钠,有点在于杂质较少没有腐蚀性。
现在国内产季戊四醇副产的生产商较多,产品供应充足。
如:银河化工
新戊二醇副产法
制法
新戊二醇生产中利用液碱产生反应,有甲醛和液碱产生反应添加催化剂产出新戊二醇及其副产甲酸钠,该甲酸钠含量一般在90%
左右颜色为类黑或者棕红,一般用于生产甲酸
三羟甲基丙烷
制法
正丁醛与甲醛水溶液在碱性催化剂作用下发生醇醛缩合反应生成2.2-二羟甲基丁醛,2.2­-二羟甲基丁醛再与过量的甲醛在强碱条件下发生交叉康尼扎罗反应生成三羟甲基丙烷,甲醛被氧化生成甲酸,甲酸与氢氧化钠中和生成甲酸钠。
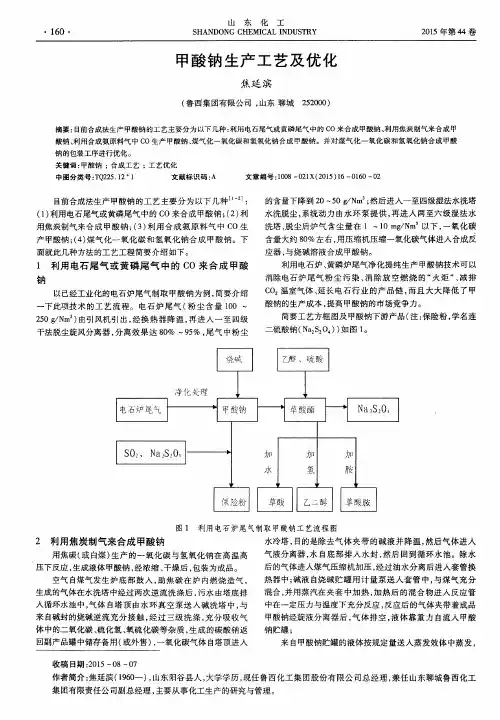

甲酸钠生产工艺
甲酸钠是一种重要的有机化工原料,广泛应用于医药、染料和化学合成等领域。
下面介绍甲酸钠的生产工艺。
甲酸钠的生产工艺主要分为以下几个步骤:
1. 原料准备:将优质甲酸和氢氧化钠固体原料准备好,确保原料的质量和纯度。
2. 中和反应:将甲酸溶液和氢氧化钠溶液按一定比例加入中和反应釜中,进行中和反应。
反应过程中,要控制温度和搅拌速度,使反应物充分混合。
3. 结晶提取:将中和反应后的混合溶液进行结晶提取。
提取过程中,可以采用真空挤压法或蒸发法。
真空挤压法先在提取设备中建立负压,然后将溶液注入设备中,通过挤压滤饼,分离出固体和液体。
蒸发法则将溶液进行加热蒸发,使溶剂蒸发掉,留下固体。
4. 干燥粉碎:将提取出的固体进行干燥处理,以去除残余的水分。
然后将干燥的固体粉碎成所需的颗粒大小。
5. 质量检验:对甲酸钠进行质量检验,检测其纯度、含水量等指标,确保产品符合标准要求。
6. 包装存储:将符合质量要求的甲酸钠进行包装和标识,然后存放在干燥、通风良好的仓库中,避免受潮和变质。
值得注意的是,甲酸钠生产工艺中需要注意安全生产,例如在氢氧化钠固体配备和搅拌过程中,要注意防止冲击和泄漏。
另外,采用环保工艺,控制废气和废水的排放。
以上是甲酸钠的生产工艺简介,每个步骤都需要严格控制操作条件和质量要求,以确保最终产品的质量和纯度。

甲酸钠现场配置步骤
第一:在未知甲酸钠浓度的情况现场做甲酸钠溶解度实验:S=m甲/100g水,充分溶解,静置24h,直到有微量沉淀为止;
第二:知道甲酸钠浓度后据附表1(甲酸钠密度和密度关系),根据现场所需甲酸钠密度、体积、PH,计算所需水、甲酸钠及氢氧化钠的量;
第三:配置时匀速加入甲酸钠量及搅拌要均匀,所配密度越高,配置难度越大,配置过程需加入除泡剂,待加入一定量甲酸钠时需量其密度,未达所需比重继续追加甲酸钠,直到达到预期密度;
第四:配置完成需搅拌12h以上,使用前也需搅拌均匀。
(备注:使用前再加入黄原胶增粘(黄原胶漏斗粘度与时间的实验见附图1),而且黄原胶会降低比重,比重1.29甲酸钠压井液增粘至马氏粘度56s时比重将降至1.275)
附表1
甲酸钠密度与浓度关系
(2008年5月11日试采工艺研究所实验结果表)
附图1黄原胶漏斗粘度与时间关系
0.30%
0.3%(加0.1%NaoH)
0.40%
0.4%(加0.1%NaoH)19
202122232425266
24
48
72144240
粘度(s )
时间(h)
XC 漏斗粘度与时间关系。

二、甲酸的生产方法甲酸生产方法主要有甲酸钠水解法、甲酰胺水解法、轻油液相氧化法,以及甲酸甲酯水解法(甲醇羰基化法)。
1980年以前,世界工业化生产甲酸均用甲酸钠法,该法消耗较高,已逐步被淘汰。
80年代初,美国、德国等公司对甲醇羰基化制甲酸甲酯的工艺进行了深入的研究,成功地开发了甲酸甲酯直接水解制甲酸的生产工艺,研究表明,该工艺是生产甲酸的最佳工艺。
2.1 甲酸主要生产方法2.1.1 甲酸钠水解法甲酸钠水解法的反应式如下:C0 + NaOH →HCOONa2HCOONa + H2SO4→2HCOOH + Na2SO4首先制得含30%的CO发生炉煤气,净化后和25~50%烧碱在160~200℃,1.4~1.8MPa下反应生成甲酸钠。
蒸发分离后,加入硫酸,反应生成甲酸和硫酸钠,再经蒸馏分离,得到纯度大于85%的成品。
该法规模一般在500t/a以下;由于生产成本高,成品质量差,且劳动条件恶劣,污染严重,因此在发达国家均已淘汰。
目前国内绝大多仍采用此方法。
2.1.2 甲酰胺水解法该法首先是CO和甲醇在4.0MPa80℃,以甲醇钠为催化剂反应生成甲酸甲酯。
C0 + CH3OH →HCOOCH3然后,甲酸甲酯与无水的氨在1.3MPa、温度65℃下反应:HCOOCH3 + NH3 →HCONH2 + CH3OH 分馏、精制后得到精制的甲酰胺。
最后由甲酰胺与硫酸发生水解反应:2HCONH2 + Na2SO4 + 2H2O →2HCOOH + (NH4)2SO4再经干燥、冷凝后即得产品,纯度为90~95%。
该法是德国BASF公司的专利,曾为欧洲甲酸生产的主要方法,流程复杂,成本较高,80年代初随着甲酸甲酯水解工艺的开发成功,已渐被淘汰。
2.1.3 轻油液相氧化法该法主要用于生产醋酸,甲酸为副产品,产量约占各种有机酸总产量的15%;此法由英国BP公司开发成功,70年代曾是国外生产甲酸的主要方法;随着美国孟山都公司甲醇低压羰基合成醋酸技术工业化后,该法已被淘汰。

引言:甲酸钠是一种重要的有机化合物,具有广泛的用途和应用领域。
本文将深入介绍甲酸钠的物理性质、化学性质、合成方法、应用领域和安全性等方面的信息,以提供一个全面的了解。
概述:甲酸钠,化学式为HCOONa,是一种白色结晶粉末,在常温下呈无臭性,可以溶解于水。
甲酸钠是一种弱酸盐,它的酸性来源于酸根离子HCOO。
在本文中,我们将详细介绍甲酸钠的物理性质、化学性质、合成方法、应用领域和安全性。
正文:一、物理性质1.外观:甲酸钠呈白色结晶粉末状。
2.溶解性:甲酸钠易溶于水,在水中形成溶液。
3.熔点:甲酸钠的熔点约为252℃。
4.密度:甲酸钠的密度约为1.919g/cm³。
二、化学性质1.酸性:甲酸钠是一种弱酸盐,其酸性来源于酸根离子HCOO。
2.还原性:甲酸钠可以被还原剂还原为甲酸和钠。
3.酸碱反应:甲酸钠可以与强碱反应盐和水。
4.氧化性:甲酸钠本身不具有氧化性。
三、合成方法1.甲酸和碱反应法:将甲酸和碱(如氢氧化钠)反应,甲酸钠和水。
2.醇酸盐法:将甲酸与一种含钠的醇酸盐(如乙酸钠)反应,甲酸钠和醇。
3.电解法:将甲酸溶液通过电解,使甲酸钠析出。
四、应用领域1.制药工业:甲酸钠在制造药物过程中作为中间体和试剂的重要原料。
2.皮革工业:甲酸钠可以用于皮革鞣制,起到固色和增强皮革柔软性的作用。
3.催化剂:甲酸钠可以作为催化剂用于有机合成反应中,具有重要的催化作用。
4.防腐剂:甲酸钠可以用作食品和饲料的防腐剂,延长其保鲜期。
5.其他行业:甲酸钠还可用于染料、农药、油田化学品等领域。
五、安全性1.甲酸钠具有一定的腐蚀性,使用时需注意防护措施。
2.避免与强氧化剂接触,以免发生危险化学反应。
3.避免吸入或接触甲酸钠粉尘,可引起呼吸道不适和皮肤刺激。
4.甲酸钠应储存在干燥、通风良好的地方,远离火源和易燃物品。
总结:甲酸钠是一种重要的有机化合物,具有广泛的用途和应用领域。
本文介绍了甲酸钠的物理性质、化学性质、合成方法、应用领域和安全性。

合成甲酸钠作业操作规程
一、岗位任务
甲酸钠是以铜洗再生气(简称再生气)为原料气(经水洗去掉氨,后经分离罐进入压缩机,(其压力严格控制在100~200毫米水柱,严禁负压操作),气体经二段压缩至20kg/cm2后,送入高压水洗塔洗去CO2(《0.3%》然后进气水分离器,再进混合器与NaOH(200~210g/L)混合。
混合后的物体输送全预热器加热(管内混合物、外套管道通入2—6kg/cm2蒸汽加热),在此期间温度可达110~160℃,同时进行反应,然后气液并流进入合成反应器,生成380~420g/L稀甲酸钠。
反应式:
CO+NaOH=HCOONa
稀甲酸钠经蒸发器浓缩后放入结晶罐结晶,结晶后的料放入离心机,甩干后,经干燥机干燥而得成品甲酸钠。
其中(200~210g/L)的稀碱是用30~32%离子膜碱与软水配制而成。
二、合成甲酸钠岗位工艺指标:
1、原料液碱:30~32%离子膜液碱
配料碱:200~210g/L
2、合成稀钠:
碱含量:lt;4g/L
碳酸钠:lt;10g/L
合成甲酸钠:390~410g/L 3、包装成品:50±0.5kg 一级二级合格
甲酸钠含量≥%959087
水份≤%0.50.51.0
氧氧化钠≤%0.51.0
氯化钠≤%0.51.0
碳酸钠≤%1.01.2
4、压缩机:
进口压力:~200mm水柱出口压力:lt;25kg
油压:0.2~0.3MPa
曲轴箱油位1/2~2/3
5、水洗塔:
水洗塔液位保持2~3灯
水洗塔出口压力20±1kg
水洗后CO2lt;0.3g/L。
甲酸钠的生产工艺
一氧化碳合成法
1 、反应原理
制法:一氧化碳和氢氧化钠溶液在160~200℃和2MPa压力下反应生成甲酸钠,然后经硫酸酸解、蒸馏即得成品甲酸。
2、工艺流程简述
甲酸钠工艺流程说明
本工程使用焦炭为原料,经造气除尘、水洗、脱碳、再除尘等工艺,取得工艺所需的一氧化碳气体,再经加热加压与氢氧化钠反应生成甲酸钠溶液,后经蒸发、分离、干燥生成固体产品甲酸钠。
季戊四醇副产法
反应原理
制法:季戊四醇生产过程中利用氢氧化钠提供碱性反应条件,在反应的后续加入甲酸与氢氧化钠中和过程的同时副产甲酸钠,季戊四醇副产的甲酸钠,颜色为白色或者类白色,含量一般在90%到95%之间,一般使用于污水处理和皮革处理。
相比于合成的甲酸钠,有点在于杂质较少没有腐蚀性。
现在国内产季戊四醇副产的生产商较多,产品供应充足。
新戊二醇副产法
制法
新戊二醇生产中利用液碱产生反应,有甲醛和液碱产生反应
添加催化剂产出新戊二醇及其副产甲酸钠,该甲酸钠含量一般在90%左右颜色为类黑或者棕红,一般用于生产甲酸
三羟甲基丙烷
制法
正丁醛与甲醛水溶液在碱性催化剂作用下发生醇醛缩合反应生成2.2-二羟甲基丁醛,2.2­;-二羟甲基丁醛再与过量的甲醛在强碱条件下发生交叉康尼扎罗反应生成三羟甲基丙烷,甲醛被氧化生成甲酸,甲酸与氢氧化钠中和生成甲酸钠。
目录1 绪论 (2)2 概述 (3)2.1 性质 (3)2.2 性状 (3)2.3 用途 (3)2.4 理化性质 (3)2.5 生产指标 (4)2.6 质量指标: (4)3 本项目研究的主要内容 (5)4 甲酸钠的生产工艺 (7)4.1 反应原理 (7)4.2 甲酸钠工艺流程说明 (7)4.2.1 造气 (7)4.2.2 净化 (9)4.2.3 压缩 (9)4.2.4 脱硫 (9)4.2.5 合成 (10)4.2.6 蒸发分离 (10)5 甲酸钠的用途 (11)5.1 用甲酸钠生产甲酸 (11)5.2 用甲酸钠生产草酸 (12)5.3 用甲酸钠生产保险粉(连二亚硫酸钠) (12)5.4 甲酸钠做为石油钻井液 (14)5.5 甲酸钠的其他用途 (14)6 测定方法及步骤 (16)致谢 (19)参考文献 (20)1 绪论在草酸生产中用一氧化碳和氢氧化钠合成甲酸钠时,由于操作条件的波动,合成液的成分组成亦相应变化。
合成液中可能含有甲酸钠、氢氧化钠、碳酸钠、碳酸氢钠等。
本文提出用pH试纸简便测定合成液的pH值,以判断当在某一pH值时,相应存在的组份及当有干扰组分存在下的分析方法及原理。
因为本分析方法毋须逐项进行,又结合常规的分析法, 故能达到简便、快速的生产控制目的。
使用焦炭为原料,经造气除尘、水洗、脱碳、再除尘等工艺,取得工艺所需的一氧化碳气体,再经加热加压与氢氧化钠反应生成甲酸钠溶液,后经蒸发、分离、干燥生成固体产品甲酸钠。
由于甲酸钠的K b=5.6×10-11,这样的弱碱显然不能用标准酸滴定。
这里采用在碱性中,甲酸钠与高锰酸钾充分反应并生成二氧化锰沉淀。
沉淀在酸性中用草酸溶解,最后用高锰酸钾滴定过量的草酸,即可求得甲酸钠的含量。
2 概述2.1 性质物理化学特性:白色单斜晶系结晶性粉末;有甲酸的气味,具有吸湿性。
易溶于水(以1:1.3 溶于水),溶于甘油,微溶于乙醇,水溶性显中性。
化学式为HCOONa·2H2O,稍有甲酸气味。
湖北泽茂化工有限公司草酸车间甲酸钠预处理岗位操作手册(版本号_______________)编制:_______________审核:_______________批准:_______________日期:_______________目录1、生产工艺规程·················································X/Y 1.1、岗位职责和要求··············································X/Y 1.1.1、岗位任务··················································X/Y 1.1.2、岗位操作范围···············································X/Y 1.1.3、岗位巡回检查···············································X/Y 1.2、生产工艺····················································X/Y 1.2.1、产品及原材料概述···········································X/Y 1.2.2、生产原理···················································X/Y 1.2.3、工艺流程简述(附:工艺流程图)·······························X/Y 1.2.4、工艺指标····················································X/Y 1.3、开车及停车操作················································X/Y 1.3.1、开车前的准备工作············································X/Y 1.3.2、正常开车····················································X/Y 1.3.3、正常停车·····················································X/Y 1.3.4、系统长期停车置换············································X/Y 1.4、正常操作要点··················································X/Y 1.5、不正常现象判断及处理·········································X/Y 1.6、生产应急预案·················································X/Y 1..6.1、突然断电···················································X/Y1.6.2、其它故障····················································X/Y2、设备操作规程··················································X/Y 2.1、设备操作·····················································X/Y 2.2、设备的维护及保养·············································X/Y2.3、主要设备一览表················································X/Y3、安全操作规程··················································X/Y 3.1、安全要求······················································X/Y 3.2、环保指标······················································X/Y 3.3、安全设施及劳动保护············································X/Y3.4安全应急预案···················································X/Y4、管理制度······················································X/Y 4.1、岗位责任制度·················································X/Y 4.2、交接班制度···················································X/Y 4.3、设备定期维护检查制度··········································X/Y 4.4、巡回检查制度·················································X/Y 4.5、岗位操作记录表················································X/Y甲酸钠预处理岗位操作手册1、生产工艺规程1.1、岗位职责和要求1.1.1、岗位任务甲酸钠处理岗位的任务是将严重结块的甲酸钠破碎至2mm以下,使甲酸钠含水降到0.5%以下,包装后供草酸钠岗位使用。
对氯苯甲酸钠生产工艺
氯苯甲酸钠的生产工艺一般包括以下几个步骤:
1. 原料准备:将苯甲酸与氯化钠进行粉碎和干燥处理,以保证原料的纯度和质量。
2. 反应反应槽中加入适量的水,加热至80-90°C左右,然后将
苯甲酸和氯化钠溶解在水中,进行中和反应。
反应过程中产生的氯化氢气体通过排气装置排出。
3. 过滤:将反应后的混合溶液进行澄清,将其中的杂质和固体颗粒通过过滤装置进行过滤。
过滤后的溶液通常是无色澄清的液体。
4. 结晶:将过滤后的溶液加热蒸发,去除部分溶剂,使得浓度上升,然后降温结晶,将溶液中的氯苯甲酸钠结晶出来。
5. 分离与干燥:将结晶出来的固体通过离心机进行分离,然后进行洗涤和干燥处理,以去除残余的溶剂和水分,得到干燥的氯苯甲酸钠产品。
6. 粉碎和包装:将干燥的氯苯甲酸钠进行粉碎,使其颗粒细小均匀,然后进行包装和存储,以便后续的应用和销售。
需要注意的是,在整个生产过程中,应该保持工艺条件的控制,确保反应的选择性和产率,以及产物的纯度。
同时还应采取适
当的环境保护措施,控制废气和废水的排放,确保生产过程的安全环保。
甲酸钠工业生产工艺流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classicarticles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!甲酸钠工业生产工艺流程1. 原料制备氯化钠溶解:将工业盐溶解于水中,制成饱和盐水。
甲酸钠生产工艺
1 反应原理制法:一氧化碳和氢氧化钠溶液在160~200℃和2MPa压力下反应生成甲酸钠,然后经硫酸酸解、蒸馏即得成品甲酸。
2 工艺流程简述(一)甲酸钠工艺流程说明本工程使用焦炭为原料,经造气除尘、水洗、脱碳、再除尘等工艺,取得工艺所需的一氧化碳气体,再经加热加压与氢氧化钠反应生成甲酸钠溶液,后经蒸发、分离、干燥生成固体产品甲酸钠。
各岗位的说明如下:1、造气将焦炭用电动葫芦提升至造气炉上部,从造气炉炉口加焦炭至炉内,焦炭在炉内与风机引(送)进的空气不充分燃烧产生一氧化碳、二氧化碳、氮气等混合气体。
主要反应方程式为:C+O2--------CO2+Q CO2+C-------2CO-Q 2C+O2--------2CO+Q 2、净化从造气炉来的混合气体进入旋风除尘器出去混合气体夹带的大部分固体小颗粒,后进入洗气塔,洗气塔以水为洗涤液,进一步除去混合气体中的固体颗粒,再进入碱洗塔以氢氧化钠溶液为循环吸收液,脱除混合气体中的部分二氧化碳气体,再经旋液分离器分离出来气体夹带的水分进入静电除尘器,通过静电除去剩余的固体小颗粒,再次净化混合气体。
净化工序主要反应方程式:CO2+2NaOH----------Na2CO3+H2O CO2+NaOH------------NaHCO
3 3、压缩净化后的混合气体进入压缩机进行两段压缩,提压至2.0~2.2Mpa,经油水分离器进入混合器,与从预热器来的碱液混合,在一定温度和压力下,碱液与大部分二氧化碳气体反应,基本除去了二氧化碳,取得工艺所需的一氧化碳气体。
压缩工序主要反应
方程式:CO2+2NaOH----------Na2CO3+H2O CO2+NaOH------------NaHCO3 4、合成从上一工序来的一氧化碳气体和氮气加热至140~150度进入合成反应器,在合成反应器中一氧化碳与氢氧化钠反应生成甲酸钠溶液,甲酸钠溶液和氮气及微量一氧化碳气体等混合物经卸压后经入旋液分离器进行气液分离,甲酸钠溶液用泵打入储罐待用,混合气体排入大气。
合成工序主要反应方程式:CO+NaOH--------HCOONa CO2+2NaOH--------Na2CO3+H2O 5、蒸发分离储罐内的甲酸钠溶液用泵输送到蒸发器,用油炉来的导热油加热,蒸发掉大部分水分,形成含量70~80%甲酸钠溶液,后用泵输送到离心机,离心机干得到5%左右的甲酸钠。
6、包装
离心后的甲酸钠溶液用热风吹到热风干燥器干燥,取得合格的甲酸钠产品,进行包装。