第五章 圆二色分析
- 格式:pdf
- 大小:2.08 MB
- 文档页数:42


圆二色谱一、圆二色谱圆二色光谱(简称CD)是应用最为广泛的测定蛋白质二级结构的方法,是研究稀溶液中蛋白质构象的一种快速、简单、较准确的方法。
它可以在溶液状态下测定,较接近其生理状态。
而且测定方法快速简便,对构象变化灵敏,所以它是目前研究蛋白质二级结构的主要手段之一,并已广泛应用于蛋白质的构象研究中。
二、圆二色谱的基本原理光是横电磁波,是一种在各个方向上振动的射线。
其电场矢量 E 与磁场矢量H 相互垂直,且与光波传播方向垂直。
由于产生感光作用的主要是电场矢量,一般就将电场矢量作为光波的振动矢量。
光波电场矢量与传播方向所组成的平面称为光波的振动面。
若此振动面不随时间变化,这束光就称为平面偏振光,其振动面即称为偏振面。
平面偏振光可分解为振幅、频率相同,旋转方向相反的两圆偏振光。
其中电矢量以顺时针方向旋转的称为右旋圆偏振光,其中以逆时针方向旋转的称为左旋圆偏振光。
两束振幅、频率相同,旋转方向相反的偏振光也可以合成为一束平面偏振光。
如果两束偏振光的振幅(强度) 不相同,则合成的将是一束椭圆偏振光。
光学活性物质对左、右旋圆偏振光的吸收率不同,其光吸收的差值ΔA ( Al -Ad) 称为该物质的圆二色性(circular dichroism,简写作CD) 。
圆二色性的存在使通过该物质传播的平面偏振光变为椭圆偏振光,且只在发生吸收的波长处才能观察到。
所形成的椭圆的椭圆率θ为:θ= tg-1 短轴/长轴根据Lambert-Beer 定律可证明椭圆率近似地为:θ= 0. 576lc (εl-εd) = 0. 576lcΔε公式中l 为介质厚度, c 为光活性物质的浓度,εl 及εd分别为物质对左旋及右旋圆偏振光的吸收系数。
测量不同波长下的θ(或Δε) 值与波长λ之间的关系曲线,即圆二色光谱曲线。
在此光谱曲线中,如果所测定的物质没有特征吸收,则其Δε值很小,即得不到特征的圆二色光谱。
当εl >ε d 时,得到的是一个正的圆二色光谱曲线,即被测物质为右旋,如果εl <ε d ,则得到一个负的圆二色光谱曲线,即被测物质为左旋。


圆二色光谱分析法引言五十年代初,生物学研究从宏观领域深入到微观领域,开创了分子生物学的新时代。
随着研究的不断深入和发展,生物学已发展成最活跃的学科之一。
手性(Chirality)是物质结构中的重要特征.即具有不能重叠的三维镜像对映异构体,它们的分子式完全相同,但其中原子或原子基团在空间的配置不同,互为镜像。
凡手性分子都具有光学活性,即可使偏振光的振动面发生旋转。
生物基础分子一般都具有手性,也都具有光学活性。
在自然界中,氨基酸有L型和D型两种对映异构体,组成蛋白质的20种氨基酸,除最简单的甘氨酸不具有手性外,其余都是L型的[1]。
手性分子都具有光学活性。
当单色左旋与右旋的圆偏振光通过某一种手性样品时,该样品对左、右旋圆偏振光的吸收不同,这叫做圆二色性(Circular Dichroism)。
其差值△A=△A L-△A R称为圆二色值,按波长扫描就得到了圆二色谱(CD谱)。
CD谱是特殊的吸收谱,它比一般的吸收谱弱几个量级,但由于它对分子结构十分敏感,因此近十几年来,CD已成为研究分子构型(象)和分子间相互作用的最重要的光谱实验之一。
利用CD研究生物大分子和药物分子,具有重要的科学意义和实用价值[2,3]。
一、蛋白质的圆二色性蛋白质是由氨基酸通过肽键连接而成的具有特定结构的生物大分子。
蛋白质一般有一级结构、二级结构、超二级结构、结构域、三级结构和四级结构几个结构层次[4-6]。
在蛋白质或多肽中,主要的光活性基团是肽链骨架中的肽键、芳香氨基酸残基及二硫桥键。
当平面圆偏振光通过这些光活性的生色基团时,光活性中心对平面圆偏振光中的左、右圆偏振光的吸收不相同,产生的吸收差值,由于这种吸收差的存在,造成了偏振光矢量的振幅差,圆偏振光变成了椭圆偏振光,这就是蛋白质的圆二色性。
圆二色性的大小常用摩尔消光系数差△ (M-1 ·cm-1 )来度量。
蛋白质的CD光谱一般分为两个波长范围,即178—250 nm为远紫外区CD光谱,250—320 nm为近紫外区CD光谱, 具有不同二级结构的蛋白质或多肽所产生CD谱带的位置、吸收的强弱都不相同。

圆二色谱实验总结圆二色谱是用来表征蛋白的二级结构和三级结构的常用方法,在界面课题组主要用来表征肽自组装体的二级结构;通常对于三级结构不予考虑。
这一方法的实验操作容易,与一般的光谱测量相同,但是形成的机制比较复杂。
在此只能说我自己理解了的部分,对于不理解的部分还需要继续查文献进行了解。
1圆二色谱的原理名称中虽有“色谱”两字,但是这一测量方法实际上是一光谱法,光谱法对应的即为电子的跃迁行为。
同时,光谱法中必然存在的定量关系就是朗伯-比尔定律,圆二色谱的方法就是建立在这一光吸收过程上的光谱方法。
1.1预备知识需要推演圆二色谱的原理用到的工具有数学工具和物理知识两个方面,分别叙述如下。
1.1.1 数学工具在推演圆二色谱的数学表达形式时,需要用到一些数学知识,主要有圆的普通方程及参数方程、椭圆的普通方程及参数方程,相关的三角函数知识,这些数学知识基本都在高中阶段学过。
首先说明圆的普通方程和参数方程:圆的普通方程即为仅对圆上点的坐标关系进行描述的方程。
圆上点的特点是对固定点(即圆心)的距离相等,设圆心的坐标为(x0, y0)半径为r,则圆的普通方程为√(x−x0)2+(y−y0)2=r通常用的是化简的形式,为讨论方便,将圆心设为原点,即得到x2+y2=r2利用同角三角函数关系,即sin²θ+cos²θ=1可将上述方程参数化,得到圆的参数方程{y=r sinθx=r cosθ使用同样的思路,可以得到椭圆的参数方程,即{y=b sinθx=a cosθ消去参数后,得到椭圆的标准方程,即x2 a2+y2b2=1上述有关于椭圆的方程中均有a≠b。
1.2 物理预备知识关于物理的预备知识是最基本的波动光学的观点。
按照波动光学的观点,光是在空间中交替传播的电磁场,电场强度的方向与磁感应强度的方向垂直。
从能量分布的角度来说,光的能量被认为主要以电场的形式传播,因而通常也将光的电场强度矢量方向定义为光矢量方向。

圆二色谱原理
圆二色谱是一种用来研究化合物结构和手性性质的重要分析方法。
它利用了分子对圆偏振光的吸收和散射的特性,通过测量样品对左旋和右旋圆偏振光的吸收差异来获取信息。
在这篇文档中,我们将详细介绍圆二色谱的原理和应用。
圆二色谱的原理可以简单地理解为分子结构对圆偏振光的选择性吸收。
当圆偏振光通过手性分子时,分子的结构和构型会决定它们对左旋和右旋圆偏振光的吸收差异。
这种差异可以通过检测样品对左旋和右旋圆偏振光的吸收强度来测量,从而得到有关分子结构和手性性质的信息。
在实际的圆二色谱实验中,常用的仪器是圆二色光谱仪。
它包括一个光源、样品室、检测器和数据处理系统。
光源发出线偏振光,经过样品后变成圆偏振光,然后被检测器检测。
通过改变样品室中的样品和检测器的位置,可以测量不同波长下的圆二色光谱,从而获取更为详细的信息。
圆二色谱在化学、生物化学、药学等领域有着广泛的应用。
在药学中,圆二色谱可以用来研究药物的手性纯度和药效学,帮助药物研发和质量控制。
在生物化学中,圆二色谱可以用来研究蛋白质和核酸的结构和构象变化,有助于理解生物大分子的功能和活性。
在化学领域,圆二色谱也可以用来研究手性催化剂和手性配体的性质,为有机合成提供重要的信息。
总之,圆二色谱作为一种重要的分析方法,具有广泛的应用前景和重要的理论意义。
通过对分子对圆偏振光的选择性吸收的测量和分析,可以获取有关分子结构和手性性质的信息,为化学和生物领域的研究提供重要的支持和帮助。
希望本文对圆二色谱的原理和应用有所帮助,谢谢阅读!。

圆二色谱原理
圆二色谱是一种用于分析物质结构和对手性化合物的光学活性的技术。
它是利用物质对左右旋光的吸收差异来进行分析的,对于手性分子的研究具有非常重要的意义。
在圆二色谱的原理中,主要涉及到两个概念,旋光度和比旋度。
旋光度是指物质溶液对圆偏振光旋转的程度,它是圆二色谱分析的基础。
当圆偏振光通过手性分子溶液时,由于分子的对称性不同,左旋光和右旋光会被不同程度地吸收,从而导致光的旋转。
这种旋转的程度就是旋光度,通常用角度表示。
比旋度是指单位长度内的旋光度,它是一个物质的固有性质,与浓度和物质的性质有关。
可以通过比旋度来判断物质的对手性程度,从而进行对手性分析。
圆二色谱的原理是基于这两个概念的。
当圆偏振光通过样品溶液时,左旋光和右旋光会被不同程度地吸收,从而形成一个圆二色信号。
通过检测这个信号的强度和波长,就可以得到样品的圆二色谱图谱。
在图谱中,不同的吸收峰代表不同的对手性分子,通过比较不同样品的圆二色谱图谱,可以进行对手性分析和结构分析。
圆二色谱的应用非常广泛,特别是在药物研发和生物化学领域。
通过圆二色谱分析,可以确定化合物的对手性纯度,从而保证药物
的有效性和安全性。
此外,圆二色谱还可以用于蛋白质的结构分析,对于研究生物大分子的结构和功能具有重要意义。
总之,圆二色谱是一种非常重要的分析技术,它通过测量物质
对圆偏振光的吸收差异来进行对手性分析和结构分析。
在化学、药
物和生物领域都有着广泛的应用前景,对于推动科学研究和技术发
展具有重要意义。
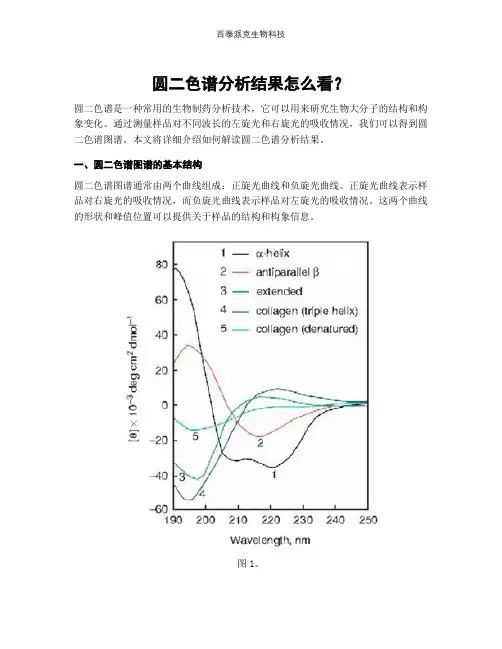
圆二色谱分析结果怎么看?圆二色谱是一种常用的生物制药分析技术,它可以用来研究生物大分子的结构和构象变化。
通过测量样品对不同波长的左旋光和右旋光的吸收情况,我们可以得到圆二色谱图谱。
本文将详细介绍如何解读圆二色谱分析结果。
一、圆二色谱图谱的基本结构圆二色谱图谱通常由两个曲线组成:正旋光曲线和负旋光曲线。
正旋光曲线表示样品对右旋光的吸收情况,而负旋光曲线表示样品对左旋光的吸收情况。
这两个曲线的形状和峰值位置可以提供关于样品的结构和构象信息。
图1。
二、峰值位置的解读圆二色谱图谱中的峰值位置可以告诉我们样品的二级结构信息。
一般来说,α-螺旋结构在190-200 nm处会出现负峰,而β-折叠结构在210-220 nm处会出现正峰。
通过观察峰值位置的变化,我们可以推断样品的二级结构变化。
三、峰值强度的解读除了峰值位置,圆二色谱图谱中的峰值强度也是解读样品结构的重要指标。
峰值强度反映了样品对旋光的吸收程度,强度越高表示吸收越强。
通过比较不同样品的峰值强度,我们可以判断它们的结构差异。
四、色谱图形的解读除了峰值位置和峰值强度,圆二色谱图谱的整体形状也提供了有关样品结构的信息。
例如,如果图谱呈现出对称的双峰形状,那么可能存在一种手性结构。
而如果图谱呈现出单峰形状,那么样品可能是非手性的。
五、结构变化的解读通过比较不同条件下的圆二色谱图谱,我们可以观察到样品结构的变化。
例如,当样品在不同温度下进行测量时,我们可以观察到峰值位置的变化,从而推断样品的热稳定性。
类似地,通过比较不同pH值下的圆二色谱图谱,我们可以了解样品的酸碱稳定性。
圆二色谱分析结果的解读需要考虑峰值位置、峰值强度、峰形、色谱图形和对比分析等因素。
通过综合分析这些指标,我们可以得出关于样品结构特征、纯度和质量变化情况的重要信息。
圆二色谱作为一种重要的分析技术,在生物制药领域具有广泛的应用前景。
百泰派克生物科技——生物制品表征,多组学生物质谱检测优质服务商。

多糖组成多样性:圆二色谱测定方法分析多糖是一类重要的生物大分子,广泛存在于生物体内,如细胞壁、细胞膜、软骨、骨骼、肌肉、皮肤、血管、眼球等组织中。
多糖的结构和组成对其生物学功能具有重要影响。
因此,多糖的分析和表征对于深入了解其生物学功能具有重要意义。
圆二色谱是一种常用的多糖分析方法,可以用于分析多糖的结构和组成。
1.多糖的结构和组成多糖是由单糖分子通过糖苷键连接而成的高分子化合物。
多糖的结构和组成对其生物学功能具有重要影响。
多糖结构包括链式结构和支链结构,链式结构包括直链和分支链。
多糖的组成包括单糖种类、单糖的连接方式和单糖的相对比例等因素。
2.圆二色谱测定方法圆二色谱是一种常用的多糖分析方法,可以用于分析多糖的结构和组成。
圆二色谱是利用多糖分子的手性结构对圆偏振光的旋转方向产生影响,从而分析多糖的结构和组成。
圆二色谱可以分析多糖的二级结构,如α-螺旋、β-折叠和无规卷曲等结构。
圆二色谱还可以分析多糖的单糖组成和连接方式等信息。
3.圆二色谱的应用圆二色谱广泛应用于多糖的分析和表征。
圆二色谱可以用于分析多糖的结构和组成,如多糖的二级结构、单糖组成和连接式等信息。
圆二色谱还可以用于分析多糖的空间结构和分子间相互作用等信息。
圆二色谱在生物医学领域中也有广泛应用,如用于分析多糖药物的结构和组成,以及多糖药物与受体的相互作用等信息。
4.圆二色谱的优势和局限性圆二色谱具有高灵敏度、高分辨率和非破坏性等优点,可以分析多糖的结构和组成等信息。
但是,圆二色谱也存在一些局限性,如需要高纯度的样品、需要专业的仪器和操作技能等。
此外,圆二色谱也不能直接分析多糖的三维结构和分子间相互作用等信息。
图1。
5.结论多糖是一类重要的生物大分子,其结构和组成对其生物学功能具有重要影响。
圆二色谱是一种常用的多糖分析方法,可以用于分析多糖的结构和组成。
圆二色谱具有高灵敏度高分辨率和非破坏性等优点,但也存在一些局限性。
圆二色谱在多糖的分析和表征中具有重要应用价值,可以为深入了解多糖的生物学功能提供重要信息。


许多生物大分子都是手性分子。
所谓手性就是具有不能重叠的三维镜像对应异构体。
一般来说,凡具有手性的分子就具有旋光活性,这一点很早就认为人们所认识并广泛应用于研究分子的非对称性结构。
振动方向在同一平面内的电磁波为平面偏振光。
当一束平面偏光通过介质时,光学活性物质分子对左、右圆偏振光的吸收不同,其差值称为圆二色性。
由于存在圆二色性,平面偏振光通过光学活性物质后,其两圆偏振光分量的强度将不同,它们合成的不再是平面偏振光,而是椭圆偏振光。
吸收随波长的变化构成圆二色谱。
圆二色谱仪利用这一原理,将平面偏振光调制成左圆偏振光和右圆偏振光,并以很高的频率交替通过样品,这两束圆偏振光通过样品产生的吸收差由光电倍增管接收检测。
圆二色谱是快速确定蛋白质和肽二级结构的方法。
在紫外区段主要的生色团是肽链,这一范围的圆二色谱包含着肽主链的构象信息。
在近紫外区占支配地位的生色基团是芳香氨基酸侧链,这一区域的圆二色谱能给出局域侧链间相互作用的信息。
在波长大于300nm 的区域,包括可见光区,对圆二色谱的贡献主要来自含有金属离子的一类生色团,这一波段的圆二色谱对于金属的氧化态、配位体以及链一链相互作用均较敏感。
不含非氨基酸发色团的肽和蛋白质在300nm 以上没有吸收或圆二色谱带。
通常由样品圆二色谱形状、谱峰位置、强度以及它们随时验条件的变化本身就可以得到很重要的结构信息。
最主要的圆二色谱参量是谱峰位置及该处摩尔椭圆率。
酰胺基是用圆二色谱观察肽和蛋白质的最重要的发色团。
已确定它的两种电子迁移方式。
n-π迁移通常很弱,在220nm附近呈一个负带。
它的能量对氢键的形成敏感。
π-π迁移一般较强,在192nm附近出现一个正带,在210nm附近出现一个负带。
а-螺旋、β-折叠构象和不规则构象的比例可用圆二色谱确定。
а-螺旋构象的特征是常在222nm和208nm处出现负带,在192nm 处为一正带。
短肽在溶液中通常不形成稳定的螺旋,但已表明加入2,2,2-三氟乙醇能使大多数肽的螺旋成分增加。
实验四—圆二色光谱实验圆二色光谱实验一、实验目的1、了解圆二色(CD)光谱的原理和使用方法。
2、学会用圆二色光谱检测蛋白质二级构象的基本原理和方法,并学会分析物质的手性。
3、了解圆二色光谱仪的基本构造,并学会使用。
二、实验原理1.CD光谱的基本知识圆二色性是研究分子立体结构和构象的有利手段。
在一些物质的分子中,没有任意次旋转反映轴,不能与镜像相互重叠,具有光学活性。
电矢量相互垂直,振幅相等,位相相差四分之一波长的左和右圆偏振光重叠而成的是平面圆偏振光。
平面圆偏振光通过光学活性分子时,这些物质对左、右圆偏振光的吸收不相同,产生的吸收差值,就是该物质的圆二色性。
圆二色性用摩尔系数系数差ΔεM来度量,且有关系式:ΔεM = εL –εR,其中,εL 和εR分别表示左和右偏振光的摩尔吸收系数。
如果εL –εR >0,则ΔεM为“+”,有正的圆二色性,相应于正Cotton效应;如果εL –εR<0,则ΔεM为“-”,有负的圆二色性,相应于负Cotton效应。
由于这种吸收差的存在,造成了矢量的振幅差,因此从圆偏振光通过介质后变成了椭圆偏振光。
圆二色性也可用椭圆度θ或摩尔椭圆度[θ]度量。
[θ]和ΔεM之间的关系式:[θ]=3300*Δε圆二色光谱表示的[θ]或ΔεM与波长之间的关系,可用圆二色谱仪测定。
一般仪器直接测定的是椭圆度θ,可换算成[θ]和ΔεM:[θ] = 100θ/cl,ΔεM= θ/33cl 其中,c表示物质在溶液中的浓度,单位为mol/L;l为光程长度(液池的长),单位为cm。
输入c和l的值,一般仪器能自动进行换算,给出所需要的关系。
2.定性分析原理圆二色光谱仪需要将平面偏振调制成左、右圆偏振光,并用很高的频率交替通过样品,因而设备复杂,完成这种调制的是电致或压力致晶体双折射的圆偏振光发生器(也称Pocker池或应力调制器)。
圆二色谱仪一般采用氙灯作光源,其辐射通过由两个棱镜组成的双单色器后,就成为两束振动方向相互垂直的偏振光,由单色器的出射狭缝排除一束非寻常光后,寻常光由CD调制器制成交变的左圆偏振光、右圆偏振光,这两束圆偏振光通过样品产生的吸收差由光电倍增管接受检测。
圆二色性主要用于测定蛋白质的立体结构圆二色性(circular dichroism, CD) 对R和L两种圆偏振光吸收程度不同的现象。
这种吸收程度的不同与波长的关系称圆二色谱,是一种测定分子不对称结构的光谱法。
在分子生物学领域中主要用于测定蛋白质的立体结构,也可用来测定核酸和多糖的立体结构。
目录∙•圆二色性∙•波长的L光和R光的光强度相等∙•各种立体结构的含量∙•圆二色谱研究核酸的化学组成词性解释【化】 CD; circular dichroism; circular dichroism (CD)又称 :圆二色性(CD )又称 :圆二色性(CD)光是一种电磁波假如用电矢量来表示,光的前进就是由矢量端点在一特定的平面里沿正弦波运动的轨迹。
对于自然光讲,正弦波振动的平面是随机的。
如有一束光,它所有的电矢量的振动平面都是相互平行的,这种光称为平面偏振光。
有一种特殊的情况,光前进的过程中电矢量绕前进轴转动,若电矢量的绝对值不变,则运动轨迹的投影是一个圆,这时就变成圆偏振。
面对光前进的方向看去,电矢量端点的圆运动可以是顺时针方向的,也可以是逆时针方向的,因此圆偏振有R与L两种。
波长的L光和R光的光强度相等[回目录]L与R两束圆偏振光在一起辐射假如L与R两束圆偏振光在一起辐射,强度、速度、频率和位相都相同,它们就会叠合成一束平面偏振光。
如波长的L光和R光的光强度相等,在光学各向异性物质中传播某一距离后,它们的综合光将变成椭圆偏振光,椭圆的长轴处于两个圆偏振的电矢量相叠合的地方。
假如两个圆偏振的传播速度也不相同,而所经的途径与上述相同,则叠合的椭圆偏振光的长轴与上面所述的椭圆偏振光的长轴相夹θ角(图1[两束圆偏振光,旋转方向相反,电矢量长度不同时,合成光是椭圆偏振光])。
某一波长有吸收由不对称分子组成的物质是光学各向异性的,即L与R两束圆偏振光在这类物质中的传播速度不相等。
假如光学各向异性物质在某一波长有吸收,那将在该时对L光和R光有不同的吸收,如该物质的吸光率是A,而对L光和R光的吸光率是A L和A R,A L和A R的差ΔA=A L-A R,称为圆二色性。
3.3.9圆二色性(Circular dichroic,CD)测定1%(w/w)的蛋清溶液调节到pH 4.0,6.0,10.0,在85oC加热不同时间,离心,取上清液,然后稀释至100~200μg/mL溶液。
对照组为天然蛋清样品。
用Jasco J-715光度计测定样品的CD谱。
测定条件设定:测定波长范围190~250 nm,25oC,比色皿光径1 mm,分辨率0.2 nm,扫描速率100 nm/min,扫描5次。
使用Jasco SSE软件确定样品的二级结构百分含量。
3.4.6蛋白质的二级结构对DH的影响蛋白酶的水解反应还受到蛋白质的结构的影响,一般结构紧密的蛋白质提供的酶切位点少于结构松散的蛋白质。
因此有必要研究蛋白质结构对DH的影响。
蛋白质的热处理可能引起二级、三级和四级结构的变化。
从二级结构看,α-螺旋结构表现蛋白质分子的有序性,而其结构如β-折叠、β-转角、无规卷曲等反映了蛋白质分子的松散性[26]。
蛋白质分子的有序性差,越有利于蛋白酶的水解。
目前,研究蛋白质构象最好的方法是x-射线衍射,但对结构复杂、柔性的生物大分子蛋白质来说,制备蛋白质单晶较为困难。
二维、多维核磁共振技术能测出溶液状态下蛋白质分子的构象,可是对分子量较大的蛋白质的计算处理非常复杂。
相比之下圆二色性是研究稀溶液中蛋白质分子构象的一种快速、简单、较准确的方法。
圆二色性在紫外区段(190~240 nm),主要生色团是肽链,这一波长范围的CD谱包含着生物大分子主链构象的信息。
在一般情况下,实验中得到的CD谱线是α-螺旋、β-折叠和无规卷曲构象的CD 谱的线性迭加[27]。
图3-7显示天然蛋清的CD谱线a在222 nm处和208 nm处呈负峰,在190 nm附近有一正峰,这是存在部分α-螺旋构象的特征。
谱线b、c、d、e在221 nm处的负谱带减弱,意味着α-螺旋的百分比减小。
谱线b、c、d、e向短波长方向移动,即发生蓝移。
由于发色团吸收光谱发生位移主要取决于它的微环境更加亲水或疏水的结果[28],因此谱线b、c、d、e蓝移的发生说明体系的亲水性降低,即疏水性增加。
圆二色光谱假象
圆二色光谱假象是指当人眼同时看到两个彩色光源,且这两个光源光谱上的颜色完全相同,但在视觉上会给人带来不同的颜色感觉。
这种现象是因为人眼对颜色的感知是通过三种锥形细胞分别对红、绿、蓝三种颜色的光敏感来实现的,而这两个看似相同的光源在红绿蓝三个通道的刺激程度不同,导致了视觉上的颜色感知差异。
具体来说,圆二色光谱假象是通过利用两个色彩互补的光源,使得红绿蓝三个通道的刺激程度不同。
例如,一个圆中央发出纯红光,周围发出互补色绿光的光源。
虽然这两个光源在光谱上的颜色是完全相同的,但由于人眼对红、绿两种颜色的敏感程度不同,圆的中央部分会被视为稍微偏红的颜色,而周围则会被视为稍微偏绿的颜色,从而产生了圆二色光谱假象。
圆二色光谱假象的发现揭示了人眼对颜色的感知是非线性的,并受到多种因素的影响。
这种现象在视觉艺术和心理学研究中有一定的应用,也有助于深入理解人眼颜色感知的机制。