cho细胞表达系统及筛选原理
- 格式:docx
- 大小:3.80 KB
- 文档页数:3

单克隆抗体CHO细胞株筛选策略探讨(一)作者 l Frank Tao编辑 l 细胞房间摘要:随着单克隆抗体技术发展,单克隆CHO细胞株筛选技术也日异月新,越来越高效,越来越智能化。
本文主要结合自身CHO细胞株开发和细胞培养经验,将目前国内外单克隆抗体CHO细胞株筛选技术进行总结,供行业内参考,促进行业健康发展;问题:如何4-6个月内,筛选到稳定的单克隆细胞株表达在3-5 g/L或以上?关键词:单克隆抗体;CHO细胞;ClonePix;单克隆影像学拍照;Beacon;1.宿主细胞抗体药物生产的宿主细胞主要NS0、HEK293、Hybridoma、SP2/0、CHO等,但CHO细胞是生产抗体药物应用最广的宿主细胞,CHO细胞类型也比较多,例如:DG44、DXB11、CHO K1、CHO-S 等。
上世纪八九十年代开始,工业上使用较早的是DHFR体系(二氢叶酸还原酶缺陷型)DG44细胞。
当细胞培养基内还有MTX(甲氨蝶呤)时,二氢叶酸还原酶被抑制,通过反馈调节,使得该基因自我扩增,连带齐上下100-1000kb的基因都会扩增,如此目的基因也得到扩增,即可以提高目的蛋白的表达量。
现在很多单抗生产的体系依然是DG44。
GS体系(谷氨酰胺合成酶)CHO-K1是近些年发展的一种基因扩增筛选系统,较DHFR系统有明显的优越性,目前在国际上得到了广泛地认可。
其原理是GS在ATP水解提供能量的同时,利用细胞内的氨和谷氨酸合成谷氨酰胺。
在缺乏外源的谷氨酰胺培养基中加入GS抑制剂甲硫氨酸亚砜亚铵(MSX),可使GS基因及与之相连的目的基因得到有效扩增,从而达到提高目的基因表达水平的目的。
该系统的优点主要在:该系统不需要基因缺陷型的CHO-K1细胞株做为宿主细胞;CHO-K1细胞易于培养,更强壮;在培养基中无需加谷氨酰胺,能够避免谷氨酰胺分解造成培养体系中氨水平高的问题,降低了工艺控制的难度,并且可有效提高细胞发酵密度和延长细胞生存时间。

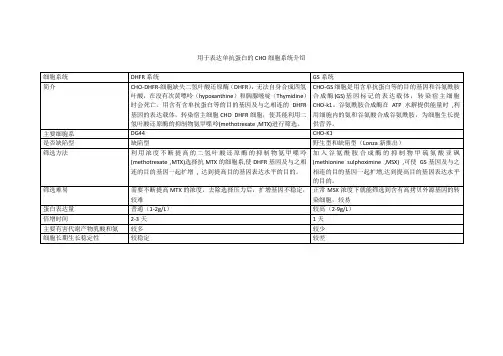

蛋氨酸亚氨基代砜(methionine sulfoximine, MSX)筛选用的是谷氨酰胺合成酶基因(glutaminesynthetase, GS)系统压力;氨甲喋呤(amethopterin, MTX)筛选用的是二氢叶酸还原酶基因(dihydrofolatereductase, dhfr)系统压力。
1. CHO细胞表达体系常用的CHO细胞系有两种:CHO和CHO(dhfr-),CHO(dhfr-)是缺失二氢叶酸还原酶的细胞株。
CHO表达系统是目前应用最广泛的真核表达系统之一,与其它表达系统相比,它具有许多优点:准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面最接近天然蛋白分子;表达产物胞外分泌,便于分离纯化;具有重组基因的高效扩增和表达能力;贴壁生长,有较高的耐受剪切力和渗透压能力,可进行悬浮培养或在无血清培养基中达到高密度,培养体积能达到1000L以上;CHO细胞属于成纤维细胞,很少分泌内源蛋白,利于外源蛋白的分离纯化。
改造CHO细胞,可更好地表达外源蛋白。
为减少大规模细胞培养过程中凋亡的发生,将bcl-2基因(细胞凋亡抑制基因)导入细胞,bcl-2基因的过量表达能抑制Gln或氧缺乏引起的细胞凋亡,减少细胞特定营养成分的消耗,提高细胞密度和目的蛋白产量。
向CHO细胞中导入p21、p27基因,可使细胞G1期延长(细胞静止),改造后细胞活力正常,营养成分消耗和代谢毒物含量有效降低,从而减少细胞凋亡、死亡,外源蛋白表达量提高,产品成本降低。
2. 载体系统借助真核基因表达调控的理论,可将较强的顺式作用元件集中到一个载体中,使其方便高效地表达外源基因。
目前,已经构建了许多真核表达载体,它们包含适当的顺式作用元件和选择标记。
顺式作用元件主要有启动子—增强子元件、转录剪切和Poly A信号等;CHO 细胞表达载体中主要有两类选择标记:非扩增基因和共扩增基因。
2.1启动子和增强子启动子是影响外源基因表达效率的关键因素。

CHO细胞无血清培养基的筛选与优化在生物制药领域,CHO 细胞(Chinese Hamster Ovary Cell,中国仓鼠卵巢细胞)因其能够高效表达重组蛋白而被广泛应用。
然而,传统的含血清培养基存在诸多问题,如血清成分复杂且批次间差异大,易引入外源病毒和支原体污染等。
因此,开发和优化 CHO 细胞无血清培养基成为了提高生物制品质量和安全性的关键环节。
一、CHO 细胞无血清培养基的重要性血清在细胞培养中曾被广泛使用,但其存在的问题不容忽视。
血清中的成分复杂且不稳定,这使得细胞培养过程难以控制和标准化。
不同批次的血清质量差异较大,可能影响细胞的生长、代谢和产物表达。
此外,血清中可能携带的病毒、支原体等污染物会给生物制品带来潜在的安全风险。
相比之下,无血清培养基具有明显的优势。
它的成分明确且稳定,便于质量控制和优化。
无血清培养基可以减少外源污染物的引入,提高生物制品的安全性。
同时,它能够为细胞提供更适宜的生长环境,促进细胞的生长和产物表达,从而提高生产效率和产品质量。
二、筛选 CHO 细胞无血清培养基的方法1、基础培养基的选择首先需要选择合适的基础培养基作为起点。
常见的基础培养基如DMEM(Dulbecco's Modified Eagle Medium,杜氏改良伊格尔培养基)、RPMI 1640 等,它们在营养成分和离子浓度等方面有所不同。
需要根据 CHO 细胞的特性和培养需求,初步筛选出几种可能适用的基础培养基。
2、添加剂的筛选在基础培养基的基础上,需要添加各种营养成分、生长因子、激素等添加剂来满足 CHO 细胞的生长和代谢需求。
例如,胰岛素、转铁蛋白、乙醇胺等对于细胞的生长和存活至关重要。
通过单独或组合添加这些添加剂,并检测细胞的生长情况、代谢指标和产物表达水平,来筛选出最优的添加剂组合。
3、化学成分的优化除了添加剂,培养基中的化学成分如氨基酸、维生素、无机盐等的浓度和比例也需要进行优化。

CHO细胞表达体系特点及CHO细胞表达疫苗来源:易生物实验浏览次数:533 网友评论0 条CHO细胞表达体系特点及CHO细胞表达疫苗关键词:细胞疫苗CHO细胞表达体系CHO细胞表达分子生物学、分子免疫学等学科的发展使基因工程疫苗具有越来越重要的地位。
在基因工程疫苗研究的动物细胞表达系统中,最具代表性的就是中国仓鼠卵巢细胞(Chinese Hamster Ovary,CHO)。
它是用来表达外源蛋白最多也最成功的一类细胞。
本文就CHO细胞表达系统在疫苗研制中的应用做一综述。
1、CHO细胞表达体系及其特点CHO细胞属于成纤维细胞,既可以贴壁生长。
也可以悬浮生长。
目前常用的CHO细胞包括原始CHO和二氢叶酸还原酶双倍体基因缺失型(DHFR-) 突变株CHO。
近年来,为降低生产成本和减少血制品带来的潜在危害性,动物细胞生产开始使用无血清培养基(SFM),但SFM往往导致细胞活力差,贴壁性差,分泌外源蛋白的能力差等缺点。
另有研究者尝试将类胰岛素生长因子IGF基因和转铁蛋白基因转入CHO细胞获得能自身分泌必需蛋白的“超级CHO”,无需在培养基中转铁蛋白和胰岛素,细胞可在sFM 中生长良好。
与其他表达系统相比,CHO表达系统具有以下的优点:(1)具有准确的转录后修饰功能,表达的蛋白在分子结构、理化特性和生物学功能方面最接近于天然蛋白分子;(2)既可贴壁生长,又可以悬浮培养,且有较高的耐受剪切力和渗透压能力;(3)具有重组基因的高效扩增和表达能力,外源蛋白的整合稳定;(4)具有产物胞外分泌功能,并且很少分泌自身的内源蛋白,便于下游产物分离纯化;(5)能以悬浮培养方式或在无血清培养基中达到高密度培养。
且培养体积能达到1000L以上,可以大规模生产。
2、CHO细胞表达疫苗(1)乙肝疫苗CHO细胞表达疫苗的种类不多,多数处于研究阶段。
目前只有CHO表达乙肝疫苗已投入生产,这是除酵母表达乙肝疫苗以外,唯一已用于人类使用的基因工程亚单位疫苗。

cho高效瞬时表达方法
CHO细胞高效瞬时表达方法是一种用于瞬时转染真核细胞的方法,该方法使用一种重组的腺病毒或质粒载体将外源基因瞬时转染入CHO细胞。
这种方法的优点是转染效率高,能够实现大规模的基因表达和生产,并且可以在短时间内完成实验。
CHO细胞高效瞬时表达方法的具体步骤包括:
1.准备重组质粒或腺病毒载体:将目的基因克隆到质粒或腺病毒载体中,并进行测序验证。
2.转染CHO细胞:将重组质粒或腺病毒载体与CHO细胞混合,通过特定的转染试剂将其导入细胞中。
3.筛选阳性克隆:在转染后的一段时间内,通过特定的筛选方法,如抗生素筛选或荧光激活细胞分选(FACS),从众多的细胞中筛选出阳性克隆。
4.扩大培养:将筛选出的阳性克隆进行扩大培养,以获得更多的目的基因产物。
5.收集产物:在目的基因产物积累到一定量后,收集产物并进行纯化和质量检测。
CHO细胞高效瞬时表达方法的应用范围广泛,可以用于抗体、重组蛋白、siRNA等生物制品的生产和研究。

C H O细胞表达系统常见问题及解析标准化管理处编码[BBX968T-XBB8968-NNJ668-MM9N]1、问:请问有人养过CHO细胞吗文献报道说用DMEM培养基来养,但我不太清楚具体是高糖还是低糖参考见解:CHO细胞用高糖DMEM养就可以了,比较好养,10%血清,小牛和胎牛都可以,长得比较慢,跟你所用的血清有一定的关系,大概需要两天传一次代。
在塑料板上比玻璃板上好养,感觉如果在玻璃板上养而且不包被的话,好像细胞不易伸展开来。
2、问:要转染钾通道入细胞,是选cho细胞呢还是hek293细胞cho细胞转染效率高吗参考见解:表达一个蛋白的时候,首先要确认你的蛋白确实表达了,因为有很多原因可以导致蛋白表达出问题(质粒序列有错误,质粒纯度低,表达的蛋白不稳定,转染效率太低等)。
所以在做任何功能性实验之前,必须要先确认蛋白的表达,通常的实验有:(1)采用免疫荧光法。
由于需要荧光二抗,比较贵。
但直观,可以确定转染效率,采用好的显微镜时,可以大致知道表达蛋白在细胞中的位置。
(2)WESTERN-BLOT。
可以确认表达的蛋白分子量,以及表达的量。
但不直观。
(3)构建一个N或C端带荧光蛋白的质粒。
这样比较费时间,同时携带的荧光蛋(通常使用GFP)有可能干扰蛋白的正常功能。
但好处是转染后可以很方便的观察转染效率,蛋白在细胞中的位置等。
当然以上方法都无法知道质粒有无发生突变,所以如果你的蛋白有表达但没有功能,首先要做一个DNA测序确认你的序列没有问题。
事实上质粒发生突变的机会比大多数人想象的要多得多!3、问:由于我要用CHO细胞生产基因工程抗体,用什么培养基能够很好的使之良好的生长参考见解:培养CHO细胞最好用F12,并且由于F12中加入了一些微量元素与无机离子,因此可以在血清很少的情况下应用,是无血清培养中常用的基础培养基,特别适合进行单细胞培养和克隆化培养。
我们的前辈曾用F12在无血清的条件下成功的克隆出CHO细胞。


CHO稳定细胞株开发步骤有哪些?稳定细胞株筛选原理详解CHO(中国仓鼠卵巢)细胞株是目前最常用的哺乳动物细胞株之一,被广泛应用于生物制药、生物技术、疫苗制备等领域。
稳定细胞株是指在细胞培养中,将外源基因集成到细胞染色体中并稳定表达的细胞群体。
稳定细胞株具有表达稳定、重现性好等优点,可用于大规模蛋白质生产。
CHO稳定细胞株开发的主要步骤如下:克隆:选择具有高表达能力的基因,将其克隆到合适的表达载体中,如pcDNA3.1、pCDM8等。
转染:将表达载体导入CHO细胞中,使其表达外源基因。
转染方式有多种,如电穿孔、钙磷共沉淀、透析等。
筛选:利用筛选标记(如耐药基因或荧光标记)对转染细胞进行筛选,筛选出高表达的克隆细胞。
扩增:将选出的细胞进行扩增,直至获得足够量的细胞。
稳定化:将稳定的克隆细胞继续培养,保持其稳定表达目标基因。
鉴定:通过Western blot、ELISA等方法对细胞株进行鉴定,验证其表达目标基因的能力和稳定性。
在CHO稳定细胞株开发过程中,还需要注意培养条件的优化,包括培养基配方、温度、CO2浓度、氧气含量等。
此外,对于不同的目标蛋白,还需要针对性地优化表达条件和纯化方法。
稳定细胞株筛选原理及方法:稳定细胞株筛选是指通过对转染后的细胞群体进行筛选,筛选出稳定集成了外源基因并稳定表达的细胞株。
其基本原理是依赖于转染细胞后外源基因的选择性筛选和纯化。
常用的稳定细胞株筛选方法有两种:抗生素筛选法:将外源基因构建在带有特定抗生素耐受基因的质粒上,转染细胞后在培养基中加入相应抗生素,使只有带有外源基因的细胞能够在抗生素的选择压下存活,其他未集成外源基因的细胞则被杀死。
选择性标记物筛选法:外源基因构建在带有选择性标记物(如荧光蛋白、酶标记等)的质粒上,转染细胞后通过标记物筛选,筛选出带有外源基因的细胞群体。
选择性标记物可以使用光学显微镜、流式细胞仪等设备进行检测和纯化。
两种筛选方法各有优缺点,抗生素筛选法虽然常用但存在一些问题,如转染细胞的抗生素耐受性存在差异,有可能导致筛选结果的不确定性;而选择性标记物筛选法可以减少抗生素对细胞的影响,但其纯化效率较低,需要更复杂的实验设备和技术。

cho细胞表达Cho细胞表达是指在生物学中,利用Cho细胞(Chinese Hamster Ovary cells)作为表达系统来表达外源蛋白质的过程。
Cho细胞是一种常用的哺乳动物细胞系,具有较高的蛋白质表达能力和稳定的遗传特性,因此被广泛应用于生物医学研究和制药工业中。
Cho细胞表达系统的优势在于其能够高效地表达外源蛋白质,并能够正确地折叠和修饰蛋白质。
Cho细胞具有相对简单的遗传背景和较低的背景蛋白质表达,可以避免其他细胞系统中常见的问题,如蛋白质聚集、不稳定、部分折叠等。
此外,Cho细胞的培养和维持相对容易,生长速度快,适应不同的培养条件,对不同的基因表达系统都具有较高的兼容性。
Cho细胞表达系统的应用范围广泛,包括生物医学研究、药物发现与研发、生物制药等领域。
在生物医学研究中,Cho细胞表达系统常被用于产生重组蛋白,如抗体、细胞因子、酶等,用于研究蛋白质功能、结构与机制。
在药物发现与研发中,Cho细胞表达系统被用于产生药物靶标蛋白、药物载体、药物代谢酶等,用于筛选和评价药物候选化合物。
在生物制药中,Cho细胞表达系统常被用于大规模生产重组蛋白药物,如单克隆抗体、重组蛋白等。
Cho细胞表达系统的建立和优化需要考虑多个因素。
首先,选择合适的载体和表达系统是关键。
常用的载体包括质粒、病毒载体等,表达系统可以是稳定转染系统或转染后选择稳定表达细胞的系统。
其次,选择合适的表达宿主细胞株和培养条件也十分重要。
Cho细胞的培养基和培养条件需要根据表达蛋白的特性和需求进行优化,包括培养基成分、温度、pH值、培养密度等。
此外,还需考虑到蛋白质折叠、修饰和纯化等后续步骤。
Cho细胞表达系统的优势也存在一些限制和挑战。
首先,Cho细胞是一种非人类细胞,因此相较于人类细胞,其表达的蛋白质可能存在差异。
其次,Cho细胞在遗传稳定性和蛋白质表达水平上存在一定的变异性,需要进行筛选和优化。
此外,Cho细胞的培养和维持相对费时费力,对于大规模的生产需求可能不太适用。
MSX加压筛选与MTX加压筛选分子生物与细胞培养蛋氨酸亚氨基代砜(methionine sulfoximine, MSX)筛选用的是谷氨酰胺合成酶基因(glutaminesynthetase, GS)系统压力;氨甲喋呤(amethopterin, MTX)筛选用的是二氢叶酸还原酶基因(dihydrofolatereductase, dhfr)系统压力。
1. CHO细胞表达体系常用的CHO细胞系有两种:CHO和CHO(dhfr-),CHO(dhfr-)是缺失二氢叶酸还原酶的细胞株。
CHO表达系统是目前应用最广泛的真核表达系统之一,与其它表达系统相比,它具有许多优点:准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面最接近天然蛋白分子;表达产物胞外分泌,便于分离纯化;具有重组基因的高效扩增和表达能力;贴壁生长,有较高的耐受剪切力和渗透压能力,可进行悬浮培养或在无血清培养基中达到高密度,培养体积能达到1000L以上;CHO细胞属于成纤维细胞,很少分泌内源蛋白,利于外源蛋白的分离纯化。
改造CHO细胞,可更好地表达外源蛋白。
为减少大规模细胞培养过程中凋亡的发生,将bcl-2基因(细胞凋亡抑制基因)导入细胞,bcl-2基因的过量表达能抑制Gln或氧缺乏引起的细胞凋亡,减少细胞特定营养成分的消耗,提高细胞密度和目的蛋白产量。
向CHO细胞中导入p21、p27基因,可使细胞G1期延长(细胞静止),改造后细胞活力正常,营养成分消耗和代谢毒物含量有效降低,从而减少细胞凋亡、死亡,外源蛋白表达量提高,产品成本降低。
2. 载体系统借助真核基因表达调控的理论,可将较强的顺式作用元件集中到一个载体中,使其方便高效地表达外源基因。
目前,已经构建了许多真核表达载体,它们包含适当的顺式作用元件和选择标记。
顺式作用元件主要有启动子—增强子元件、转录剪切和Poly A信号等;CHO细胞表达载体中主要有两类选择标记:非扩增基因和共扩增基因。
蛋氨酸亚氨基代砜(methionine sulfoximine, MSX)筛选用的是谷氨酰胺合成酶基因(glutaminesynthetase, GS)系统压力;氨甲喋呤(amethopterin, MTX)筛选用的是二氢叶酸还原酶基因(dihydrofolatereductase, dhfr)系统压力。
1. CHO细胞表达体系常用的CHO细胞系有两种:CHO和CHO(dhfr-),CHO(dhfr-)是缺失二氢叶酸还原酶的细胞株。
CHO表达系统是目前应用最广泛的真核表达系统之一,与其它表达系统相比,它具有许多优点:准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面最接近天然蛋白分子;表达产物胞外分泌,便于分离纯化;具有重组基因的高效扩增和表达能力;贴壁生长,有较高的耐受剪切力和渗透压能力,可进行悬浮培养或在无血清培养基中达到高密度,培养体积能达到1000L以上;CHO细胞属于成纤维细胞,很少分泌内源蛋白,利于外源蛋白的分离纯化。
改造CHO 细胞,可更好地表达外源蛋白。
为减少大规模细胞培养过程中凋亡的发生,将bcl-2基因(细胞凋亡抑制基因)导入细胞,bcl-2基因的过量表达能抑制Gln或氧缺乏引起的细胞凋亡,减少细胞特定营养成分的消耗,提高细胞密度和目的蛋白产量。
向CHO细胞中导入p21、p27基因,可使细胞G1期延长(细胞静止),改造后细胞活力正常,营养成分消耗和代谢毒物含量有效降低,从而减少细胞凋亡、死亡,外源蛋白表达量提高,产品成本降低。
2. 载体系统借助真核基因表达调控的理论,可将较强的顺式作用元件集中到一个载体中,使其方便高效地表达外源基因。
目前,已经构建了许多真核表达载体,它们包含适当的顺式作用元件和选择标记。
顺式作用元件主要有启动子—增强子元件、转录剪切和Poly A信号等;CHO细胞表达载体中主要有两类选择标记:非扩增基因和共扩增基因。
2.1启动子和增强子启动子是影响外源基因表达效率的关键因素。
CHO细胞(中国仓鼠卵巢细胞)表达系统CHO细胞表达系统原理分子生物学、分子免疫学等学科的发展使基因工程疫苗具有越来越重要的地位。
在基因工程疫苗研究的动物细胞表达系统中,最具代表性的就是中国仓鼠卵巢细胞(Chinese Hamster Ovary,CHO)。
它是用来表达外源蛋白最多也最成功的一类细胞。
本文就CHO细胞表达系统在疫苗研制中的应用做一综述。
CHO细胞表达体系及其特点诞生于70年代末的基因工程药物因其具有其他药物无法比拟的优点,已迅速成为制药工业中一个引人瞩目的领域。
1995年美国基因工程药物销售额约为48亿美元,1997年超过60亿美元,年增长率达20%以上。
各国政府将其视为新的经济增长热点而给予了大力支持。
基因工程药物研究与开发的主要环节包括:①基因的克隆和基因工程菌的构造;②重组细胞的培养;③目的产物的分离纯化等。
针对这些主要环节,研究人员正致力于高效表达、培养工艺及下游分离纯化等方面的研究。
随着基因工程技术的不断发展,目前已有多种表达系统可用于生产具有医疗价值的人或动物来源的蛋白质(表1)。
大肠杆菌(E.coli)是使用最早的表达系统,其显著优点是易于操作,产量高,成本低,但由于用E.coli生产的蛋白质药物因缺乏糖基化而在人体内易被降解,因此它的药放大大降低。
此外,它还存在易产生内毒素和包涵体的问题。
真核细胞中CHO细胞是目前重组糖基蛋白生产的首选体系;因为与其他表达系统相比,它具有许多优点:①具有准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面最接近于天然蛋白分子;②具有产物胞外分越功能,便于下游产物分离纯化;③具有重组基因的高效扩增和表达能力;④具有贴壁生长特性,且有较高的耐受剪切力和渗透压能力,可以进行悬浮培养,表达水平较高;⑤CHO细胞属于成纤维细胞(fibroblast),很少分泌自身的内源蛋白,利于外源蛋白的启分离。
但CHO细胞培养成本高,条件难掌握,易污染,在一定程度上影响了它的广泛应用。
CHO细胞(中国仓鼠卵巢细胞)表达系统CHO细胞表达系统原理分子生物学、分子免疫学等学科的发展使基因工程疫苗具有越来越重要的地位。
在基因工程疫苗研究的动物细胞表达系统中,最具代表性的就是中国仓鼠卵巢细胞(Chinese Hamster Ovary,CHO)。
它是用来表达外源蛋白最多也最成功的一类细胞。
本文就CHO细胞表达系统在疫苗研制中的应用做一综述。
CHO细胞表达体系及其特点诞生于70年代末的基因工程药物因其具有其他药物无法比拟的优点,已迅速成为制药工业中一个引人瞩目的领域。
1995年美国基因工程药物销售额约为48亿美元,1997年超过60亿美元,年增长率达20%以上。
各国政府将其视为新的经济增长热点而给予了大力支持。
基因工程药物研究与开发的主要环节包括:①基因的克隆和基因工程菌的构造;②重组细胞的培养;③目的产物的分离纯化等。
针对这些主要环节,研究人员正致力于高效表达、培养工艺及下游分离纯化等方面的研究。
随着基因工程技术的不断发展,目前已有多种表达系统可用于生产具有医疗价值的人或动物来源的蛋白质(表1)。
大肠杆菌(E.coli)是使用最早的表达系统,其显著优点是易于操作,产量高,成本低,但由于用E.coli生产的蛋白质药物因缺乏糖基化而在人体内易被降解,因此它的药放大大降低。
此外,它还存在易产生内毒素和包涵体的问题。
真核细胞中CHO细胞是目前重组糖基蛋白生产的首选体系;因为与其他表达系统相比,它具有许多优点:①具有准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面最接近于天然蛋白分子;②具有产物胞外分越功能,便于下游产物分离纯化;③具有重组基因的高效扩增和表达能力;④具有贴壁生长特性,且有较高的耐受剪切力和渗透压能力,可以进行悬浮培养,表达水平较高;⑤CHO细胞属于成纤维细胞(fibroblast),很少分泌自身的内源蛋白,利于外源蛋白的启分离。
但CHO细胞培养成本高,条件难掌握,易污染,在一定程度上影响了它的广泛应用。
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 201611209263.9(22)申请日 2016.12.23(71)申请人 浙江海隆生物科技有限公司地址 312000 浙江省绍兴市滨海新城马欢路398号科创中心2号楼5楼(72)发明人 钱泓 吴有强 卞广林 张强 徐玉兰 车影 吴素芳 查银河 (74)专利代理机构 北京乾诚五洲知识产权代理有限责任公司 11042代理人 付晓青 李广文(51)Int.Cl.C12N 5/10(2006.01)C12N 15/85(2006.01)C12N 15/65(2006.01)(54)发明名称一种CHO单克隆细胞株的筛选方法和应用(57)摘要本发明公开了一种CHO单克隆细胞株的筛选方法和应用,该方法包括以下步骤:1)在pEE12.4载体上面插入一种抗生素筛选标记基因;2)将目的基因插入1)中改造的pEE12.4的多克隆位点中;3)将2)中构建的重组质粒转染CHO细胞;4)加压筛选得到阳性CHO细胞;5)从阳性细胞中筛选得到高表达目的蛋白的CHO单克隆细胞株。
使用本发明的方法在CHO单克隆细胞株筛选时能够显著提高筛选效率,节约筛选时间;且在批量构建真核表达载体时能够显著提高工作效率和降低成本。
权利要求书1页 说明书8页 附图2页CN 107964535 A 2018.04.27C N 107964535A1.一种CHO单克隆细胞株的筛选方法,其特征在于,所述方法包括以下步骤:1)在pEE12.4载体上面插入一种抗生素筛选标记基因,以得到改造的pEE12.4的多克隆位点;2)将目的基因插入步骤1)中改造的pEE12.4的多克隆位点中,以获得构建的重组质粒;3)将步骤2)中构建的重组质粒通过转染试剂转染CHO细胞;4)加压筛选得到阳性CHO细胞;5)从阳性CHO细胞中筛选得到高表达目的蛋白的CHO单克隆细胞株。
cho细胞表达系统及筛选原理
Cho细胞表达系统及筛选原理
一、引言
Cho细胞表达系统是一种常用的哺乳动物细胞表达系统,被广泛应用于重组蛋白的生产。
本文将介绍Cho细胞表达系统的原理以及其在蛋白质筛选中的应用。
二、Cho细胞表达系统的原理
Cho细胞是一种中国仓鼠卵巢细胞系,具有较高的生长速度和蛋白质表达能力。
Cho细胞表达系统主要包括以下几个关键步骤。
1. 转染
将目标基因导入Cho细胞中,通常使用质粒转染法或病毒载体转染法。
质粒转染法通过将目标基因插入质粒DNA中,然后利用转染试剂将质粒DNA导入细胞内。
病毒载体转染法则通过构建携带目标基因的病毒载体,将其感染到Cho细胞中。
2. 选择性筛选
为了确保只有转染成功的细胞能够表达目标蛋白,通常在培养基中添加适当的选择性抗生素,如G418或葡萄糖酸钾。
只有转染成功的细胞才能抵抗抗生素的作用,存活下来。
3. 扩增和表达
经过筛选的细胞将被扩增培养,以获得足够数量的细胞进行大规模
蛋白质表达。
通常选择合适的培养基和培养条件,以提高细胞的生长速度和蛋白质表达水平。
4. 蛋白质纯化
经过表达的目标蛋白质需要进行纯化,以去除其他杂质。
常用的纯化方法包括亲和层析、离子交换层析、凝胶过滤层析等。
通过这些方法,可以获得高纯度的目标蛋白质。
三、Cho细胞表达系统在蛋白质筛选中的应用
Cho细胞表达系统在蛋白质筛选中具有以下优势。
1. 高表达水平
Cho细胞具有较高的蛋白质表达能力,能够快速产生大量目标蛋白。
这对于需要大量蛋白质的研究和工业应用非常有利。
2. 真核细胞表达
与原核细胞表达系统相比,Cho细胞表达系统能够实现真核细胞蛋白质表达。
这使得Cho细胞表达系统适用于需要进行正确的蛋白质翻译修饰、蛋白质折叠和组装的蛋白质研究。
3. 可选择性筛选
通过添加适当的选择性抗生素,可以筛选出成功表达目标蛋白的细胞。
这样可以确保筛选后的细胞具有较高的表达水平和纯度。
4. 灵活性
Cho细胞表达系统可以应用于多种类型的蛋白质,包括单链抗体、重组蛋白、酶等。
它还可以适应多种表达策略,如稳定细胞线和临时表达。
5. 成本效益
相对于其他哺乳动物细胞表达系统,Cho细胞表达系统具有较低的成本。
这使得它成为许多研究实验室和生物制药公司的首选。
四、结论
Cho细胞表达系统是一种常用的哺乳动物细胞表达系统,具有高表达水平、真核细胞表达、选择性筛选、灵活性和成本效益等优势。
在蛋白质筛选中,Cho细胞表达系统可以快速高效地产生目标蛋白,为研究和应用提供了重要工具。
未来,随着技术的不断发展,Cho 细胞表达系统将在蛋白质研究和生物制药领域发挥更大的作用。