对氨基苯磺酰胺
- 格式:pdf
- 大小:101.32 KB
- 文档页数:2

广州大学化学化工学院本科学生综合性、设计性实验报告实验课程有机化学基础实验实验项目磺胺的合成-多步骤合成对氨基苯磺酰胺专业班级学号姓名指导教师开课学期至学年学期时间年月日磺胺的合成—多步骤合成对氨基苯磺酰胺姓名:摘要:对氨基苯磺酰胺作为一种简单的磺胺药,投入大量生产。
能抑制多种细菌和少数病毒的生长和繁殖,用于防治多种病菌感染。
本实验以苯为原料经过硝化、还原、酰胺化、氯磺化、氨置换、水解及中和等一系列反应,得到磺胺。
最后通过测定熔点和红外光谱图鉴定磺胺的结构。
关键词:对氨基苯磺酰胺、磺胺药物,红外光谱Abstract:As a simple sulfa drugs, Sulfanilamide put into mass production. Sulfa drugs can inhibit the growth and multiplication of certain kinds of bacteria and a few virus for the preventing bacteria infections. In this experiment, benzene was treated by nitration, reduction, acylation, chlorine, ammonia substitution, hydrolysis and a series of reactions to get sulfanilamide. The structure of sulfanilamide was characterized by melt point and IR spectra analysis.Key words: Ammonium p-aminobenzene sulfonic acid, sulfa drugs, IR前言:磺胺药物是含磺胺基团合成抗菌药的总称,能抑制多种细菌和少数病毒的生长和繁殖,用于防治多种病菌感染。

制药工艺学开题报告题目:磺胺的制备及工艺条件考察学生:学号: 25院(系):生命科学与工程学院专业:制药工程指导教师:2011年 3月 12日制药工艺学实验开题报告一·实验题目:磺胺的制备及工艺条件的考察1.1磺胺及磺胺类药物简介1.1.1发展历程:磺胺类药物的发现,开创了化学治疗的新纪元,使死亡率很高的细菌性传染疾病得到了控制。
同时它的作用机制的阐明为药物研究提供了新的思路——代谢拮抗。
早在1908年,磺胺就被合成,但当时仅作为合成偶氮染料的中间体,无人注意到它的医疗价值。
直到1932年Domagk发现了百浪多息,可以使鼠、兔免受链球菌和葡萄球菌的感染,次年报告了用百浪多息治疗由葡萄球菌引起败血症的第一病例,引起了世界范围的极大兴趣。
令人奇怪的是“百浪多息”只有在体内才能杀死链球菌,而在试管内则不能。
而由于乙酰化是体内代谢的常见反应,因此推断百浪多息在体内代谢成磺胺,而产生抗菌作用。
然后证明磺胺在体内外均有抑菌作用。
从此之后,磺胺名字很快在医疗界广泛传播开来;磺胺类药物的研究工作发展极为迅速。
1937年制出“磺胺吡啶”,1939年制出“磺胺噻唑”,1941年制出了“磺胺嘧啶”……至1946年共合成了5500余种磺胺类化合物,并有20余种作为合成抗菌药在临床上使用。
磺胺类药物在细菌性传染的化学治疗上,有卓越的功效。
它的发现以及随之而来的一系列新的磺胺药物合成上的研究成果,是医疗事业上一件有极重要意义的事。
人类依靠了磺胺类药物,在与病菌作战中,取得过空前的胜利。
许多严重的危机人们生命安全的疾病,诸如产褥热、丹毒、猩红热、败血症以及肺炎、骨髓炎、流行性脑膜炎、细菌性痢疾和各种创伤传染及眼耳鼻喉等的化脓性传染等,都纷纷低头;它的治疗功效,在化学治疗学上,写下了光辉的一页。
1.1.2磺胺(对氨基苯磺酰胺)【结构式】:【化学名】对氨基苯磺酰胺【中文通用名称】磺胺【英文通用名称】Sulfanilamide【其他名称】磺酰胺、对苯胺磺酰胺、对磺酰胺苯胺。

对氨基苯磺酰胺氨基苯磺酰胺是一种化学物质,常用作抗菌剂及催化剂。
它是由苯磺酰氯与氨基苯酚反应得到的产物。
氨基苯磺酰胺具有一定的化学活性和广泛的应用领域,在医药、化工等领域发挥着重要作用。
首先,氨基苯磺酰胺在医药领域被广泛用作抗菌剂。
它具有良好的抑菌特性,对多种病原菌有较强的抑制作用。
通过抑制菌体内的蛋白质合成,氨基苯磺酰胺能够有效地抑制细菌的生长和繁殖。
同时,它对多种革兰氏阳性菌和革兰氏阴性菌都具有较好的抗菌活性,对耐药菌种类也有一定的杀菌作用。
因此,氨基苯磺酰胺被广泛应用于医药领域的抗生素研发和制备中,对于治疗感染疾病有着重要的意义。
此外,氨基苯磺酰胺还可以作为催化剂用于有机合成反应中。
由于其分子结构中含有活泼的氨基与磺酰基团,使得它具有一定的亲核性和电子云密度,可以作为亲核试剂与其他化合物发生加成反应。
氨基苯磺酰胺作为催化剂的应用领域广泛,可用于合成有机分子、药物合成、染料合成等多个领域。
通过调整反应条件和催化剂的用量,可实现不同类型反应的高效催化合成。
此外,氨基苯磺酰胺还具有一定的化学稳定性和热稳定性,使得它在高温、酸碱等恶劣条件下仍能保持较好的活性。
这使得氨基苯磺酰胺在工业生产过程中得到了广泛应用。
比如,在染料工业中,氨基苯磺酰胺可以作为催化剂参与染料分子的合成反应,提高染料的生产效率和质量。
然而,氨基苯磺酰胺的应用也存在一些问题。
首先,酮类化合物对氨基苯磺酰胺具有一定的抑制作用。
在某些特定的反应条件下,氨基苯磺酰胺可能会与酮类化合物发生副反应,降低反应的效率和选择性。
因此,在设计催化反应时需要注意这一问题,选择合适的反应条件和催化剂。
总结来说,氨基苯磺酰胺是一种重要的化学物质,具有广泛的应用领域。
它在医药、化工等领域发挥着重要的作用,具有抗菌和催化反应等多重功能。
然而,对于其应用还需要进一步的研究和优化,以提高其效率和选择性。
希望未来能有更多的科学家关注氨基苯磺酰胺的研究,推动其在不同领域的应用发展。

药物设计之磺胺类药物的改造磺胺类药物的发现,开创了化学治疗的新纪元,使死亡率很高的细菌性传染疾病得到了控制。
磺胺类药物的母体对氨基苯磺酰胺(sulfanilamide)又称为磺胺,早在1980年就被合成,但当时仅作为合成偶氮染料的中间体,无人注意到它的医疗价值。
直到1932年磺胺类化合物改造生成的百浪多息(prontosil)治疗了有葡萄球菌引起的败血症的第一病例,才引起了世界范围的极大兴趣。
磺胺类的药物的作用机制有许多学说,最为广泛被认可的胃Wood-Fields学说。
该学说认为磺胺类药物能与细菌生长所必须的对氨基苯甲酸(PABA)产生竞争性拮抗,干扰了细菌的酶系统对PABA的利用,PABA是叶酸的组成部分,叶酸为微生物生长中的必要物质,也是构成体内叶酸辅酶的基本原料。
PABA在二氢叶酸合成酶的催化下,与二氢蝶啶焦磷酸酯及谷氨酸或二氢蝶啶焦磷酸酯对氨基苯甲酰谷氨酸(PABG)合成二氢叶酸。
再在二氢叶酸还原酶作用下还原成四氢叶酸,为细菌合成核酸提供叶酸辅酶。
Bell-Roblin指出,磺胺类药物之所以能和PABA竞争性拮抗,是由于分子大小与电荷分布极为相似的缘故。
由于磺胺类药物和PABA的这种类似性,使得在PABG的生物合成中,磺胺类药物可以取代PABA的位置,生成无功能的化合物,妨碍了PABG的生物合成。
PABG 经二氢叶酸还原酶作用还原为四氢叶酸,后进一步合成辅酶F。
辅酶F为DNA合成中所必须的嘌呤、嘧啶碱基的合成提供一碳单位。
人体作为微生物的宿主,可以从食物中摄取PABG,因此,磺胺类药物不影响正常叶酸代谢,而微生物靠自身合成PABG,一旦叶酸代谢受阻,生命就不能继续,因此微生物对磺胺类药物都敏感。
通过查阅相关资料,得出磺胺类药物的构效关系如下:(1)对氨基苯磺酰胺结构是必要的结构。
即苯环上的氨基与磺酰胺基必须在对位,在邻位或间位无抑菌作用。
(2)芳氨基的氮原子上一般没有取代基,若有取代基则必须在体内易被酶分解或还原为游离的氨基才有效,否则无效。

![磺胺类药物[常识]](https://uimg.taocdn.com/085e4cd09fc3d5bbfd0a79563c1ec5da50e2d623.webp)
磺胺类药物( Sulfonamides, SAs) 是指具有对氨基苯磺酰胺结构的一类药物的总称, 其通过干扰细菌的酶系统对氨基苯甲酸的利用而发挥抑菌作用, 后者是微生物生长必需物质叶酸的组成部分。
自20世纪30年代研究证明了SAs抑菌的基本结构后, 相继合成了各种SAs, 由于其抗菌谱广, 价格低廉, 目前仍是兽医临床和畜牧养殖业中最常用的药物添加剂之一, 但也带来了食品安全和环境污染等系列问题。
研究表明与其它常用抗生素相比, SAs可能更易诱导菌株应选择压力而产生耐药性。
此外,SAs药物还会导致过敏反应、尿和造血功能紊乱等副作用。
如磺胺二甲基嘧啶等可能诱发啮齿类动物如鼠的甲状腺增生, 对其激素样效应和潜在致癌性质正在进一步研究中。
由于SAs在体内作用和代谢的时间较长, 通过任何途径摄入的磺胺都有可能在人体中蓄积, 蓄积浓度超过一定值时将对人体机能造成损害。
因此, 联合国食品法典委员会(CAC) 和许多国家规定, 食品和饲料中SAs总量以及磺胺二甲基嘧啶等单个SAs的量均不得超过011mg/kg。
而且伴随兽药残留毒理学的发展和风险分析手段的进步, 各国对SAs在动物源性食品中的残留限量做出了越来越严格的规定, 如日本对食用动物肌肉中磺胺二甲基嘧啶的最大残留限量规定为方法检测低限, 即0101mg/kg。
关于SAs残留的检测从早期的分光光度法、荧光法、薄层色谱法到近些年的液相色谱法、气相色谱- 质谱法、液相色谱- 质谱法、毛细管电泳法和超临界流体色谱法, 几乎所有的分析理论和技术在SAs残留分析中都得到了研究和应用,其中采用最多的筛选方法是反相高效液相色谱法(HPLC) , 后来发展的酶联免疫吸附测试方法( EL ISA) 作为筛选方法也得到了广泛的应用。
但是这些检测方法都存在处理方法繁琐, 操作时间长及只能检测单个磺胺类药物的问题。
基于细菌受体分析的CharmⅡ放射免疫法的样品前处理提取方法简便, 具有灵敏度高, 特异性强的特点,并且可以检测磺胺类残留总量, 已经为欧盟国家和美国FDA 认可并且应用于初筛分析, 目前国内尚未见有关鳗鱼的检测报道。


毕业论文实验方案实验原料,中间产物,目标产物的物理化学性质:苯胺:无色油状液体。
熔点-6.3℃,沸点184℃,相对密度1.02 (20/4℃),相对分子量93.128,加热至370℃分解。
稍溶于水,易溶于乙醇、乙醚等有机溶剂。
暴露于空气中或日光下变为棕色。
醋酸酐:无色透明液体。
有强烈的乙酸气味。
味酸。
有吸湿性。
折光率极高。
溶于氯仿和乙醚,缓慢地溶于水形成乙酸。
与乙醇作用形成乙酸乙酯。
相对密度 1.080。
熔点-73℃。
沸点139℃。
折光率1.3904。
闪点54℃。
自燃点400℃。
低毒,半数致死量(大鼠,经口)1780mG/kG。
易燃。
有腐蚀性。
勿接触皮肤或眼睛,以防引起损伤。
有催泪性。
结晶醋酸钠:无色透明结晶或白色颗粒。
在干燥空气中风化,相对密度1.45,熔点58℃。
溶于水,水溶液呈碱性;微溶于乙醇。
浓盐酸:盐酸为无色液体,在空气中冒白雾(由于盐酸有强挥发性,与水蒸气结合形成小液滴),有刺鼻酸味。
粗盐酸或工业盐酸因含杂质氯化铁而带黄色。
乙酰苯胺:乙酰苯胺,学名N-苯(基)乙酰胺,白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体。
氯磺酸:氯磺酸(化学式:ClSO2OH)是一种无色或淡黄色的液体,具有辛辣气味,在空气中发烟,是硫酸的一个-OH 基团被氯取代后形成的化合物。
分子为四面体构型,取代的基团处于硫酸与硫酰氯之间,有催泪性,主要用于有机化合物的磺化,制取药物、染料、农药、洗涤剂等。
浓氨水:是氨气的水溶液,无色透明且具有刺激性气味。
易挥发,具有部分碱的通性,由氨气通入水中制得,主要用作化肥。
碳酸钠:碳酸钠,俗名苏打、大大苏打、纯碱、洗涤碱,化学式:Na₂CO₃,普通情况下为白色粉末,为强电解质。
密度为2.532g/cm³,熔点为851℃,易溶于水,具有盐的通性。
对乙酰氨基苯磺酰氯:熔点(℃)149,白色至灰色晶体.不溶于水,溶于苯、乙醚、丙酮、氯仿、二氯化乙烯。

化学品安全技术说明书编号:MSDS-029磺胺别名:磺胺一:标识【危化品名称】:磺胺【中文名】:对氨基苯磺酰胺【英文名】:p-aminobenzenesulfonamide【分子式】:C6H8N2O2S【相对分子量】:172.22【CAS号】:63-74-1【危险性类别】:二:主要组成与性状【主要成分】:【外观与性状】:白色颗粒或粉末状结晶,无臭,味微苦。
【主要用途】:是磺胺类药物中最简单的一种,用于生化研究、有机合成三:健康危害【侵入途径】:【健康危害】:接触磺胺类的工人,主诉有干咳、食欲不振、口中有恶味、头痛、头晕、易疲乏、精神萎靡、工作后思睡等。
遇热分解放出有毒的氮氧化物和氧化硫。
四:急救措施【皮肤接触】:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟。
就医。
【眼睛接触】:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。
就医。
【吸入】:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
【食入】:饮足量温水,催吐。
就医。
五:燃爆特性与消防【闪点】:无意义【引燃温度】:无意义【燃爆下限】:无意义【爆炸上限】:无意义【危险特性】:遇明火、高热可燃。
其粉体与空气可形成爆炸性混合物, 当达到一定浓度时, 遇火星会发生爆炸。
受高热分解放出有毒的气体。
【灭火方法】:消防人员须戴好防毒面具,在安全距离以外,在上风向灭火。
灭火剂:雾状水、泡沫、干粉、二氧化碳、砂土。
六:泄漏应急处理【泄漏应急处理】隔离泄漏污染区,限制出入。
切断火源。
建议应急处理人员戴防尘口罩,穿一般作业工作服。
不要直接接触泄漏物。
小量泄漏:避免扬尘,小心扫起,置于袋中转移至安全场所。
大量泄漏:收集回收或运至废物处理场所处置。
七:储运注意事项【储运注意事项】:储存于阴凉、通风的库房。
远离火种、热源。
防止阳光直射。
包装密封。
应与氧化剂分开存放,切忌混储。
配备相应品种和数量的消防器材。
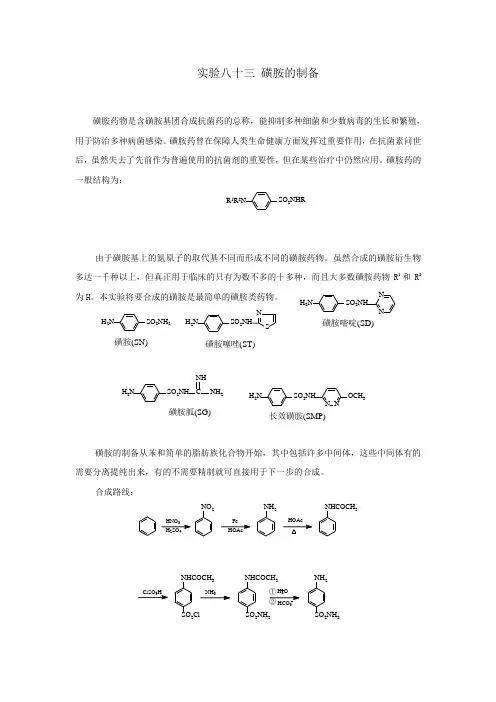
实验八十三 磺胺的制备磺胺药物是含磺胺基团合成抗菌药的总称,能抑制多种细菌和少数病毒的生长和繁殖,用于防治多种病菌感染。
磺胺药曾在保障人类生命健康方面发挥过重要作用,在抗菌素问世后,虽然失去了先前作为普遍使用的抗菌剂的重要性,但在某些治疗中仍然应用。
磺胺药的一般结构为:由于磺胺基上的氮原子的取代基不同而形成不同的磺胺药物。
虽然合成的磺胺衍生物多达一千种以上,但真正用于临床的只有为数不多的十多种,而且大多数磺胺药物R 1和R 2为H 。
本实验将要合成的磺胺是最简单的磺胺类药物。
磺胺的制备从苯和简单的脂肪族化合物开始,其中包括许多中间体,这些中间体有的需要分离提纯出来,有的不需要精制就可直接用于下一步的合成。
合成路线:SO 2N H RR 1R 2N SO 2N H 2H 2N磺胺(SN )3H SO N O 2Fe N H 2N H C OC H 3C lSO 3H N H C O C H 3SO 2Cl N H C O C H 3SO 2N H 2N H 2SO 2N H 2H N H 3②H 2N SO 2N HNS磺胺噻唑(ST )H 2NSO 2N HNN磺胺嘧啶(SD )H 2NSO 2N HCN H 2N H磺胺胍(SG )H 2N SO 2N HN NO CH 3长效磺胺(SM P)一、 乙酰苯胺的制备Preparation of acetanilide【目的与要求】1. 掌握苯胺乙酰化反应的原理和实验操作。
2. 进一步熟悉固体有机物的提纯的方法——重结晶。
【基本原理】芳胺的乙酰化在有机合成中有着重要的作用, 例如保护氨基。
一级和二级芳胺在合成中通常被转化为它们的乙酰化衍生物,以降低芳胺对氧化降价的敏感性或避免与其它功能基或试剂(如RCOCl ,-SO 2Cl ,HNO 2等)之间发生不必要的反应。
同时,氨基经酰化后,降低了氨基在亲电取代(特别是卤化)中的活化能力,使其由很强的第Ⅰ类定位基变为中强度的第Ⅰ类定位基,使反应由多元取代变为有用的一元取代;由于乙酰基的空间效应,对位取代产物的比例提高。
药物化学实验报告实验课程:药物化学实验项目:对氨基苯磺酰胺的制备时间:2010年12月05日对氨基苯磺酰胺的制备一、目的要求:1、通过对氨基苯磺酰胺的制备,掌握酰氯的氨解和乙酰氨基衍生物的水解。
2、进一步熟悉回流重结晶等基本操作。
二、基本原理:对氨基苯磺酰胺可以看作是磺胺类药物的母体三、实验材料:1.器材:电加热搅拌油浴锅、电子天平、铁架台、球形冷凝管、100 mL三口烧瓶、温度计、50 mL烧杯、玻璃棒、100 mL量筒、抽滤瓶(布氏漏斗)、洗瓶、胶头滴管、PH试纸2.试剂:乙酰氨基苯磺酰氯、浓氨水(28%, d=0.9)、稀盐酸(6M)、固体碳酸钠3.主要试剂及产物的性质试剂熔点℃沸点℃水溶性性状化学性质毒性对乙酰氨基苯磺酰氯149 426.8 不溶于水白色至灰色晶体。
易溶于乙醇、乙醚,溶于热苯、热氯仿。
LD50=16500mg/kg(小鼠经口)氨水-77 165 与水以任意比溶无色澄清液体挥发性、腐蚀性、水溶液呈弱碱性、不稳定性、沉淀性、还原性低毒、LD50=350 mg/kg碳酸钠851 ——21g(20℃)白色粉末状,是固体盐的通性无毒稀盐酸-114.8(纯) 108.6(20%)与水以任意比溶无色澄清液体1与酸碱指示反应 2和活泼的金属反应生成盐和氢气3与某些盐反应4与碱反应生成盐和水 5与某些金属氧化物反应生成盐和水低毒对氨基苯磺酰胺164--166 °C7.5 g/Lat 25 ºC白色颗粒或粉末状结晶,无臭。
味微苦。
微溶于冷水、乙醇、甲醇、乙醚和丙酮,易溶于沸水、甘油、盐酸、氢氧化钾及氢氧化钠溶液,不溶于氯仿、乙醚、苯、石油醚。
中毒4.投料比试剂分子量(Mr)质量/体积摩尔数(mol) 摩尔比Ρ(g/ml)对乙酰氨基苯磺酰氯233.5 5g 0.021 1 0.059 浓氨水35.045 35 mL ——0.104稀盐酸36.46 20 mL ———实验步骤 实验内容实验现象第一步 对乙酰氨基苯磺酰胺的制备1.将乙酰氨基苯磺酰氯 5 g 加入50 mL 烧杯中,在搅拌下慢慢加入35mL 浓氨水(28%, d=0.9)立即起放热反应,生产糊状反应物,加完氨水后继续搅拌,以除去多余的氨。
对氨基苯磺酰胺氨基苯磺酰胺(Sulfanilamide)是一种常见的有机化合物,化学式为C6H8N2O2S。
它是一种白色结晶粉末,常用于医学和化学实验中。
氨基苯磺酰胺最早由德国化学家Gerhard Domagk在20世纪30年代发现。
当时,他的研究小组正在寻找一种有效的抗菌剂来对抗感染。
他们在实验中发现,氨基苯磺酰胺对多种病原体具有抗菌作用,尤其对革兰氏阳性菌和葡萄球菌属菌株特别有效。
氨基苯磺酰胺的抗菌机制是通过抑制细菌生长。
它可以与细菌体内的二氢叶酸合成酶结合,阻断叶酸的合成。
由于叶酸对于细菌的生长和复制十分重要,这种抑制作用使得细菌无法正常进行新的DNA和蛋白质的合成,最终导致细菌的死亡。
正是因为氨基苯磺酰胺的抗菌作用,它被广泛应用于医学领域。
在过去的几十年里,氨基苯磺酰胺被用来治疗多种感染症,包括结核病、肺炎和脓疱病等。
然而,随着时间的推移,一些细菌对氨基苯磺酰胺产生了耐药性,使得它的疗效有所下降。
除了在医学领域的应用外,氨基苯磺酰胺还广泛用于化学实验中。
由于它的结晶性质和相对较低的价格,它常常被用作有机合成的起始原料。
尤其在药物合成中,氨基苯磺酰胺也被用作合成一些抗生素、痛风药和止痛药等药物的中间体。
然而,虽然氨基苯磺酰胺有着广泛的应用前景,但也需要注意到它可能的副作用和毒性。
在使用过程中,一些人可能会对氨基苯磺酰胺产生过敏反应,如皮疹和呼吸不畅等症状。
此外,长期大剂量使用氨基苯磺酰胺还可能引起一些不良反应,如贫血、肝功能异常等。
因此,在使用氨基苯磺酰胺时,需要注意使用剂量和持续时间,以避免不必要的风险。
综上所述,氨基苯磺酰胺是一种常见的有机化合物,具有广泛的应用领域。
它的抗菌作用使得它成为医药领域的重要抗生素之一,同时也在化学实验中被广泛应用。
然而,在使用过程中需要注意副作用和潜在的毒性。
我们应该在合适的条件下合理使用氨基苯磺酰胺,以确保其安全有效地发挥作用。
实验 对氨基苯磺酰胺的制备一、实验目的1. 学习对氨基苯磺酰胺的制备方法,掌握苯环上的磺化反应、酰氯的氨解和乙酰氨基衍生物水解反应;2. 巩固回流、脱色、重结晶及抽滤等基本操作。
二、实验原理对氨基苯磺酰胺是一种最简单的磺胺药,俗称SN 。
它是以乙酰苯胺为原料,然后再氯磺化和氨解,最后在酸性介质中水解除去乙酰基而制得。
乙酰苯胺的氯磺化需要用过量的氯磺酸[1],1 mol 的乙酰苯胺至少要用2 mol 的氯磺酸,否则会有磺酸生成。
过量氯磺酸的作用是将磺酸转变为磺酰氯。
反应式: NHCOCH 3+ 2HOSO 2Cl NHCOCH 32Cl+ H 2SO 4 + HCl NHCOCH 32Cl + NH 3NHCOCH 32NH 2+ HCl NH 2SO 2NH 2NHCOCH 32NH 2+ H 2O++ CH 3COOH三、实验步骤1. 对乙酰氨基苯碘酰氯在干燥的100 mL 三口烧瓶中,加入5 g (0.037 mol )干燥的乙酰苯胺,用小火加热熔化[2],瓶壁上若有少量水气凝结,应用干净的滤纸吸去。
边冷却边转动烧瓶使熔化物在瓶壁上凝结成薄层,将烧瓶置于冰水浴中充分冷却后,接上氯化氢吸收装置,迅速加入 13 mL (0.192 mol )氯磺酸。
反应迅速发生,若反应过于激烈,可用冰水浴冷却。
但如果不反应,可将烧瓶温热。
待反应缓和后,轻轻摇动烧瓶使固体全溶,然后再在温水浴中加热10 ~ 15 min 使反应完全,直至无氯化氢气体产生[3]。
将反应瓶在冷水中充分冷却后,于通风橱中在强烈搅拌下,将反应液以细流慢慢倒入盛75 g 碎冰的烧杯中[4],用少量冷水洗涤反应瓶,洗涤液倒入烧杯中。
搅拌数分钟,并尽量将大块固体粉碎[5],使之成为颗粒小而均匀的白色固体。
抽滤收集,用少量冷水洗涤,压干,立即进行下一步反应。
2.对乙酰氨基苯磺酰胺将上述粗产物移入四口圆底烧杯中,装配好吸收装置,在不断搅拌中慢慢加入18mL (0.457mol)浓氨水,立即发生放热反应并产生白色糊状物。
对氨基苯磺酰胺结构式
氨基苯磺酰胺是一种有机化合物,其标准分子式为 C6H7N2O2S,它有一个化学结构式
C6H6N2S(OH)2。
氨基苯磺酰胺化合物是一种重要的有机化合物,由一个苯环、一个二胺基和一个磺酸基组成。
其中,苯环的两端分别结合了羟基,中间则二胺基通过氮原子与苯环相连。
而二胺基
的一端分别与磺酸基结合,形成一个大的环状化合物。
这种化合物可以用于多种重要化学反应,例如:脱水反应和酯化反应等。
聚合物材料的合成甚至生物活性药物的合成等,在合成路线中都有重要作用。
例如,氨基苯磺酰胺在羟基
四氢呋喃酰胺合成中发挥重要作用。
此外,这种化合物还可以用于有机太阳能电池的合成,可大大提高这种材料的效率。
另外,氨基苯磺酰胺也可以用作农药,用于杀灭害虫和真菌。
它的作用很多,可以防治植
物疾病以及杀死蚊蝇、蚂蚁等害虫。
此外,它还可以用于生物识别,被用于临床检测疾病
抗原和抗体的存在情况。
总之,氨基苯磺酰胺(C6H7N2O2S)是一种重要的有机化合物,它可以用于合成类聚氨
酯材料、制备植物激素等农药、用于临床检测疾病抗原和抗体存在情况,因此具有较广泛的应用前景。
对氨基苯磺酰胺(磺胺)的合成一、实验目的1, 了解氯磺化反应的原理及操作方法。
2, 了解氨基的保护与原理。
二,实验原理磺胺是磺胺药物的最基本结构,也是药性的基本结构。
磺胺类药物是指具有 对氨基苯磺酰胺结构的一类药物的总称,是一类用于预防和治疗细菌感染性疾病 的化学治疗药物。
磺胺药物种类可达数千种,其中应用较广并具有一定疗效的就 有几十种。
磺胺药是现代医学中常用的一类抗菌消炎药,其品种繁多,已成为 一个庞大的家族了。
可是,最早的磺胺却是染料中的一员。
在某次偶然的机会, 人们发现这种红色的染料对细菌具有很强的抑制作用,从而将它应用于药物,并 在二十世纪上特别是一次与二次世界大战期间乃至到现在依然是一种应用非常 广泛的抗菌药物。
磺胺(对氨基苯磺酰胺)的合成步骤有如下:路线一:苯胺法 2)HCO q 3 路线二:氯苯法[1]路线三:二苯脲法⑵NHCOCH 3 NHCOCH 3 NHCOCH 3 N H 2ClSO_H -3 NH3 1)H 3OSO 2Cl SO 2NH 2 SO 2NH 2Cl Cl ClSO 3 HSO 3Cl *SO 3H SO 2ClNH 4OH NH 4OHCu 2ONH 2SO 2NH 2SO 2NH 2本实验将采用路线一。
三、 实验药品与仪器:药品:5g 乙酰苯胺,氯磺酸,浓氨水,浓盐酸,碳酸钠。
仪器:锥形瓶,抽滤瓶,烧瓶,布氏漏斗。
四、 实验步骤:将5克干燥的乙酰苯胺将入到干燥的250ml 锥形瓶中,用温火加热溶解乙酰苯胺,搅拌油状物以让溶解物附在锥形瓶底部。
冰浴冷却锥形瓶使油状物固化, 一次性迅速加入10ml 氯磺酸(密度1.77g/ml )。
然后连接预先配置好的氢氧化 钠溶液收集氯化氢气体。
将锥形瓶从冰浴中取出进行搅拌,氯化氢气体剧烈的释放出来,如果反应太 过剧烈,可放冷水中进行冷却。
当反应变缓后,可轻轻摇晃使固体全部溶解。
待 固体全部溶解后,用蒸气浴加热锥形瓶10min 至不在产生氯化氢气体为止,这过 程中必须进行尾气处理。
磺胺类磺胺类药物一般为白色或微黄色结晶性粉末,遇光易变质,色渐变深,大多数本类药物在水中溶解度极低,较易溶于稀碱,但形成钠盐后则易溶于水,其水溶液呈强碱性。
分子式:C6H8O2N2S 分子量: 172.20密度: 1.08 熔点:164-167摄氏度作用与用途:磺胺类药物能抑制革兰氏阳性菌及一些阴性菌。
对其高度敏感的细菌有:链球菌、肺炎球菌、沙门氏菌、化脓棒状杆菌、大肠杆菌。
对葡萄球菌、肺炎杆菌、巴氏杆菌、炭疽杆菌、志贺氏杆菌、亚利桑那菌等有抑制作用,对危害家禽的某些原虫也有作用。
磺胺类药主要作用是抑制细菌的繁殖,因有些细菌生长时,需利用对氨基苯甲酸。
氨基苯甲酸和二氢喋啶在二氢叶酸合成酶的作用下,合成二氢叶酸;二氢叶酸在二氢叶酸还原酶的作用下,又生成四氢叶酸;四氢叶酸再进一步形成活化型四氢叶酸,也就是辅酶F,它能传递一碳基团参与嘌呤、嘧啶核苷酸合成。
由于磺胺类药的化学结构与氨基苯甲酸很象,可与氨苯甲酸竞争二氢叶酸合成酶,妨碍二氢叶酸的形成,最终影响细菌核蛋白的合成,从而抑制细菌的生长繁殖。
对磺胺类药敏感的细菌,在体内外均能获得耐药性,而且对一种磺胺产生耐药性后,对其它磺胺也往往产生交叉耐药性,但耐磺胺类药的细菌对其它抗菌药物仍然敏感。
在家庭自备的小药箱里,磺胺可算是常驻部队中的重要一员。
当人们一有了炎症,如尿道炎、肠炎、呼吸道疾病时,也往往会先想到“吃点磺胺吧”。
的确,磺胺在治疗炎症方面具有见效快、疗效确切及价格低廉的优点,但是,与其他药相比,磺胺属于“讲究”比较多的药,而且这些“讲究”一旦被忽视,就会让你多出一些病痛和烦恼。
在日常服用普通药物时,人们一般都知道应该喝一大杯水以便将药物顺利服下的道理,但是在服用磺胺时,就不是一大杯水能打发的了了。
解放军305医院消化内科主任医师王志津说,由于磺胺药在尿液中的溶解度很小,为了增加其溶解度,最好的办法是尽可能地多饮水,从而通过增加尿量来降低尿中药物的浓度。
南昌大学化学实验中心
有机化学实验
实验指导书:有机化学实验(兰州大学、复旦大学编)
综合性实验项目名称 对氨基苯磺酰胺的制备
一、实验目的和要求
1、掌握由乙酰苯胺经氯磺化,氨解和水解等多步反应制备磺胺药物的原理和方法。
2、掌握气体捕集器的使用,回流,脱色,重结晶等操作。
二、实验基本原理
乙酰苯胺经过氯磺化,氨解与水解等反应转变为对氨基苯磺酰胺(磺胺)。
三、主要仪器设备及实验耗材:
实验耗材:乙酰苯胺5.0g (0.037mol ), 氯磺酸12.5ml (0.19mol ),浓氨水:35ml,浓盐酸,碳酸钠
主要仪器:搅拌棒、尾气吸收装置、减压抽滤装置及常规玻璃仪器 四、实验步骤 (一) 对乙酰氨基苯磺酰氯的制备
1、投料和反应:①干燥的100mL 锥形瓶中加入5.0g 干燥的乙酰苯胺,石棉网上小火加热熔化,冷却使熔化物凝结成块。
②冰水浴中充分冷却后,一次加入12.5mL 氯磺酸(通风橱中),立即装好如图反应装置。
③待固体全部溶解后,温水浴中加热10分钟至不再有HCl 产生为止。
2、 后处理: 冰水冷却,通风橱中,强烈搅拌下细流慢慢倒入盛有120g 碎冰的大烧杯中,搅拌,抽滤得白色固体,少量冷水洗涤,粗产品直接用于下步制备。
(二) 对乙酰氨基苯磺酰胺的制备
上述粗产物放入烧杯,搅拌下慢慢加入17.5mL 浓氨水,继续搅拌15min,然后加入10mL 水,石棉网上小火加热10分钟以除去多余的氨。
冷却,抽滤,冷水洗涤,得粗产品,直接用于下步水解。
(三) 对氨基苯磺酰胺(磺胺)的制备
1、 反应:100mL 圆底烧瓶中加入上述粗品和3.5mL 浓HCl,投入沸石,石棉网上小火回流
南昌大学化学实验中心0.5h,至全部产品溶解后冷却至室温。
如溶液呈黄色,并有极少量固体,则需加入少量活性炭煮沸5分钟,抽滤得滤液。
2、 后处理:滤液转入大烧杯中,搅拌下加固体碳酸钠(约4g)中和至PH=7~8,冷却,抽滤,洗涤。
3、 精制:粗品用水重结晶,产量约3~4g。
4、 测定熔点:纯对氨基苯磺酰胺为白色叶片状晶体,熔点:165~166℃。
五、实验关键及注意事项
1、氯磺酸对皮肤有强烈的腐蚀性,在空气中冒出大量HCl 气体。
遇水会发生猛烈的放热反应,所以反应中所用仪器及药品必须干燥。
废液不能倒入水槽,应倒入废液缸。
2、氯磺化过程中,有大量氯化氢气体产生,所以装置应严密,在通风橱中进行。
导气管的末端应接近水面,但不能插入水面,否则可能倒吸而引起严重事故。
六、思考题
1. 为什么苯胺要乙酰化后再氯磺化?直接氯磺化行吗? 2. 如果理解对乙酰氨基苯磺酰胺是两性物质?试用反应式表示磺胺与稀酸和稀碱的作用。