九年级上册化学 元素
- 格式:doc
- 大小:40.65 KB
- 文档页数:3

课题3元素【基础主干落实】一、元素1.概念:质子数(即核电荷数)相同的一类原子的总称。
2.分类:金属元素、非金属元素和稀有气体元素。
3.在地壳中的含量:按质量分数,含量在前四位的元素:O、Si、Al、Fe。
4.化学性质:在化学反应前后,元素的种类不会改变。
二、元素符号1.书写:“一大二小”,由一个字母表示的要大写;由两个字母表示的,第一个字母大写,第二个字母必须小写。
2.意义(1)宏观:表示一种元素,如“N”表示氮元素。
(2)微观:表示这种元素的1个原子,如“C”表示1个碳原子。
3.物质的组成与构成(1)宏观上,物质是由元素组成的,如水是由氢元素与氧元素组成的。
(2)微观上,物质是由粒子构成的,如水是由水分子构成的,水分子是由氢原子和氧原子构成的,1个水分子是由2个氢原子和1个氧原子构成的。
三、元素周期表1.原子序数:元素周期表按元素原子核电荷数递增的顺序给元素编了号。
原子序数=核电荷数=质子数。
2.元素周期表的结构(1)元素周期表有7个周期,16个族。
(2)单元格信息【漫画辨析】元素种类由质子数决定,质子数相同的原子与该原子得失电子后形成的离子属于同一种元素。
【妙法指引】(1)元素的原子核外有几个电子层,该元素就位于第几周期。
(2)每个周期开头是金属元素(第一周期除外),靠近尾部是非金属元素,结尾是稀有气体元素。
【重点案例探析】考点元素周期表及其应用【典题1】(2023·绥化中考)元素周期表是学习化学的重要工具,如图为元素周期表中部分元素的相关信息,利用下表回答相关问题。
(1)原子序数为7和15的两种元素的化学性质相似,是因为两种元素的原子最外层电子数相同。
(2)O2-核外电子排布与氖原子相同。
(3)铝、硅、磷三种元素位于元素周期表中同一周期,是因为三种元素的原子核外电子层数相同。
【典题2】(2023·湘潭中考改编)2023全球6G技术大会3月22日在南京召开。
硅(Si)是制作芯片不可缺少的材料,在元素周期表中的信息及原子结构示意图如图1所示,请结合图2回答下列问题。


化学九年级上册化合价口诀元素符号一、化合价的定义化合价是指原子在化合物中相对于最稳定的负离子(通常是氧)或者正离子的电价,通常表示原子价的大小。
化合价是物质化学性质的重要指标,也是化学计算和方程式配平的基础。
化合价的计算方法有以下几种:1. 根据元素的族和周期计算化合价;2. 根据化合物的结构和成键情况进行计算。
二、元素符号和化合价1. 元素符号元素符号是由元素名称的第一个英文字母大写,第二个英文字母小写的组合,如H(氢)、O(氧)、Na(钠)等。
元素符号表明了该元素的身份,也方便在化学方程式中使用。
2. 化合价以下是常见元素的化合价口诀:① ⅠA族元素(碱金属类)的化合价永远是+1;② ⅣA族元素的化合价除了在自身化合物中是+4或-4外,其他永远是+4;③ ⅤA族元素的化合价一般是+5,也可能是+3或者+1;④ ⅥA族元素的化合价一般是-2,也可能是-1、+2或者+4;⑤ ⅦA族元素的化合价一般是-1。
三、化合价应用实例以下是一些常见元素的化合价及应用实例:1. 氢(H)氢的化合价一般是+1。
HCl(氢氯酸)中氢的化合价是+1。
2. 氧(O)氧的化合价一般是-2。
H₂O(水)中氧的化合价是-2。
3. 氯(Cl)氯的化合价一般是-1。
NaCl(氯化钠)中氯的化合价是-1。
4. 碳(C)碳的化合价一般是+4或-4。
CO₂(二氧化碳)中碳的化合价是+4;CH₄(甲烷)中碳的化合价是-4。
5. 铁(Fe)铁的化合价一般是+2或+3。
FeO(氧化铁)中铁的化合价是+2;Fe₂O₃(三氧化二铁)中铁的化合价是+3。
四、结论化合价是化学中一个重要的概念,通过学习元素符号和化合价口诀,可以帮助我们更好地理解元素的化合价,并且能够应用到实际的化学计算和方程式配平中。
希望同学们能够牢记化合价口诀,掌握元素符号和化合价的相关知识,从而在化学学习中取得更好的成绩。
化学九年级上册化合价口诀元素符号五、化合价的应用化合价的掌握对于化学方程式的平衡非常重要。


第三单元物质构成的奥秘课题3元素课本核心知识点精讲知识点1元素1.元素的概念元素是质子数(即核电荷数)相同的一类原子的总称。
2.元素的分类及分布3.元素的化学性质:元素的化学性质取决于原子最外层电子数,物质在发生化学反应时,原子的种类不变,元素的种类也不变。
4.物质的宏观组成与微观构成知识点2元素符号1.元素符号的书写(1)由一个字母表示的元素符号要大写,如C、H、O、S等。
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如Na、Ca、Cl等。
2.元素符号表示的意义(1)宏观上表示一种元素。
·(2)微观上表示该元素的一个原子。
(3)对于某些金属、固态非金属、稀有气体的元素符号,还可以表示该元素组成的物质。
(4)若元素符号前面加上数字,该符号只能表示该原子的个数。
例1(2022浙江乐清期中)下列关于元素符号“H”的说法中,正确的是()①表示氢元素②表示氢气③表示1个氢原子④表示1个氢分子A.①②B.②③C.①③D.②④答案:C解析:“H”是氢的元素符号,可表示氢元素或1个氢原子。
知识点3元素周期表1.原子序数元素周期表按元素原子核电荷数递增的顺序给元素编号,叫做原子序数。
原子中,原子序数=核电荷数=质子数=核外电子数。
2.元素周期表的结构(1)横行:每一横行叫一个周期,共有7个周期。
每周期(第一周期除外)以金属元素开始,再过渡到非金属元素,以稀有气体元素结束。
(2)纵列:每一个纵列叫做一个族(8、9、10三个纵列共同组成一个族)。
3.单元格信息(以碳元素为例)例2(2022陕西陇县期中)元素周期表是学习化学的重要工具。
如图是元素周期表的一部分,请回答下列问题:(1)表中①所示元素的名称是________,其元素符号为________。
(2)X2-与Ar的核外电子排布相同,则X的元素符号是________。
(3)元素周期表中同族和同周期元素具有一定的相似性和变化规律,同族元素化学性质相似的原因是________相同。

九年级上册化学知识点(完整版)第一章元素及其周期性元素的概念元素是指由同一种原子构成,具有相同的原子序数(即原子核中质子数相同)和化学性质的物质。
元素周期表元素周期表是将元素按照原子序数大小排列成一张表,表头为元素符号,表格中的元素按照一定规律分布。
元素周期表中的一行为一个周期,元素周期表中的一列为一个族。
元素周期表的构造依据是元素原子的电子结构及其周期性规律。
周期表上元素的分类元素周期表中的元素可分为金属、非金属和半金属三类。
•金属元素是指性质落在半导体和非金属之间的元素。
•非金属元素是指那些数字属于瞬时、振荡、瞬变或有独立共振结构的元素或离子。
•半金属元素通常被描述为同时具有金属和非金属的性质,比如硼、硅等。
元素周期性元素周期性是指周期表中每个周期内,元素的性质随原子序数的增加呈现出一定的规律性。
元素的周期趋势和族内变化规律元素周期性的表现有周期性的趋势和族内的变化规律。
1.原子半径的变化规律随原子序数的增大,原子半径逐渐递增;原子半径和化学元素周期数成反比关系;原子半径和原子核电荷数成正比关系。
2.电离能和电子亲和能的变化规律随原子序数增大,电离能逐渐增大;电子亲和能和化学元素周期数成正比关系;电子亲和能和原子核电荷数成反比关系。
3.金属的化学性质和半径的变化规律金属原子的化学性质随原子半径和电子密度变化而变化。
原子半径越大,电子密度越低,相应的,金属原子的化学性质越活泼。
第二章化学式和化合式化学式化学式是指用化学符号表示化合物所含元素种类和原子数的符号组合。
1.分子式分子式是化合物分子中各原子的种类与相对数目所表示的化学式。
2.电离式电离式是指化合物在水中或熔融状态下离子化的化学式。
3.范德华(分子)式范德华式是指在离子化学式的基础上,表示分子中各原子在空间中的排列方式和分子的化学性质。
化合价化合价是化合物中元素的化学结合力大小的一种量度,用于表示元素或原子在化合物中所起的化学作用性质。


九年级上册化学知识点元素化学是一门研究物质组成、性质和变化规律的科学。
在九年级上册的化学课程中,我们将学习许多与元素相关的知识点。
本文将介绍九年级上册化学课程中所包含的一些主要元素及其特点。
一、氢(H)氢是最轻的元素,它是宇宙中丰度最高的元素之一。
氢气无色、无味、无臭,燃烧时形成水。
在化学反应中,氢常以H2的形式出现。
氢在工业和能源生产中具有重要的应用,如氢燃料电池。
二、氧(O)氧是地球上最常见的元素,占地壳的大部分。
氧气是一种无色、无味、无臭的气体,它是呼吸和燃烧过程中必不可少的物质。
氧气常以O2的形式存在。
氧还与其他元素结合形成氧化物,例如水(H2O)和二氧化碳(CO2)。
三、碳(C)碳是一种非金属元素,存在于地球上的有机物质中。
它具有多种形态,如金刚石和石墨。
碳还是生命的基础,所有有机物质都含有碳元素。
它能与氧、氢和其他元素形成共价键,构成化合物。
四、氮(N)氮是大气中的主要成分之一,占据了空气的78%。
氮气是一种无色、无味、无毒的气体,不支持燃烧。
氮还存在于大量生物分子中,包括蛋白质和核酸。
在工业上,氮广泛用作肥料和化学工业原料。
五、氯(Cl)氯是一种常见的非金属元素,常以Cl2的形式存在。
它是一种黄绿色的气体,具有强烈的刺激性气味。
氯具有强氧化性,常用于消毒和杀菌。
氯化物在自然界和生物体内广泛存在,如食盐(氯化钠)和胃酸(氯化氢)。
六、铁(Fe)铁是地壳上最常见的金属元素之一,它具有良好的导电和导热性能。
铁在建筑、制造和交通运输等行业中广泛应用,如制造钢铁和制动器件。
铁还是血红蛋白的组成成分,在体内起着携氧的重要作用。
七、铜(Cu)铜是一种重要的工业金属,具有良好的导电性和导热性。
它常被用于制造导线、管道和电器设备。
铜也是一种重要的生物元素,参与多种酶的催化反应。
八、金(Au)金是一种非常重要的贵金属,具有很高的价值和抗腐蚀性。
金在珠宝、投资和电子行业中广泛应用。
它还具有一定的生物活性,被用于医学和生物学研究。

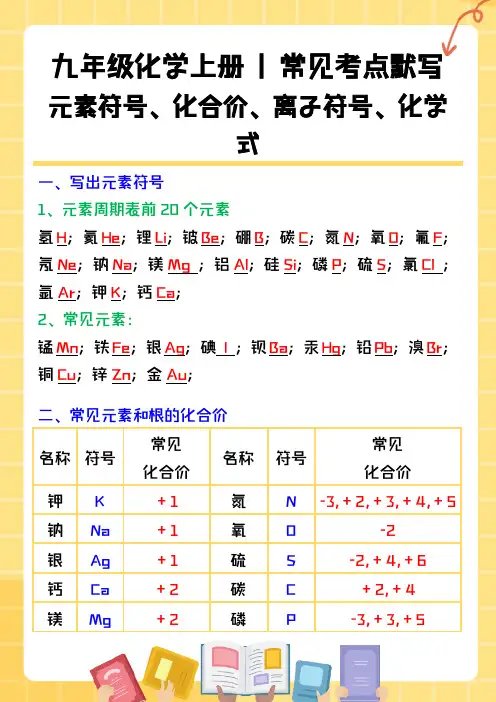
九年级化学上册 | 常见考点默写元素符号、化合价、离子符号、化学式一、写出元素符号1、元素周期表前20个元素氢H;氦He;锂Li;铍Be;硼B;碳C;氮N;氧O;氟F;氖Ne;钠Na;镁Mg;铝Al;硅Si;磷P;硫S;氯Cl;氩Ar;钾K;钙Ca;2、常见元素:锰Mn;铁Fe;银Ag;碘 I ;钡Ba;汞Hg;铅Pb;溴Br;铜Cu;锌Zn;金Au;二、常见元素和根的化合价名称符号常见化合价名称符号常见化合价钾K+1氮N-3,+2,+3,+4,+5 钠Na+1氧O-2银Ag+1硫S-2,+4,+6钙Ca+2碳C+2,+4镁Mg+2磷P-3,+3,+5铜Cu+1,+2锌Zn+2锰Mn +2,+4,+6,+7硅Si+4铝Al+3氢氧根OH--1 氢H+1硫酸根SO42--2氯Cl -1,+1,+5,+7碳酸根CO32--2铁Fe+2,+3铵根NH4++1氟F-1硝酸根NO3--1三、写出下列离子的符号氢离子H-;氧离子O2-;氟离子F-;钠离子Na+;镁离子Mg2+;铝离子Al3+;硫离子S2-;氯离子Cl-;钾离子K+;钙离子Ca2+;铁离子Fe3+;铜离子Cu2+;亚铁离子Fe2+;氢氧根离子OH-;硫酸根离子SO42-;硝酸根离子NO3-;碳酸根离子CO32-;铵根离子NH4+;碳酸氢根离子HCO3-;四、写出下列物质的化学式1、单质三原子:臭氧O3;双原子:氧气O2;氯气Cl2;氢气H2;碘I2;溴Br2;单原子:稀有气体:氦气He;氩气Ar;氖气Ne;金属:铜Cu;银Ag;水银Hg;锌Zn;铁Fe;其他:磷P;金刚石C;硫S;碳C;石墨C;2、化合物氧化物:氧化铝Al2O3;水H2O;干冰CO2;氧化铜CuO;三氧化硫SO3;过氧化氢H2O2;二氧化硫SO2;氧化钾K2O;氧化钙CaO;一氧化碳CO;二氧化锰MnO2;四氧化三铁Fe3O4;五氧化二磷P2O5;氯化物:氯化钠NaCl;氯化铜CuCl2;氯化银AgCl;氯化氢HCl ;氯化镁MgCl2;氯化铁FeCl3;硫化物:硫化氢H2S;硫化钠Na2S;硫化锌ZnS;其他:氯酸钾KClO3;硫酸钾K2SO4;碳酸钙CaCO3;锰酸钾K2MnO4;高锰酸钾KMnO4;硫酸H2SO4;氢氧化钙Ca(OH)2;氢氧化钾KOH;氢氧化铝Al(OH)3;碳酸钠Na2CO3;碳酸铵(NH4)2CO3;。

九年级上册化学教材中涉及到的物质及其化学式一、1~18号元素及符号:氢H氦He锂Li铍Be硼B碳C氮N氧O氟F氖Ne钠Na镁Mg铝Al硅Si磷P硫S氯Cl氩Ar二、其他常见的元素及符号:钾K钙Ca锰Mn铁Fe铜Cu锌Zn银Ag钡Ba铂Pt金Au汞Hg碘I铅Pb锡Sn溴Br三、教材上常见的物质及化学式:水H2O石灰石CaCO3硫酸铜晶体(胆矾蓝矾)CuSO4•5H2O氢氧化钠NaOH稀盐酸(氯化氢)HCl二氧化碳CO2铁锈(氧化铁)Fe2O3铜绿Cu2(OH)2CO3氢氧化铜Cu(OH)2酒精(乙醇)C2H5OH 氧气O2氮气N2碳酸钠粉末Na2CO3氧化铜CuO氧化汞HgO五氧化二磷P2O5氦He氖Ne氩Ar氪Kr氙Xe氡Rn硝酸HNO3一氧化氮NO二氧化硫SO2二氧化氮NO2臭氧O3四氧化三铁Fe3O4氯化钙CaCl2高锰酸钾KMnO4锰酸钾K2MnO4二氧化锰MnO2过氧化氢H2O2氯酸钾KClO3氯化钾KCl浓氨水NH3·H2O氢气H2氯化氢HCl氯气Cl2碳酸钙CaCO3明矾KAl(SO4)2·12H2O溴化钠NaBr 氧化铝Al2O3三氧化硫SO3碘化钾KI硝酸钠NaNO3硝酸铵NH4NO3亚硝酸钠NaNO2碘酸钾KIO3 碳酸氢氨NH4HCO3硫酸亚铁FeSO4氧化镁MgO生石灰CaO氯化锌ZnCl2一氧化碳CO澄清石灰水(主要是氢氧化钙)Ca(OH)2碳酸H2CO3臭氧O3甲烷CH4碳酸氢钠NaHCO3硫酸锌ZnSO4四、化合价记忆口诀:钾钠氢银正一价,氟氯溴碘负一价,钙镁锌钡正二价,通常氧是负二价,铜正一正二铝正三,铁有正二和正三,碳有正二和正四,硫有负二正四和正六,硫碳锰酸根负二,硝氯氢氧髙锰负一,还有一个正一价,铵根一定要记清。
五、涉及到的方程式:4P+5O2==2P2O5 2CuO+C==2Cu+CO2↑S+O2==SO2 CO2+C==2CO2Fe2O3+3C==4Fe+3CO↑ H2O2==H2O+O23Fe+2O2==Fe3O4 CaCO3==CaO+CO2↑CaCO3+2HCl==CaCl2+H2CO3 H2O==H2+O2KClO3==KCl+O2↑ H2CO3==CO2+H2OFe+CuSO4==FeSO4+Cu 2CO+O2==2CO22Mg+O2==2MgOCuO+CO==Cu+CO2O2+2H2==2H2O 2C+O2==2COCaO+H2O==Ca(OH)2 CuO+H2==Cu+H2OC2H5OH+3O2==2CO2+3H2OCuSO4+2NaOH==NaSO4+Cu(OH)22KMnO4==K2MnO4+MnO2+O2↑CaCO3+2HCl==CaCl2+CO2↑+H2OCO2+Ca(OH)2==CaCO3↓+H2OZn+H2SO4==ZnSO4+H2↑一、1~18号元素及符号:氢___ 氦___锂___铍___硼___碳___氮___氟___氖___钠___镁___铝___硅___磷___硫___氯___氩___二、其他常见的元素及符号:钾___钙___锰___铁___铜___锌___银___钡___铂___金___汞___碘___铅___锡___溴___三、教材上常见的物质及化学式:水____石灰石____硫酸铜晶体(胆矾蓝矾)____氢氧化钠____稀盐酸(氯化氢)____二氧化碳____铁锈____铜绿____氢氧化铜____酒精(乙醇)____氧气____氮气____碳酸钠粉末____氧化铜____氧化汞____五氧化二磷____氦__氖__氩__氪__氙__氡__硝酸____一氧化氮____二氧化硫____二氧化氮____臭氧____四氧化三铁____氯化钙____高锰酸钾____锰酸钾____二氧化锰____过氧化氢____氯酸钾____氯化钾____浓氨水____氢气____氯化氢____氯气____碳酸钙____明矾________氧化铁____溴化钠____ 氧化铝____ 三氧化硫____ 碘化钾____ 硝酸钠____ 硝酸铵____亚硝酸钠____碘酸钾____碳酸氢氨_______硫酸亚铁____ 氧化镁 ____生石灰____ 氯化锌____一氧化碳____ 澄清石灰水____碳酸____ 臭氧____ 甲烷____碳酸氢钠____ 硫酸锌____。
氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙氢H 氦He 锂Li 铍Be 硼B 碳C 氮N 氧O 氟F 氖Ne 钠Na 镁Mg 铝Al 硅Si 磷P 硫S 氯Cl 氩Ar 钾K 钙Ca序号元素名称符号1 铬Cr 铌Nb 铝Pb2 镍Ni 钽Ta 铋Bi3 硅Si 氢H 锕Ac4 锰Mn 碳C 铈Ce5 铝Al 氧O 铍Be6 磷P 钠Na 铯Se7 钨W 镁Mg 锆Zr8 钼Mo 硫S 镧La9 钒V 氯Cl 钡Ba10 钛T 钾K 汞Hg11 铜Cu 锌Zn 钙Ca12 铁Fe 银Ag 碘I13 硼B 锡Sn 溴Br14 钴Co 锑Sb 氟F15 氮N 金Au 烯土Re1 铬铌铝2 镍钽铋3 硅氢锕4 锰碳铈5 铝氧铍6 磷钠铯7 钨镁锆8 钼硫镧9 钒氯钡10 钛钾汞11 铜锌钙12 铁银碘13 硼锡溴14 钴锑氟15 氮金烯土常用化学元素符号表序号元素名称符号1 Cr Nb Pb2 Ni Ta Bi3 Si H Ac4 Mn C Ce5 Al O Be6 P Na Se7 W Mg Zr8 Mo S La9 V Cl Ba10 T K Hg11 Cu Zn Ca12 Fe Ag I13 B Sn Br14 Co Sb F15 N Au Re初中化学基础知识总结和常用口诀一、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3 碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2 (工业用盐、有毒)。
九年级上册化学金属知识点化学金属是九年级上册化学学习中的重要内容之一。
本文将介绍九年级上册化学金属的相关知识点,包括金属元素、金属特性、金属的制备和应用等内容。
一、金属元素金属元素是构成金属的基本物质。
九年级上册化学学习中,我们常见的金属元素包括铁(Fe)、铜(Cu)、锌(Zn)、铝(Al)等。
这些金属元素具有以下特点:导电性好、导热性好、延展性好、强度高等。
二、金属特性1. 导电性金属具有良好的导电性,是因为金属中的自由电子可以自由移动。
这也是为什么金属制成的导线可以传导电流的原因。
2. 导热性金属具有良好的导热性,是因为金属中的自由电子和金属离子的热运动能够很快传递热量。
所以,金属是热传导的良好材料。
3. 延展性和韧性金属具有良好的延展性和韧性,可以通过轧制、拉制等方式制成各种形状的线材和板材,这也是金属广泛应用于工业生产中的原因之一。
4. 强度金属的强度通常较高,可以用于制造各种承重构件。
三、金属的制备1. 金属的矿石提炼大多数金属是从矿石中提取出来的。
矿石中的金属通常以氧化物、硫化物等形式存在,通过冶炼反应将金属从氧化物或硫化物中还原出来,得到纯净的金属。
2. 电解法某些金属可以通过电解法制备出来。
电解法是利用电解质溶液中的金属离子,在电解过程中还原出金属。
四、金属的应用金属在生活中和工业生产中有广泛的应用。
以下是几个常见的金属应用:1. 铁的应用铁是工业生产中重要的金属之一,广泛用于建筑、制造机械设备和交通工具等领域。
2. 铝的应用铝是重要的金属材料,具有轻质、耐腐蚀等特点,广泛应用于制造飞机、汽车、铁路车辆等。
3. 锌的应用锌是重要的金属材料,常用于镀锌处理,提高铁制品的耐腐蚀性。
4. 铜的应用铜是导电性能良好的金属,广泛应用于电气设备、电线电缆等领域。
总结:九年级上册化学金属知识点包括金属元素、金属特性、金属的制备和应用等,通过了解这些知识点,我们可以更好地理解金属的性质和应用,进一步探索化学学科的奥秘。
⼈教版九年级化学上册必背知识点(完整)⼀、化学⽤语1、常见元素及原⼦团的名称和符号⾮⾦属: O氧 H氢 N氮 Cl氯 C碳 P磷 S硫⾦属: K钾 Ca钙 Na钠 Mg镁 Al铝 Zn锌 Fe铁 Cu铜 Hg汞 Ag银 Mn锰 Ba钡原⼦团(根):氢氧根硝酸根碳酸根OH- NO3- CO3 2-硫酸根磷酸根铵根SO4 2- PO43- NH4+2、化合价⼝诀(1) 常见元素化合价⼝诀:⼀价氢氯钾钠银;⼆价氧钙钡镁锌;三五氮磷三价铝;铜汞⼀⼆铁⼆三;⼆、四、六硫四价碳;三、许多元素有变价,四、条件不同价不同。
(2) 常见原⼦团(根)化学价⼝诀:⼀价硝酸氢氧根;⼆价硫酸碳酸根;三价常见磷酸根;通常负价除铵根。
(3) 熟练默写常见元素的常⽤的化合价+1价 K+ 、Na+ 、H+ 、Ag+ 、NH4++2价 Ca2+ 、Ba2+ 、Mg2+ 、Zn2+ 、Cu2+ 、 Hg2+、亚Fe2++3价 Fe3+ ,Al3+-1价 Cl-、OH-、NO3-4.必须熟记的制取物质的化学⽅程式(1)实验室制取氧⽓⼀: 2KMnO4===K2MnO4+MnO2+O2↑(2)实验室制取氧⽓⼆: 2H2O2 ===2H2O+O2↑(3) 实验室制取氧⽓三: 2KClO3===2KCl+3O2↑(4) 实验室制法CO2: CaCO3+2HCl==CaCl2+H2O+CO2↑(5) 实验室制取氢⽓: Zn+H2SO4==ZnSO4+H2↑(6) 电解⽔制取氢⽓: 2H2O===2H2↑+O2↑(7)湿法炼铜术(铁置换出铜):Fe+CuSO4==FeSO4+Cu(8)炼铁原理: 3CO+Fe2O3===2Fe+3CO2(9)⽣灰⽔[Ca(OH)2 ]的制取⽅法:CaO+H2O==Ca(OH)2(10)⽣⽯灰(氧化钙)制取⽅法:CaCO3 ===CaO+CO2↑⼆、⾦属活动性顺序:⾦属活动性由⾄弱:K Ca Na Mg Al , Zn Fe Sn Pb (H) ,Cu Hg Ag Pt Au 。