对硝基苯酚的制备
- 格式:docx
- 大小:63.22 KB
- 文档页数:4
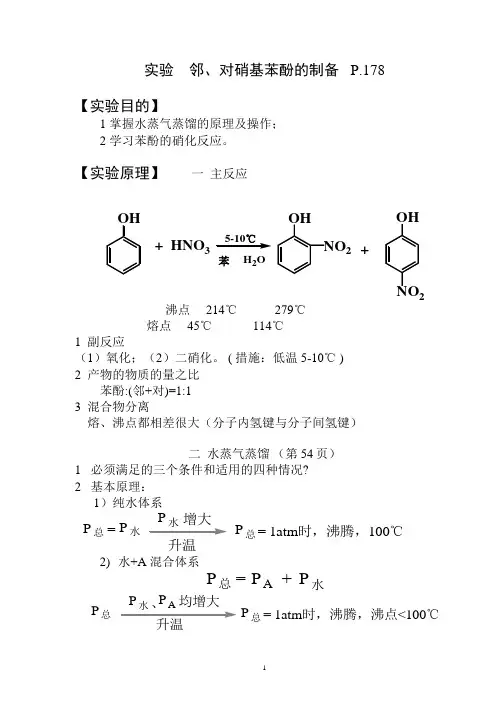
实验邻、对硝基苯酚的制备 P.178【实验目的】1 掌握水蒸气蒸馏的原理及操作;2 学习苯酚的硝化反应。
【实验原理】一主反应+ HNO3苯22+H2O沸点 214℃ 279℃熔点 45℃ 114℃1 副反应(1)氧化;(2)二硝化。
( 措施:低温 5-10℃ )2 产物的物质的量之比苯酚:(邻+对)=1:13 混合物分离熔、沸点都相差很大(分子内氢键与分子间氢键)二水蒸气蒸馏(第54页)1 必须满足的三个条件和适用的四种情况?2 基本原理:1)纯水体系P水升温PP总= 1atm时,沸腾,100℃P总=2)水+A 混合体系P总=P P水+AP总P P均增大P总= 1atm时,沸腾,沸点<100℃馏出液:含水、A。
【实验装置与步骤】一反应装置二水蒸气蒸馏装置1 蒸汽发生器:产生蒸汽,加沸石,安全管的作用及位置。
2 导气管:保持通畅、下斜,水夹的作用。
3 蒸馏过程:先蒸出苯,后蒸出邻硝基苯酚。
三实验步骤(P.179,方法二,自行整理并记录实验现象)【注意事项】1 逐滴滴入浓硝酸,才能维持温度5-10℃。
2 对位产物重结晶后的滤液,不要倒掉。
3 水蒸气蒸馏时,可以在三颈烧瓶的底部另加热少许。
4 必要时,可以不用石棉网,直接给蒸汽发生器加热。
5 反应残液处理:加10毫升1% NaOH溶液。
【实验结果】1 产品的颜色、形状:2 产率产率 =M 理论M邻×100%邻:产率 =M理论M对×100%对:总产率 =M理论M 对×100%M邻+3 实验得失分析:【问题与讨论】 第179页: 1、2题3 简单的流程图,说明邻、对硝基苯酚二者从混合物到纯品的过程。

MIL-53(Fe)的合成及其催化还原对硝基苯酚的研究杨宇珩;张丹;孟秀红;段林海【摘要】利用溶剂热合成法制备金属有机骨架材料MIL-53(Fe).通过X射线衍射仪(XRD)、电子扫描电镜(SEM)、傅立叶变换红外光谱仪(FTIR)表征手段对材料的晶相结构及组成成分进行分析.常温常压下,通过催化还原对硝基苯酚的反应考察MIL-53 (Fe)的催化活性.结果表明,MIL-53(Fe)的催化活性良好,5 min对硝基苯酚的转化率达到96.8%.【期刊名称】《化工科技》【年(卷),期】2018(026)005【总页数】4页(P5-8)【关键词】MIL-53 (Fe);对硝基苯酚;催化还原【作者】杨宇珩;张丹;孟秀红;段林海【作者单位】辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001;辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001;辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001;辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001【正文语种】中文【中图分类】TB383;O643.36对硝基苯酚是一种重要的工业原料。
随着化工行业的迅猛发展,大量的对硝基苯酚排放到人类赖以生存的环境中。
由于对硝基苯酚具有毒性大、化学稳定性好、降解难的特点,使其成为最难治理的一类污染物[1-4]。
然而,对硝基苯酚的还原产物对氨基苯酚毒性相对较低,并且在医药、染料、橡胶等工业行业有着极为广泛的应用。
尤其在医药行业,对氨基苯酚是合成扑热息痛(对乙酰氨酚)、安妥明(对氯苯氧基甲基丙酸乙醇)、心得宁、维生素B1等的中间体[5-7]。
目前有两种将对硝基苯酚催化还原转变为对氨基苯酚的方法[8]。
(1)对硝基苯酚铁粉还原。
在酸性条件下,铁粉作为还原剂,将对硝基苯酚还原成对氨基苯酚。
该工艺的缺点是工艺路线长导致生产成本高,所制备的产品质量低劣,且需要存放大量的铁渣废料造成环境污染。
(2)对硝基苯酚催化加氢。
在催化剂的作用下,对硝基苯酚与氢气反应生成对氨基苯酚。


对硝基苯酚原料-概述说明以及解释1.引言1.1 概述概述硝基苯酚是一种重要的化学原料,具有广泛的应用领域。
它是一种含有硝基基团的苯酚衍生物,其化学结构中的硝基基团赋予了它许多独特的化学特性。
硝基苯酚可以通过多种方法合成,其制备方法的不断发展为其在工业生产中的应用提供了可靠的技术支持。
在本文中,我们将对硝基苯酚原料进行综合介绍。
首先,我们将描述硝基苯酚的定义和特性,包括其化学结构、物理性质、化学性质等方面。
其次,我们将探讨硝基苯酚的制备方法,包括传统的化学合成方法以及新兴的生物转化方法。
我们将对每种制备方法的原理、技术要点和应用领域进行详细的分析和讨论。
硝基苯酚作为一种重要的化学原料,具有广泛的应用领域。
它广泛用于染料、医药、农药、橡胶、塑料、涂料等工业领域。
在染料工业中,硝基苯酚常用作有机合成染料的中间体,通过对硝基苯酚的进一步反应可以合成多种颜色的染料。
在医药领域,硝基苯酚是一种有效的抗菌剂,可用于药物的制备和防腐剂的添加。
在农药领域,硝基苯酚作为杀菌剂和杀虫剂,对农作物的保护起着重要的作用。
此外,硝基苯酚还可以用于合成各种塑料和橡胶,以及制备具有特殊功能的涂料。
尽管硝基苯酚原料在许多领域有着重要的应用,但其制备方法仍面临一些挑战。
传统的化学合成方法往往需要高温高压条件下进行,反应条件较为苛刻,产率不高。
因此,寻求更加环保、高效的制备方法是目前的研究重点之一。
生物转化方法作为一种新兴的制备方法,具有底氏菌法、真菌法、微生物法等多种途径,其具有反应条件温和、高选择性和环境友好等优点,对硝基苯酚的制备具有重要意义。
本文将对硝基苯酚原料的重要性进行总结,并展望其未来的发展方向。
我们认为,随着科学技术的不断进步,硝基苯酚的制备方法将更加多样化和高效化,同时在应用领域中将有更广阔的发展前景。
我们期待硝基苯酚原料在未来的研究和应用中能够发挥更大的作用,为推动化学工业的发展做出更大的贡献。
文章结构部分的内容可以包括以下方面:文章结构部分主要介绍了整篇文章的组织结构和各个部分的内容,它可以帮助读者更好地了解整篇文章的逻辑框架和思路。

对硝基苯酚(PNP)英文别名:p-Nitrophenol;Phenol,4-nitro-;4-Nitrophenol;4-Hydroxynitrobenzene分子式:C6H5NO3 分子量:139.11 结构式:物理化学性质:纯品为浅黄色结晶。
无味。
熔点114-116℃,沸点279℃,闪点169℃,相对密度1.479(20/4℃)。
常温下微溶于水(1.6%,25℃),不易随蒸汽挥发。
易溶于乙醇、氯仿及乙醚。
溶于酸液时,淡黄色逐渐退去,PH3-4之间,几乎无色。
溶于碱液时,颜色加深。
能升华。
最简易的制备法:将对硝基氯苯与氢氧化钾在氨中于75℃加热3h,反应后用盐酸酸化,即得对硝基酚。
储存注意事项:储存于阴凉、通风的库房;远离火种、热源;包装密封;应与氧化剂、还原剂、碱类、食用化学品分开存放,切忌混储。
采用防爆型照明、通风设施。
禁止使用易产生火花的机械设备和工具。
储区应备有合适的材料收容泄漏物。
健康危害:对硝基苯酚对皮肤有强烈刺激作用;能经皮肤和呼吸道吸收;动物实验可引起高铁血红蛋白血症,体温升高,肝、肾损害。
急性毒性:LD50:250 mg/kg(大鼠经口)。
危险特性:遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。
受热分解放出有毒的氧化氮烟气。
液相色谱的检测方法(HPLC:High performance liquid chromatographic):色谱柱:柱长25 cm,内径4.6 mm,不锈钢柱柱填料:反相C18柱(C18键合固定相,5~6μm)柱温:55℃流动相:甲醇:水=50:50流速:1.O mL/min检测器波长:318 nm例如:有关我课题的底物(IDAN)和产物(IDA)标样样品的液相色谱图如下:3.372min出得峰是底物IDAN;5.739min出得峰是产物IDA;打完样品后经操作可以找到一个有关峰面积的数据表格防护措施:呼吸系统防护:空气中浓度较低高时,佩带防毒面具。

对硝基苯酚的分子式硝基苯酚,化学式为C6H5NO3,是一种有机化合物。
它由苯环上的一个氢原子被硝基取代而得到。
硝基苯酚是一种重要的化工原料,在医药、染料和农药等领域有广泛的应用。
硝基苯酚是一种白色结晶固体,可溶于酒精、醚和苯等有机溶剂。
它具有较高的熔点和沸点,对光和热稳定性较差。
硝基苯酚可以通过苯酚与硝酸反应制备而得到。
在制备过程中,硝酸与苯酚发生酯化反应,生成硝基苯酚。
硝基苯酚是一种强酸性物质,可以与碱发生中和反应。
它可以被还原为苯酚,还可以被氧化为二硝基苯酚。
硝基苯酚具有一定的毒性,对皮肤和眼睛有刺激作用,吸入过多会对呼吸系统造成危害,因此在生产和使用过程中需要注意安全防护措施。
硝基苯酚在医药领域有广泛的应用。
它可以用于合成药物,如抗菌药物和抗肿瘤药物等。
硝基苯酚还可以用作防腐剂,常用于防腐木材和皮革制品。
此外,硝基苯酚还可以用于染料和颜料的制备,可以产生多种颜色的化合物。
硝基苯酚还有一些其他的应用。
它可以用于制备农药,如杀虫剂和除草剂等。
硝基苯酚也可以用于制备烟火药和火药原料。
此外,硝基苯酚还可以用于电子工业中的电子元件的制备。
除了硝基苯酚外,还存在一些类似结构的化合物,如二硝基苯酚和三硝基苯酚。
它们在结构上与硝基苯酚相似,但具有不同的物化性质和应用领域。
硝基苯酚是一种重要的化工原料,具有广泛的应用。
它在医药、染料、农药和电子等领域都有重要的作用。
在使用硝基苯酚时,需要注意安全防护,避免对人体和环境造成危害。
通过进一步的研究和开发,硝基苯酚的应用领域还有很大的发展潜力。


对硝基酚编辑目录1基本信息2物理性质3制备方法4用途5储存条件6应急处置7风险术语1基本信息中文名称:对硝基酚[1]对硝基苯酚英文名称:p-Nitrophenol中文别名:对硝基苯酚;4-硝基苯酚;;4-硝基-1-羟基苯;英文别名:p-Nitrophenol;Phenol,4-nitro-;4-Nitrophenol;4-Hydroxynitrobenzene分子式:C6H5NO3分子量:139.11CAS号:100-02-7EINECS 登录号:202-811-72物理性质纯品为浅黄色结晶。
无味。
熔点114-116℃,沸点279℃,闪点169℃,相对密度1.479(20/4℃)。
常温下微溶于水(1.6%,25℃),不易随蒸汽挥发。
易溶于乙醇、氯仿及乙醚。
溶于酸液时,淡黄色逐渐退去,PH3-4之间,几乎无色。
溶于碱液时,颜色加深。
能升华。
3制备方法由对硝基氯苯经水解、酸化而得。
将浓度为137-140g/L的氢氧化钠溶液2320-2370L 加入水解锅中,再加入600kg熔融的对硝基氯苯。
加热至152℃,锅内压力为0.4MPa,然后停止加热,水解反应放热使温度和压力自然上升至165℃、约0.6MPa。
保持3h后取样检查反应终点,反应结束后将水解物冷至120℃。
将600L水和50L浓硫酸加到结晶锅中,压入上述水解物,并冷却到50℃左右,加入浓硫酸使刚果红试纸呈紫色,继续冷至30℃,抽滤,离心甩水,得含量90%以上的对硝基酚约500kg,收率92%。
另一种制备法是将对硝基氯苯与氢氧化钾在氨中于75℃加热3h,反应后用盐酸酸化,即得对硝基酚。
4用途用作农药、医药、染料等精细化学品的中间体。
用于制造非那西丁、扑热息痛、农药1605、显影剂米妥尔、对硝基酚硫化草绿GN、硫化还原黑CL、硫化还原黑CLB、硫化还原蓝RNX、硫化红棕B3R。
也用作皮革防霉剂以及酸值指示剂。
用作染料中间体、医药及农药的原料用作酸碱指示剂和分析试剂,也用于有机合成用作染料、医药及农药的中间体,也用作酸碱指示剂用作皮革防腐剂。


2020年04月一种对硝基苯酚的制备方法宋龙锋陈伟兴俞佳愚和西彬(浙江闰土股份有限公司,浙江绍兴312369)摘要:对硝基苯酚是一种重要的化工和医药中间体,本文介绍了一种对硝基苯酚的合成方法,通过优化工艺,具有工艺简单、产品质量高、污染小等优点,具有良好的发展前景。
文章考察了反应物料配比、反应温度、反应时间、后处理方式等条件对产物产率和纯度的影响。
最终确定对硝基氯苯投料量200g ,氢氧化钠115g ,水670g ,157℃保温1h ,167℃保温3.5h 为较合适的工艺条件。
产物收率为93.34%,纯度为99.41%。
关键词:对硝基氯苯;对硝基苯酚;中间体1实验部分1.1主要试剂和设备仪器氢氧化钠(工业品),对硝基氯苯(99%,浙江闰土股份有限公司),盐酸(30%,工业品)。
气相色谱仪(GC-14C ,岛津公司);气质联动仪(7820A+5977B );恒速搅拌器(上海梅香仪器有限公司),电子节能控温仪(ZNHW-Ⅱ,上海予华仪器设备有限公司);循环水真空泵(SHZ-D Ⅲ,上海予华仪器设备有限公司),高压反应釜(大连润昌石化设备有限公司)。
1.2反应条件探索1.2.1反应方程式对硝基氯苯碱性水解成对硝基苯酚钠,再酸化得到成品对硝基苯酚。
1.2.2反应步骤在1L 高压釜中加入200g 对硝基氯苯,在670g 水中加入107gNaOH ,全部溶解后,投入1L 高压釜中,拧紧釜盖,检查无漏后升温至157℃后搅拌1h ,体系稳定后再升温至167℃反应3h ;后处理:反应物料转入2000ml 烧杯,升温至80℃,缓慢加入600g+50g 浓硫酸的稀酸溶液,加毕,搅拌0.5h ,降温至45℃左右,再缓慢降温至30℃以下结晶析料。
1.3最佳工艺确定通过单因素变量控制实验,逐步确定各物料比例、反应时间、反应温度、保温时间以及后处理方式,来确定最佳反应工艺。
1.3.1考察后处理方式1.3.1.1加入水量对反应的影响表1反应完毕,加入水量对反应的影响序号12345水/g 100300400500600纯度/%98.1098.2298.4598.2398.39收率/%94.6993.3992.2491.0189.70实验反应完毕,将反应物料转移至2000烧杯中,考察酸化时加入水量对于产品纯度收率的影响,从表中我们可以看出,随着水量的增加,纯度基本没什么影响,不过收率持续下降。

实验三十九邻硝基苯酚和对硝基苯酚的制备1. 掌握酚类物质硝化原理和方法;2. 掌握水蒸汽蒸馏的操作。
芳香族硝基化合物一般是由芳香族化合物直接硝化制得的。
根据被硝化物的活性,可以利用稀硝酸、浓硝酸和浓硫酸的混合酸来进行硝化。
C O NO 2 HNO 3 H 2 S O 4 H2O 50~55 + + 芳香族化合物的硝化反应和卤代反应一样,是一个亲电子取代反应,以苯的硝化为例,它是按下面的历程进行的:混合酸中浓硫酸的作用主要是有利于硝基正离子的生成,因而提高了反应速率。
硝化反应的速率和其他的芳香族亲电子取代反应一样,要受芳环上已有取代基团的影响,芳环上如已有了一个第二类取代基(间位定位基),硝化反应便难于进行,因此可以控制在一元硝化阶段。
如果要在苯环上引入第二个硝基,就需要更为强烈的反应条件。
例如用硝基苯制备间二硝基苯时,通常使用发烟硝酸和浓硫酸的混合酸作为硝化剂,反应温度也要高一些。
NO 2 NO 2 H 2 S O 4 C O NO 2 HNO 3 + 发烟()浓95 相反芳环上如已有一个第一类取代基(邻对位定位基),使硝化反应容易进行。
例如苯酚的硝化比苯容易得多,只需要用稀硝酸,在室温下就可顺利地进行。
苯酚硝化后得到的产物是一个邻硝基苯酚和对硝基苯酚的混合物。
由于邻硝基苯酚通过分子内的氢键能形成螯合环沸点较对位的为低,同时在沸水中的溶解度较对位的小得多,易随水蒸汽挥发,因此可借水蒸汽蒸馏来将这两个异构体分开。
HNO 3 + H 2 SO 4 2 NO 2 + + + + H 3 O + HSO 4 - 2 NO 2 + NO 2 H [ ] NO 2 + H + OH NO 2 2 0 OH + HNO 3 NO 2 OH + (稀)℃O N O H O 副反应:OH O O O O [O] (红色)+ 250mL 三颈瓶、滴液漏斗、直形冷凝管、蒸馏头、热水漏斗、减压抽滤装置、烧杯、锥形瓶等苯酚14.1g、浓硫酸21mL、硝酸钠23g、浓盐酸在250mL 三颈圆底烧瓶中加入60mL 水,慢慢加入21mL 浓硫酸(38g,0.34mol)及23g 硝酸钠(约0.27mol) [注1] ,将烧瓶置于冰水浴中冷却。
实验四邻、对硝基苯酚的制备课时数:6学时教学目标:通过本项目学习硝化反应,了解邻、对硝基苯酚的制备原理及方法,应用水蒸汽蒸馏操作方法分离提纯有机化合物。
教学内容:一、实验目的要求:1、了解邻、对硝基苯酚的制备原理及方法.2、复习水蒸汽蒸馏操作。
二、实验原理:邻硝基苯酚中-NO2与-OH易形成分子内氢键形成稳定六元环,故bp比对硝基苯酚低,水溶性小,挥发性大,能随水蒸汽挥发,故可用水蒸汽蒸馏分离。
三、实验装置:1、水蒸汽蒸馏装置2、简单回流装置3、热滤简易装置:(见重结晶实验教案)四、实验重点:1、学习硝化反应。
2、应用水蒸汽蒸馏操作方法分离提纯有机化合物。
(见肉桂酸制备的教案)五、实验注意点:1、苯酚对皮肤有较大腐蚀性,取用注意安全。
加水是为了降低其熔点。
2、控制反应温度:10-15℃,超过20℃会有较多副产物。
3、酚与酸不互溶,续不断摇动使充分接触,以均匀反应,避免局部过热。
4、残酸须倒净洗净,否则水汽蒸馏时,产物会氧化或硝化。
倾倒酸液前,放冷冻箱30min 以上使充分冷却,可看到焦油状液体呈针状晶体析出。
5、洗涤时,用冰水,少量多次,洗至接近中性。
6、水汽蒸馏前,冷凝管中若有邻硝基苯酚析出时,可调小或关闭冷却水,让热蒸汽通过,使其熔化。
7、重结晶邻硝基苯酚:加约10ml 40℃乙醇,溶解后再用温水调至恰好出现浑浊,再加少量乙醇至澄清。
8、反应瓶中残留物含有对硝基苯酚(可由重结晶析出),还有副产物2-4-二硝基苯酚,毒性大,能渗透皮肤吸收,应加稀碱液处理后再倒入废液缸。
8。
对硝基苯酚的总结硝基苯酚是一种有机化合物,化学式为C6H5NO3、它是一种潜在的有害物质,同时也具有一定的用途。
在本文中,我们将对硝基苯酚的性质、制备方法、用途以及安全性进行详细的探讨。
硝基苯酚的主要性质:硝基苯酚是一种无色或微黄色的固体,具有刺激性气味。
其熔点为44至46°C,沸点为276°C,密度为1.326 g/cm^3、硝基苯酚可以溶解于醇、乙醚和苯等有机溶剂中,不溶于水。
在空气中稳定,但会受热分解,产生有害气体。
硝基苯酚的制备方法:硝基苯酚可以通过硝基化反应制备而成。
常用的方法是将苯酚与硝酸反应,在适当的条件下加热,用硫酸催化,生成硝基苯酚。
该反应通常在低温下进行,以减少副反应的生成。
硝基苯酚也可以通过间位亲电取代反应制备得到。
硝基苯酚的用途:硝基苯酚在化工领域有广泛的应用。
首先,由于硝基苯酚具有杀菌和防腐的作用,因此被用作护肤品、洗发水、皮肤药膏等产品中的防腐剂。
其次,硝基苯酚被用作橡胶加工的催化剂,可以促进橡胶的固化反应,提高橡胶的耐磨性和耐老化性能。
此外,硝基苯酚还可以用作染料、颜料和染料中间体的合成原料。
硝基苯酚的安全性:硝基苯酚属于一种有害物质,具有一定的毒性。
其刺激性较强,可能对眼睛、皮肤和呼吸道造成刺激和损害。
长期暴露于硝基苯酚的环境中,还可能导致慢性毒性作用和致癌作用。
因此,在接触硝基苯酚时需要注意使用个人防护装备,避免直接接触和吸入。
同时,要注意储存硝基苯酚的安全性,避免与可燃物和氧化剂等物质接触,以防止事故的发生。
综上所述,硝基苯酚作为一种有机化合物,具有一定的用途和化学活性。
然而,由于其有害物质的特性,需要在使用和储存时注意安全性,并采取相应的防护措施。
只有做到全面了解硝基苯酚的性质和特点,才能更好地应用和管理硝基苯酚。
实验乙酸乙酯的制备反应式:操作步骤:在250ml 三颈瓶中,放入24ml95%的乙醇,在振摇下分批加入24ml 浓硫酸,混合均匀,并加入几粒沸石,旁边两口分别插入125ml 滴液漏斗及温度计,漏斗末端及温度计的水银球浸入液面以下,距瓶底约0.5~1cm 。
中间开口装一蒸馏弯管与直型冷凝管连接,冷凝管末端连接接液管,伸入150ml 锥形瓶中。
将24ml95%乙醇及24ml 冰醋酸(约25.2g ,0.42mol )的混合液,由125ml 滴液漏斗滴入蒸馏瓶内约15ml 。
然后,将三颈瓶在石棉网上用小火加热,使瓶内反应温度维持在110~120℃。
这时在蒸馏管口有液体蒸出来,再从滴液漏斗慢慢滴入其余的混合液。
控制滴入速度和馏出速度大致相等,并维持反应温度在110~120℃之间,滴加完毕,继续加热数分钟,直到温度至130℃时不再有液体馏出为止。
馏出液中含有乙酸乙酯及少量乙醇、乙醚、水和醋酸。
在此馏出液中慢慢加入饱和碳酸钠溶液(约20ml ),时加摇动,用pH 试纸检验,酯层呈中性。
将混合液移入分液漏斗,充分摇动(注意活塞放气)后,静置。
分去下层溶液,酯层用20ml 饱和食盐水洗涤后,再每次用20ml 饱和氯化钙溶液洗涤两次,酯层自漏斗上口倒入干燥的150ml 锥形瓶中,用无水硫酸镁(或无水硫酸钠)干燥。
将干燥的粗乙酸乙酯滤入干燥的50ml 蒸馏瓶中,进行水浴蒸馏,收集73~78℃的馏分,产量21~25g (产率57~68%)。
纯乙酸乙酯的沸点为77.06℃,折光率 1.3723。
实验阿斯匹林的制备【实验目的】1学习酚酰化成酯的原理及方法,了解有关药物制备的知识;2复习重结晶和测熔点的操作。
【原理】主反应CH 3COOH +CH 3CH 2OH 浓H SO 110~120℃CH 3COOC 2H 5+H 2On D 20OHCOOH O CCH 3O CH 3C O CCH 3O O 水杨酸乙酰水杨酸(阿斯匹林)++CH 3COOH浓H 副反应一:OHCOOH +COOH HO OH COO COOH +H 2O O COO COOH OH COO COOH CH 3C O CCH 3O O+CH 3C O +CH 3COOH 措施:控制温度在70℃左右。
实验令邻、对硝基苯酚的制备P.178
【实验目的】
1掌握水蒸气蒸馏的原理及操作;
2学习苯酚的硝化反应。
【实验原理】一主反应
沸点214 C 279C
熔点45 C 114C
1副反应
(1)氧化;(2)二硝化。
(措施:低温5-10C ) 2产物的物
质的量之比
苯酚:(邻+对)=1:1
3混合物分离
熔、沸点都相差很大(分子内氢键与分子间氢键)
二水蒸气蒸馏(第54页)
1必须满足的三个条件和适用的四种情况?
2基本原理:
1 )纯水体系
P
水增大》P总=1atm时,沸腾,100C
升温
2)水+A混合体系
NO2
P
总=P A + P水
P总P水、PA土匀增大升
P总=1atm时,沸腾,沸点<100 C 温
二水蒸气蒸馏装置
1蒸汽发生器:产生蒸汽,加沸石,安全管的作用及位置。
2导气管:保持通畅、下斜,水夹的作用。
3蒸馏过程:先蒸出苯,后蒸出邻硝基苯酚。
【注意事项】
1逐滴滴入浓硝酸,才能维持温度5-10C 。
2对位产物重结晶后的滤液,不要倒掉。
3水蒸气蒸馏时,可以在三颈烧瓶的底部另加热少许。
4必要时,可以不用石棉网,直接给蒸汽发生器加热。
5反应残液处理:加10毫升1% NaOH 溶液。
【实验结果】
馏出液:含水、A 。
【实验装置与步骤】 一反应装置
铁圈
铁架台 l ;inL 沐硝酸 温度计 L - gIU L <7
5 5m 外
“ * 5 t 4 0 1
础
三实验步骤
1产品的颜色、形状:
2产率
M
邻
邻:产率= X100%
M
理论
M
对
对:产率= X100%
M
理论
M
邻+ M对
总产率二X100%
M
理论
3实验得失分析:
【问题与讨论】第179页:1、2题
3简单的流程图,说明邻、对硝基苯酚二者从混合物到纯品的过程。