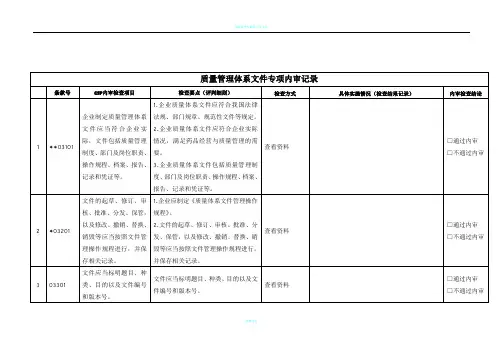
质量管理文件专项内审记录表
- 格式:doc
- 大小:49.00 KB
- 文档页数:5
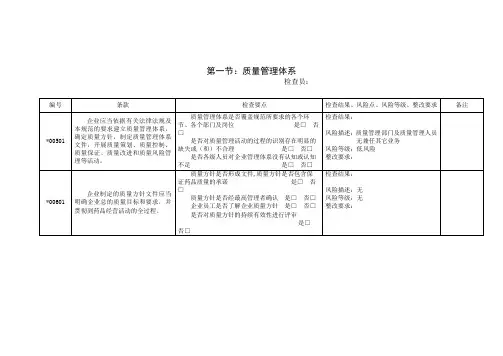

内部审核检查记录表模板内部审核检查记录表模板如下:
公司名称: _____________
审核日期: _____________
审核人员: _____________
审核范围: _____________
审核目的: _____________
审核依据: _____________
一、审核内容及结果:
1. 问题描述: _____________
审核结果: _____________
2. 问题描述: _____________
审核结果: _____________
3. 问题描述: _____________
审核结果: _____________
二、审核发现的非符合项:
1. 非符合项描述: _____________
对应的审核标准/要求: _____________
2. 非符合项描述: _____________
对应的审核标准/要求: _____________
3. 非符合项描述: _____________
对应的审核标准/要求: _____________
三、纠正和预防措施:
1. 针对非符合项的纠正和预防措施: _____________
2. 针对非符合项的纠正和预防措施: _____________
3. 针对非符合项的纠正和预防措施: _____________
四、审核结论:
审核结论: _____________
审核人员签名: _____________
日期: _____________。

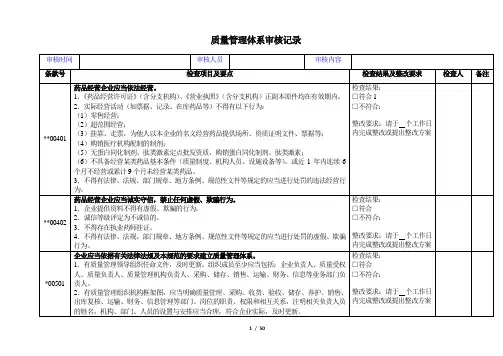

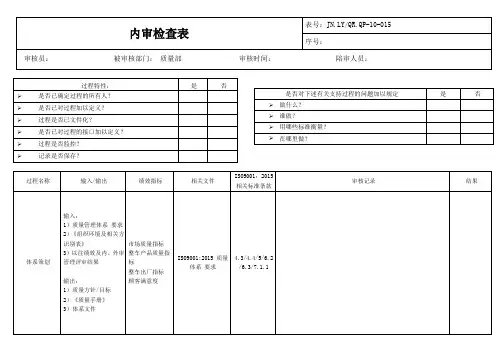

环境管理体系内部审核检查表及现场记录表目录1-5、公司领导6-13、行政办公室14-22、贯标办23-24材料设备处25-28、技术质量处29-36、生产计划处37-38、经营处39-49、项目部环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表R14—01 第页环境管理体系内部审核检查表及现场记录表。

质量体系文件变更专项内审*******有限公司内审目录**********药业有限公司***[201*]01号关于成立公司内审小组的决定公司各部、室:为了确保公司质量管理体系的正常进行,规范GSP实施情况,公司决定成立专项内审小组,小组成员有以下人员组成:组长: ***成员: ** ** ***特此通知*******药业有限公司201*年**月**日**********药业有限公司公司专项内审计划一审核目的:确保《药品经营质量管理规范》运行的适宜性、充分性、有效性,确保公司的质量体系能够持续有效的运行.公司质量部门根据目前业务繁忙的状况,经与各部门经理协商后,决定于201*年月日列出公司内部审核计划,交与总经理同意后,与201*年月日到201*年月日对公司质量体系运行情况进行内部审核。
二审核范围:1、组织机构与人员职责2、人员培训3、设施与设备4、经营活动的整个流程(采购、收货、验收、储存养护、运输、销售等环节)三审核依据:《药品管理法》、《中华人民共和国药品管理法实施办法》、新修订GSP,以及本公司的质量管理体系文件。
四审核组组成:组长***组员*** ** ***五审核方法:采取现场检查,看资料及现场提问的方式.六时间:定于201*年**月**日进行********药业有限公司201*年**月** 日******有限公司内审方案一、目的确保《药品经营质量管理规范》运行的适宜性、充分性、有效性,确保公司的质量体系能够持续有效的运行。
二、依据1、中华人民共和国药品管理法2、中华人民共和国药品管理法实施办法3、药品经营质量管理规范(2012年修订)4、本公司的质量管理体系文件三、检查时间201*年** 月 **日四、检查地点***质量部五、审核范围1、组织机构与人员职责2、人员培训3、设施与设备4、经营活动的整个流程(采购、收货、验收、储存养护、运输、销售等环节)六、安排与分工审核小组组长:***组员: *** ** ******:主要负责组织机构和人员职责**:主要负责人员培训***: 主要负责设施设备、储存、收货与验收等**: 主要负责采购销售等七、附件:内审记录公司内部审核报告根据最新版GSP(2012修订版)要求,公司于201*年月日成立内审小组对公司质量管理体系进行内部评审,内容包括公司的质量方针和目标、组织机构、设施设备、人员培训、硬件系统等,对工作质量、药品质量、服务质量、环境质量等环节,通过看现场、查资料、提问题等方式进行检查,同事对被审核部门存在的问题进行分析,找出问题的原因,对存在的问题提出纠正措施和有建设性的意见,并进行综合评价,以确定公司质量管理体系的有效性和可靠性。
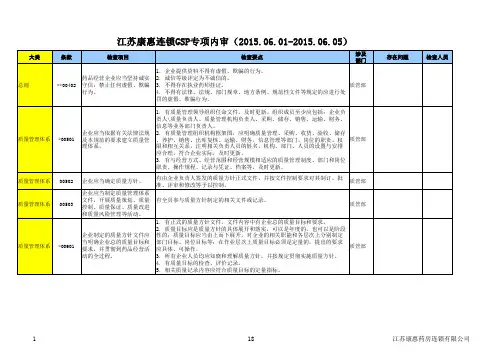
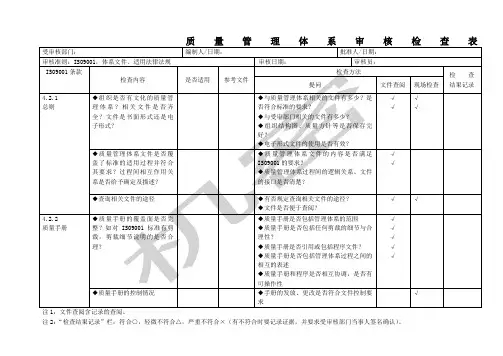
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
续表注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。
续表注1:文件查阅含记录的查阅。
注2:“检查结果记录”栏:符合○,轻微不符合△,严重不符合×(有不符合时要记录证据,并要求受审核部门当事人签名确认)。