3第三章 电解质溶液
- 格式:ppt
- 大小:709.00 KB
- 文档页数:31






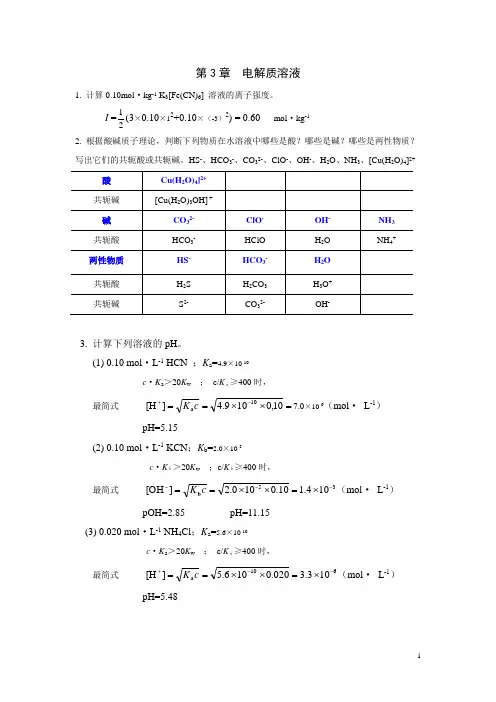
第3章 电解质溶液1. 计算0.10mol ·kg -1 K 3[Fe(CN)6] 溶液的离子强度。
I =21(3×0.10×12+0.10×(-3)2) = 0.60 mol ·kg -12. 根据酸碱质子理论,判断下列物质在水溶液中哪些是酸?哪些是碱?哪些是两性物质?写出它们的共轭酸或共轭碱。
HS -、HCO 3-、CO 32-、ClO -、OH -、H 2O 、NH 3、[Cu(H 2O)4]2+3. 计算下列溶液的pH 。
(1) 0.10 mol ·L -1 HCN ;K a =4.9×10-10c ·K a >20K w ; c/K a≥400时,最简式 =⨯⨯==H -+10,0109.4][10c K a 7.0×10-6(mol · L -1)pH=5.15(2) 0.10 mol ·L -1 KCN ;K b =2.0×10-5c ·K b>20K w ;c/K b≥400时, 最简式 35104.110.0100.2][---⨯=⨯⨯==OH c K b (mol · L -1)pOH=2.85 pH=11.15(3) 0.020 mol ·L -1 NH 4Cl ;K a =5.6×10-10c ·K a >20K w ; c/K a≥400时,最简式 610103.3020.0106.5][--+⨯=⨯⨯==H c K a (mol · L -1)pH=5.48(4) 500mL 含0.17g NH3溶液。
K b=1.8×10-5(mol·L-1)4[] 6.010--OH===⨯(mol·L-1)pOH=3.22 pH=10.784. 实验测得某氨水的pH为11.26,已知K b(NH3)=1.8×10-5,求氨水的浓度。

高二化学第三章水溶液中的离子平衡第一节一、强弱电解质1、电解质:在或状态下能够导电的叫做电解质。
2、电解质分类强电解质强酸强碱按照程度盐弱酸弱电解质弱碱水3、思考:1)、Cu、食盐水是电解质吗?为什么?2)、电解质一定能导电吗?3)、电解质溶液中各微粒的存在形式?强电解质溶液中:离子分子弱电解质溶液中:离子分子4)、强电解质的导电性一定强于弱电解质吗?电解质溶液的导电性强弱与什么因素有关?5)有下列物质:①CH3COONa ②Ba(OH)2 ③CaCO3 ④SO2 ⑤Cl2⑥H2O ⑦C2H5OH ⑧NH4Cl ⑨C6H5OH其中(填序号)属于强电解质的是_____________,属于弱电解质的是________________ 二、弱电解质的电离平衡影响电离平衡的外界因素①温度,促进电离。
②浓度,加水稀释电离。
按要求完成下列表格的内容:写出电离方程式,并判断外界条件对平衡移动的影响。
练习题:1、下列物质中,属于强电解质的是()A、CO2B、盐酸C、BaSO4D、NaOH溶液2.下列物质中,能够导电而且是电解质的是()A.熔融的氢氧化钠B.稀盐酸C.硝酸钾晶体 D. 融化的铁3、下列叙述中正确的是()A、氯化钠溶液能导电,所以氯化钠溶液是电解质;B、固体氯化钠不导电,所以氯化钠不是电解质;C、氯化氢溶液能导电,所以氯化氢是电解质;D、氯气(Cl2)溶于水能导电,所以氯气是电解质,3、电解质溶于水后电离出的阴、阳离子是能够导电的,而且溶液的导电能力与溶液中离子所带的电荷的浓度有关,下列溶液的导电能力最强的是( ) A、0.2 mol/L NaCl溶液B、0.15 mol/L MgCl2溶液C、0.2 mol/L BaCl2溶液D、0.25 mol/L HCl溶液4、在做溶液导电性的实验装置中盛一定量的CuSO4溶液,此时通电,灯泡发光,再不断的加入某种物质,会发现灯泡逐渐变暗,直至熄灭,持续加入该物质灯泡会再次逐渐变亮,据此分析加入的物质是( ) A、Zn粒B、BaCl2溶液C、KOH溶液D、Ba(OH)2溶液5.常温下,关于等体积、等浓度的盐酸和醋酸说法正确的是()A.溶液中的氢离子浓度相等B.溶液中微粒的种类一样多C.导电能力盐酸大于醋酸,中和等量的氢氧化钠时消耗的物质的量一样多D.分别加入完全相同的足量镁条,与盐酸反应的起始速率快,与醋酸反应最终产生的氢气多高二化学第三章水溶液中的离子平衡第二节一、水的电离平衡1、定义,纯水中,氢离子与氢氧根离子的乘积为K W = c(H+) . c(OH-)25℃时,K W = c(H+) . c(OH-) =实验测定,该温度下,稀溶液中都有这样的关系,即K W = c(H+) . c(OH-) =2、如果温度高于25℃时,水的电离程度,K W值。



第3课时电解质溶液中微粒间的关系一、溶液中的守恒关系1.电荷守恒电解质溶液中阳离子所带的电荷总数与阴离子所带的电荷总数相等。
即电荷守恒,溶液呈电中性。
(1)解题方法①分析溶液中所有的阴、阳离子。
②阴、阳离子浓度乘以自身所带的电荷数建立等式。
(2)举例如:Na2CO3溶液中①Na+、H+、CO2-3、HCO-3、OH-。
②1×c(Na+)+1×c(H+)=2×c(CO2-3)+1×c(HCO-3)+1×c(OH-)。
化简得:c(Na+)+c(H+)=2c(CO2-3)+c(HCO-3)+c(OH-)。
2.元素质量守恒在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生了变化,就该离子所含的某种元素来说,其质量在反应前后是守恒的,即元素质量守恒。
(1)解题方法①分析溶质中的特定元素的原子或原子团间的定量关系(特定元素除H、O元素外)。
②找出特征元素在水溶液中的所有存在形式。
(2)举例如:Na2CO3溶液中①n(Na+)n(CO2-3)=21,即n(Na+)=2c(CO2-3),CO2-3在水中部分会水解成HCO-3、H2CO3,共三种含碳元素的存在形式。
②c(Na+)=2[c(CO2-3)+c(HCO-3)+c(H2CO3)]。
3.质子守恒方法一:可以由电荷守恒与元素质量守恒推导出来。
如Na2CO3中将电荷守恒和元素质量守恒中的金属阳离子消去得c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3)。
方法二:质子守恒是依据水的电离平衡:H2O H++OH-,水电离产生的H+和OH-的物质的量总是相等的,无论在溶液中由水电离出的H+和OH-以什么形式存在。
如:Na2CO3溶液中即c(OH-)=2c(H2CO3)+c(HCO-3)+c(H3O+)或c(OH-)=2c(H2CO3)+c(HCO-3)+c(H+)。
二、溶液中离子浓度比较的四种类型1.不同溶液中同一离子浓度比较要考虑溶液中其他离子对该离子的影响,如:在相同浓度的下列溶液中①NH4Cl,②CH3COONH4,③NH4HSO4,④(NH4)2SO4,⑤(NH4)2CO3,c(NH+4)由大到小的顺序:④>⑤>③>①>②。
第3课时电解质溶液中微粒间的关系[核心素养发展目标] 1.会分析判断常见电解质(酸、碱、盐)溶液中的粒子种类。
2.分析判断常见单一溶液中的粒子浓度的大小比较。
3.掌握电解质溶液中粒子浓度间的三个守恒关系。
一、溶液中的守恒关系1.电荷守恒电解质溶液中阳离子所带的电荷总数与阴离子所带的电荷总数相等,即电荷守恒,溶液呈电中性。
(1)解题方法①分析溶液中所有的阴、阳离子。
②阴、阳离子浓度乘以自身所带的电荷数建立等式。
(2)举例如:Na2CO3溶液中①Na+、H+、CO2-3、HCO-3、OH-。
②1×c(Na+)+1×c(H+)=2×c(CO2-3)+1×c(HCO-3)+1×c(OH-)。
化简得c(Na+)+c(H+)=2c(CO2-3)+c(HCO-3)+c(OH-)。
2.元素质量守恒在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生了变化。
就该离子所含的某种元素来说,其质量在变化前后是守恒的,即元素质量守恒。
(1)解题方法①分析溶质中的特定元素的原子或原子团间的定量关系(特定元素除H、O元素外)。
②找出特定元素在水溶液中的所有存在形式。
(2)举例如:Na2CO3溶液中①n(Na+)n(CO2-3)=21,即n(Na+)=2n(CO2-3),CO2-3在水中部分会水解成HCO-3、H2CO3,共三种含碳元素的存在形式。
②c(Na+)=2[c(CO2-3)+c(HCO-3)+c(H2CO3)]。
3.质子守恒方法一:可以由电荷守恒与元素质量守恒推导出来。
如Na2CO3中将电荷守恒和元素质量守恒中的金属阳离子消去得c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3)。
方法二:质子守恒是依据水的电离平衡:H2O H++OH-,水电离产生的H+和OH-的物质的量总是相等的,无论在溶液中由水电离出的H+和OH-以什么形式存在。
如:Na2CO3溶液中即c(OH-)=2c(H2CO3)+c(HCO-3)+c(H3O+)或c(OH-)=2c(H2CO3)+c(HCO-3)+c(H+)。