萃取与蒸馏操作
- 格式:doc
- 大小:26.50 KB
- 文档页数:2

高中化学蒸馏和萃取的教案
实验名称:蒸馏和萃取
实验目的:通过蒸馏和萃取实验掌握这两种分离技术的原理和操作方法。
实验材料:
1. 水,甲醇,氯仿等实验用溶液
2. 蒸馏器,试管,冷凝器等实验仪器
实验步骤:
1. 蒸馏实验
(1)将实验溶液置于蒸馏瓶中。
(2)将蒸馏瓶与冷却水冷凝器连接好。
(3)加热蒸馏瓶中的溶液,控制火力,观察溶液的沸腾情况。
(4)收集蒸馏液,观察收集管中的液体。
2. 萃取实验
(1)将两种不相溶的溶液放入漏斗中。
(2)将萃取剂滴加入漏斗中的溶液中。
(3)轻轻地摇动漏斗,使两种溶液充分接触混合。
(4)将漏斗静置一段时间,待两种溶液分层后,打开下部阀门放出底层的溶液。
实验原理:
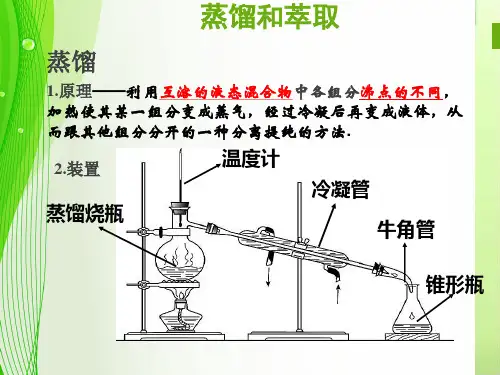
1. 蒸馏:利用液体的沸点不同,将液体混合物加热至液体沸腾,然后再以气体形式冷凝回液体的分离方法。
2. 萃取:利用萃取剂选择性溶解其中一种物质,达到物质的分离目的。
实验注意事项:
1. 实验操作时要小心谨慎,注意安全。
2. 蒸馏瓶与冷凝器连接处要严密,避免蒸气外泄。
3. 萃取剂的选择要根据实际情况确定,注意可溶性和选择性。
实验总结:
通过本次蒸馏和萃取实验,我们掌握了这两种分离技术的原理和操作方法,同时也了解了不同条件下的溶液分离效果的差异。
在今后的实验中,我们将进一步运用这两种技术,提高我们的实验技能和分析能力。

高中化学蒸馏和萃取教案课题:高中化学实验——蒸馏和萃取教学目标:1. 了解蒸馏和萃取的原理及应用;2. 掌握蒸馏和萃取的操作步骤;3. 培养学生的实验操作能力和观察分析能力。
教学重点:1. 蒸馏和萃取的原理和应用;2. 蒸馏和萃取的操作步骤;3. 实验室安全操作规范。
教学难点:1. 蒸馏和萃取的实验操作技巧;2. 掌握蒸馏和萃取的适用范围。
教学准备:1. 实验室用具:蒸馏器、冷凝管、烧杯、玻璃棒等;2. 实验材料:水、酒精、食盐等。
教学过程:一、导入(5分钟)教师简要介绍蒸馏和萃取的概念及应用,并引入实验内容。
二、实验操作(30分钟)1. 蒸馏操作步骤:(1)准备实验仪器;(2)在烧杯中放入水和酒精混合物,用火加热;(3)观察瓶口处是否有气泡产生,收集冷凝后的水和酒精分离液。
2. 萃取操作步骤:(1)准备实验仪器;(2)在烧杯中放入水和食盐混合物,搅拌均匀;(3)加入有机溶剂,振荡混合;(4)观察并分层,分离出上层有机相。
三、实验总结(10分钟)学生根据观察结果和实验操作经验,总结蒸馏和萃取的应用场景及操作技巧,并与同学分享。
四、实验讨论(10分钟)学生与教师共同讨论实验中遇到的问题和现象,并探讨蒸馏和萃取在生活中的实际应用。
五、课堂作业(5分钟)布置相关练习题,巩固学生对蒸馏和萃取的理解。
教学反思:通过本次实验,学生不仅掌握了蒸馏和萃取的基本原理和操作步骤,还培养了实验操作能力和观察分析能力。
在今后的学习中,学生可以更好地理解化学实验的重要性和实际应用价值。


高中化学蒸馏与萃取实验操作口诀
蒸馏操作实验
隔网加热冷管倾,上缘下缘两相平。
需加碎瓷防暴沸,热气冷水逆向行。
解释:
1. 隔网加热冷管倾:" 冷管" 这冷凝管。
意思是说加热蒸馏烧瓶时要隔石棉网(防止蒸馏烧瓶因受热不均匀而破裂),在安装冷凝管时要向下倾斜。
2. 上缘下缘两相平:意思是说温度计的水银球的上缘要恰好与蒸馏瓶支管接口的下缘在同一水平线上。
萃取操作实验
萃剂原液互不溶,质溶程度不相同。
充分振荡再静置,下放上倒切分明。
解释:
1. 萃剂原液互不溶,质溶程度不相同:“萃剂”指萃取剂;“质”指溶质。
这两句的意思是说在萃取操作实验中,选萃取剂的原则是:萃取剂和溶液中的溶剂要互不相溶,溶质在萃取剂和原溶剂中的溶解度要不相同(在萃取剂中的溶解度要大于在原溶液中的溶解度)。
2. 充分振荡再静置:意思是说在萃取过程中要充分震荡,使萃取充分,然后静置使溶液分层。
3. 下放上倒切分明:这句的意思是说分液漏斗的下层液从漏斗脚放出,而上层液要从漏斗口倒出。
热气冷水逆向行:意思是说冷却水要由下向上不断流动,与热的蒸气的流动的方向相反。

“蒸馏、结晶、萃取”的操作注意事项江苏省如皋市江安中学 胡海鹏 226534“蒸馏、结晶、萃取”是利用有机物与杂质物理性质的差异将他们分离和提纯的基本方法,为了同学们更好地掌握它们,本人将这些实验操作中的注意点列出如下:1.蒸馏蒸馏是指把液体加热至沸腾,使液体变为蒸气,然后蒸气又重新冷凝成液体的过程。
这一过程可以把液体中所夹带的杂质除去而提纯液体。
蒸馏亦可看成是根据物质沸点不同,提纯物质的一种方法。
根据物质性质的不同,蒸馏的方法可分为常压蒸馏、减压蒸馏和分馏几种。
在蒸馏时应注意以下几点:① 蒸馏烧瓶所盛液体,不得超过烧瓶容积的32,不得少于烧瓶容积的31。
② 蒸馏时不得将液体全部蒸干。
③ 测量蒸馏物沸点的温度计,其感温部位(如图:水银温度计的水银球)应位于支管口口部。
④ 冷凝管中水流方向下口进、上口出(如图),水流速度不必太快,只要能使蒸气在通过冷凝管后全部转化成液体即可。
⑤ 为防止蒸馏烧瓶中的液体暴沸,需向其中加入几粒沸石或碎瓷片。
⑥ 如溜出物的沸点小于100℃,一般可用水浴加热。
⑦ 如果一次蒸馏要得到两种以上的液体,就叫分馏。
分馏的产品成分由温度计所示的不同温度来控制。
当盛接一种液体时,发现温度有明显的变化(无论热源给热多少,只要蒸馏出是同一种物质,温度计就不会有明显变化),说明第二种分馏物开始排出,于是盛接馏分的容器就要更换。
2.结晶:结晶是使固体物质从溶液中以晶体状态析出的过程,是提纯、分离固体物质的重要方法之一。
结晶的方法一般有2种:一种是蒸发溶剂法,它适用于温度对溶解度影响不大的物质。
沿海地区“晒盐”就是利用的这种方法。
另一种是冷却热饱和溶液法。
此法适用于温度升高,溶解度也增加的物质。
如北方地区的盐湖,夏天温度高,湖面上无晶体出现;每到冬季,气温降低,纯碱(Na 2CO 3·10H 2O)、芒硝(Na 2SO 4·10H 2O)等物质就从盐湖里析出来。
结晶的注意点:① 在蒸发过程中要不断搅拌,以免液滴飞溅。

蒸馏与萃取知识点总结一、蒸馏的基本原理蒸馏是一种通过液体和气体之间的相互转化实现分离的方法。
其基本原理是根据混合物中不同成分的沸点差异,利用加热使液体汽化,然后再通过冷却使其重新凝结成液体,从而实现对混合物的分离。
在蒸馏过程中,当混合物加热至其最低沸点成分的沸点时,该成分开始汽化,然后与其他成分一起进入蒸馏器。
接着,混合物的汽化蒸气通过冷却管道,使得其中的低沸点成分冷凝成液体,而高沸点成分则继续沿着管道流动。
最终,低沸点成分和高沸点成分被分离开来。
二、蒸馏的技术步骤1、设备准备:蒸馏设备通常包括蒸馏瓶、冷凝管、加热装置等,首先需要对蒸馏设备进行清洁和检查,以确保设备的正常运行。
2、混合物投料:将待分离的混合物投入蒸馏瓶中,并加入合适的溶剂或添加剂,以提高混合物的汽化性能。
3、加热:通过加热装置使混合物开始汽化,此过程中需要控制加热温度和时间,避免混合物过热或沸腾。
4、冷却:将蒸馏瓶中的汽化蒸气引入冷凝管中,通过冷却使其冷凝成液体,然后收集冷凝液。
5、收集产品:根据不同成分的沸点差异,分别收集冷凝液中的不同成分,从而实现对混合物的分离。
三、蒸馏的应用领域1、化工领域:蒸馏广泛应用于石油、化工、塑料等工业中,用于分离和提纯化学品和燃料。
2、制药领域:在制药生产中,蒸馏用于分离提纯药物、药物中间体和原料药。
3、实验室应用:在实验室中,蒸馏常用于分离提纯实验试剂和有机合成产物。
四、蒸馏的操作技巧1、控制加热温度:加热温度过高会导致混合物过热和沸腾,影响蒸馏效果;加热温度过低会使混合物汽化不完全,影响分离效果。
2、选择合适的冷却系统:选择合适的冷却系统可以提高蒸馏效率,减少能耗,确保冷凝液的质量。
3、操作注意安全:蒸馏过程中需要注意火源的安全,避免发生火灾和烫伤等意外伤害。
五、萃取的基本原理萃取是一种利用两种互不溶的溶剂来分离物质的方法,其基本原理是根据不同物质在不同溶剂中的溶解度差异,利用这种差异来实现物质的分离。

蒸发蒸馏萃取的操作方法蒸发蒸馏和萃取是常用的分离和纯化技术,在化学实验和工业生产中都得到了广泛应用。
下面我将详细介绍蒸发蒸馏和萃取的操作方法。
一、蒸发蒸馏操作方法:1. 样品制备:首先,需要准备待分离的混合物样品。
根据实验要求,可以选择固体-固体、固液或液体-液体混合物进行分离。
2. 蒸发装置准备:将蒸发瓶或烧瓶放在蒸发装置内,将冷凝管连接在瓶口上方,通过橡胶塞使两者紧密连接。
3. 设置加热设备:将蒸发瓶或烧瓶放在加热器上,根据需要设置和调整加热温度。
4. 开始蒸发:将待分离混合物溶液倒入蒸发瓶或烧瓶中,轻轻加热,使混合物开始蒸发。
在这个过程中,挥发性成分会蒸发,而非挥发性成分则会残留在容器中。
5. 冷凝收集:蒸发的挥发性成分会通过冷凝管冷凝成液体,并滴入冷凝瓶中。
这样,我们就可以将分离出来的纯化溶液进行收集。
6. 冷凝水槽:为了增加蒸发的效果,可以在冷凝管附近设置一个水槽,用冷水冷却冷凝管,提高冷凝效果。
二、萃取操作方法:1. 提取溶剂:首先,准备一种合适的溶剂,能够与待提取物质有较好的溶解性,且与其他杂质不溶,并且容易挥发或蒸馏。
常用的溶剂有醚类、酯类、醇类等。
2. 样品制备:将待提取的混合物溶液倒入一个漏斗或分液漏斗中,加入一定量的提取溶剂。
3. 摇匀:轻轻摇动漏斗,使混合物中的成分充分接触和混合。
摇匀的时间一般为1-2分钟。
4. 混合物分离:停止摇匀后,将漏斗放置在一个支架上,使其静置一段时间,等待混合物中的液相和固相发生分离。
5. 分离两相:打开漏斗的开关,将分液漏斗中的底层液相慢慢放出。
需要注意的是,在放液的过程中,要停下来,观察提取溶剂是否已经滴干,并视情况控制分离速度。
6. 溶剂回收:将分离得到的上层液相转移到一只锥形瓶中,使用适当的方法回收提取溶剂。
回收的溶剂可以进行进一步使用。
以上就是蒸发蒸馏和萃取的操作方法。
蒸发蒸馏通过加热和冷凝的方法,实现了挥发性成分和非挥发性成分的分离。


乙醇和水的分离操作方法乙醇和水是常见的溶液系统,在一些工业和实验室应用中需要将乙醇和水进行分离操作。
下面将介绍常用的两种分离乙醇和水的操作方法:蒸馏法和萃取法。
一、蒸馏法蒸馏是一种通过不同液体的沸点差异来进行分离的方法。
乙醇和水的沸点差异为乙醇沸点78.5℃,水沸点100℃。
因此,蒸馏法是一种有效的分离乙醇和水的方法。
1.原理通过升温加热溶液,使乙醇和水分别蒸发,然后通过冷凝回收乙醇和水分离。
2.实验步骤(1)准备溶液:将乙醇和水按一定比例混合得到溶液。
(2)装置蒸馏设备:将溶液倒入蒸馏烧瓶中,用橡皮塞和减压虹吸装置密封好。
(3)开始蒸馏:打开水泵开关,加热蒸馏烧瓶,使其升温。
水蒸气进入蒸馏烧瓶后与乙醇混合蒸发,然后被冷凝管冷凝成水滴。
(4)回收分离:乙醇蒸汽通过冷凝管后流入收集瓶,水滴被接收瓶收集。
3.注意事项(1)温度控制:蒸馏过程中要控制加热温度,使溶液保持在乙醇的沸点附近,防止乙醇过度蒸发,影响分离效果。
(2)蒸馏速率:蒸馏速度应适中,过快或过慢都会影响分离效果。
(3)安全措施:操作过程中要注意安全,避免乙醇和水的挥发产生危险气体导致火灾。
二、萃取法萃取法是利用两个不同溶剂对分子之间亲疏水性差异的利用,通过将目标物质从一个溶剂萃取到另一个溶剂中进行分离。
1.原理乙醇是有机溶剂,亲油性较强,而水是亲水性较强的溶剂。
通过调整萃取溶剂的选择和条件,可以使乙醇在不同溶剂中的溶解度差异较大,从而实现分离。
2.实验步骤(1)准备溶液:将乙醇和水按一定比例混合得到溶液。
(2)选择萃取溶剂:选择一个对乙醇具有高溶解度但对水具有低溶解度的有机溶剂作为萃取溶剂。
(3)萃取操作:将溶液和萃取溶剂加入分液漏斗中,摇匀使两相充分接触,待分层后分离两相。
(4)反复萃取:将分离的乙醇相和水相分别保存,再次加入新鲜萃取溶剂进行反复萃取,增大分离效果。
(5)分离回收:分离出的乙醇相和水相通过蒸发或其他方法进行溶剂回收。
3.注意事项(1)溶剂选择:选择合适的有机溶剂进行萃取,溶剂的挥发性、毒性和环境影响要考虑到。

蒸馏萃取的操作方法有几种
蒸馏萃取是一种常用的分离纯化技术,操作方法主要有以下几种:
1. 简单蒸馏:将混合物加热,并收集温度达到混合物中某一组分的沸点时蒸发出的气体,再通过冷凝使其变回液态,从而将该组分分离出来。
适用于组分沸点差异较大的情况。
2. 精馏:在简单蒸馏的基础上,通过在蒸发器和冷凝器之间加装填物(如隔板、真空环形塔等),增加有效接触面积,提高馏出液的纯度。
适用于组分沸点差异较小的情况。
3. 水蒸气蒸馏:将混合物加热,并通入热蒸汽,使其在液体表面汽化,再通过冷凝收集冷凝液。
适用于高沸点、热敏性或极易挥发的物质。
4. 气相萃取:通过将混合物暴露于悬浮或稳定的气体流中,使易挥发组分转移到气相中,而其他组分仍停留在固相或液相中,从而实现分离纯化。
适用于易挥发物质的分离。
5. 溶剂萃取:将混合物与适当的溶剂接触,使目标物质溶于溶剂中,而其他组分没有溶解度或溶解度较低,再通过分离溶液和溶剂的方法,将目标物质从混合物中分离出来。
适用于沸点相近且溶剂选择合适的情况。
以上是一些常见的蒸馏萃取操作方法,根据实际情况和需要,还可以结合其他分离技术进行操作。
同时蒸馏萃取使用说明方法蒸馏萃取是一种常用的化学分离技术,通过利用物质的不同沸点将混合物中的成分分离出来。
与传统的蒸馏方式不同,同时蒸馏萃取是将蒸馏和萃取两种操作同时进行,使得萃取效率更高、操作更简便。
本文将介绍同时蒸馏萃取的使用方法及注意事项。
一、准备工作在进行同时蒸馏萃取之前,首先需要准备好实验器材和试剂。
具体的准备工作包括:1. 实验器材:蒸馏容器、加热设备、冷凝器、收集容器等。
2. 试剂:混合物样品、萃取剂等。
二、操作步骤1. 将混合物样品倒入蒸馏容器中,并加入适量的萃取剂。
2. 将蒸馏容器与冷凝器连接好,并确保密封性良好。
3. 开启加热设备,逐渐升温,使混合物样品沸腾。
4. 同时,通过冷凝器的冷却作用,使混合物蒸气在冷凝器中凝结。
5. 蒸馏过程中,收集冷凝器中凝结的液体,即为所需的蒸馏产物。
三、注意事项1. 安全操作:同时蒸馏萃取需要使用加热设备,要注意火源的安全,避免发生火灾事故。
2. 选择合适的萃取剂:根据混合物的成分和性质选择合适的萃取剂,以提高蒸馏的效率。
3. 控制加热温度:适当控制加热温度,以避免过高温度造成混合物烧焦或有害气体释放。
四、常见问题解答1. 同时蒸馏萃取与传统的蒸馏方式有何区别?同时蒸馏萃取是将蒸馏和萃取两种操作同时进行,使得萃取效率更高、操作更简便。
传统的蒸馏方式需要分开进行这两个过程。
2. 为什么要使用萃取剂?萃取剂能够提高目标物质的浓度,降低其他杂质的含量,以便更好地提取目标物质。
3. 如何选择合适的萃取剂?选择合适的萃取剂需要考虑混合物的成分和性质,以及目标物质的溶解性和选择性。
总结:同时蒸馏萃取是一种高效、简便的化学分离技术,能够快速地将混合物中的成分分离出来。
在使用同时蒸馏萃取时,我们需要进行一些准备工作,并按照操作步骤进行实验。
同时,安全操作和合理选择萃取剂也是非常重要的。
相信通过本文的介绍,读者对同时蒸馏萃取的使用方法已有了一定的了解。
同时蒸馏萃取原理
同时蒸馏萃取是一种常用的分离提取技术,利用物质在不同温度下的挥发性差异,通过同时进行蒸馏和萃取来分离混合物的组分。
其原理如下:首先,将待提取的混合物置于蒸馏瓶中,并添加适量的溶剂或水。
然后,通过加热使溶剂沸腾,并使气相通过冷凝管,冷凝管中的冷却器使气相冷却为液相,此过程称为蒸馏。
随着蒸馏的进行,混合物中具有较高挥发性的成分会首先蒸发出来,通过冷凝器被收集起来。
与此同时,通过分液漏斗将蒸馏瓶中残留的液相与萃取溶剂进行反复的摇匀混合,使混合物中具有亲喜水性的成分溶解在溶剂中,此过程称为萃取。
经过多次的蒸馏和萃取后,原混合物中具有挥发性较低或亲喜水性较弱的成分将逐渐被分离出来,而挥发性较高或亲喜水性较强的成分则会富集于溶剂中。
最后,可以通过对得到的溶剂进行蒸发或其他方法进行浓缩,得到目标成分的提取物。
同时蒸馏萃取技术广泛应用于化学实验、制药工业、食品工业等领域中,用于提取纯化有机物、提取药物、提取香精香料等。
同时蒸馏萃取使用说明方法一、实验准备1.蒸馏装置:同时蒸馏装置由加热装置、冷凝管、收集容器和温度控制装置等组成。
确保蒸馏装置的密封性和安全性,检查冷凝管和收集容器是否完整无损。
2.混合物制备:将待提取的混合物准备好,并记录其成分和浓度。
确保混合物的pH值和溶液浓度在合适范围内。
二、仪器设备1.加热装置:使用电热器、加热炉或其他加热设备,确保温度控制准确可靠。
2.冷凝管:选择合适大小和材质的冷凝管,确保冷凝效果好。
3.收集容器:选择透明的容器,用于收集提取物。
4.温度控制装置:使用温度控制器或温度计,确保实验过程中的温度控制准确。
三、操作步骤1.将混合物倒入蒸馏瓶中,装上冷凝管和收集容器。
2.打开加热装置,加热蒸馏瓶中的混合物。
控制加热功率和加热时间,使混合物中的挥发性物质蒸发。
3.当挥发性物质蒸发到达一定程度时,将冷凝管的冷却水开启。
冷凝管中的冷却水使蒸发的挥发性物质冷凝成液体,从而分离出来。
4.收集冷凝液体的提取物。
根据需要,可以将提取物保存在收集容器中,或者进一步进行后续的分析和处理。
四、注意事项1.安全操作:在进行同时蒸馏萃取时,要注意安全操作。
确保实验环境通风良好,避免挥发性物质对人体造成伤害。
2.温度控制:控制蒸馏过程中的温度,避免过高的温度对挥发性物质的破坏。
3.冷却:确保冷凝管中的冷却水充足,以保持良好的冷凝效果。
同时,也要注意冷凝管的安全操作,避免冷却液泄漏或受损。
4.清洁:实验结束后,要及时清洗蒸馏装置和收集容器,以防沉积物的积累影响下次实验的结果。
总之,同时蒸馏萃取是一种简单有效的化学分离技术,广泛应用于提取和分离挥发性物质。
在进行同时蒸馏萃取实验时,需要注意实验准备、仪器设备、操作步骤和注意事项。
只有在正确操作的前提下,才能获得准确可靠的实验结果。
蒸馏和萃取的区别化学知识点
蒸馏和萃取的区别化学知识点
一、蒸馏操作考前须知
〔1〕在蒸馏烧瓶中放少量碎瓷片,防止液体暴沸。
〔2〕温度计水银球的位置应与支管口下端位于同一程度线上。
〔3〕蒸馏烧瓶中所盛放液体不能超过其容积的2/3,也不能少于1/3。
〔4〕冷凝管中冷却水从下口进,上口出。
〔5〕加热温度不能超过混合物中沸点最高物质的沸点。
二、蒸馏和萃取的区别
1、定义不同
〔1〕蒸馏是利用物质的沸点不同,通过加热沸腾的方法,对混合物进展别离。
〔2〕萃取是利用A物质在B溶剂和C溶剂中的溶解才能不同,把A物质从B物质提取到C溶剂里。
2、优点和用途不同
〔1〕蒸馏是一种热力学的别离工艺,优点在于不需使用系统组分以外的其它溶剂,从而保证不会引入新的杂质。
〔2〕萃取,又称溶剂萃取或液液萃取,广泛应用于化学、冶金、食品等工业,通用于石油炼制工业。
3、别离原理不同
〔1〕蒸馏是利用混合物中不同组分的沸点不同进展别离。
〔2〕萃取是利用不同组分在不同溶剂中溶解不同进展别离。
4、发生的条件不同
〔1〕蒸馏条件:蒸馏装置的安装、加热装置的选择、温度的选择、溶剂的选择。
〔2〕萃取条件:萃取剂不与溶质发生反响;萃取剂不与原来的溶剂混溶或者反响;溶质在萃取剂中的溶解度远大于原来溶剂。