原子吸收光谱法的应用【仪器分析】
- 格式:ppt
- 大小:477.00 KB
- 文档页数:34



原子吸收光谱仪的原理、构成、操作及应用领域详解一、原子吸收光谱仪原理原子吸收光谱仪的原理是根据物质基态原子蒸汽对特征辐射吸收的作用来进行金属元素分析。
1、原子吸收光谱的产生任何元素的原子都是由原子核和核外电子组成。
原子核是原子的中心体,核正电,电子荷负电,总的负电荷与原子核的正电荷数相等。
电子沿核外的圆形或椭圆形轨道围绕着原子核运动,同时又有自旋运动。
电子的运动状态由波函数0描述。
求解描述电子运动状态的薛定愕方程,可以得到表征原子内电子运动状态的量子数n、L、m,分别称为主量子数、角量子数和磁量子数。
原子核外的电子按其能量的高低分层分布而形成不同的能级,因此一个原子核可以具有多种能级状态。
能量最低的能级状态称为基态能级(Eo),其余能级称为激发态能级,而能量最低的激发态则称为第一激发态。
一般情况下,原子处于基态,核外电子在各自能量最低的轨道上运动。
如果将一定外界能量如光能提供给该基态原子,当外界光能量恰好等于该基态原子中基态和某一较高能级之间的能级差△E时,该原子将吸收这一特征波长的光,外层电子由基态跃迁到相应的激发态而产生原子吸收光谱。
2、原子吸收光谱仪基本原理仪器从光源辐射出具有待测元素特征谱线的光,通过试样蒸气时被蒸气中待测元素基态原子所吸收,由辐射特征谱线光被减弱的程度来测定试样中待测元素的含量。
3、原子吸收光谱仪方法原理原子吸收是指呈气态的原子对由同类原子辐射出的特征谱线所具有的吸收现象。
当辐射投射到原子蒸气上时,如果辐射波长相应的能量等于原原子吸收光谱仪子由基态跃迁到激发态所需要的能量时,则会引起原子对辐射的吸收,产生吸收光谱。
基态原子吸收了能量,最外层的电子产生跃迁,从低能态跃迁到激发态。
原子吸收光谱根据郎伯-比尔定律来确定样品中化合物的含量。
已知所需样品元素的吸收光谱和摩尔吸光度,以及每种元素都将优先吸收特定波长的光,因为每种元素需要消耗一定的能量使其从基态变成激发态。
检测过程中,基态原子吸收特征辐射,通过测定基态原子对特征辐射的吸收程度,从而测量待测元素含量。

原子吸收光谱法如何测定金属原子吸收光谱法(Atomic Absorption Spectroscopy,简称AAS)是一种常用于测定金属及其离子的分析方法。
它利用金属原子对特定波长的光吸收的特性来确定样品中金属的浓度。
本文将介绍AAS的基本原理、仪器设备以及实验操作步骤。
一、基本原理AAS的基本原理是利用金属原子在吸收特定波长的光时产生特征的光吸收现象。
当吸收光线经过样品中的金属原子时,根据杰贝特-朗伯定律,被吸收的光强与样品中金属原子的浓度成正比关系。
通过测定吸收光的强度可以确定样品中金属原子的浓度。
二、仪器设备进行原子吸收光谱测定金属需要以下仪器设备:1.原子吸收光谱仪:包括光源、进样器、光栅、光电倍增管等部件。
2.电子天平:用于准确称量样品。
3.雾化器:将液态样品转化为气溶胶状态供光谱仪测定。
4.标准溶液:用于校准仪器和制备样品的不同浓度标准溶液。
三、实验操作步骤进行原子吸收光谱测定金属的实验主要包括以下步骤:1.样品处理:将待测金属样品溶解在适当溶剂中,并过滤除去悬浮物和杂质。
2.准备标准曲线:准备一系列浓度递增的标准溶液,并利用原子吸收光谱仪分别测定它们的吸光度。
3.扣除背景:测定雾化剂或溶剂的吸光度作为背景信号,并将样品的吸光度减去背景信号。
4.测定样品吸光度:利用原子吸收光谱仪测定样品的吸光度,并记录下来。
5.绘制标准曲线:将浓度与吸光度绘制成图表,得到标准曲线。
6.测定样品浓度:根据样品的吸光度和标准曲线,确定样品中金属的浓度。
四、注意事项在进行原子吸收光谱测定金属时,需要注意以下事项:1.样品的处理过程应确保完全溶解和去除杂质,以避免对吸光度测定的影响。
2.标准溶液的浓度应尽可能覆盖待测样品中金属的浓度范围,以获得准确的测定结果。
3.背景信号的扣除要准确可靠,以保证测定结果的准确性。
4.在测定过程中,要及时记录样品和标准溶液的吸光度值,并注意仪器的校准和维护。
五、应用领域原子吸收光谱法广泛应用于环境监测、食品安全、医药生化和金属材料等领域。

原子吸收光谱法在食品检验中的应用随着人们生活质量的不断提高,越来越重视食品安全,尤其是食品中重金属的含量检测已成为人们关注的焦点。
原子吸收光谱法是检测食品中重金属较有效的方法。
标签:原子吸收光谱法;食品检验;应用前言现代的食品中都会或多或少存在一些重金属元素,如果食品重金属元素过多,则会对人体的健康造成损害。
因此,对于食品进行重金属检测具有重要的意义。
运用原子吸收光谱法可以对食品中多项重金属元素进行测定,具有分析干扰少、准确度高、灵敏度高等良好的检测效果。
1 原子吸收光谱法概述现阶段,检测部门已经将原子吸收光谱法作为检测食品质量的重要方法,究其原因,主要是这项检测方法具有良好的适用性,其检测步骤较为简单,准确性也较高。
原子吸收光谱法主要是基于待测元素的基态原子蒸汽对其特征谱线的吸收,由特征谱线的特征性和谱线被减弱的程度对待测元素进行定性定量分析的一种仪器分析的方法。
实际应用这项检测方法的过程中,也可能受到一些局限。
例如,在测定不同元素时需更换不同光源灯,不利于多种元素的同时分析。
常用的原子吸收光谱发有以下几种:1.1 石墨炉原子吸收光谱检测如果在检测食品重金属元素时应用的原子化器为石墨炉,则需要确保石墨炉的质量满足检测的需求,尤其是其中的管材,需要选择优质的石墨作为原材料,然后通过电加热加快内部原子转化的速度,继而充分发挥吸收光谱检测方法的运用效果。
1.2 火焰原子吸收检测这项检测方法是通过利用火焰原子吸收这一特性,对光谱进行有效检测,通过将样品在火焰中燃烧,实现对样品的原子化处理,从而对食品重金属元素进行有效测定。
1.3 氢化物吸收光谱法氢化物检测法早在20世纪中期就被外国学者创造出来。
该方法结合了原子光谱和砷化氢元素,因为外界环境因素可能会对检测流程带来一定影响,所以在使用该方法检测食品重金属元素过程中,需要借助还原剂的功能,将初生态氢转化为具有共价性质的挥发物质,在完成上述流程后,就可以利用载气流的方式,对食品中的重金属元素进行测定。


第七章原子吸收光谱法1.原子吸收光谱的历史2.原子吸收光谱的特点3.原子吸收光谱与紫外可见吸收光谱的区别4.原子吸收光谱分析过程第一节概述1. 原子吸收光谱的历史◆1802年,沃拉斯顿(Wollaston)在研究太阳连续光谱时,首次发现太阳连续光谱中出现暗线。
◆1817年,夫琅和费(Fraunhofer)研究太阳连续光谱时再次发现这些暗线,但无法解释暗线产生的原因。
2/1363/1361825年,法国著名哲学家孔德在哲学讲义中说“恒星的化学组成是人类绝对不能得到的知识”◆1859年,本生、基尔霍夫研究碱金属和碱土金属火焰光谱时,发现钠蒸气发出的光通过温度较低的钠蒸气时,会引起钠光的吸收,并且钠在光谱中位置相同。
发射线与暗线D◆太阳光谱暗线:太阳外围大气圈中钠原子对太阳光谱中钠辐射特征波长光进行吸收的结果。
4/1365/136太阳中含有94种稳定和放射性元素:氢(71%)、氮(27%)、氧、碳、氖、硅、铁等。
◆1955年,澳大利亚物理学家Walsh(沃尔什)发表了著名论文《原子吸收光谱法在分析化学中的应用》,奠定了原子吸收光谱法的基础。
◆1960年以后,原子吸收光谱法得到迅速发展,成为微量、痕量金属元素的可靠分析方法。
6/1362. 原子吸收光谱法的特点✓检出限低:10-10~10-14g。
✓准确度高:1%~5%。
✓选择性好:一般情况下共存元素无干扰。
✓应用范围广:可测定70多种元素。
✗缺点:难熔元素、非金属元素测定困难,不能实现多元素同时分析。
7/1363. 原子吸收与紫外可见吸收的区别✓相同点:利用物质对辐射的吸收进行分析。
✗不同点:◆吸收机理不同:紫外可见为溶液中分子或离子宽带吸收,带宽为几纳米至几十纳米;原子吸收为气态基态原子的窄带吸收,带宽仅为10-3nm。
◆光源不同。
◆试样处理、实验方法及对仪器的要求不同。
8/1364. 原子吸收光谱分析过程◆确定待测元素。
◆选择该元素相应锐线光源,发射出特征谱线。

第五章原子吸收光谱法Chapter FiveAtomic Absorption SpectrumFor Short:AAS第一节基本原理一、原子吸收光谱分析概述1、原子吸收光谱的起源18世纪初,人们便开始观察和研究原子吸收光谱-----太阳光谱中的暗线。
1955年,澳大利亚物理学家瓦尔西发表了著名论文“原子吸收光谱在化学分析中的应用”,奠定了原子吸收光谱分析法的理论基础。
1955年,原子吸收光谱作为一种分析方法开始应用。
并在60年代得到迅速发展和普及。
2、什么是原子吸收光谱?溶液中的金属离子化合物在高温下能够解离成原子蒸气,两种形态间存在定量关系。
当光源发射出的特征波长光辐射通过原子蒸气时,原子中的外层电子吸收能量,特征谱线的光强度减弱。
光强度的变化符合朗伯-比耳定律,进行定量分析。
它是基于物质所产生的原子蒸气对特征谱线的吸收作用来进行定量分析的一种方法。
❖原子与分子一样,吸收特定能量后,产生基态→激发态跃迁;产生原子吸收光谱,即共振吸收。
❖原子由基态→第一激发态的跃迁,最易发生。
❖每种原子的核外电子能级分布不同,当产生由基态→第一激发态的跃迁时,吸收特定频率的辐射能量。
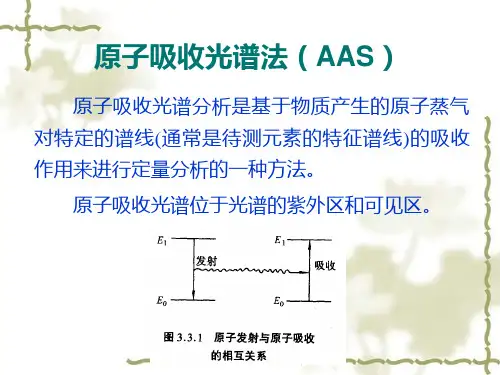
二、共振线:共振吸收线——电子从基态跃迁至第一激发态所产生的吸收谱线称为共振吸收线(简称共振线)。
共振发射线——电子从第一激发态再跃回基态时,则发射出同样频率的辐射,对应的谱线称为共振发射线(也简称共振线)。
原子的共振线的吸收共振线称为元素的特征谱线,因为:各种元素的原子结构和外层电子排布不同。
所以不同元素的原子从基态激发成第一激发态(或由第一激发态跃回基态)时,吸收(或发射)的能量不同,因此各种元素的共振线各有其特征性。
共振线又称为元素的灵敏线,因为:这种从基态到第一激发态的跃迁最容易发生,因此对大多数元素来说,共振线是指元素所有谱线中最灵敏的谱线。
在原子吸收光度法中,就是利用处于基态的待测原子蒸气对从光源发射的共振发射线的吸收来进行分析的。


原子吸收光谱仪应用
原子吸收光谱仪是一种常见的分析仪器,广泛应用于化学、生物、环境、医药等领域。
其工作原理是利用原子在特定波长的光线下吸收能量,从而测量样品中某种特定原子的含量。
该仪器具有高精度、高灵敏度、快速分析等优点。
在化学领域中,原子吸收光谱仪通常用于分析金属离子、有机污染物等样品中的元素含量。
在生物领域中,该仪器可以用于分析生物样品中的微量元素,如铁、锌、铜等。
在环境领域中,原子吸收光谱仪可以用于分析水体、大气中的污染物含量。
在医药领域中,该仪器可以用于分析药品中的元素含量,确保药品的安全性和质量。
总之,原子吸收光谱仪在各个领域中都有着广泛的应用。
其高精度、高灵敏度、快速分析等特点,为科研人员和工程技术人员提供了一种有效的分析手段,促进了科学技术的发展和进步。
- 1 -。
实验一火焰原子吸收光谱法测定水中钙含量一、实验原理在使用锐线光源条件下,基态原子蒸汽对共振线的吸收,符合朗伯-比尔定律,即:A=lg(I0/I)=KLN0在试样原子化时,火焰温度低于3000 K时,对大多数元素来讲,原子蒸汽中基态原子的数目实际上十分接近原子总数。
在一定实验条件下,待测元素的原子总数目与该元素在试样中的浓度呈正比。
则:A= c用A-c标准曲线法或标准加入法,可以求算出元素的含量。
二、仪器与试剂1.仪器(1)TAS原子吸收分光光度计;钙空心阴极灯。
(2)10mL移液管一支(3)100 mL容量瓶六个(4)2mL移液管一支2.试剂(1)1.0g.L-1钙标准储备液(2)50 mg.L-1钙标准使用液(老师完成)配制用水均为二次蒸馏水。
三、实验步骤1. 配制钙系列标准溶液:2.0,4.0,6.0,8.0,10.0 mg.L-1。
(老师完成)2. 工作条件的设置(老师完成,具体实验过程中可能有变动,注意在实验过程中记录。
)(1)吸收线波长Ca 422.7 nm(2)空心阴极灯电流 4 mA(3)狭缝宽度0.1 mm(4)原子化器高度 6 mm(5)空气流量 4 L.min-1,乙炔气流量1.2 L.min-13. 钙的测定(1)样品:移10.00 mL自来水于50 mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
(学生在C209食品分析实验室完成,韶关地处石灰岩地区,水的硬度比较高。
如果稀释5倍钙离子浓度仍然在检测线性范围之外,则需要继续稀释。
)(2)加标样品:移10.00 mL自来水样和2.50 mL50 mg.L-1钙标准使用液于50 mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
(学生在C209食品分析实验室完成。
请大家查阅资料,学习加标回收率的概念。
)(3)在最佳工作条件下,以蒸馏水为空白,测定钙系列标准溶液和自来水样、加标的自来水样吸光度A。
(老师和学生在B102共同完成)4. 实验结束后,用蒸馏水喷洗原子化系统2 min,按关机程序关机。