双水杨醛缩乙二胺Schiff 碱
- 格式:doc
- 大小:119.00 KB
- 文档页数:6

水杨醛缩乙二胺希夫碱与牛血清白蛋白的相互作用及抑菌活性研究庞绪良;赵培然;董建方;叶新辉;李连之【摘要】合成了水杨醛缩乙二胺希夫碱化合物.利用紫外可见吸收光谱、荧光光谱和圆二色光谱法研究了水杨醛缩乙二胺希夫碱与牛血清白蛋白(BSA)的相互作用.结果表明,该希夫碱化合物与BSA形成了复合物,导致BSA的构象发生变化,使BSA的内源性荧光发生静态猝灭,计算得到了希夫碱化合物与BSA相互作用的热力学参数.体外抑菌实验表明该希夫碱对大肠杆菌具有一定的抑菌活性.【期刊名称】《聊城大学学报(自然科学版)》【年(卷),期】2017(030)002【总页数】6页(P45-49,55)【关键词】水杨醛缩乙二胺希夫碱;牛血清白蛋白;光谱;抑菌活性【作者】庞绪良;赵培然;董建方;叶新辉;李连之【作者单位】聊城大学化学化工学院,山东聊城252059;聊城大学化学化工学院,山东聊城252059;聊城大学化学化工学院,山东聊城252059;聊城大学化学化工学院,山东聊城252059;聊城大学化学化工学院,山东聊城252059【正文语种】中文【中图分类】O626希夫碱(Schiff base)是指由醛或酮与伯氨缩合而成的含有亚胺或甲亚胺的一类有机化合物,希夫碱化合物是由H. Schiff在1864年首次发现而得名[1],随后希夫碱化合物被广泛深入的研究[2].希夫碱中含有碳氮双键,其杂化轨道上的N原子具有孤对电子,因而在化学和生化反应中具有重要意义.希夫碱是一类重要的化学分析试剂和良好的有机化学配体,其本身还具有一定的抗菌、抗炎、抗肿瘤、抗病毒的生物学活性[3].研究表明,希夫碱及其衍生物已广泛应用于医疗、催化、材料、生化反应等方面.蛋白质作为生命功能的执行者,是生物体的重要组成成分.血清白蛋白是可溶性蛋白质,许多小分子化合物药物通过与人血清白蛋白结合运输到体内.近些年来,有很多关于希夫碱及其衍生物与BSA相互作用的研究报道[4-6].因此,研究药物分子与蛋白的结合方式及其在血液中的运输机制是非常重要的[7].我们曾报道过L-丝氨酸水杨醛希夫碱镍(Ⅱ)配合物的合成、结构及与DNA的相互作用[8].本文中我们合成了水杨醛缩乙二胺希夫碱化合物,利用紫外可见吸收光谱、荧光光谱和圆二色光谱法研究了该化合物与牛血清白蛋白(BSA)的相互作用.1.1 试剂与仪器乙二胺、水杨醛、无水甲醇均为市售分析纯试剂,BSA购自北京拜尔迪生物技术有限公司,三羟甲基氨基甲烷(Tris)购自AMRESCO公司,BSA存储液用10 mmol·L-1 Tris-HCl (pH=7.1)缓冲液配制,浓度由(ε280=43 824 L·mol-1·cm-1 确定.Nicolet 460 型红外光谱仪(KBr压片),X-4显微熔点仪(未经矫正),Lambda 750型紫外分光光度计(Perkin Elmer, 美国),F-7000荧光光谱仪,JASCO J-810 型圆二色光谱仪(Japan).1.2 希夫碱化合物的合成与表征量取0.05 mol(3.5 ml)的乙二胺于圆底烧瓶中,并加入30 mL甲醇,在50 ℃的条件下加热搅拌0.5 h,然后慢慢滴加0.1 mol (21 mL)的水杨醛溶液,加热回流2 h后泠却至室温,过滤至平底试管中,在室温下缓慢挥发,一周后得到黄色片状晶体,产率约76%.该希夫碱晶体熔点为125 ℃.希夫碱化合物的IR(cm-1):3 433.6 (s, υO-H);1 636.2 (s, υC=N).希夫碱的结构在Bruker Smart-1000 CCD 型单晶衍射仪上进行了测定.1.3 希夫碱化合物与BSA的相互作用1.3.1 紫外可见吸收光谱.用10 mmol·L-1 Tris-HCl(pH=7.1)缓冲溶液配制一系列试样,保持BSA(8.0 μmol·L-1)的浓度不变,希夫碱化合物的浓度逐渐增大,将配好的试样混合均匀后放置在室温条件下2.5 h后测定BSA的紫外可见吸收光谱,用缓冲溶液或不同浓度化合物的溶液作为参比,光谱在240-400 nm 波长范围内测定.1.3.2 荧光光谱.用10 mmol·L-1 Tris-HCl (pH=7.1)缓冲溶液配制一系列试样,保持BSA(8.0 μmol·L-1)浓度不变,逐渐加大希夫碱化合物的浓度.将试样混合均匀,然后在室温条件下放置2.5 h,分别于298 K、303 K和308 K三个温度下恒温后测定BSA的荧光光谱.激发波长: 280 nm,发射波长范围:290-460 nm,狭缝宽度:Ex=Em=2.5 nm;扫描速度:600 nm·min-1.1.3.3 圆二色光谱测定.用10 mmol·L-1 Tris-HCl(pH=7.1)缓冲液配制试样,其中BSA浓度为4.5×10-7 mol·L-1,化合物的浓度是10 μmol·L-1,测定时以同浓度的缓冲溶液或化合物缓冲溶液作为参比,分别测定BSA及BSA与化合物混合液在190-250 nm波长范围内的圆二色光谱,混合均匀室温下放置2.5 h后测定.扫描速度为200 nm·min-1,路径长度为 1 cm,响应时间为1 s,累积次数为3次. 1.4 抑菌实验用纸片扩散法进行体外抑菌实验.将大肠杆菌(E.coli) BL21(DE3)菌液(A550 = 0.75)均匀地涂在M-H琼脂培养基的培养皿上,然后将灭菌过的滤纸片(8.0 mm)平铺在培养皿上,缓慢向滤纸片上注上10 μL浓度为2.5 mmol·L-1希夫碱的水溶液,另取一个滤纸片注上10 μL蒸馏水作为参比,最后放在恒温培养箱内在32 ℃培养20 h,观察抑菌圈,测量抑菌圈的直径.2.1 化合物的表征红外光谱采用KBr压片法,在400-4 000 cm-1范围收集数据.希夫碱化合物在3 433.6 cm-1 处的强吸收峰是由于O-H的伸缩振动,1 636.2 cm-1处强而尖的特征吸收峰可以说明希夫碱(CN)结构的生成.化合物的晶体结构测定结果与文献[9]一致.图1为该希夫碱化合物的分子结构图.2.2 希夫碱化合物与BSA的作用2.2.1 紫外可见吸收光谱.在研究小分子化合物与蛋白质的作用中,常用紫外可见吸收光谱来检测蛋白质的构象变化.BSA在280 nm左右的吸收峰是由于蛋白质肽链上色氨酸、酪氨酸和苯丙氨酸上的杂环π-π*和n-π*的跃迁引起的[10].图2为不同浓度的希夫碱存在时BSA的紫外吸收光谱(希夫碱化合物本身在278 nm处吸收很弱,没有吸收峰).从图2中可以看出,随着希夫碱浓度的增加,在278 nm处的吸收峰逐渐上升且略有蓝移,而且在400 nm处出现了一个新的吸收峰,此峰随着希夫碱浓度的增加明显增大.这说明该希夫碱化合物与BSA上的氨基酸残基发生了相互作用,形成了基态复合物.2.2.2 荧光光谱.荧光光谱法具有选择性好且灵敏度高的优点.因此,被广泛应用于研究药物分子与蛋白的作用中.BSA中的色氨酸(Trp)、酪氨酸(Tyr)和苯丙氨酸(Phe)是荧光生色基团,而且这些氨基酸残基对微环境的变化都较敏感,通常作为荧光光谱的检测靶标.在一定激发波长下,BSA的荧光光谱的变化在一定程度上反映了蛋白质荧光生色基团的微环境变化[11].图3、图4和图5为不同温度下,不同浓度的希夫碱对BSA溶液的荧光猝灭光谱.由图3可以看出,随着希夫碱浓度的增加,BSA在330 nm处的荧光强度逐渐降低,说明该希夫碱化合物与BSA发生了相互作用,影响了蛋白质荧光生色团微环境的变化,从而导致BSA的内源性猝灭.荧光猝灭有静态猝灭和动态猝灭两类.动态猝灭是与扩散有关的,当温度升高时,溶液的黏度将会下降,从而导致分子的运动加快,从而使分子的扩散系数增大,猝灭常数就会增大.当发生静态猝灭时,随着温度的升高会引起复合物的稳定性降低,使猝灭程度减弱,猝灭常数就会减小.为了解希夫碱化合物对BSA的猝灭类型,通常先按动态猝灭处理,常使用Stern-Volmer方程[12]式中用F0 和F分别表示未加入希夫碱和加入希夫碱后的荧光峰强度;Kq 是BSA猝灭常数,τ0 为没有加猝灭剂时荧光物质的荧光寿命,其值约为10-8 s;Ksv是Stern-Volmer 猝灭常数;[Q]来表示希夫碱化合物的浓度.图3、图4和图5中的内嵌图分别为该体系在不同温度下的荧光猝灭光谱和F0/F对[Q]作图.由F0/F对[Q]作图求得化合物的猝灭常数Ksv(298 K)= 1.36×104 L·mol-1,Ksv(303K)=9.22×103 L·mol-1,Ksv(308 K)=8.25×103L·mol-1. 进而可求得Kq (298 K)=1.36×1012 L·mol-1·s-1,Kq (303 K)=9.22×1011 L·mol-1·s-1,Kq (308 K)=8.25×1011 L·mol-1·s-1.可以看出,希夫碱化合物的Kq要远远大于最大扩散碰撞猝灭速率常数2×1010 L·mol-1·s-1.随着温度的升高,其猝灭常数也逐渐减小,进一步说明了该希夫碱化合物对BSA的猝灭过程并不是由分子碰撞和扩散所产生的动态猝灭,而是希夫碱化合物与BSA相互作用后形成了不发光的基态复合物而引起的静态猝灭.希夫碱化合物对BSA的作用方式属于两者之间形成复合物的静态猝灭.通常假设BSA上有n个且相同的结合位点,则BSA的荧光强度与希夫碱化合物浓度的关系可以用下面的双对数公式进行描述[13]式中KA是结合常数,n是结合位点数,[Q]是猝灭剂的浓度.图6是lg[(F0-F)/F]对lg[Q]作图,由该图可以求得在不同温度下的结合常数分别为KA(298K)=3.07×105 L·mol-1,KA(303 K)=6.69×103 L·mol-1,KA(308K)=4.96×103 L·mol-1;结合位点数分别为:n(298 K) = 1.3,n(303 K)=0.92,n(308 K)=0.95.这说明该希夫碱化合物与BSA是以1∶1结合的,即两者之间存在一个结合位点.从热力学的观点可考察希夫碱化合物与BSA之间的结合力(氢键、疏水键、静电作用或范德华力等).根据求得的不同温度下的结合常数(KA),运用热力学公式(3)来计算反应的自由能变值(ΔG).通过计算求得ΔG(298 K) =-31.3 kJ·mol-1,ΔG(303 K) =-22.2 kJ·mol-1,ΔG(308 K) =-21.8 kJ·mol-1.利用反应自由能变值对温度作图求得焓变(ΔH)和熵变(ΔS)分别为:ΔH =-313.0 kJ·mol-1,ΔS =-950 J·mol-1·K-1.Ross[14]等人经过大量的研究,得出了小分子与蛋白质的结合作用力与热力学参数之间的关系,当焓变与熵变同时大于零时,可认为疏水作用力占主导;当焓变与熵变同时小于零时,则可认为是氢键或者范德华力;如果焓变较小(或接近于零)且熵变大于零,则可能为静电作用力.因此,我们得出希夫碱与BSA之间主要靠氢键或范德华力相互作用.但由于BSA的结构复杂,它与希夫碱化合物之间不可能是单一的作用力,而是多种作用力之间的相互结合.2.2.3 圆二色光谱.圆二色光谱法是研究蛋白质构象变化及与小分子作用的一种快捷、较准确的方法.图7是该希夫碱化合物对BSA圆二色光谱的影响图.由图7得知,BSA在208 nm和222 nm处有两个明显的特征负峰,这是典型的α-螺旋结构[15].加入化合物后,谱图的形状和峰位没有发生显著的变化,但峰强度减弱.这说明化合物的加入对BSA产生了影响,导致BSA的构象发生了变化.我们可通过公式⑸求出α-螺旋值[16]式中cp是BSA的摩尔浓度,n是氨基酸残基数(BSA为583),l是路径长度(1 cm).计算得BSA的α-螺旋值含量在加入化合物后从原来47.6%降到41.4%,说明希夫碱化合物与BSA的相互作用使BSA的二级结构产生了影响.原因可能是希夫碱化合物通过氢键等作用与α-螺旋的氨基酸残基发生相互作用,从而改变了α-螺旋结构,导致BSA中的α-螺旋量降低.2.3 抗菌实验初步体外抑菌实验结果说明该希夫碱化合物对大肠杆菌E.coli BL21(DE3)有较好的抑菌活性,其平均抑菌圈直径约为15 mm.对于其它菌落的抑菌活性需要进一步的研究,希望能为探索高效低毒的抗菌药物提供一定的参考.合成了水杨醛缩乙二胺希夫碱化合物,利用紫外可见吸收光谱、荧光光谱和圆二色光谱法研究了水杨醛缩乙二胺希夫碱与BSA的相互作用.结果表明,该希夫碱化合物与BSA形成1∶1的复合物,使BSA的内源性荧光发生静态猝灭,导致BSA的α-螺旋含量减少.体外抑菌实验表明该希夫碱对大肠杆菌具有一定的抑菌活性.这些结果为探讨希夫碱化合物与BSA相互作用的分子机理提供了有用的信息.【相关文献】[1] Schiff H. Mittheilungen aus de m Universitäts laboratorium in pisa: eine neue reihe organischer basen[J]. Eur J Org Chem, 2010, 131(1):118-119.[2] Choudhary N F, Leigh G J, Hitchcock P B. Six-coordinate vanadyl tetradentate Schiff base complexes with methanol, methoxide, water or fluoride as the sixth ligand[J]. Inorg Chim Acta, 2000, 310(1):10-20.[3] Desai S Β, Desai P B, Desai K R. Synthesis of some schiff bases, thiazolidinones and azetidinones derived from 2,6-diaminobenzo[1,2-d:4,5-d'] bisthiazole and their anticancer activities[J]. Heterocycl Commun, 2001, 7(1):83-90.[4] Raynor J B, Labauze G. Use of electron spin resonance spectroscopy to study the interaction between cobalt schiff base complexes and phosphines or phosphites in solution[J]. Inorg Chim Acta, 1980, 40(1):X10- X10.[5] Zhang Q, Ni Y, Kokot S. Combined voltammetric and spectroscopic analysis of small molecule-biopolymer interactions: The levodopa and serum albumin system[J]. Talanta, 2012, 88(1):524-532.[6] Zhang L, Cai Q Y, Cai Z X, et al. Interactions of bovine serum albumin with anti-cancer compounds using a proteon XPR36 array biosensor and molecular docking.[J]. Molecules, 2016, 21(12):1706.[7] Sathyadevi P, Krishnamoorthy P, Alagesan M, et al. Synthesis, crystal structure,electrochemistry and studies on protein binding, antioxidant and biocidal activities of Ni(II) and Co(Ⅱ) hydrazone complexes[J]. Polyhedron, 2012, 31(1):294-306.[8] 丁菲菲,丁名成,魏强,等.L-丝氨酸水杨醛希夫碱镍(Ⅱ)配合物的合成、结构及与DNA的相互作用[J].聊城大学学报:自然科学版,2016,29(1):37-42.[9] Pahor N B, Calligaris M, Nardin G, et al. N, N′-ethylenebis(salicylideneimine)[J]. Acta Crystallogr B, 1978, 34(4):1 360-1 363.[10] Wang Y Q, Zhang H M, Zhang G C, et al. Interaction of the flavonoid hesperidin with bovine serum albumin: A fluorescence quenching study[J]. J Lumin, 2007, 126(1):211-218.[11] Toneatto J, Argüello G A. New advances in the study on the interaction of[Cr(phen)2(dppz)]3+, complex with biological models; association to transporting proteins[J]. J Inorg Biochem, 2011, 105(5):645-651.[12] Albrecht C. Joseph R. Lakowicz: Principles of fluorescence spectroscopy, 3rd Edition[J]. Anal Bioanal Chem, 2008, 390(5):1 223-1 224.[13] Hu Y J, Liu Y, Wang J B, et al. Study of the interaction between monoammonium glycyrrhizinate and bovine serum albumin[J]. J Pharm Biomed Anal, 2004, 36(4):915-919. [14] Ross P D, Subramanian S. Thermodynamics of protein association reactions: forces contributing to stability[J]. Biochemistry, 1981, 20(11):3096.[15] Liu J, Tian J, He W, et al. Spectrofluorimetric study of the binding of daphnetin to bovine serum albumin[J]. J Pharm Biomed Anal, 2004, 35(3):671-677.[16] Purdie N, Swallows K A. Analytical applications of polarimetry, optical rotatory dispersion, and circular dichroism[J]. Anal Chem, 1989, 61(2):77A-89A.。



2020 年 12Dec. 20206 ]Issue 6江西科技师范大学学报Journal of Jiangxi Science & Technology Normal University双水杨醛缩苯胺席夫碱的制备及性能研究张文雄,高飞*,李帅,郭心茹,王吉江,杨豫平*(江西科技师范大学化学化工学院,江西南昌330013)摘要:近年来,以席夫碱类化合物与金属配位作用为基础的荧光探针检测技术越来越受到人们的广泛关注,以席夫碱为方向开发的新型荧光探针分子应用于金属离子的检测是一种行之有效的方法。
本文以2,2-二(4-f 基苯基)丙烷、三氯甲烷、氢氧化钠为原料,通过Reimer-Tiemann 反应,先制备双水杨醛,再和苯胺进行缩合反应得到双水杨醛席夫碱结构,并通过 一步确认。
通过紫外分光光度计与荧光光谱分析的表征,确定了该化合物与金属离子配位的特性。
关键词:席夫碱;荧光探针;离子探测中图分类号:0622.6文献标识码:A 文章编号:2096-854X (2020)06-0030-04Study on Preparation and Performance of Schiff Base ofDissalicylidene AnilineZhang Wenxiong ,Gao Fei *, Li Shuai ,Guo Xinru ,Wang Jijiang ,Yang Yuping *(1. School of Chemistry & Chemical Engineering, Jiangxi Science & Technology Normal University,Nanchang 330013, Jiangxi, P.R. China )Abstract : In recent years, fluorescent probe detection technology based on the coordination of Schiff basecompounds and metals have attracted more and more attention. The new fluorescent probe molecules developed in thedirection of schiff bases are used in the detection of metal ions has become an effective method. In this paper, 2,2-bis (4-hydroxyphenyl)propane, chloroform, and sodium hydroxide were used as raw materials to prepare salicylaldehyde through Reimer -Tiemann reaction, and then condensation reaction with aniline to obtain salicylaldehyde Schiff and further confirmed by nuclear magnetic resonance that the synthesized product is consistent with the target product. The coordination characteristics of the compound and copper ions were determined by ultraviolet spectrophotometer andfluorescence spectrum analysis.Key words : Schiff base, fuorescent probe, ion detection—、前言荧光检测由于具有操作简单和高检测线的特点,因而作为一种用途被广泛的运用于分析化学% 生物化学和细胞化学等[1-3]o 荧光传感器的主要作用是通过荧光增强(或荧光猝灭)来放大分子水平的金属离子和传感器之间的键合作用席夫碱是一类含C=N 结构的化合物,德国化学 家Hugo Schiff 在1864年首次报道了席夫碱的合成叫经过两百多年无数化学家及相关领域专家的收稿日期:2020-09-27 修回日期:2020-10-30 接受日期:2020-10-30基金项目:江西科技师范大学青012计划项目(2019QNBJRC007)。


双水杨醛缩乙二胺Schiff 碱及其钴(Ⅱ)配合物的合成与表征摘要:本实验以水杨醛、乙二胺、硝酸镍为原料,采用加热、回流等方法合成了席夫碱配体及其Ni(Ⅱ)配合物。
并采用红外光谱、EDTA直接滴定法、测定熔点等途径对化合物进行表征。
关键词:水杨醛;乙二胺;席夫碱;氯化钴;红外光谱水杨醛及其衍生物是重要的有机合成中间体。
由水杨醛及其衍生物与胺类化合物反应生成的席夫碱与其金属配位生成的金属配合物在医药、催化、分析化学、腐蚀和光致变色领域有着重要应用,因而受到人们的广泛关注。
本文对回流条件下双水杨醛缩乙二胺Schiff 碱及其钴(Ⅱ)配合物的合成进行了研究,并对其进行表征。
一、实验部分(一)主要仪器和药品药品:水杨醛、乙二胺、95%乙醇、85%乙醇、无水乙醇、2mol/L HCl溶液、Co·6H2O。
仪器:天平、红外光谱仪、熔点仪、毛细管圆底烧瓶、磁力搅拌器、球形冷凝管、布氏漏斗、温度计、酸式滴定管(50mL)、锥形瓶、烧杯。
材料:滤瓶、pH试纸反应物参数:名称乙二胺水杨醛氯化钴西佛碱分子量60.1 122 238 268.1g/mol密度g/ml 0.9000 1.1656 1.92(二)实验原理1.双水杨醛缩乙二胺Schiff碱及其镍(Ⅱ)配合物的合成Schiff碱的合成是涉及到加成、重排、消去等过程的一种缩合反应。
反应物的立体结构及电子效应在合成中起着重要作用,其反应机理如下图:本实验采用水杨醛和乙二胺在75℃的条件下用回流法制备相应的Schiff碱,反应方程式如下所示:席夫碱基团通过碳氧双键(-C=N-)上的氮原子与相邻的具有孤对电子的氧(O)、硫(S)、磷(P)原子作为给体与金属原子配对,所以氮原子相邻位置存在这类原子的Schiff碱往往具有高配位能力。
(三)实验装置图(四)实验内容1.Schiff 碱配体及其镍(Ⅱ)配合物的合成实验步骤现象记录(1)Schiff 碱配体的合成在装有回流冷凝管和搅拌器的圆底烧瓶中加入6ml水杨醛和30ml无水乙醇,开动搅拌器搅拌。

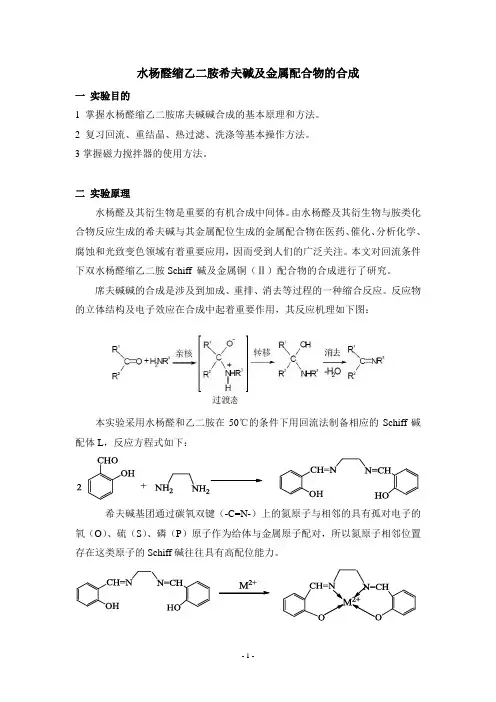
水杨醛缩乙二胺希夫碱及金属配合物的合成一实验目的1 掌握水杨醛缩乙二胺席夫碱碱合成的基本原理和方法。
2 复习回流、重结晶、热过滤、洗涤等基本操作方法。
3掌握磁力搅拌器的使用方法。
二实验原理水杨醛及其衍生物是重要的有机合成中间体。
由水杨醛及其衍生物与胺类化合物反应生成的希夫碱与其金属配位生成的金属配合物在医药、催化、分析化学、腐蚀和光致变色领域有着重要应用,因而受到人们的广泛关注。
本文对回流条件下双水杨醛缩乙二胺Schiff 碱及金属铜(Ⅱ)配合物的合成进行了研究。
席夫碱碱的合成是涉及到加成、重排、消去等过程的一种缩合反应。
反应物的立体结构及电子效应在合成中起着重要作用,其反应机理如下图:本实验采用水杨醛和乙二胺在50℃的条件下用回流法制备相应的Schiff碱配体L,反应方程式如下:希夫碱基团通过碳氧双键(-C=N-)上的氮原子与相邻的具有孤对电子的氧(O)、硫(S)、磷(P)原子作为给体与金属原子配对,所以氮原子相邻位置存在这类原子的Schiff碱往往具有高配位能力。
M2+为金属离子(M2+分别为Cu2+、Zn2+、Ni2+、Mn2+、Ni2+等离子)二仪器和药品1 仪器100mL三口烧瓶恒压滴液漏斗磁力搅拌器玻璃塞抽滤瓶烧杯2 药品水杨醛(相对分子质量122.12,密度1.17g/cm³乙二胺(相对分子质量60.10,密度0.90g/cm³无水乙醇乙酸铜、硝酸钴、乙酸锰、乙酸锌、硝酸锌、氯化镍三实验步骤1 希夫碱配体(L)的合成步骤移取5.2mL(0.05mol)的水杨醛与15 mL的无水乙醇溶于三口瓶中,再量取1.8mL(0.025mol)的乙二胺与10mL的无水乙醇于烧杯中搅拌溶解。
将三口瓶固定在搅拌器上,开启仪器,将乙二胺的无水乙醇溶液逐滴滴加到三口瓶中,恒温55℃反应1小时。
反应结束。
抽滤得黄色的固体,干燥称重并计算产率。
反应装置图如下:乙二胺的无水乙醇溶液2 希夫碱配体(L)与金属离子(M2+)的反应步骤称取1.34g(0.005mol)配体L,与20 mL的无水乙醇混合溶解于三口瓶中,在称取金属盐,若为乙酸铜时质量为1g(0.005mol)。
化学实验题第七套题除去⼄醚中的过氧化物,应选⽤下列哪种试剂?答案Na2SO4FeSO4KI-淀粉Fe2(SO4)3溶液分馏实验中,对馏出速度的要求是:答案2~3秒1滴每秒1~2滴越快越好1~2秒1滴环⼰醇的制备实验中,分离环⼰醇和⽔采取的⽅法是:答案⽔蒸⽓蒸馏常压蒸馏分馏减压蒸馏关于恒沸混合物,下列说法中错误的是:答案具有固定的组成可⽤分馏来进⾏分离平衡时⽓相和液相组成相同下列各组物质中,都能发⽣碘仿反应的是哪⼀组?答案甲醛和丙酮⼄醇和1-丁醇甲醛和⼄醛⼄醇和丙酮欲除去环⼰烷中的少量环⼰烯,最好采⽤哪种⽅法?答案⽤浓硫酸洗涤⽤臭氧氧化分解后分馏⽤浓氢氧化钠溶液洗涤⽤HBr处理后分馏列有机试剂中能使FeCl3显⾊的是:答案⾁桂酸⼄酰苯胺⽔杨酸下列化合物中,碱性最强的是:答案OH-RO-NH2-R-有机化合物的性质主要取决于哪个因素?答案有机化合物分⼦间的聚集状态所含官能团的种类、数⽬和分⼦量构成分⼦的各原⼦间的组成⽐例构成分⼦的各原⼦间的空间排列下列分⼦中哪⼀个不含有离域⼤π键?答案CH3CONH2NO2CO2C=C=CH2H区分邻苯⼆甲酸与⽔杨酸的⽅法是:答案加Na放出H2⽤LiAlH4还原加热放出CO2久置的苯胺呈红棕⾊,⽤哪种⽅法精制?答案⽔蒸⽓蒸馏.活性炭脱⾊过滤蒸馏减压蒸馏实验结束后,拆除装置时,⾸先是:答案关闭冷却⽔移开热源打开安全阀拆除反应瓶以丁酸和⼄醇发⽣酯化反应制备丁酸⼄酯的实验中,加⼊苯的作⽤是:答案作反应物的溶剂带出⽣成的⽔降低反应温度下列说法错误的是:答案有机化合物在⼀定的压⼒下具有⼀定的沸点降低压⼒可降低化合物的沸点共沸物是组成明确的化合物具有固定沸点的液体不⼀定都是纯化合物苯胺-⼄醚溶液中含有微量⽔,可⽤哪种⼲燥剂⼲燥?答案KOHP2O5NaCaCl2下列化合物中,哪⼀个的烯醇式含量⾼?答案CH3COCH3CH3COCH2COCH3CH3COCH2COOC2H5CH3CHO问题18⽔蒸⽓蒸馏时,下列正确的说法是:答案被馏出的有机物在⽔中的溶解度⼩被馏出的有机物在⽔中的溶解度⼤被馏出的有机物饱和蒸⽓压⽐⽔⼩问题19下列化合物在光照下分别与溴的四氯化碳溶液作⽤,反应最快的是:答案苯环⼰烷氯苯甲苯问题20⽤熔点法判断物质的纯度,主要是观察:答案初熔温度全熔温度熔程长短三者都不对问题21鸡蛋⽩溶液与茚三酮试剂有显⾊反应,说明鸡蛋⽩结构中有:答案肽键游离氨基芳环问题22下列化合物,哪⼀个与⽔不相混溶?答案丙酮四氢呋喃吡啶苯⼄酮问题23鉴别⼄酰⼄酸⼄酯和⼄酰丙酸⼄酯可以⽤:答案卢卡斯试剂羰基试剂斐林试剂FeCl3溶液问题24下列四种化合物,哪种酸性最强?答案环戊⼆烯环庚三烯苯问题25下列负离⼦中,亲核性最强的是:答案RCOO-HO-RO-ArO-问题26下列化合物中哪个不发⽣Cannizzaro反应?答案对甲基苯甲醛甲醛⼄醛三甲基⼄醛问题27下列化合物中哪⼀个⽔溶性最⼩?答案(CH3)2NH(CH3)3N(CH3)4N+Cl-CH3NH2问题28与亚硝酸反应能放出氮⽓的是:(C2H5)4N+Br-(C2H5)2NHC2H5NH2(C2H5)3N问题29下列物质不能与Fehling试剂反应的是:答案苯甲醛麦芽糖果糖甲醛问题30下列物质中,不能发⽣碘仿反应的是:答案甲醛丙酮⼄醛⼄醇问题31下列化合物与Lucas试剂反应最快的是:答案仲丁醇环⼰醇苄醇问题32下列哪⼀种化合物能与氯化亚铜氨溶液作⽤产⽣红⾊沉淀?答案苯⼄烯2-丁烯1-丁炔2-丁炔问题33锌粉在制备⼄酰苯胺实验中的主要作⽤是:答案防⽌苯胺被氧化防⽌暴沸防⽌苯胺被还原脱⾊问题34某⼀有机化合物的红外光谱图中,位于2240 cm-1处有⼀尖锐的强吸收峰,试判断该谱带属于何种官能团的特征吸收:答案羰基氰基羟基问题35有机化合物的紫外光谱基于分⼦中电⼦的何种跃迁?答案n→π*和n→σ*π→π*和n→π*π→π*和n→σ*σ→σ*和n→σ*问题36下列化合物中哪⼀个沸点最⾼?答案邻硝基苯酚苯甲醚苯对硝基苯酚问题37顺-2-丁烯与溴加成,下列说法错误的是:答案经过环状溴鎓离⼦历程得到⼀种化合物得到⼆种化合物问题38下列哪⼀种化合物能被⾼锰酸钾氧化?答案⼰⼆酸甲酸苯甲酸丙酸问题39卤仿反应必须在什么条件下进⾏?答案中性溶液质⼦溶剂碱性溶液酸性溶液问题39卤仿反应必须在什么条件下进⾏?答案中性溶液质⼦溶剂碱性溶液答案⼄酰胺甲胺氨吡啶问题41⼲燥含有少量⽔的⼄酸⼄酯,可选⽤的⼲燥剂是:答案⾦属钠氢氧化钠⽆⽔硫酸镁⽆⽔氯化钙问题42苦味酸分⼦中含有哪⼀种基团?答案羰基羧基磺酸基羟基问题43重结晶使⽤活性炭脱⾊时,活性炭应在什么情况下加⼊?答案待固体有机物全部溶解、溶液稍冷后,再加⼊活性炭在溶液沸腾时加⼊与固体有机物充分混合后加⼊到溶剂中制备甲基橙时,N,N-⼆甲基苯胺与重氮盐偶合发⽣在:答案间位对位邻位邻、对位问题45⽤氯苯和镁反应制备苯基氯化镁时,选⽤的溶剂是:答案⼄醚苯四氢呋喃丙酮问题46鉴别⼄醇和丁醇可以⽤下列哪个试剂?答案Tollen试剂I2/NaOH溶液Lucas试剂问题47下列情况下可使⽤⽔蒸⽓蒸馏进⾏分馏的是:答案与⽔能完全互溶的有机化合物不含氢键的有机化合物与⽔不相混溶的有机化合物易挥发的有机化合物问题48下列哪个反应可以使⽤分⽔器来提⾼收率?答案⽤环⼰醇制备环⼰烯⽤正丁醇制备正丁醚⽤⼄醇和⼄酸制备⼄酸⼄酯⽤⼄醇制备⼄醚问题49⼲燥含有少量⽔的苯⼄酮,可选⽤:答案⽆⽔硫酸镁氢氧化钠⾦属钠以S N2机理发⽣亲核取代反应时,最活泼的是哪⼀个化合物?答案Ar-BrCH3BrC2H5Br(CH3)3CBr问题51下列说法正确的是:答案两个熔点相同的化合物⼀定为同⼀物分液漏⽃中的有机层应从上⼝倒出分离邻硝基苯酚和对硝基苯酚混合物可⽤⽔蒸汽蒸馏蒸馏是收集到的液体具有恒定的沸点,那么这⼀液体是纯化合物问题52酒⽯酸的化学名称是:答案2-羟基丁酸2-羟基丁⼆酸2,3-⼆羟基丁酸2,3-⼆羟基丁⼆酸问题532354问题54下列分⼦中相邻共价键的夹⾓最⼩的是:H2OCCl4NH3BF3问题55鉴别苯酚和环⼰醇可⽤下列哪个试剂?答案FeCl3溶液羰基试剂斐林试剂⼟伦试剂问题56⽆⽔氯化钙作适⽤于⼲燥下列哪类有机物?答案烃、醚醇、酚醛、酮问题57有机实验室经常选⽤合适的⽆机盐类⼲燥剂⼲燥液体粗产物,⼲燥剂的⽤量直接影响⼲燥效果。

Co-salen配合物的合成
双水杨醛缩乙二胺合钴配合物[Co(Salen)]具有类卟啉结构, 是典型的具有载氧功能的仿酶模型化合物, 能有效地活化分子氧, 在合成上经常用于烯烃的分子氧环氧化, 醇的选择性催化氧化以及催化氧化Baeyer-Villiger反应等, 由于其优良的吸氧功能, 可以加快氧化反应的速率。
而且Co(Salen)原料易得、合成方法简单。
1、配体salen的合成
取2.5克乙二胺和8.5ml水杨醛溶解于18ml甲醇中,在冰水浴中搅拌30min,静置15min后,用G3玻璃滤器减压抽滤,用1ml乙醚洗涤,在33℃下真空干燥,得淡黄色固体,再用160ml无水乙醇重结晶,在33℃下真空干燥,得到黄色晶体,即为配体salen,熔点:125-125.5℃。
合成西佛碱的反应的条件温和,无需加热,当室温较高时,可用冰水浴。
整个过程处理方便。
2、Co-salen配合物的合成
取3.48克配体salen溶解于150ml热的甲醇中,另取3.24克CoAc2·4H2O 溶解于20ml温水中,迅速转移到上述甲醇溶液中,加热回流1h,冷却、过滤、在50℃下真空干燥,即得红褐色的Co-salen配合物,熔点:大于300℃。
合成路线图如下:。
小时之后检测溶液的荧光发射光谱变化,当Fe 3+或者Hg 2+加入其中之后后,荧光探针在451 nm 时都出现强的发射峰,其中前者更强一些。
3 席夫碱的应用进展席夫碱的应用非常广泛,在各个领域都可以发挥其作用。
下面针对席夫碱在药物领域、材料领域以及催化领域的应用情况。
具体如下。
3.1 药物领域应用随着科学技术发展速度的不断加快,席夫碱本身所具备的特殊医学性质受到了学术研究领域和应用领域的重视。
研究人员通过从药物领域角度进行研究发现,席夫碱类化合物具有非常强的配位能力,而且生物药理活性非常好,在应用的过程中,其他方面也具有优越的性能[2]。
通过这些研究可以验证,席夫碱是一种具有非常大的潜力的治疗药物,也可以作为功能材料使用。
安晓雯针对这方面的问题进行研究,经过化学试验,合成了3个水杨醛Schiff 氧钒配合物,通过对配合物进行研究,同时分析载药脂质体对肝肿瘤细胞的作用,发现其抑制效果良好。
胡国强对这方面的问题进行研究,采用了合成几种含碱性侧链的单席夫碱的方法,并对非对称双席夫碱进行合成研究,在实验中对癌细胞的体外活性进行研究,发现双席夫碱结构具有非常强的抗癌活性,特别是均三唑环,有双供电子取代基连接,此时潜在的活性就会充分体现出来,课件其具有药物研究价值。
石德清针对这方面的问题进行研究,将N 1-(2-四氢呋喃烷基)-5-氟尿嘧啶作为原料,与1,4-二澳丁烷进行化学反应,获得N 1-(2-四氢呋喃烷基)-N 3-(4-溴丁基)-5-氟尿嘧啶,经过与氨基酸席夫碱的钾盐缩合,就可以获得新的化合物,其具有非常好的抗肿瘤活性。
马永超针对这方面的内容进行研究,主要研究的内容是三氮唑席夫碱衍生物碱,其所发挥的作用是诱导分化人的肝癌细胞SMMC-7721,通过研究结果可以表明,三氮唑席夫碱衍生物对人肝癌SMMC-7721细胞具有非常好的抗增殖作用,可以促进癌细胞的分化[3]。
冯驸将芴经硝化、还原得到2-氨基芴充分利用起来,之后与各种芳香醛缩和,就可以蝴蝶相应的席夫碱类化合物,通过进行试验所获得的结果可以明确,多数的化合物都有非常好的抑菌效应,活性非常强。
化学与生物工程2011,Vol.28No.7Chemistry &Bioen gineering55基金项目:黑龙江省教育厅资助项目(1030129)收稿日期:2011-04-28作者简介:李翠勤(1978-),女,河南人,硕士,讲师,主要从事精细化学品合成及聚烯烃的化学改性。
E mail:licuiqin78@163.com 。
doi:10.3969/j.issn.1672-5425.2011.07.013水杨醛缩胺类双席夫碱过渡金属配合物的合成与表征李翠勤1,孟祥荣2,张 鹏1,景常荣2,刘长环1,朱秀雨1(1.东北石油大学化学化工学院,黑龙江大庆163318;2.大庆石化公司化工一厂,黑龙江大庆163714)摘 要:以水杨醛与乙二胺为原料,通过席夫碱反应合成一类水杨醛缩胺类双席夫碱,并进一步与铜、锌、镍3种金属离子络合得到3种过渡金属配合物;采用元素分析、红外光谱和紫外光谱对席夫碱及其金属配合物的结构进行表征。
结果表明,合成的水杨醛缩乙二胺配体分子结构与理论结构相符,且分别与铜、锌、镍离子络合形成了稳定的过渡金属配合物。
关键词:水杨醛;席夫碱反应;金属配合物中图分类号:O 625.62 文献标识码:A文章编号:1672-5425(2011)07-0055-03席夫碱是一类非常重要的配体,通过改变连接的取代基、变化电子给予体原子本性及其位置,便可开拓出许多从链状到环状、从单齿到多齿的性能迥异、结构多变的席夫碱配体,这些配体可以与周期表中大部分金属离子形成不同稳定性的配合物[1,2]。
目前,研究较多的是水杨醛及其衍生物的席夫碱,其中水杨醛缩胺类双席夫碱是一类有代表性的离域 共轭有机分子,在合成上具有极大的灵活性和强络合作用,因具有良好的电子转移性质而成为人们研究的热点[3,4]。
此类席夫碱具有一个N,N,O,O 构成的空腔,可以容纳金属离子,形成稳定的金属配合物[5]。
张英菊等[6]对水杨醛缩乙二胺配体结构研究表明,水杨醛缩乙二胺配体失去两个酚羟基上的氢,随后与Ni 、M n 等过渡金属离子形成稳定的四齿配合物,该配合物的稳定性随配位原子数的增加而增大。
新型Schiff碱缓蚀剂的研究进展方晓君;张娟涛;陈长风;白真权;张国超【摘要】综述了Schiff碱缓蚀剂在金属腐蚀与防护领域的研究进展,为Schiff碱作为缓蚀剂的应用提供了实验和理论基础,也为缓蚀剂的进一步开发进行了有益的探索。
%The recent developments of novel Schiff base inhibitors in corrosion and protection field are reviewed in this paper, in order to provide theoretical and experimental foundation for the application of novel Schiff base inhibitors, and offer exploration for further exploitation of inhibitors.【期刊名称】《腐蚀与防护》【年(卷),期】2012(033)004【总页数】4页(P353-356)【关键词】Schiff碱;缓蚀剂;研究进展【作者】方晓君;张娟涛;陈长风;白真权;张国超【作者单位】中国石油大学北京材料科学与工程系,北京102249/中国石油集团石油管工程技术研究院,西安710065;中国石油集团石油管工程技术研究院,西安710065;中国石油大学北京材料科学与工程系,北京102249;中国石油集团石油管工程技术研究院,西安710065;中国石油集团石油管工程技术研究院,西安710065【正文语种】中文【中图分类】TG174.42在油气井开采过程中,油井酸化是增产的主要措施之一。
目前,油井酸化是借助于酸化压裂设备把盐酸、土酸(氢氟酸与盐酸混合液)或其它酸溶液注入地层,通过酸液对岩石的溶蚀作用,扩大油层岩石的渗透通道,溶解渗流通道中的堵塞物或造成人工裂缝,使油气通道畅通,以达到油气增产的目的[1]。
双水杨醛缩乙二胺Schiff 碱及其镍(Ⅱ)配合物的合成与表征
摘要:本实验以水杨醛、乙二胺、硝酸镍为原料,采用加热、回流等方法合成了席夫碱配体及其Ni(Ⅱ)配合物。
并采用红外光谱、EDTA直接滴定法、测定熔点等途径对化合物进行表征。
关键词:水杨醛;乙二胺;席夫碱;镍;红外光谱
水杨醛及其衍生物是重要的有机合成中间体。
由水杨醛及其衍生物与胺类化合物反应生成的席夫碱与其金属配位生成的金属配合物在医药、催化、分析化学、腐蚀和光致变色领域有着重要应用,因而受到人们的广泛关注。
本文对回流条件下双水杨醛缩乙二胺Schiff 碱
及其镍(Ⅱ)配合物的合成进行了研究,并对其进行表征。
一、实验部分
(一)主要仪器和药品
药品:水杨醛、乙二胺、95%乙醇、85%乙醇、无水乙醇、2mol/L HCl溶液、Ni(NO3)2·6H2O。
仪器:天平、红外光谱仪、熔点仪、毛细管圆底烧瓶、磁力搅拌器、球形冷凝管、布氏漏斗、温度计、酸式滴定管(50mL)、锥形瓶、烧杯。
材料:滤瓶、pH试纸
反应物参数:
(二)实验原理
1.双水杨醛缩乙二胺Schiff碱及其镍(Ⅱ)配合物的合成
Schiff碱的合成是涉及到加成、重排、消去等过程的一种缩合反应。
反应物的立体结构及电子效应在合成中起着重要作用,其反应机理如下图:
本实验采用水杨醛和乙二胺在75℃的条件下用回流法制备相应的Schiff碱,反应方程式如下所示:
席夫碱基团通过碳氧双键(-C=N-)上的氮原子与相邻的具有孤对电子的氧(O)、硫(S)、磷(P)原子作为给体与金属原子配对,所以氮原子相邻位置存在这类原子的Schiff碱往往具有高配位能力。
2.金属配合物的表征
(1)金属配合物的稳定性受很多因素的影响,通常可以用加热或改变溶液的酸碱性来破坏。
(2)游离出来的Ni离子在pH=10条件下,以紫脲酸铵为指示剂用EDTA直接滴定,由此可计算出Ni的量。
(3)用熔点仪测定配体及其配合物的熔点。
(4)用红外光谱仪测定配体席夫碱及其配合物的红外光谱图。
(三)实验装置图
(四)实验内容
1.Schiff 碱配体及其镍(Ⅱ)配合物的合成
2.化合物的表征
3.不同条件对席夫碱合成的影响
表1 配合物的合成数据记录
表2 不同反应时间对Schiff碱合成产率的影响表
实验条件:溶液PH=9,水浴温度75℃
表3 不同反应温度对Schiff碱合成产率的影响表
实验条件:溶液PH=9,反应时间60min
表4 溶液不同PH对Schiff碱合成产率的影响表
实验条件:水浴温度75℃,反应时间60min
4.熔点的测定
二、实验数据分析
1.实验数据记录:
2.配体产率计算:
m理论=n理论×M配体=
产率=m产品/m理论=
4.配合物产率计算:
配合物理论产量m理论:
n配体=m配体/M配体=
三、结果分析与讨论:。