实验肥皂的制备
- 格式:docx
- 大小:9.75 KB
- 文档页数:1

肥皂制取的原理
肥皂制取的原理是通过皂化反应将动植物油脂中的三酸甘油酯转化为甘油和皂基盐。
皂基盐由长链脂肪酸与碱反应形成,其中碱一般为氢氧化钠或氢氧化钾。
在制取肥皂的过程中,首先将动植物油脂与碱溶液混合,加热搅拌。
碱能够溶解油脂,并与油脂中的脂肪酸发生皂化反应,生成皂基盐。
这个过程是一个水解反应,同时生成甘油。
接着,通过加热去除反应中剩余的水分,并增加混合物的浓度。
浓缩后的混合物冷却并过滤,去除其中的杂质。
这样得到的浓汁继续加热蒸发,直到形成固体的皂基盐。
最后,将固体的皂基盐切割成形状各异的肥皂块,再经过晾晒和成熟处理,使其逐渐硬化,使得肥皂具有稳定的形状和质地。
总之,肥皂制取的原理是通过皂化反应将动植物油脂中的脂肪酸与碱反应生成皂基盐,同时生成甘油。
最后通过干燥和成熟处理,得到最终的肥皂产品。

草木灰制肥皂实验步骤简介肥皂是一种常见的洗涤用品,它具有清洁、杀菌和去除油脂的作用。
而草木灰制肥皂则是一种传统的制皂方法,利用草木灰中的碱性成分与动植物油脂反应生成皂化物。
本实验将介绍草木灰制肥皂的实验步骤。
材料与设备•草木灰:可以从燃烧过的木材或植物中获取。
•动植物油脂:可以使用橄榄油、花生油等常见油脂。
•水:用于溶解草木灰和稀释油脂。
•火锅:用于加热混合溶液。
•温度计:用于测量混合溶液的温度。
•搅拌棒:用于搅拌混合溶液。
实验步骤步骤一:准备草木灰水溶液1.将一定量的草木灰放入一个容器中。
2.加入适量的水,与草木灰充分搅拌,使草木灰溶解在水中。
3.静置一段时间,待草木灰沉淀到底部。
4.将上层清澈的草木灰水溶液取出备用。
步骤二:制备油脂溶液1.选择一种动植物油脂作为原料,如橄榄油或花生油。
2.将一定量的油脂倒入一个容器中。
3.加入适量的水,与油脂充分混合。
4.用温度计测量混合溶液的温度,并记录下来。
步骤三:混合草木灰水溶液和油脂溶液1.将步骤一中制备好的草木灰水溶液倒入步骤二中制备好的油脂溶液中。
2.用搅拌棒充分搅拌混合溶液,直至形成均匀的混合物。
步骤四:加热混合溶液1.将步骤三中得到的混合溶液倒入火锅中。
2.将火锅加热至60-70摄氏度,并保持稳定的温度。
3.持续加热混合溶液,直至它开始变得黏稠。
步骤五:冷却与固化1.关闭火源,让加热后的混合溶液自然冷却至室温。
2.当混合溶液冷却到一定程度时,它会逐渐固化成块状物质。
3.将固化后的物质取出,用刀切割成所需形状和大小的肥皂。
实验注意事项1.实验过程中应注意安全,避免接触高温溶液和燃烧物。
2.在制备草木灰水溶液时,应充分搅拌使草木灰溶解,并去除沉淀。
3.混合草木灰水溶液和油脂溶液时,要确保充分搅拌均匀。
4.加热混合溶液时要控制好温度,避免过高或过低。
5.在固化过程中要等待足够的时间,以确保肥皂完全固化。
结论通过以上步骤,我们成功地制备了草木灰制肥皂。

肥皂的制作的实验报告(共10篇)实验一:肥皂的制作实验目的:掌握肥皂的制备方法,理解肥皂的制作过程及其化学原理。
实验原理:肥皂是通过油脂和碱溶液的反应制得的。
脂肪酸在碱性介质下水解成为石碱盐和甘油。
石碱盐是肥皂的主要成分。
实验仪器:量杯、三角瓶、磁力搅拌器、电子天平、试管、滴管、玻璃棒、平衡杆、温度计。
实验材料:食用油、NaOH、水、酒精、酚酞指示剂等。
实验步骤:1.在天平上精确称取随意确定的食用油20g,并将其倒入三角瓶中。
2.称量NaOH 4.25g,并在试管中加入30mL的蒸馏水中,搅动至NaOH溶解。
3.将NaOH溶液倒入三角瓶中的油中搅动,使其完全混合。
4.加热至沸腾,并继续加热5min。
5.用滴管滴加些许的酚酞指示剂,得到淡红色的混合物。
6.不断搅拌,加入适量的酒精,颜色逐渐变浅。
7.冷却后剥离肥皂,用水冲洗,待风干。
实验结果:得到了白色的肥皂。
实验结论:通过上述实验,成功制备出白色肥皂。
肥皂的制作是一种化学反应,它的原料是食用油和NaOH溶液。
这是非常有趣的实验,可以让人深入了解化学反应的过程。
然而,需要注意的是,NaOH是一种腐蚀性化学物质,使用时一定要小心谨慎。
实验二:肥皂的表面张力实验实验原理:表面张力是指液体表面上的分子间相互作用力和分子间和固体表面(容器壁)间的相互作用力所形成的张力,仅存在于液体和气体接触面上。
表面张力的大小与分子间作用力有关。
实验仪器:容器、水、肥皂碎、纸片等。
实验材料:五种不同品牌的肥皂。
1.分别将五种肥皂放入容器中,并加适量的水搅拌。
2.在每个容器中,放入纸片,计时。
3.观察五种肥皂的表面张力,记录时间。
实验结果:不同肥皂的表面张力不同,表面张力最小的是排名第一的肥皂,最大的是排名第五的肥皂。
实验结论:通过表面张力实验,我们已经确定了五个不同品牌肥皂的表面张力。
我们发现,表面张力最强的肥皂较难在水表面上停留很长一段时间,而表面张力最小的肥皂则能停留很长一段时间。

肥皂的制备及其原理
肥皂的制作及其原理
⼀、实验名称
肥皂的制作及其原理
⼆、实验⽬的
1.了解肥皂的性质
2.懂得如何制备肥皂
3.掌握盐析的原理
三、实验原理
1.肥皂是脂肪酸⾦属盐的总称。
通式为RCOOM,式中RCOO为脂肪酸根,M为⾦属
离⼦。
⼴义上,油脂、蜡、松⾹或脂肪酸等和碱类起皂化或中和反应所得的脂肪酸盐,皆可称为肥皂。
肥皂能溶于⽔,有洗涤去污作⽤。
肥皂的各类有⾹皂,⼜称盥洗皂、
⾦属皂和复合皂。
2.油脂的主要成分是⾼级脂肪酸的⽢油酯,油脂在碱性条件下⽔解⽣成肥皂的主要成分
——⾼级脂肪酸的钠盐。
⽅程式如下
四、主要试剂及仪器
1.试剂:猪油(或其他动植物脂或油),NaOH,95%酒精,饱和⾷盐⽔。
2.仪器:150及300mL烧杯各⼀个,玻棒、酒精灯、⽯棉⽹,三脚架。
五、实验步骤
六、注意事项
1.皂化反应时要保持混合液的原有体积,不能让烧杯⾥的混合液煮⼲或者溅溢到烧杯外⾯。
2.加热时若不⽤⽔浴,则需⽤⼩⽕。
七、数据记录与处理
⼋、思考题
1.加热时为什么要慢慢加热?
答:使其能够均匀受热,反应能够更加充分。

皂化反应实验过程与现象
皂化反应是一种化学反应,通常是通过碱与脂肪酸的反应来制备肥皂。
这种反应在日常生活中十分常见,因为肥皂是我们日常生活中必不可少的清洁用品。
本文将介绍皂化反应的实验过程和现象。
实验过程:
1. 准备所需材料:
-脂肪酸(如椰子油、橄榄油等)
-碱(如氢氧化钠、氢氧化钾等)
-水
-酚酞指示剂
-玻璃棒
-烧杯和容量瓶
2. 在烧杯中加入一定量的脂肪酸。
3. 用容量瓶加入适量的水,并将其加入烧杯中,直到脂肪酸完全覆盖。
4. 加入少量的酚酞指示剂,搅拌均匀。
5. 在另一个烧杯中,加入一定量的碱。
6. 逐渐将碱溶液加入脂肪酸中,并用玻璃棒搅拌。
7. 持续搅拌,直到混合物变得均一。
8. 对混合物进行酸碱指示剂的测试,直到指示剂变色,说明反应完成。
现象:
皂化反应是一种酸碱中和反应,它会将脂肪酸和碱中的羧酸根离子结合在一起,形成肥皂和甘油。
当碱溶液加入脂肪酸时,混合物会开始变得混浊。
这是由于烷基酸钠(肥皂)和甘油在水中形成的微小胶体颗粒。
随着反应的进行,混合物会变得越来越粘稠,并最终形成固体块状物质。
此时,反应已经完成,我们可以用酸碱指示剂进行测试,以确定反应是否发生。
总的来说,皂化反应是一种简单而有趣的实验。
它不仅可以让我们了解化学反应的基本原理,同时也是制备肥皂的重要步骤。
通过实验,我们可以更好地理解自然界中发生的化学反应,并探索更多有趣的化学现象。
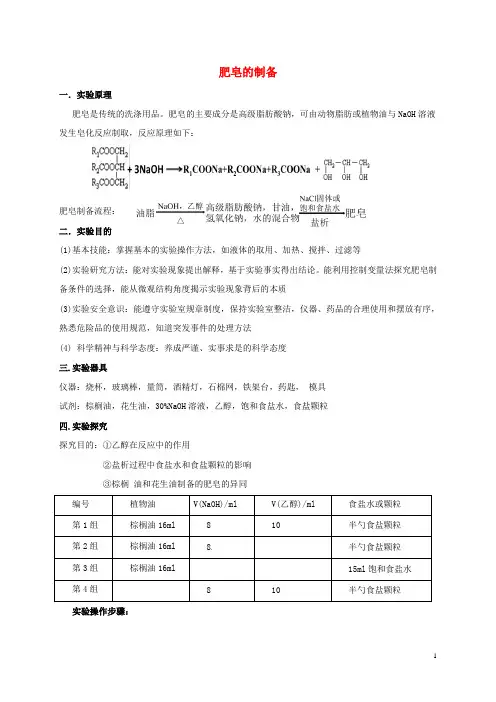
肥皂的制备一.实验原理肥皂是传统的洗涤用品。
肥皂的主要成分是高级脂肪酸钠,可由动物脂肪或植物油与NaOH溶液发生皂化反应制取,反应原理如下:肥皂制备流程:二.实验目的(1)基本技能:掌握基本的实验操作方法,如液体的取用、加热、搅拌、过滤等(2)实验研究方法:能对实验现象提出解释,基于实验事实得出结论。
能利用控制变量法探究肥皂制备条件的选择,能从微观结构角度揭示实验现象背后的本质(3)实验安全意识:能遵守实验室规章制度,保持实验室整洁,仪器、药品的合理使用和摆放有序,熟悉危险品的使用规范,知道突发事件的处理方法(4) 科学精神与科学态度:养成严谨、实事求是的科学态度三.实验器具仪器:烧杯,玻璃棒,量筒,酒精灯,石棉网,铁架台,药匙,模具试剂:棕榈油,花生油,30%NaOH溶液,乙醇,饱和食盐水,食盐颗粒四.实验探究探究目的:①乙醇在反应中的作用②盐析过程中食盐水和食盐颗粒的影响③棕榈油和花生油制备的肥皂的异同实验操作步骤:向皂化产五.课堂学习活动设计学生实验结束后,根据四组对比实验,设计了三个课堂学习活动,并阐述课堂学习活动设计的意图。
学习活动1:乙醇对反应的影响,加入乙醇的作用?请从乙醇,水和酯结构的角度分析乙醇具有上述作用的原因。
活动设计意图分析:通过第一组和第二组的对比实验,让学生直观的体会乙醇在整个反应过程中起到溶解碱,又溶解油脂,使皂化反应在均相(同一溶剂的溶液)中充分接触,加快反应速率的作用,再从微观结构的角度理解乙醇起到溶解作用的本质原因。
如图1所示:图1 乙醇,水和软脂酸甘油酯的结构分析软脂酸甘油酯能和乙醇溶解一方面是由于软脂酸甘油酯中羰基氧和乙醇中羟基氢间存在氢键,另一方面是由于乙醇中烃基和软脂酸甘油酯中长链的烃基间存在范德华力,是这两种分子间力相互作用的结果。
乙醇、水和软脂酸甘油酯的结构分析乙醇溶解性的实质,使学生的视野从宏观走向微观,从现象转向本质,让学生形成从实验现象背后揭示微观本质的探究思路,拓宽学生的分析实验现象的思路。

肥皂的制备方法一、肥皂的原料和工具准备制作肥皂所需的原料主要包括植物油(如橄榄油、椰子油、棕榈油等)、碱性物质(如氢氧化钠或氢氧化钾)、水以及添加剂(如香精、色素等)。
工具方面,需要准备一个大容器用来混合材料、一个搅拌器或勺子用来搅拌、一个温度计用来监测温度、模具用来整形肥皂。
二、制作肥皂的步骤1. 准备工作:将植物油、碱性物质和水按照一定比例称量好,保证原料的准确性。
2. 溶解碱性物质:将碱性物质慢慢加入水中,搅拌溶解直至完全溶解,注意保持安全距离,避免碱溶液溅到皮肤上。
3. 加入植物油:将溶解好的碱溶液倒入大容器中,再将植物油倒入,用搅拌器或勺子搅拌均匀,直至形成乳化液。
4. 混合搅拌:继续搅拌乳化液,直至达到搅拌到浆糊状的状态,这个过程称为皂化反应。
5. 加入添加剂:根据需要,可以在浆糊状的状态下加入香精、色素等添加剂,搅拌均匀。
6. 倒入模具:将搅拌好的肥皂浆糊倒入模具中,可以选择不同的形状和大小。
7. 静置固化:将模具中的肥皂放置在通风干燥的地方,静置固化,一般需要数小时至数天不等。
8. 切割成块:待肥皂完全固化后,可以将其取出并切割成所需大小的肥皂块。
9. 晾干储存:将切割好的肥皂块放置在通风干燥的地方,晾干储存,以便后续使用。
三、注意事项1. 在制作肥皂时,应戴上手套、护目镜等防护用具,避免碱溶液溅到皮肤或眼睛上。
2. 搅拌时要均匀有力,确保原料充分混合。
3. 在加入添加剂时,应根据个人喜好和需要适量添加,避免添加过多导致肥皂过于香浓或色彩过于浓烈。
4. 切割肥皂时要使用锋利的刀具,并注意安全,避免划伤皮肤。
5. 制作肥皂的环境要通风良好,避免有异味或灰尘污染。
通过以上步骤,我们可以制作出自己喜欢的肥皂,既环保又健康。
制作肥皂也是一项有趣的手工活动,可以根据个人口味和喜好调配不同的香味和颜色,制作出独一无二的肥皂。
同时,在制作肥皂的过程中,我们也可以了解到肥皂的原理和化学反应,充实自己的知识。

实验一肥皂的制备及去污能力测定一、实验目的①学习洗涤剂的基本知识,熟悉肥皂、透明皂的制造原理和方法。
②掌握肥皂、透明皂的制备工艺和制备技术;③了解洗涤剂去污能力测定的方法。
二、实验原理肥皂是高级脂肪酸金属盐(钠、钾盐为主)类的总称,包括软皂、硬皂、香皂和透明皂等。
肥皂是最早使用的洗涤用品,对皮肤刺激性小,具有便于携带,使用方便、去污力强、泡沫适中和洗后容易去除等优点。
所以尽管近年来各种新型的洗涤剂不断涌现,但它仍是一种深受用户欢迎的去污和沐浴用品。
以各种天然的动、植物油脂为原料,经碱皂化而制得肥皂,是目前仍在使用的生产肥皂的传统方法。
CH2OCOR1CH2OCOR2CH2OCOR3NaOHH OCH2OHCH2OHCH2OHR1COONaR2COONaR3COONa 3不同种类的油脂,由于其组成有别,皂化时需要的碱量不同。
碱的用量与各种油脂的皂化值(完全皂化l g油脂所需的氢氧化钾的毫克数)和酸值有关。
以下是一些油脂的皂化值。
现将用于制肥皂的主要原料的性质和作用进行简单的介绍。
油脂油脂指植物油和动物脂肪,在制肥皂过程中它提供长链脂肪酸。
由于以C12~C18的脂肪酸所构成的肥皂洗涤效果最好,所以制肥皂的常用油脂是椰子油(C12为主)、棕榈油(C16~C18为主)、猪油或牛油(C16~C18为主)等。
脂肪酸的不饱和度会对肥皂品质产生影响。
不饱和度高的脂肪酸制成的皂,质软而难成块状,抗硬水性能也较差。
所以通常要把部分油脂催化加氢使之成为氢化油(或称硬化油),然后与其它油脂搭配使用。
碱主要使用碱金属氢氧化物。
由碱金属氢氧化物制成的肥皂具有良好的水溶性。
由碱土金属氢氧化物制得肥皂一般称作金属皂,难溶于水,主要用作涂料的催干剂和乳化剂,不作洗涤剂使用。
皂化油脂的精练:(1)脱胶处理(水化法,酸炼法):用于除去溶解于油脂中的磷脂质、蛋白质以及结构复杂的胶质和粘液质。
(2)脱酸处理(碱炼法):除去游离酸。
(3)脱色处理(使用活性白土或活性炭的物理吸附脱色,化学氧化脱色):除去油脂中的各种色素。

肥皂与化学实验报告实验目的本实验的目的是通过制备肥皂的过程,了解肥皂的化学组成、制备方法以及其在清洁和去污方面的应用。
实验原理肥皂是一种由脂肪酸钠或脂肪酸钾和碱反应生成的盐类。
在制备肥皂的过程中,通过将油脂与碱反应,使油脂中的三酸甘油酯水解为甘油和脂肪酸。
而脂肪酸与碱反应后形成的盐即为肥皂。
具体的化学反应可以表示为:油脂+ NaOH →甘油+ 脂肪酸钠实验材料1. 植物油:200ml2. NaOH:20g3. 酒精:30ml4. 水:400ml5. 烧杯、玻璃棒、玻璃器皿等实验用具实验步骤1. 将200ml植物油倒入玻璃器皿中。
2. 称取20g的NaOH。
3. 在烧杯中加入30ml的酒精,然后将NaOH加入酒精中,并搅拌使其溶解。
4. 将溶解好的酒精与NaOH的混合液缓慢倒入装有植物油的玻璃器皿中,并不断搅拌。
5. 继续搅拌,直到混合物开始变得稠固状。
6. 将塑料薄膜覆盖在玻璃器皿上,使混合物充分反应。
7. 将玻璃器皿放置在室温下,静置一晚,待肥皂凝固。
8. 用水冲洗凝固后的肥皂,使其完全清洁。
9. 将肥皂切成适当大小的块状,并晾干。
实验结果与分析经过制备,我们成功得到了一块坚固的肥皂。
肥皂的形状和质地均与市售的肥皂相似。
在制备过程中,植物油与NaOH反应生成了肥皂,同时产生了甘油作为副产物。
肥皂的生成使得原本不溶于水的油脂变成了可溶性的,从而提高了清洁能力。
甘油具有保湿和抗菌的特性,常用于化妆品和药品中。
实验总结通过本次实验,我们深入了解了肥皂的化学组成和制备过程。
肥皂作为一种常用的清洁用品,在日常生活中发挥着重要的作用。
通过肥皂的制备实验,我们更加清楚地了解了油脂与碱的反应原理,以及肥皂的应用领域。
然而,在实验中也需要注意安全问题。
NaOH是一种强碱,具有腐蚀性,在操作过程中应避免接触皮肤和眼睛。
实验结束后需及时清洗实验器材,并注意妥善处理废液。
总的来说,这次肥皂制备实验让我们对肥皂的制备原理、化学反应过程和应用有了更加全面的了解。

二、各种肥皂的制取[原理]高级脂肪酸盐(主要是碱金属钾、钠)虽是肥皂的主要成分,但由于需要不同,制造过程的步骤不同,以及应用原料、水质的不同,会产生很多不同的肥皂。
使用肥皂洗涤能去污,也能使皮肤发生易干裂的现象。
为此,在不影响去污的基础上,采用中性油脂、橄榄油、羊毛脂等,就可制得过脂皂。
[用品]1.仪器烧瓶、硬试管、铁架台及附件、搅拌玻璃棒、烧杯、温度计、导管、乳胶管和酒精灯等。
2.试剂皂液、蓖麻油、松香、糖、乙醇、甘油、椰子油、10mol·L-1氢氧化钠溶液、氢氧化钾溶液、棕榈油、植物油、月桂醚硫酸二乙醇胺盐、椰子酰二乙醇胺、亚麻仁、硬脂酸乙二醇酯、二乙醇按、烷基醚硫酸铵、合成蜡、月桂基硫酸钠、椰子酰丙基甜菜碱、柠檬酸、氯化钠、椰子油酸、油酸、三乙醇胺、苦杏仁油、皂用抗氧剂、聚乙二醇、季铵化合物、去离子水、硅酸镁铝、丙二醇、氢氧化钠溶液(密度1.168g/cm3)、精制豆油、葵子油、香料、二氧化钛等。
[操作](一)液体皂和软皂1.液体皂。
在盛水的烧杯中要保持水温达到70~72℃后,慢慢加入椰子油酰丙基甜菜碱,不断搅匀,待降温至58℃时,再加防腐剂和香料,并持续搅拌半小时,用柠檬酸调到pH6.0±2,再用氯化钠调节粘度,等到温度低于46℃时,即可以取出。
液体皂的配方如下:合蜡1.5%,月桂基硫酸钠29.0%,椰子酰二乙醇胺2%,椰子酰丙基甜菜碱6%,水61.5%。
这种肥皂能使皮肤脱脂,合成蜡能以珍珠般的泡沫提高柔润感,它在皮肤上行成无油腻感的保护膜。
2.软皂。
在烧瓶中放进亚麻油或大豆油50mL并在水浴上加热,保持80℃时,把10mol·L-1氢氧化钠溶液60mL慢慢加入瓶内,随加随振荡,或搅拌,使其成透明的肥皂液,再把5mL乙醇倒入、不断溶解,如透明就可以蒸发一段时间。
当看到液体有淡黄色、黄绿色和黄棕色的透明、且粘滑的软块出现时,即可倾出。
软皂可用于外科手术前洗手,作灌肠剂时调成5%的溶液,制成搽剂,也可以医治关节神经痛等。

肥皂的制备实验步骤嘿,朋友们!今天咱来聊聊肥皂的制备实验步骤,这可有意思啦!先说说准备工作吧,就像要出门得先收拾好自己一样。
得准备好油脂,这可是肥皂的重要原料呢,就像做饭得有食材呀!然后呢,还得有碱液,这碱液就像是给肥皂注入灵魂的魔法药水。
还有模具呀,这就是肥皂成型的小窝啦!接下来就开始动手啦!把油脂加热融化,这感觉就像是给油脂洗了个舒服的热水澡。
然后慢慢把碱液加进去,可别一下子倒太多哦,就像给汤调味一样,得慢慢加。
这时候可得小心,别让碱液溅到自己身上,不然可就糟糕啦!然后就是搅拌啦,不停地搅拌,就好像在给它们跳一场欢快的舞蹈。
看着油脂和碱液慢慢融合在一起,变得越来越浓稠,嘿,这感觉真奇妙!就像是看着两个陌生人慢慢变成好朋友一样。
等搅拌得差不多了,就把这混合物倒入模具里。
哎呀呀,这就像是给它们找到了一个温暖的家。
然后把模具放一边,让它们安安静静地待着,等着慢慢变成肥皂。
在这个过程中,可别着急哦,就像等待一朵花慢慢开放一样,得有耐心。
说不定你会忍不住一直去看看它们,心里想着:“哎呀,怎么还没好呀!”哈哈,这就是期待的心情呀!等呀等呀,终于到了脱模的时候啦!小心翼翼地把肥皂从模具里取出来,哇,一块崭新的肥皂就出现啦!看着自己亲手做出来的肥皂,是不是心里特别有成就感呢?想想看,以后洗手的时候就可以用自己做的肥皂啦,那感觉肯定不一样。
而且你还可以根据自己的喜好,加入一些香味呀,或者加点颜色,让肥皂变得独一无二。
做肥皂的实验就像是一场小小的冒险,有惊喜,有期待,还有满满的成就感。
朋友们,不妨自己动手试试呀,说不定你会爱上这个有趣的过程呢!反正我是觉得挺好玩的,相信你们也一定会喜欢的!就这么愉快地决定啦,赶紧去试试吧!。
一、实验目的1. 掌握肥皂的制备方法。
2. 理解肥皂的制作过程及其化学原理。
3. 了解肥皂在生产过程中的注意事项。
二、实验原理肥皂的制备原理是油脂与碱溶液发生皂化反应,生成高级脂肪酸钠(肥皂)和甘油。
化学方程式如下:\[ (C_{17}H_{35}COO)_3C_3H_5 + 3NaOH \rightarrow 3C_{17}H_{35}COONa +C_3H_5(OH)_3 \]三、实验材料与仪器材料:1. 新鲜动物脂肪(如牛油)5g2. 95%乙醇6ml3. 40%氢氧化钠溶液6ml4. 热饱和食盐水60ml5. 烧杯、玻璃棒、滤纸、药匙、试管、热水、铁丝框仪器:1. 微热设备2. 烧杯3. 玻璃棒4. 滤纸5. 药匙6. 试管8. 铁丝框四、实验步骤1. 准备阶段:将新鲜动物脂肪切成小块,放入烧杯中。
2. 溶解阶段:向烧杯中加入6ml 95%乙醇,用微热设备加热,使脂肪完全溶解。
3. 反应阶段:在溶解后的反应液中加入6ml 40%氢氧化钠溶液,边搅拌边加热,直至反应液变成黄棕色黏稠状。
4. 检测阶段:用玻璃棒蘸取反应液,滴入装有热水的试管中,振荡。
若无油滴浮在液面上,说明反应液中的油脂已完全反应;否则,继续加热使反应完全。
5. 盐析阶段:在反应液中加入60ml热的饱和食盐水,搅拌,使反应液中的物质盐析出来。
6. 分离阶段:用药匙将浮在液面上的固体物质取出,用滤纸或纱布沥干,挤压成块,即为肥皂。
五、实验现象1. 加入NaOH后,反应液变成棕黄色黏稠状。
2. 挤压成块后,肥皂呈乳白色固体,并有淡淡的腥味。
六、实验结果与分析1. 实验结果表明,通过皂化反应,我们可以成功制备肥皂。
2. 在实验过程中,反应液颜色的变化和盐析现象都是皂化反应发生的标志。
3. 通过控制反应条件,我们可以制备出不同类型的肥皂。
七、注意事项1. 在加热过程中,要注意控制温度,避免过热导致反应液溢出。
2. 在搅拌过程中,要小心操作,避免溅出反应液。
第1篇一、实验目的1. 了解肥皂的制备原理及工艺流程。
2. 掌握手工肥皂的制作方法,包括皂化反应、皂化液搅拌、入模、保温、脱模、切割和晾干等步骤。
3. 培养实验操作技能,提高实验数据分析能力。
二、实验原理肥皂的制备过程主要涉及皂化反应,即碱催化下的酯水解反应。
在皂化反应中,油脂与氢氧化钠(NaOH)发生反应,生成高级脂肪酸钠(肥皂)和甘油。
具体反应式如下:油脂+ NaOH → 高级脂肪酸钠 + 甘油三、实验材料与仪器1. 实验材料:- 椰子油 100g- 棕榈油 150g- 橄榄油 250g- 氢氧化钠 73g- 水 219g- 精油、香精(可选)- 超脂油脂(可选)2. 实验仪器:- 化工量杯- 温度计- 不锈钢锅- 橡皮刮刀- 打蛋器(或电动搅拌器)- 计量匙- 模子- 手套- 磅秤- 护目镜(或眼镜)- 围裙- 刀子- 刮刀- 模型- 温度计- 量匙- 不锈钢杯- 电子称四、实验步骤1. 称量:准确称量所需氢氧化钠的量,并加入配方所需水量。
注意:氢氧化钠具有腐蚀性,请在通风处使用并小心谨慎。
2. 溶解:将氢氧化钠加入水中,搅拌至完全溶解。
待溶液温度降至50度左右。
3. 加热油脂:将椰子油、棕榈油和橄榄油加入不锈钢锅中,加热至50度左右。
4. 搅拌:将碱水慢慢倒入油锅中,并充分搅拌均匀。
5. 皂化反应:继续搅拌皂液,观察皂液逐渐变为浓稠,用刮刀划过能有明显不会消失的痕迹(约30分钟)。
6. 添加香料:如需添加精油、香精或超脂油脂,搅拌均匀。
7. 入模:将皂液倒入模具中,并用刮刀刮平。
8. 保温:将模具放入泡沫箱或包裹毛毯进行保温,约24~48小时后即可脱模。
9. 脱模与切割:将肥皂从模具中取出,切成适当大小。
10. 晾干:将肥皂置于通风处晾干,避免日光直射。
11. 使用:4周后即可使用。
五、实验结果与分析1. 通过实验,成功制备出手工肥皂,验证了皂化反应原理。
2. 在实验过程中,注意控制皂化反应的温度、时间和搅拌程度,以保证肥皂的质量。
制备肥皂原理
肥皂是一种常见的清洁用品,其制备的原理是通过皂化反应将油脂或脂肪酸与碱发生化学反应,生成皂基和甘油。
制备肥皂的关键步骤如下:
1. 提取油脂:选择植物油或动物脂肪作为原料,可以使用冷压、溶剂提取等方法将油脂从植物或动物的种子、果实或组织中提取出来。
2. 精炼油脂:通过去除杂质、酸值调整等工艺步骤,使得油脂达到制备肥皂的要求。
3. 配制碱液:使用氢氧化钠或氢氧化钾与水反应,生成碱液。
4. 反应混合:将精炼的油脂和配制好的碱液混合,搅拌均匀。
5. 皂化反应:在搅拌过程中,碱液与油脂中的脂肪酸发生皂化反应。
皂化反应是一种酯水解反应,通过将脂肪酸与碱反应,生成皂基和甘油。
6. 放置静置:将反应混合物放置一段时间,让其中的皂基和未反应的酯类等杂质沉淀。
7. 分离甘油:将沉淀的混合物经过过滤、离心等操作分离出甘油。
8. 清洗与干燥:用热水反复清洗分离出的肥皂。
清洗过程中可加入食盐,以帮助肥皂凝固。
清洗完毕后,将肥皂晾干。
以上便是制备肥皂的原理和步骤,通过以上反应和处理,我们可以得到洗净力强、质地柔软的肥皂。
实验三 肥皂的制备一、目的要求1. 了解肥皂的制取过程,认识油脂的重要性质——皂化反应;2. 通过实验激发学生的学习兴趣,训练实验操作技能;3. 通过实验培养学生严谨、求实的科学态度和科学方法。
二、实验原理脂肪或油脂和强碱在一定温度下水解产生脂肪酸钠盐和甘油的混合物,称为皂化反应。
若把氯化钠加入到反应混合物中,可通过盐析作用,把产生的脂肪酸钠分离出来,即可得到肥皂。
皂化反应反应式如下:CHOCOR CH 2OCORCH 2OCOR + 3NaOHCH 2OHCHOHCH 2OH R 基可能不同,但生成的R-COONa 都可以做肥皂。
常见的R-有:C 17H 38-:8-十七碳烯基。
R-COOH 为油酸。
C 15H 31-:正十五烷基。
R-COOH 为软脂酸。
C 17H 35-:正十七烷基。
R-COOH 为硬脂酸。
三、实验仪器和药品1. 仪器150毫升烧杯2个,玻棒、酒精灯、石棉网,三脚架,量筒、托盘天平、药匙、纱布、冰箱。
2. 试剂药品猪油(或其他动植物脂或油),40% NaOH 溶液,95%酒精,50%酒精 饱和食盐水:称9g 溶于25ml 水中。
四、实验步骤1. 在150ml 烧杯里,盛8ml 植物油和8ml 95%的酒精,然后加7ml 40%的NaOH 溶液。
用玻棒搅拌,使其溶解。
2. 把烧杯放在石棉网上,用酒精灯小火加热,并不断用玻璃捧搅拌,直到混合物变稠。
当烧杯内的液体快煮干时,加入20ml 50%的酒精溶液。
3. 继续加热直到把一滴混合物加到水中时,在液体表面不再形成油滴为止。
4. 取25ml 加热后的饱和食盐溶液慢慢加到皂化完全的粘稠液中,边加边搅拌,使它们互溶。
置于冰箱冷却10分钟后,有固体物质盐析上浮,待固体物质全部析出后用药匙取出,用滤纸或纱布沥干,挤压成块,即为肥皂。
5. 用天平称量肥皂的质量,并计算产率。
产率=肥皂的质量/油脂的体积×100%。
五、注意事项1. 皂化时,边搅拌边加入乙醇,使油脂与碱液混为一相,加速皂化反应的进行,缩短反应时间。
一、实验目的1. 了解香皂的制备原理和工艺流程。
2. 掌握香皂制备的基本操作步骤。
3. 通过实验,提高动手操作能力和分析问题、解决问题的能力。
二、实验原理香皂的制备原理是利用油脂与碱(如氢氧化钠)发生皂化反应,生成脂肪酸钠盐(即肥皂)和甘油。
在制备过程中,需要控制反应条件,如温度、时间、pH值等,以确保肥皂的质量。
三、实验材料与仪器1. 实验材料:- 植物油(如橄榄油、棕榈油等)- 氢氧化钠- 纯净水- 香精- 色素- 碱液- 烧杯- 搅拌棒- 温度计- 量筒- 电子秤- 香皂模具2. 实验仪器:- 烧杯(500mL)- 搅拌棒- 温度计- 量筒- 电子秤- 香皂模具四、实验步骤1. 准备工作:- 称取适量的植物油、氢氧化钠、纯净水、香精和色素。
- 将烧杯洗净,并用温度计检测其温度。
2. 制备碱液:- 将称取的氢氧化钠加入烧杯中。
- 慢慢加入纯净水,边加边搅拌,直至氢氧化钠完全溶解。
- 将溶液加热至50℃左右,保持一段时间,以便提高反应速度。
3. 制备肥皂:- 将称取的植物油加入烧杯中。
- 将加热至50℃的碱液缓慢倒入植物油中,边倒边搅拌。
- 搅拌过程中,注意观察溶液的pH值,控制在8.5-9.5之间。
- 继续搅拌,使油脂与碱液充分反应,直至形成均匀的肥皂浆。
4. 加入香精和色素:- 在肥皂浆中加入适量的香精和色素,搅拌均匀。
5. 倒入模具:- 将搅拌均匀的肥皂浆倒入香皂模具中。
- 轻轻震动模具,使肥皂浆分布均匀。
6. 成型与脱模:- 将模具放置在通风处,让其自然冷却凝固。
- 冷却至室温后,轻轻取出香皂。
五、实验结果与分析1. 实验结果:- 成功制备出具有香味的彩色香皂。
2. 实验分析:- 在制备过程中,控制好反应条件(如温度、pH值等)对肥皂质量有很大影响。
- 加入适量的香精和色素,可以改善香皂的口感和外观。
- 通过本次实验,掌握了香皂制备的基本操作步骤,提高了动手操作能力。
六、实验总结通过本次香皂制备实验,我们了解了香皂的制备原理和工艺流程,掌握了香皂制备的基本操作步骤。
消泡剂的选择:
肥皂的制备:
药品:硬脂酸、植物油、氯化钠、氢氧化钠、乙醇、氢氧化钾仪器设备:酒精灯、蒸发皿、玻璃棒、烧杯
实验原理
实验步骤
8毫升植物油,8毫升无水乙醇,4毫升30%的氢氧化钠加入到铁架台上的蒸发皿中,点燃酒精灯用玻璃棒不断搅拌,待混合物变稠时用胶头滴管吸取混合物加入到盛有水的烧杯中并不断搅拌,观察直至水面无油滴时停止加热。
将蒸发皿放到冷水浴中降温,向混合物中加入20毫升蒸馏水,继续放在冷水中冷却,一段时间后向蒸发皿中加入氯化钠饱和溶液,有白色固态物质析出浮在水面上。
最后将蒸发皿中的混合物进行抽滤,滤去含有甘油的虑液剩下为肥皂。
实验二肥皂的制备及蚕丝皂碱法脱胶实验实验肥皂的制备
【实验目的】
1、了解肥皂的制备原理和制备方法
2、了解盐析的原理和方法
【实验原理】
脂肪或油脂和强碱在一定温度下水解产生一种脂肪酸钠盐和甘油的混合物,把氯化钠加入到反应混合物中,通过盐析作用,把产生的脂肪酸钠分离出来。
皂化反应得反应式如下:
CH2OCOR
| 加热
CHOCOR + 3NaOH ----> 3R-COONa + CH2OH-CHOH-CH2OH
|
CH2OCOR
R基可能不同,但生成的R-COONa都可以做肥皂。
常见的R-有:
C17H33-:8-十七碳烯基。
R-COOH为油酸。
C15H31-:正十五烷基。
R-COOH为软脂酸。
C17H35-:正十七烷基。
R-COOH为硬脂酸
【实验过程】
一、实验准备
1、仪器:烧杯、量筒、温度计、恒温水浴锅、刻度吸量管、吸耳球、电子天平
2、药品:植物油、氢氧化钠、乙醇、食盐
二、操作步骤
在一个小烧杯中加入5 mL 植物油,5 mL30 %氢氧化钠溶液(mol)和3 mL醇,并将小烧杯置于盛水的大烧杯中,加热大烧杯,同时搅拌大烧杯中小烧杯中的溶液。
20分钟后取出小烧杯,直接加热,至溶液变成奶油般的糊状物,向其中加入5mL热的氯化钠的饱和溶液并搅拌,这一步操作称“盐析”。
静置,冷却,将混合物上层固体取出并用水洗净。
将所得固体放到水中,充分振荡,观察其现象与普通肥皂是否相同。
三、实验报告
计算肥皂的产率。