基因工程制药-3 表达
- 格式:ppt
- 大小:11.12 MB
- 文档页数:74

第一章绪论填空题1. 生物技术制药的特征高技术、高投入、高风险、高收益、长周期。
2. 生物药物广泛应用于医学各领域,按功能用途可分为三类,分别是治疗药物、预防药物、诊断药物。
3.现代生物药物已形成四大类型:一是应用DNA重组技术制造的基因重组多肽、蛋白质类治疗剂;二是基因药物;三是来自动物植物和微生物的天然生物药物;四是合成与部分合成的生物药物;4.生物技术的发展按其技术特征来看,可分为三个不同的发展阶段,传统生物技术阶段;近代生物技术阶段;现代生物技术阶段。
5.生物技术所含的主要技术范畴有基因工程;细胞工程;酶工程;发酵工程;蛋白质核酸工程和生化工程;选择题1.生物技术的核心和关键是(A )A 细胞工程B 蛋白质工程C 酶工程D 基因工程2. 第三代生物技术( A )的出现,大大扩大了现在生物技术的研究范围A 基因工程技术B 蛋白质工程技术C 海洋生物技术D细胞工程技术3.下列哪个产品不是用生物技术生产的(D )A 青霉素B 淀粉酶C 乙醇D 氯化钠4. 下列哪组描述(A )符合是生物技术制药的特征A高技术、高投入、高风险、高收益、长周期B高技术、高投入、低风险、高收益、长周期C高技术、低投入、高风险、高收益、长周期D高技术、高投入、高风险、低收益、短周期5. 我国科学家承担了人类基因组计划(C )的测序工作A10% B5% C 1% D 7%名词解释1.生物技术制药采用现代生物技术可以人为的创造一些条件,借助某些微生物、植物或动物来生产所需的医学药品,称为生物技术制药。
2.生物技术药物一般说来,采用DNA重组技术或其它生物新技术研制的蛋白质或核酸来药物称为生物技术药物。
3.生物药物生物技术药物是重组产品概念在医药领域的扩大应用,并与天然药物、微生物药物、海洋药物和生物制品一起归类为生物生物药物。
简答题1.生物技术药物的特性是什么?生物技术药物的特征是:(1)分子结构复杂(2)具有种属差异特异性(3)治疗针对性强、疗效高(4)稳定性差(5)免疫原性(6)基因稳定性(7)体内半衰期短(8)受体效应(9)多效应和网络效应(10)检验特殊性2.简述生物技术发展的不同阶段的技术特征和代表产品?(1)传统生物技术的技术特征是酿造技术,所得产品的结构较为简单,属于微生物的初级代谢产物。
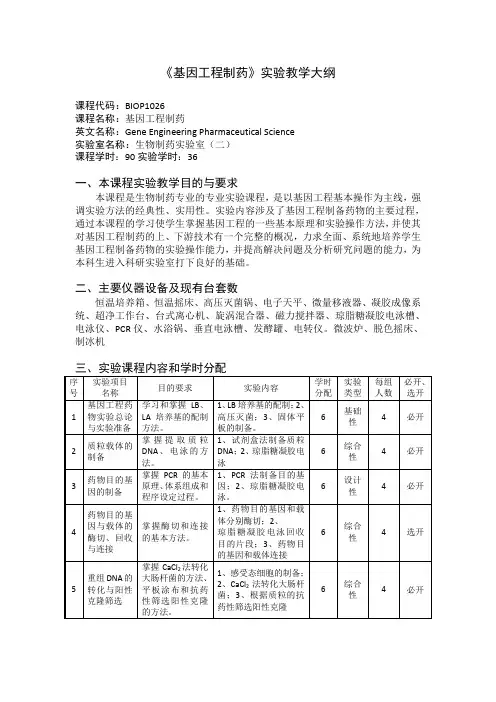
《基因工程制药》实验教学大纲课程代码:BIOP1026课程名称:基因工程制药英文名称:Gene Engineering Pharmaceutical Science实验室名称:生物制药实验室(二)课程学时:90实验学时:36一、本课程实验教学目的与要求本课程是生物制药专业的专业实验课程,是以基因工程基本操作为主线,强调实验方法的经典性、实用性。
实验内容涉及了基因工程制备药物的主要过程,通过本课程的学习使学生掌握基因工程的一些基本原理和实验操作方法,并使其对基因工程制药的上、下游技术有一个完整的概况,力求全面、系统地培养学生基因工程制备药物的实验操作能力,并提高解决问题及分析研究问题的能力,为本科生进入科研实验室打下良好的基础。
二、主要仪器设备及现有台套数恒温培养箱、恒温摇床、高压灭菌锅、电子天平、微量移液器、凝胶成像系统、超净工作台、台式离心机、旋涡混合器、磁力搅拌器、琼脂糖凝胶电泳槽、电泳仪、PCR仪、水浴锅、垂直电泳槽、发酵罐、电转仪。
微波炉、脱色摇床、制冰机三、实验课程内容和学时分配四、考核方式1、实验报告:本门课程要求实验报告应具有“实验目的与要求、原理、实验基本过程、实验结果与讨论”等几个方面的内容。
2、考核方式(1)实验课的考核方式:本课程按等级制评定与考核,评分标准分为:A、B、C、D、E五个等级。
考核主要包括两部分:实验操作技能、实验报告(包括实验预习报告)。
(2)实验课考核成绩确定,实验课成绩占课程总成绩的比例等:在该课程的评定分数中,实验课内容占30%,其中实验课考核又分为两部分,即实验操作技能占实验课总分数的60%、实验报告(包括实验预习报告)占实验课总分数的40%。
五、实验教材、参考书1、教材:自编参考楼士林主编《基因工程》,科学出版社20072、参考书目:(1)基因工程技术实验指导,钟卫鸿主编,化学工业出版社 2007(2)基因工程实验指导,朱旭芬主编,高等教育出版社,2006(3)基因工程实验技术,彭秀玲编著,湖南科学技术出版社 1997《酶工程制药》实验教学大纲课程代码:BIOP1027课程名称:酶工程制药英文名称:Enzyme Engineering Pharmaceutical science实验室名称:药学院实验中心生物制药实验室课程学时:90实验学时:36一、本课程实验教学目的与要求本课程实验教学的目的是让学生掌握酶制剂的发酵生产方法、酶的固定化原理与操作方法、酶分子的修饰原理和实验方法等,加深学生对抽象的理论内容的理解;通过实验训练,培养学生的动手操作能力和观察能力,正确掌握实验仪器的使用方法和实验操作技能,培养学生独立解决问题的能力和严谨的科学态度。


基因工程在生物制药领域的应用探讨作者:匡光永来源:《中国民商》2021年第08期摘要:随着经济社会的发展,生物制药领域开始引入基因工程技术,使用基因工程技术对自身进行改造和发展。
本文从生物制药领域中的基因操作技术分析概念入手,进行以基因工程为基础的其中几类药物类型的分析,从而了解基因工程生物制药所面临的机遇以及需要解决的问题,从而使其得到更好的发展。
关键词:基因工程;生物制药;前景一、生物制药领域中的基因操作技术分析(一)基因大分子分离技术DNA大分子的分离技术,最常用的是DNA电泳。
在电泳之前,首先要提取基因所在的位置,以细菌的质粒DNA为例,现阶段使用的提取方法是碱裂解法,具体是将含有质粒的大肠杆菌用NaOH和SDS混合的变性液进行处理,再用高速离心机离心处理,从而将质粒DNA分离出来。
进一步地,如果想要分离出目的DNA片段,就需要用到DNA电泳技术,常用的电泳是琼脂糖凝胶电泳和聚丙烯酰胺凝胶电泳。
凝胶电泳的原理其实很简单,DNA是一种多聚阴离子,将其放置在电场中,DNA分子就会迁移到正电极的方向,DNA分子的长度越长,携带的净电荷越多,向正电极方向迁移的速率就越快,因此,在电场强度一定的条件下,DNA 分子的迁移速率取决于DNA片段的大小和构型。
电泳的步骤为:配胶-制胶板-样品的处理-点样-电泳-检测。
(二)PCR技术PCR技术,即聚合酶链式反应,是一种体外快速扩增特定DNA片段的技术,可以实现短时间内少量甚至微量DNA分子的大量扩增。
PCR技术是分子克隆技术的基石,是基因工程中必不可少的技术。
PCR技术的原理来源于DNA的半保留复制,在生物体内,DNA的复制过程分为三个阶段:复制的起始、延伸和终止,PCR也分为三个阶段:高温变性、复性和延伸,这三个阶段不断的循环往复,从而得到大量的目的基因。
PCR技术已广泛应用于基因的克隆,分子探针的制备和基因定位等实验中,在生物制药领域中也常用于诊断试剂的开发。



基因工程制药基因工程制药是指利用生物技术手段,通过基因克隆、遗传工程、细胞培养等技术制备的药物。
相比传统的制药技术,基因工程制药具有高效、精准、无毒副作用等优点。
本文将从基因工程制药的概念、制备过程、应用、发展现状等方面进行介绍。
一、基因工程制药的概念基因工程制药是指利用遗传工程技术,将DNA序列插入到细胞内,使细胞能够表达人类所需的有效蛋白质,从而制备出符合医疗需求的药物。
基因工程制药的研发已成为制药业的重要领域,具有广阔的市场前景和潜力。
二、基因工程制药的制备过程基因工程制药的制备过程包括基因选择、基因克隆、载体构建、转染细胞、发酵培养和纯化等步骤。
1、基因选择基因工程制药的制备过程首先要选择适合人体治疗的基因,可以是已知的治疗目标基因,也可以是新发现的疾病相关基因。
2、基因克隆基因克隆是将目标基因从DNA分子复制到载体上的过程。
其中包括PCR扩增、酶切、连接和转化等步骤,最终得到包含目标基因的重组载体。
3、载体构建为了使目标基因的表达量达到较高水平,需要将目标基因克隆到适合的载体中。
典型的载体包括质粒和病毒。
4、转染细胞将重组载体转染到宿主细胞中,宿主细胞将目标基因表达成蛋白质。
常用的宿主细胞有哺乳动物细胞和真菌等。
5、发酵培养将转染后的细胞进行大规模培养,加入培养基和营养成分,进行培养和生长。
由于基因工程制药药物的生产量较大,通常采用发酵技术进行生产。
6、纯化将发酵得到的药物纯化出来,使其达到医药级别要求。
通常采用多种分离纯化技术,如超滤、离子交换和透析等,得到纯度高、活性好的药物制剂。
三、基因工程制药的应用基因工程制药已经广泛应用于多种疾病的治疗中,如慢性病、肿瘤、代谢性疾病和遗传性疾病等。
其中常见的基因工程制药药物有类风湿关节炎药物、肿瘤靶向药物、生长激素、重组人胰岛素和重组人血小板等。
1、类风湿关节炎药物抗肿瘤类药物通过影响免疫系统来治疗类风湿关节炎。
这些药物通常在类风湿关节炎患者无法耐受非甾体类抗炎药物和光合作用药物时使用。




基因工程制药名词解释基因工程制药是指利用基因工程技术生产药物的过程。
以下是基因工程制药常见名词的解释:1. 基因工程:基因工程是一种利用生物技术改变生物体遗传物质的方法。
通过人为选择和转移与特定功能相关的基因,可以改良生物体的性状或让其产生特定的产物。
2. 表达载体:表达载体是指一种DNA分子,用于传递外源基因到宿主细胞中,并使外源基因能够表达出目标蛋白质。
表达载体通常包括启动子、转录终止信号、选择性标记基因等元素。
3. 重组蛋白质:重组蛋白质是通过基因工程技术在外源表达系统中合成的蛋白质。
这些蛋白质通常是具有特定功能或药理学活性的,例如抗体、生长因子和酶等。
4. 重组DNA技术:重组DNA技术是指将不同来源的DNA片段组装到一起,形成新的DNA序列。
这项技术是进行基因工程研究和制药生产的关键步骤之一。
5. 基因转导:基因转导是将外源基因转移到宿主细胞中的过程。
通常通过病毒载体或非病毒载体传递外源基因到宿主细胞中,从而使宿主细胞表达目标蛋白质。
6. 选择标记基因:选择标记基因是用于筛选宿主细胞是否成功转导外源基因的标志性基因。
常见的选择标记基因包括抗生素抗性基因或含有发光标记的基因。
7. 纯化:纯化是将合成的重组蛋白质从杂质中分离出来的过程。
常见的纯化方法包括亲和纯化、离子交换层析和凝胶过滤。
8. 质量控制:质量控制是对基因工程制药产品的开发、生产和分析过程进行监控,以确保产品的质量符合国际质量标准。
质量控制包括产品的物理、化学和生物学测试等。
9. 免疫学制剂:免疫学制剂是一种通过基因工程技术生产的用于治疗疾病的药物。
免疫学制剂包括疫苗、单克隆抗体等,可通过调节和加强免疫系统来预防和治疗疾病。
10. 基因治疗:基因治疗是一种利用基因工程技术修复或替代患者缺陷基因的治疗方法。
通过将正常的基因导入患者体内,可修复或恢复患者体内缺少或异常的基因功能,从而治疗疾病。
基因工程技术在生物制药领域的应用和发展
基因工程技术在生物制药领域的应用和发展具有重要作用,主要表现在以下几个方面:
1. 基因工程生产重组蛋白:通过基因工程技术,可以将感兴趣的基因转入微生物、动植物等宿主中,使其表达所需的蛋白质。
这样可以大规模生产许多重要的蛋白质药物,如细胞因子、抗体、血液凝块因子和疫苗等。
2. 基因工程合成药用基因:通过基因工程技术,可以合成药用基因,用于治疗遗传性疾病。
例如,基因工程合成的血细胞凝聚促进因子(EPO)可以用于治疗贫血,基因工程合成的人胰岛素用于治疗糖尿病等。
3. 基因工程开发新型药物:基因工程技术可以将多个基因从不同的生物体中组合、修饰或改造,创造出新的药物。
例如,通过基因工程技术,可以将人体细胞中的基因导入小鼠胚胎中,产生具有人类免疫系统的小鼠,用于评估新药的疗效和安全性。
4. 基因编辑技术的应用:随着CRISPR-Cas9等基因编辑技术的发展,基因工程技术在生物制药领域的应用进一步扩大。
通过基因编辑技术,可以精确修改生物体的基因组,用于研究疾病机制、开发新药和治疗遗传性疾病等。
未来,随着基因工程技术的进一步发展和创新,生物制药领域的应用也将得到更广泛的推广和应用。
基因工程技术将为药物研发提供更多可能性,加速新药的开发和生产,进而改善人们的健康水平。
基因工程制药(一) (二) (三) (四) (五) (六) (七) (八) (九) (十)概述 基因工程药物生产的基本过程 目的基因的获得 基因表达 基因工程菌的稳定性 基因工程菌生长代谢的特点 基因工程菌发酵 基因工程药物的分离纯化 基因工程药物的质量控制 基因工程药物制造实例(九)基因工程药物的质量控制原核生物表达的重组蛋白质量检测重组蛋白的质量控制指标包括:重组蛋白的鉴别(序列) 重组蛋白的纯度(杂质的类型) 重组蛋白的活性(检测方法) 重组蛋白的安全性 重组蛋白的稳定性 重组蛋白的一致性(构象与构型)原核细菌表达的重组蛋白产物的质量检测项目与方法检测项目 检测项目 检测方法 检测方法产品是否含内毒素 产品是否含内毒素 蛋白质是否变异 蛋白质是否变异 甲硫氨酸是否被甲酰化 甲硫氨酸是否被甲酰化家兔热原法 家兔热原法 肽谱、HPLC、等电聚焦、毛细管电泳 肽谱、HPLC、等电聚焦、毛细管电泳 肽谱、质谱、HPLC、Edman分析 肽谱、质谱、HPLC、Edman分析蛋白质是否变性、聚合、脱氨基 SDS-PAGE、凝胶层析、等电聚焦、质 蛋白质是否变性、聚合、脱氨基 SDS-PAGE、凝胶层析、等电聚焦、质 谱、HPLC、毛细管电泳、Edman分析 谱、HPLC、毛细管电泳、Edman分析 配体是否脱落 配体是否脱落 氨基酸是否发生取代 氨基酸是否发生取代 SDS-PAGE、免疫分析 SDS-PAGE、免疫分析 氨基酸分析、肽谱、质谱、毛细管电泳 氨基酸分析、肽谱、质谱、毛细管电泳是否被细菌、病毒、支原体等污染 微生物学检测 是否被细菌、病毒、支原体等污染 微生物学检测药物的特点 含量少 活性高 安全、可靠 有效基因工程药物研发过程临床前 临床实验 新药申请 批准投放市场新药研究进度表临床前试验 年数 1 2 3 期 4 5 期 6 7 ~ 期 8 批准 9 10人数-20~80人100~300人1000~3000人动物 实验安全性 剂量 70疗效长期毒性通过率(%)30-3520-3020IND (Investigational New Drug Application) NDA (New Drug Application) PLA (Production License Application)基因工程药物(1)活细胞作为表达系统 (2)化学性质:活性蛋白质或多肽; 相对分子量 较大,结构复杂;性质或剂量,对理化条件的 要求高 (3)全过程严格控制、鉴定质量基因工程药物生产工艺过程 种子的贮存培养种子细胞株分离纯化除菌过滤半成品检定成品检定基因工程药物质量控制 原材料的质量控制培养过程质量控制分离纯化过程的质量控制 目标产品的质量控制一、原材料的质量控制确保编码药品的DNA序列的正确性,重组微生物来自单一克隆,所用质粒纯而稳定,以保证产品质量的安全性和一致性。
基因工程制药的基本过程
基因工程制药的基本过程包括:
1.选择目标基因:首先要从所有存在的基因中根据需要选择目
标基因。
2.克隆目标基因:将目标基因克隆到适当的载体中。
在这个过
程中,需要使用不同的限制性内切酶和连接酶对DNA进行操作,将目标基因插入到载体中。
3.转化目标细胞:利用转化技术将重组的载体带有目标基因的DNA转化到目标生物体的细胞中。
4.筛选获得重组生物体:利用适当的筛选技术,筛选出带有目
标基因并且表达该基因的细胞。
筛选的方法可以是选择性培养基、DNA杂交、荧光染色等。
5.表达目标蛋白:在获得重组生物体后,利用适当的生产条件(例如温度、pH值、培养基等)刺激目标基因表达目标蛋白。
6.纯化目标蛋白:利用各种生物化学纯化技术对目标蛋白进行
分离和纯化。
7.制剂和药物研发:将纯化的目标蛋白进行制剂开发和药物研发,包括剂型设计、剂量确定、毒理学和临床试验等。
简述基因工程制药的基本流程基因工程制药是利用基因工程技术来开发和生产药物的过程。
它涉及到多个步骤和方法,以下是基本流程的简要概述:1. 目标基因的选择:首先确定需要表达的目标基因,该基因可能是人类或其他生物体产生的具有治疗作用的蛋白质或多肽。
2. 基因克隆:利用DNA重组技术将目标基因从其自然来源中分离出来,并将其插入到适当的表达载体中,以便将基因导入到宿主细胞中。
3. 基因导入和表达:将经过修饰的表达载体导入到宿主细胞中,这可以通过多种方法实现,如转染、电穿孔或基因枪等。
一旦基因在宿主细胞中被导入,它将开始表达并产生目标蛋白质。
4. 培养和扩增:在适当的培养条件下,培养宿主细胞以扩增转基因细胞群。
这通常需要使用培养基和特定的生长因子来促进细胞生长和表达目标蛋白质。
5. 蛋白质纯化和分离:通过选择合适的纯化方法,如离子交换层析、凝胶过滤、亲和层析等,将目标蛋白质从细胞中纯化出来。
这可以帮助去除杂质并提高目标蛋白质的纯度和活性。
6. 质量控制:对纯化后的蛋白质进行质量控制检测,包括对其纯度、结构和活性的分析。
这确保生产的药物符合安全和有效的标准。
7. 药物制剂:将纯化后的目标蛋白质制备成具有良好稳定性和生物可用性的药物制剂。
这可能涉及到药物配方、缓冲剂的选择、冻干或液体制剂的制备等。
8. 临床试验和批量生产:经过严格的临床试验验证其安全性和有效性后,药物可以进行批量生产。
这包括大规模的生产、包装、贮存、分发和监管,以确保药物的质量和安全。
通过这些基本流程,基因工程制药能够生产出大量具有疗效的蛋白质药物,用于治疗多种疾病,并为人类健康做出贡献。