(完整版)第一章第一节原子结构与性质
- 格式:ppt
- 大小:3.73 MB
- 文档页数:12

可编辑修改精选全文完整版第一章原子结构与性质本章说明本章在学生已有原子结构知识的基础上,进一步深入研究了原子结构,简述了构造原理及运用构造原理进行原子核外电子排布;运用电子云的概念,图文并茂地描述了原子轨道。
在比较系统而深入介绍原子结构知识的基础上,使学生比较容易理解元素周期表的结构及元素周期律的知识,为后续章节内容的学习奠定了基础。
本章内容比较抽象,易成为学习难点。
作为本书的第一章,教材从内容和形式上都比较注意激发和保持学生的学习兴趣,注重培养学生的化学学科核心素养。
一、教材分析本章教材充分考虑了初中化学和高中化学(必修)中的原子结构知识的基础,注意知识的衔接与深化。
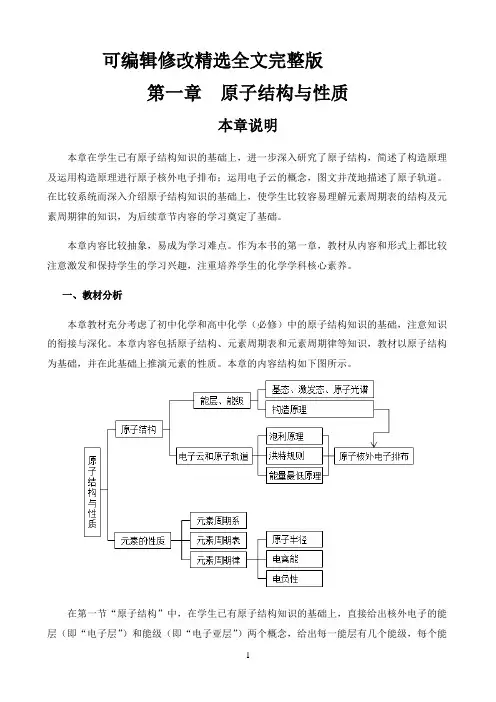
本章内容包括原子结构、元素周期表和元素周期律等知识,教材以原子结构为基础,并在此基础上推演元素的性质。
本章的内容结构如下图所示。
在第一节“原子结构”中,在学生已有原子结构知识的基础上,直接给出核外电子的能层(即“电子层”)和能级(即“电子亚层”)两个概念,给出每一能层有几个能级,每个能级最多可以容纳的电子数,并在能级的基础上引出原子的基态和激发态,以及原子光谱。
有了能层和能级的概念,教材直接给出构造原理,并根据构造原理进行核外电子排布。
这样一来,教材中没有出现四个量子数的概念,降低了学习难度。
构造原理是一个经验规律,构造原理直接给出了原子核外电子排布的次序。
该节在描述原子核外电子的运动状态时,借助电子云的概念,形象地引出了原子轨道。
有了原子轨道的概念,运用原子轨道对原子核外电子的排布作进一步研究,进而介绍了泡利原理和洪特规则,以及能量最低原理。
在第二节“原子结构与元素的性质”中,首先,从元素周期律、元素周期系的角度说起元素周期表,然后,根据构造原理得出的核外电子排布,解释了元素周期系的基本结构,再通过“探究”栏目要求学生进一步认识元素周期表的结构。
关于元素周期律,教材重点讨论原子半径、电离能和电负性的周期性变化。
另外,多样化的图表是本章在呈现方式上的特点。
第一章原子结构与性质课标要求1.了解原子核外电子的能级分布,能用电子排布式表示常见元素的(1~36号)原子核外电子的排布。
了解原子核外电子的运动状态。
2.了解元素电离能的含义,并能用以说明元素的某种性质3.了解原子核外电子在一定条件下会发生跃迁,了解其简单应用。
4.了解电负性的概念,知道元素的性质与电负性的关系。
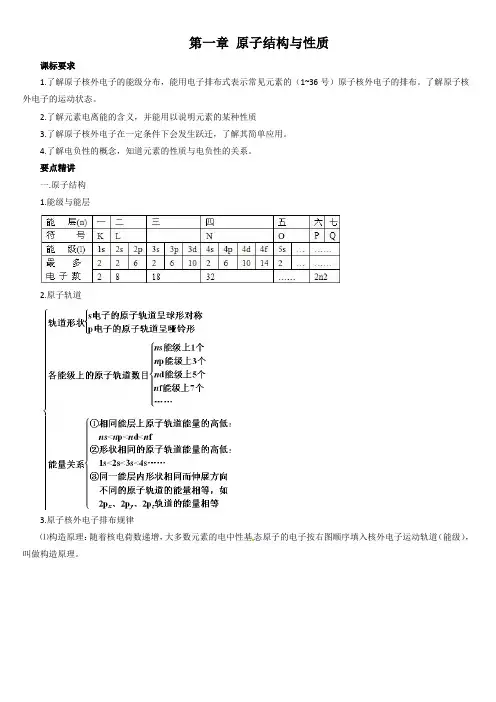
要点精讲一.原子结构1.能级与能层2.原子轨道3.原子核外电子排布规律⑴构造原理:随着核电荷数递增,大多数元素的电中性基态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
能级交错:由构造原理可知,电子先进入4s 轨道,后进入3d 轨道,这种现象叫能级交错。
说明:构造原理并不是说4s 能级比3d 能级能量低(实际上4s 能级比3d 能级能量高),而是指这样顺序填充电子可以使整个原子的能量最低。
也就是说,整个原子的能量不能机械地看做是各电子所处轨道的能量之和。
(2)能量最低原理 现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量最低原理。
构造原理和能量最低原理是从整体角度考虑原子的能量高低,而不局限于某个能级。
(3)泡利(不相容)原理:基态多电子原子中,不可能同时存在4个量子数完全相同的电子。
换言之,一个轨道里最多只能容纳两个电子,且电旋方向相反(用“↑↓”表示),这个原理称为泡利(Pauli )原理。
(4)洪特规则:当电子排布在同一能级的不同轨道(能量相同)时,总是优先单独占据一个轨道,而且自旋方向相同,这个规则叫洪特(Hund )规则。
比如,p3的轨道式为或,而不是洪特规则特例:当p 、d 、f 轨道填充的电子数为全空、半充满或全充满时,原子处于较稳定的状态。
即p0、d0、f0、p3、d5、f7、p6、d10、f14时,是较稳定状态。
前36号元素中,全空状态的有4Be 2s22p0、12Mg 3s23p0、20Ca 4s23d0;半充满状态的有:7N 2s22p3、15P 3s23p3、24Cr 3d54s1、25Mn 3d54s2、33As 4s24p3;全充满状态的有10Ne 2s22p6、18Ar 3s23p6、29Cu 3d104s1、30Zn 3d104s2、36Kr 4s24p6。


第一章原子结构与性质第一节原子结构(第1课时)一、原子与元素1.原子:2.元素:3.同位素:因此同一元素具有不同的核素,即同一元素具有多种原子,既原子种类多于元素种类。
二、能层与能级核外电子因能量不同而在与核距离不同的能层(相当于电子层)运动,用___________等表示;同一能层中的电子能量不同和运动区域不同而分为不同的能级,用______________等表示。
每一能层和能级中运动的电子数目是有限度的——电子层最大容量原理:若用n来表示能层数,则每一能层中运动的电子数目为______(次外层最多只能容纳_________个电子;倒数第三层最多只能容纳_________个电子)。
ns、np、nd等能级中最多只能容纳的电子数:若s、p、d等分别用1、3、5等表示,则它们分别最大容量则是2、6、10等,即其所表示数字的二倍,但与n无关。
三、构造原理1.构造原理就是电子的排布顺序,它遵循三个基本原理(1)能量最低原理:原子的排布总是尽先进入能量最低的轨道,只有当能量最低的轨道占满后,电子才依次进入能量稍高的轨道,原子的电子排布总是使整个原子的能量处于最低状态。
各能级能量高低顺序:E(1s)<E(2s)<E(3s);E(ns)<E(np)<E(np)<E(nd)<E(nf)能级交错现象:E(ns)<E[(n-2)f]<E[(n-1)d]<E(np)(2)泡利不相容原理:在任何一个原子轨道中最多都只能容纳2个电子,而且自旋方向相反(分别用“↑”、“↓”表示不同的自旋方向)。
(3)洪特规则:当电子排布在同一能级不同的轨道时,总是优先单独占据一个轨道而且自旋方向相同。
同步训练:1.主族元素A和B可形成组成为AB2的离子化合物,则A、B两原子的最外层电子排布分别为A.ns2np2和ns2np4B.ns1和ns2np4C.ns2和ns2np5D.ns1和ns22.某元素的原子3d能级上有1个电子,它的N能层上电子数是A.0B.2C.5D.83.比较下列多原子的各轨道的能量高低:(1)1s,3d (2)3s,3p,3d (3)2p,3p,4p4.下列关于多电子原子核外电子的运动规律的叙述正确的是A.核外电子是分层运动的B.所有电子在同一区域里运动C.能量高的电子在离核近的区域运动D. 能量低的电子在离核近的区域绕核旋转5.主族元素原子失去最外层电子形成阳离子,主族元素的原子得到电子填充在最外层形成阴离子。



化学-选择性必修第2册-基础知识汇总第一章原子结构与性质第一节原子结构第1课时能层与能级基态与激发态一、能层与能级1920年,丹麦科学家玻尔在氢原子模型基础上,提出构造原理,开启了用原子结构解释元素周期律的篇章。
1925年以后,玻尔的“壳层”落实为“能层”与“能级”,厘清了核外电子的可能状态,复杂的原子光谱得以诠释。
1936年,德国科学家马德隆发表了以原子光谱事实为依据的完整的构造原理。
1.能层(1)含义:根据核外电子的能量不同,将核外电子分为不同的能层(电子层)。
(2)序号及符号能层序号一、二、三、四、五、六、七……分别用K、L、M、N、O、P、Q……表示,其中每层所容纳的电子数最多为2n2个。
(3)能量关系能层越高,电子的能量越高,能量的高低顺序为E(K)<E(L)<E(M)<E(N)<E(O)<E(P)<E(Q)。
2.能级(1)含义:根据多电子原子的同一能层的电子的能量也可能不同,将它们分为不同能级。
(2)表示方法:分别用相应能层的序数和字母s、p、d、f等表示,如n能层的能级按能量由低到高的排列顺序为n s、n p、n d、n f等。
3.能层、能级与最多容纳的电子数能层一二三四五六七……(n)符号K L M N O P Q……能级1s2s2p3s3p3d4s4p4d4f5s……………………最多22626102610142……………………电子281832………………2n2数由上表可知:(1)能层序数等于该能层所包含的能级数,如第三能层有3个能级。
(2)s、p、d、f各能级可容纳的最多电子数分别为1、3、5、7的2倍。
(3)原子核外电子的每一能层最多可容纳的电子数是2n2(n为能层的序数)。
二、基态与激发态原子光谱1.基态原子与激发态原子(1)基态原子:处于最低能量状态的原子。
(2)激发态原子:基态原子吸收能量,它的电子会跃迁到较高能级,变成激发态原子。
(3)基态、激发态相互间转化的能量变化激发态原子基态原子吸收能量释放能量,主要形式为光2.光谱(1)光谱的成因及分类(2)光谱分析:在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析。
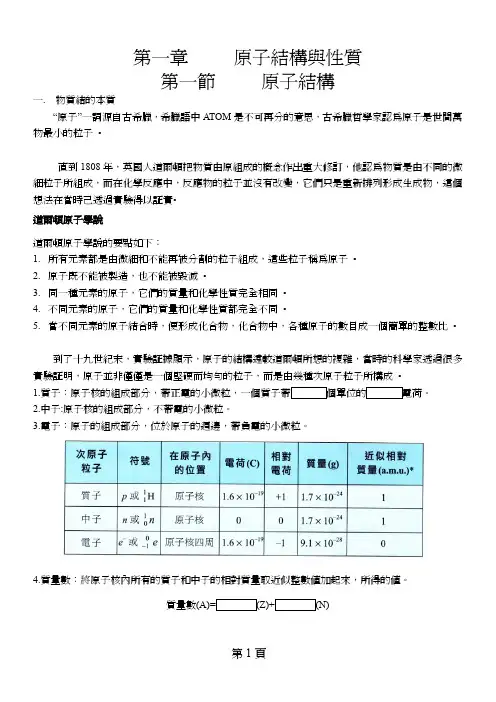
第一章原子結構與性質第一節原子結構一. 物質結的本質“原子”一詞源自古希臘,希臘語中ATOM是不可再分的意思,古希臘哲學家認為原子是世間萬物最小的粒子◦直到1808年,英國人道爾頓把物質由原組成的概念作出重大修訂,他認為物質是由不同的微細粒子所組成,而在化學反應中,反應物的粒子並沒有改變,它們只是重新排列形成生成物,這個想法在當時己透過實驗得以証實◦道爾頓原子學說道爾頓原子學說的要點如下:1.所有元素都是由微細和不能再被分割的粒子組成,這些粒子稱為原子◦2.原子既不能被製造,也不能被毀滅◦3.同一種元素的原子,它們的質量和化學性質完全相同◦4.不同元素的原子,它們的質量和化學性質都完全不同◦5.當不同元素的原子結合時,便形成化合物,化合物中,各種原子的數目成一個簡單的整數比◦到了十九世紀末,實驗証據顯示,原子的結構遠較道爾頓所想的複雜,當時的科學家透過很多實驗証明,原子並非僅僅是一個堅硬而均勻的粒子,而是由幾種次原子粒子所構成◦1.質子:原子核的組成部分,帶正電的小微粒,一個質子帶個單位的電荷。
2.中子:原子核的組成部分,不帶電的小微粒。
3.電子:原子的組成部分,位於原子的週邊,帶負電的小微粒。
4.質量數:將原子核內所有的質子和中子的相對質量取近似整數值加起來,所得的值。
質量數(A)=(Z)+(N)5.同位素在同一種元素的原子中,當中有一些質子數目相同(即相同的原子序),但其中子數目並不相同(即不同質量數),這些原子稱為同位素。
例如:氯(Cl)的兩種同位素可寫成:豐度(自然界中的原子含量)的計算:一種元素的相對子原子質量是指該元素的各種同位素在碳-12標度上的相對同位素質量的平均值。
由於35Cl 和37Cl 的相對豐度分別是75.77和24.23,因此氯的相對原子質量可由以下的簡單計算中求得:則銅的相對原子質量為:.例1 已知自然界氧的同位素有16O ,17O ,18O ,氫的同位素有H ,D 。

第一章《原子结构与性质》知识点归纳一、原子的诞生宇宙大爆炸之后,逐渐形成了氢、氦等轻元素。
随着恒星的演化和核聚变反应,产生了更多的元素。
二、能层与能级能层:根据多电子原子的核外电子的能量差异,将核外电子分成不同的能层,分别用 K、L、M、N、O、P、Q 表示,离核越近,能量越低。
能级:在同一能层中,电子的能量也有所不同,又分为不同的能级。
例如,K 能层只有 1 个能级 s,L 能层有 2 个能级 s、p,M 能层有 3 个能级 s、p、d 等。
三、构造原理与电子排布式构造原理:随着核电荷数递增,电子按照能级顺序填充,遵循能量最低原理。
电子排布式:用数字在能级符号右上角标明该能级上排布的电子数。
例如,钠原子的电子排布式为 1s²2s²2p⁶3s¹。
四、能量最低原理、泡利原理和洪特规则能量最低原理:原子的电子排布遵循构造原理,使整个原子的能量处于最低状态。
泡利原理:一个原子轨道最多只能容纳2 个电子,且自旋方向相反。
洪特规则:当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,且自旋方向相同。
五、原子结构与元素周期表周期:周期数等于能层数。
族:主族元素的族序数等于最外层电子数,副族元素的族序数与价电子排布有关。
分区:根据价电子排布,可将元素周期表分为 s 区、p 区、d 区、ds 区和 f 区。
六、元素周期律原子半径:同周期从左到右原子半径逐渐减小,同主族从上到下原子半径逐渐增大。
电离能:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量。
同周期从左到右电离能逐渐增大,同主族从上到下电离能逐渐减小。
电负性:用来描述不同元素的原子对键合电子吸引力的大小。
同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小。
七、原子轨道s 轨道:呈球形,只有 1 个伸展方向。
p 轨道:呈哑铃形,有 3 个伸展方向。
d 轨道:有 5 个伸展方向。
八、电子云电子云是电子在核外空间出现概率的形象化描述。

第一章 原子结构与性质一.原子结构1.能级与能层2.原子轨道3.原子核外电子排布规律⑴构造原理:随着核电荷数递增,大多数元素的电中性基态原子的电子按右图顺序填入核外电子运动轨道(能级),叫做构造原理。
能级交错:由构造原理可知,电子先进入4s 轨道,后进入3d 轨道,这种现象叫能级交错。
说明:构造原理并不是说4s 能级比3d 能级能量低(实际上4s 能级比3d 能级能量高),而是指这样顺序填充电子可以使整个原子的能量最低。
也就是说,整个原子的能量不能机械地看做是各电子所处轨道的能量之和。
(2)能量最低原理现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,简称能量说明:构造原理和能量最低原理是从整体角度考虑原子的能量高低,而不局限于某个能级。
(3)泡利(不相容)原理基态多电子原子中,不可能同时存在4个量子数完全相同的电子。
换言之,一个轨道里最多只能容纳两个电子,且电旋方向相反(用“↑↓”表示),这个原理称为泡利(Pauli )原理。
(4)洪特规则当电子排布在同一能级的不同轨道(能量相同)时,总是优先单独占据一个轨道,而且自旋方向相同,这个规则叫洪特(Hund )规则。
比如,p3的轨道式为或,而不是。
洪特规则特例:当p 、d 、f 轨道填充的电子数为全空、半充满或全↑↓ ↑↓ ↓ ↓ ↑ ↑ ↑充满时,原子处于较稳定的状态。
即p0、d0、f0、p3、d5、f7、p6、d10、f14时,是较稳定状态。
前36号元素中,全空状态的有4Be 2s22p0、12Mg 3s23p0、20Ca 4s23d0;半充满状态的有:7N 2s22p3、15P 3s23p3、24Cr 3d54s1、25Mn 3d54s2、33As 4s24p3;全充满状态的有10Ne 2s22p6、18Ar 3s23p6、29Cu 3d104s1、30Zn3d104s2、36Kr 4s24p6。
4. 基态原子核外电子排布的表示方法(1)电子排布式①用数字在能级符号的右上角表明该能级上排布的电子数,这就是电子排布式,例如K:1s22s22p63s23p64s1。