海水的综合利用
- 格式:doc
- 大小:319.00 KB
- 文档页数:4

证对市爱幕阳光实验学校铁路高三化学复习:第二章课题2 海水的综合利用一.海水中盐的利用——氯碱工业(1)设备:离子交换膜电解槽。
离子交换膜只允许Na+通过。
(2)化学反阴极:2H++2e-===H2↑(复原反)阳极:2Cl--2e-===Cl2↑(氧化反)化学方程式:2NaCl+2H2O 2NaOH+H2↑+Cl2↑。
(3)粗盐的精制①目的:除去泥沙,使Ca2+、Mg2+、Fe3+、SO42-离子的含量到达要求。
②原因:Ca2+、Mg2+在碱溶液中形成的沉淀及泥沙会破坏离子交换膜,而SO42-会引入杂质。
③试剂:BaCl2、Ca(OH)2、Na2CO3、稀盐酸。
用BaCl2除去SO42-,用Ca(OH)2除去Mg2+、Fe3+,用Na2CO3除去Ba2+及Ca2+,所加沉淀剂稍过量。
④工艺流程在进入电解槽前需通过离子交换树脂进一步除去Ca2+、Mg2+离子,以防破坏离子交换膜。
⑤有关反方程式Ba2++SO42- ===BaSO4↓,Mg2++2OH-===Mg(OH)2↓,Fe3++3OH-===Fe(OH)3↓,Ca2++CO32-===CaCO3↓,Ba2++CO32- ===BaCO3↓,CO32-+2H+===H 2O +CO2↑。
二.海水提溴(1)工艺流程(2)反原理Cl2+2NaBr===2NaCl+Br23Br2+3Na2CO3===5NaBr+NaBrO3+3CO2↑三.海水提镁(1)工艺流程(2)主要化学反①制备石灰乳:CaCO 3CaO+CO2↑CaO+H2O===Ca(OH)2②沉淀Mg2+:Mg2++Ca(OH)2===Mg(OH)2↓+Ca2+③制备MgCl2:Mg(OH)2+2HCl===MgCl2+2H2O④电解MgCl2:MgCl2(熔融) Mg+Cl2↑(3)生产中用的平衡原理①沉淀溶解平衡原理a.向海水中参加沉淀剂Ca(OH)2,由于c(OH-)增大,Mg(OH)2的溶解度小于Ca(OH)2,那么最大程度地将Mg2+转化为Mg(OH)2沉淀。


海水的综合利用归纳南靖一中沈建忠2010、09、15海水中平均含盐3.5%,含多种矿物质,如钠、钙、钾、溴、碘、锶等。
海水资源包括:能量、生物、化学、矿物、及空间资源。
利用潮汐能量发电,各种化学物质被综合利用,海水还是人类未来重要的淡水来源、新的能源和人类的空间资源。
问题1:海水的综合利用有哪些方面?(1)海水的直接利用;(2)海水的淡化;(3)制盐和以盐为原料的盐化工;(4)提取海水中溶存的有用元素。
一、海水中水资源的利用——获取淡水1、途径:通过海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。
2、海水淡化的方法及其特点:海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等。
原理:蒸溜法分离海水;优点:蒸馏法的历史最久,技术和工艺也比较完善;缺点:成本较高,难推广应用。
二、海水中的化学资源1、特点:种类多、总储量大、富集程度低含80多种元素,以氢、氧、氯、钠、镁、硫、钙、钾等较多。
被称为“元素的故乡”。
海水中铀多达45亿吨是已知陆地铀矿储量的4500倍。
氘有50亿吨足够人类用上千万年2、从海水中提取物质的方法(1)从海水中提取食盐如何制盐?NaCl、海水晒盐A 、粗盐的成份及精制:a 、粗盐:含较多的氯化镁和氯化钙及泥沙b 、提纯实验步骤:溶解、过滤、结晶。
(请说说:过滤操作的要点;玻璃棒的使用;结晶操作要点;)c 、请设计实验室除去NaCl 中混有的Ca 2+、Mg 2+离子的方法(需要仪器及实验步骤):(答案:溶解,加稍过量的氢氧化钙,再加入稍过量的碳酸钠溶液,过滤;在滤液中加入稍过量的盐酸,蒸发结晶。
)B 、海水晒盐后的“卤水”中还有哪些盐含量较高?氯化镁 碘化钾 溴化钾 (2)海水提取镁试剂①溶液Mg(OH)2沉淀试剂②MgCl 2溶液Mg无水MgCl 2熔融电解(1)Ca(OH)2(2)过滤(3)盐酸(4)MgCl 2(熔融)电解Mg + Cl 2 ↑海水(含Mg 2+)过量(3)、海带中提取碘的实验 原理: I - —— I 2 检验I 2: 用淀粉溶液检验,看它是否变蓝。






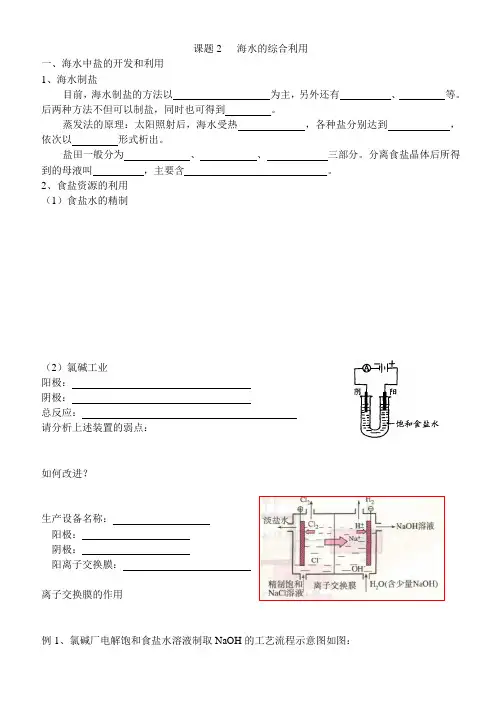
课题2 海水的综合利用一、海水中盐的开发和利用1、海水制盐目前,海水制盐的方法以为主,另外还有、等。
后两种方法不但可以制盐,同时也可得到。
蒸发法的原理:太阳照射后,海水受热,各种盐分别达到,依次以形式析出。
盐田一般分为、、三部分。
分离食盐晶体后所得到的母液叫,主要含。
2、食盐资源的利用(1)食盐水的精制(2)氯碱工业阳极:阴极:总反应:请分析上述装置的弱点:如何改进?生产设备名称:阳极:阴极:阳离子交换膜:离子交换膜的作用例1、氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如图:依据图,完成下列填空:(1)粗盐中含有的较多的可溶性杂质(氯化镁、氯化钙、硫酸钠等)和。
(2)工业食盐含有较多杂质,精制过程中加NaOH的作用是。
(3)在电解过程中,与电源正极相连的电极上所发生的反应为。
与电源负极相连的电极附近,溶液的pH .(填“升高”、“不变”、“降低”)(4)粗盐中硫酸钠含量较高,必须添加钡试剂除去硫酸根离子,该钡试剂可以是A.Ba(OH)2 B.Ba(NO3)2C.BaCl2(5)为了有效地除去氯化镁、氯化钙、硫酸钠,加入试剂的合理顺序为A.先加入NaOH,后加入Na2CO3,再加入钡试剂B.先加入NaOH,后加入钡试剂,再加入Na2CO3C.先加入钡试剂,后加入NaOH,再加入Na2CO3D.先加入钡试剂,后加入Na2CO3,再加入NaOH(6)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过(填写操作名称)、冷却、过滤除去NaCl.(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,Cl2和NaOH溶液充分接触,产物是NaClO和氯化钠和水,请写出Cl2和NaOH溶液反应的化学方程式。
※海水中提取化学物质的一般方法二、海水提溴——法基本流程:1、氯化氯化之前要将海水,原因是。
氯化反应:2、吹出用或将溴吹出。
3、吸收用还原剂使溴单质变为HBr,再用将其氧化成溴产品。

第四章第二课时海水资源的综合利用海水淡化与化工生产,能源技术相组合制备氯化钠食用工业原料生产烧碱纯碱,Na Cl 2,盐酸,漂白粉制取Mg ,K ,Br 2,I 2及其化工产品获得其他物质和能量:铀和重水开发海洋药物开发新能源:潮汐能,波浪能一、海水资源的综合利用1、 海水制盐(1)方法:把海水引到盐滩上,利用日光和风力使水分蒸发,得到食盐。
(2)食盐的用途:氯碱工业:2NaCl +2H 2O=====电解2NaOH +Cl 2↑+H 2↑制钠和氯气2NaCl(熔融)=====电解2Na +Cl 2↑ 制盐酸Cl 2+H 2=====点燃2HCl制漂白剂Cl 2+2NaOH===NaCl +NaClO +H 2O制纯碱:NaCl +CO 2+H 2O +NH 3=== NaHCO 3↓+NH 4Cl NaHCO 3=== Na 2CO 3+CO 2↑+H 2O2、 海水提溴:(1)氯化氯气氧化溴离子,在pH=3.5的酸性条件下效果最好,所以在氯化之前要将海水酸化。
(2)吹出当海水中的Br 一被氧化成Br 2以后,用空气将其吹出。
另外,也可以用水蒸气,使溴和水蒸气一起蒸出。
(3)吸收目前比较多的是用二氧化硫作还原剂,使溴单质转化为HBr ,再用氯气将其氧化得到溴产品。
化学方程式如下:2NaBr + Cl 2 === Br 2 +2NaClSO 2+Br 2+2H 2O===4H ++2Br -+SO 2-42 HBr +Cl 2===2 HCl +Br 2 2、海水提镁: (1)工艺流程△(2)主要化学反应①制备石灰乳:CaCO 3 === CaO + CO 2 ↑ ,CaO + H 2O === Ca(OH)2 ②沉淀Mg 2+: MgCl 2+Ca(OH)2===Mg(OH)2↓+CaCl 2③制备MgCl 2:Mg(OH)2+2HCl===MgCl 2+2H 2O, MgCl 2·6H 2O=====HClMgCl 2+6H 2O 制备Mg: MgCl 2(熔融)=====电解Mg +Cl 2↑3、海水提碘(1)工业海带中提碘1)流程:海带―→浸泡―→氧化―→过滤―→提纯―→碘单质 2)主要反应的原理:Cl 2+2KI===2KCl +I 2 (2)海带中含有碘元素的检验1)主要反应的原理:H ++2I -+H 2O 2===I 2+2H 2O二、侯氏制碱法NaCl +CO 2+H 2O +NH 3=== NaHCO 3↓+NH 4ClNaHCO 3=== Na 2CO 3+CO 2↑+H 2O 物质分离的几种方法:定义:物质的分离是指通过适当的方法,把混合物中的几种物质分开(要还原成原来的形式),分别得到几种比较纯净的物质。
第二单元化学与资源开发利用课题二海水的综合利用第1课时教学目标1.了解氯碱工业反应原理;正确书写电极反应方程式和电解的总化学方程式.2.初步了解电解槽的简单结构及食盐水的精制.3.常识性介绍以氯碱工业为基础的化工生产。
4.通过电解食盐水的实验,培养学生的观察能力、分析归纳能力和利用化学原理解决实际问题的能力。
5.通过阅读材料,培养学生的自学能力。
6.通过对实验现象的观察,掌握观察实验的方法和步骤,准确记录实验现象,正确分析实验现象,探究实验规律的方法.通过讨论,激发学生的求知欲,闪现智慧火花,培养创新意识。
教学重点氯碱工业反应原理。
教学难点氯碱工业反应原理。
教学方法演示实验法教学用具1.实验仪器:铁架台、U型管、石墨电极、导线、电流表、直流电源。
2.实验药品:饱和氯化钠溶液。
3.幻灯片若干张。
课时安排2课时引入新课:本节课我们学习电解饱和食盐水制烧碱—-又称氯碱工业。
我们学习的主要目标是掌握工业上制取氯气和烧碱的反应原理,初步了解化工生产设备、原料及其精制、生产流程.【板书】第二节氯碱工业一、电解饱和食盐水反应原理【演示】实验装置如右图:【投影】实验步骤:1.按装置图安装好仪器。
2.向U型管中注人饱和食盐水,接通电源。
3.向阴阳两极滴加几滴酚酞溶液,把湿润的淀粉碘化钾试纸分别放在阴阳两极试管口上方。
【设疑】电解池两极上各有什么现象产生?【提问】请描述实验现象,试判断出结论。
【学生回答】(相互补充)1.两极均产生气体。
2.阴极区附近溶液出现红色,有碱生成。
3.阳极淀粉碘化钾试纸变蓝,气体有刺激性气味,应是Cl2.【阅读讨论】阅读教材,看后相互讨论,推选代表回答产生这种现象的原因。
【小结并板书】师生共同总结:在阴极:由于2H++2e— = H2↑,H+不断被消耗,促进H2OH++OH—向右移动,破坏了水的电离平衡,c(OH-)相对的增大了,因此,在阴极附近形成了氢氧化钠溶液.【提问】写出电解的总的化学反应方程式。
海水的综合利用
复习目标:
1.掌握氯碱工业、海水提溴、海水冶炼镁的化学原理;
2.了解海水的综合利用,认识化学科学发展对自然资源利用的作用。
复习重点、难点:氯碱工业、海水提溴、海水冶炼镁的化学原理。
课时划分:一课时
教学过程
知识梳理
海水中储有大量的化学物质,储量可观的就有__多种化学元素,其中__多种可以被人类提取利用,海水素有“液体工业原料”之美誉。
一、海水中盐的开发与利用
1、海水制盐的方法主要有三种,即:__法、__析法和__法。
2、食盐资源的利用
(1)电解饱和食盐水反应原理
阴极:__________阳极:___________
总反应:____________________
(2)生产设备名称:_____电解槽
阳极:金属钛网(涂钛钌氧化物)
阴极:碳钢网(有镍涂层)
阳离子交换膜:只允许阳离子通过,把电解槽隔成阴极室和阳极室。
防止____________,避免_________________。
(3)食盐水的精制
思考问题:①用什么方法除去泥沙?____。
②用什么试剂除去Ca2+、Mg2+、Fe3+、2-?③所用试剂只有过量才能除净这些杂质,你能设计一个合理的顺序逐一除杂吗?
SO
4
【例题1】氯碱工业中用离子交换膜法电解制碱的主要生产流程示意图如下:
依据上图完成下列填空:
(1)与电源正极相连的电极上所发生反应的化学方程式为___________________;与电源负极相连的电极附近,溶液的pH__________(选填“不变”“升高”“降低”)。
(2)工业食盐含Ca2+、Mg2+、Fe3+等杂质,精制过程中发生反应的离子方程式为______________________。
(3)如果粗盐中SO
42-含量较高,必须添加钡试剂除去SO
4
2-,该钡试剂可以是_____(选填
a、b、c)。
a.Ba(OH)
2 b.Ba(NO
3
)
2
c.BaCl
2
(4)为有效除去Ca2+、Mg2+、SO
4
2-,加入试剂的合理顺序为___________(选填a、b、c)。
a.先加NaOH,后加Na
2CO
3
,再加钡试剂
b.先加NaOH;后加钡试剂,再加Na
2CO
3
c.先加钡试剂,后加NaOH,再加Na
2CO
3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、
_______________(填写操作名称)除去NaCl。
(6)由图示可知用离子交换膜法电解制碱工艺中___________产品可循环使用。
(7)已知NaCl在60℃的溶解度为37.1 g,现电解60℃精制饱和食盐水1 371 g 经分析,电解后溶液密度为1.37 g·cm-3,其中含有20gNaCl,则电解后NaOH的物质的量浓度为__________mo1·L-1。
解析:本题取材于新教材第三册第四单元电解原理及其应用中的氯碱工业。
本题以氯碱工业为主线突出考查了元素及其化合物这一主干知识,通过本题的解答可归纳如下知识点:
(1)在电解饱和NaCl溶液时,电解池阴极附近溶液的pH为什么会升高?这是因为当电解
时Na+、H+趋向阴极,而H+放电能力比Na+强,故H+在阴极放电:2H++2e=H
2
↑,而H+在阴极不断放电打破了水的电离平衡,使阴极附近溶液中c(OH-),c(H+),故电解一段时间后阴
极因生成NaOH 而使溶液的pH 升高。
(2)离子交换膜法电解制碱技术是氯碱工业发展的方向,同以前无隔膜法电解制碱技术相比避免了Cl 2进入阴极区与Na0H 溶液接触发生如下反应:Cl 2+2NaOH =NaCl+NaClO+H 2O ,影响产品的质量。
答案:(1)2Cl —2e=Cl 2 ↑ 升高
(2)Ca 2+
+CO 32-=CaCO 3 ↓;Mg 2+
+2OH -=Mg(OH)2↓ ;Fe 3+
+3OH -
=Fe(OH)3↓
(3)a 、c (4)b 、c (5)蒸发 过滤 (6)NaCl (或淡盐水) (7)7.14 二、海水提溴
1、氧化:工业上从海水中提取溴时,首先通氯气于pH 为3.5左右晒盐后留下苦卤(富含Br -离子)中置换出Br 2,化学方程式:__________________。
2、吹出:然后用空气把Br 2吹出,再用Na 2C03溶液吸收,即得较浓的NaBr 和NaBrO 3溶液:
化学方程式:__________________。
最后,用硫酸将溶液酸化,Br 2即从溶液中游离出来:化学方程式:__________________。
3、吸收:用还原剂二氧化硫使溴单质变为HBr ,再用氯气将其氧化成溴产品:化学方程式:______________、__________________。
三、海水提镁
[知识链节]回顾写出金属镁的主要化学反应方程式。
[海水提镁](1)用Ca (OH )2将海水和苦卤中的Mg 2+沉淀出来成为Mg (OH )2,再加入HCl 即可得到MgCl 2(2)然后在HCl 的气氛中将MgCl 2溶液转变为无水MgCl 2,最后电解熔融状态的MgCl 2,即可制得镁:
↑
+22Cl Mg MgCl 通电
思考:如何由贝壳制得氢氧化钙?
【例题2】从海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图。
⎪⎩
⎪
⎨⎧⎩⎨⎧−−→−−−→−∙−−−−−→−−−−→−−−−−→−−−→−→Mg Cl MgCl O H MgCl OH Mg NaCl 22
222)(6)(通电
脱水
加盐酸蒸发、浓缩、结晶加石灰水
饱和溶液电解精制无水烧碱和氯气粗盐海水
根据示意图回答下列问题:
(1)粗盐中含有Ca 2+
、Mg 2+
、-
24SO 等杂质离子,精制时所用试剂为盐 酸、BaCl 2溶液、
NaOH 溶液、Na 2CO 3溶液,加入试剂的顺序是 。
(2)电解饱和食盐水的总反应的化学方程式为 。
(3)工业上MgCl 2·6H 2O 晶体在 气氛中加热脱水,通入此种气体的作用是 。
可选用药品:MgCl 2·6H 2O 晶体、NaCL(s)、KClO 3(s)、MnO 2、浓H 2SO 4、浓HCl 、稀NaOH 溶液。
仪器:见下图(装置可重复使用)。
a.组装氯化氢气体发生器,应选用的仪器(用编号A 、B 、…填入)是 ;有关的化学方程式是 。
b.按HCl 气流方向,其余装置的连接顺序(用数字①、②…填入)是:( ) ( )( ) ( )( ) ( )( )
c.各装置中应放的药品为:A. ,B. ,C. ,D. ,E. 。
d.B 装置的作用是 ,B 中能观察到的现象是 。
解答:(1)NaOH 、BaCl 2、Na 2CO 3、HCl (2)2NaCl+2H 2O
电解
2NaOH+2H 2+Cl 2
(3)干燥的HCl ,防止MgCl 2·6H 2O 受热脱水时水解。
aE ,C , NaCl+H 2SO 4(浓)
△
NaHSO 4+HCl
b ⑤、①、②、③、⑦、④、③
c 浓H 2S 4,稀NaOH ,NaCl(s),MgCl 2·6H 2O ,浓H 2SO 4
d 吸收HCl 气体,白色酸雾。
四、制备重水有三种方法。
蒸馏法:这种方法只能得到纯度为92%的重水;电解法:可得99.7%的重水,但消耗电能特别大。
化学法:水-硫化氢交换法和氨-氢交换法。